牛血紅蛋白催化香豆素體系熒光光度法測定過氧化氫
單雅琦,陳永寧,張容琿,唐寧莉
(桂林理工大學 化學與生物工程學院,廣西 桂林 541004)
?
牛血紅蛋白催化香豆素體系熒光光度法測定過氧化氫
單雅琦,陳永寧,張容琿,唐寧莉
(桂林理工大學 化學與生物工程學院,廣西 桂林541004)
摘要:在pH 3.5的NaOH-H2SO4緩沖溶液中,牛血紅蛋白催化H2O2氧化香豆素生成7-羥基香豆素,導致體系的熒光強度明顯增強。該氧化產物在456 nm處有最大熒光強度。實驗表明:在456 nm處,體系的熒光增加值ΔF與H2O2的濃度在3.940×10-7~7.880×10-5mol/L范圍內呈良好的線性關系,相關系數r為0.998 5,檢出限為1.25×10-8mol/L。據此建立了一種簡單、靈敏度高的檢測水樣中痕量H2O2的熒光新方法。該方法已用于雨水及消毒液中H2O2的測定,結果滿意。
關鍵詞:過氧化氫;牛血紅蛋白;香豆素;熒光法
過氧化氫普遍存在于自然生態體系中,是生物和環境系統中存在的一種重要中間產物,在食品科學、醫學、化學、生物、環境保護等眾多領域應用廣泛。它是大氣中氫過氧自由基(HOO·)濃度的指標, 還可與還原劑(如Fe2+)反應導致羥基自由基(HO·)的形成,HO·是大氣和地表水中最重要的氧化劑成分之一。許多研究表明,過氧化氫可以氧化二氧化硫,從而導致大氣中硫酸的形成。因此,對過氧化氫的檢測具有重要意義。
到目前為止, 已經有很多方法用于檢測過氧化氫,例如分光光度法[1]、 熒光光度法[2-3]、 色譜法[4-5]、 化學發光法[6-7]、 電化學法[8-9]、 原子吸收光譜法[10]、 共振散射光譜法[11-12]、 滴定法[13]等。 其中熒光分析法是一種具有高靈敏度、 高選擇性的方法, 并且酶催化體系測定過氧化氫具有靈敏度高、 檢出限低等優點。 由于血紅蛋白具有鐵卟啉輔基(天然過氧化物酶(HRP)的活性中心), 并且有三維空間結構特點, 因此具有催化活性, 可用于酶催化反應體系中。 筆者以牛血紅蛋白(Hb)為過氧化物模擬酶,催化H2O2氧化香豆素生成7-羥基
香豆素,該氧化產物在456 nm處產生強熒光,據此建立了一種測定痕量H2O2的新方法。
1實驗部分
1.1主要儀器
Cary Eclipse熒光光度計(美國 VARIAN);PHS-3C精密pH計(上海雷磁儀器廠);501型超級恒溫器(上海市實驗儀器廠)。
1.2主要試劑
牛血紅蛋白工作液(Hb, 國藥集團化學試劑有限公司),準確稱取0.064 5 g摩爾質量為64 500 g/mol的牛血紅蛋白,用水溶解配成濃度為1.0×10-5mol/L的Hb工作液,于4 ℃冰箱儲存。H2O2(汕頭市西隴化工廠有限公司)儲備溶液, 取2 mL 30% H2O2稀釋至500 mL,用高錳酸鉀法標定得準確濃度為3.94×10-2mol/L,于4 ℃冰箱儲存。H2O2工作溶液,7.88×10-4mol/L,臨用前由儲備液稀釋得到。香豆素(國藥集團化學試劑有限公司)溶液,4.0×10-4mol/L。NaOH-H2SO4緩沖溶液, pH 3.0~5.0,由0.2 mol/L NaOH與0.2mol/L H2SO4溶液按一定比例混合配成。HAc-NaAc緩沖溶液,pH 3.0~5.0, 由0.2 mol/L HAc與0.2 mol/L NaAc溶液按一定比例混合配成。Britton-Robinson(B-R)緩沖溶液,pH 3.0~5.0,0.04 mol/L的HAc、H3BO3、H3PO4溶液等體積混合,然后用0.2 mol/L的NaOH溶液按一定比例混合配成。
實驗中所用到的試劑均為分析純,水均為二次去離子水。
1.3實驗方法
在10 mL具塞比色管中,分別加入3.0 mL NaOH-H2SO4緩沖液(pH 3.5)、1.8 mL香豆素溶液、1.0 mL Hb溶液和一定量的H2O2工作液,用二次水定容至10 mL,搖勻,于50 ℃水浴中反應60 min后, 以不加H2O2的溶液為試劑空白, 用1 cm石英比色皿,在熒光光度計上于激發波長330 nm、發射波長456 nm處測定加有過氧化氫溶液的熒光強度F和試劑空白的熒光強度F0,并計算熒光差值ΔF=F-F0。
2結果與討論
2.1體系的熒光光譜
圖1為不同體系的熒光光譜:由曲線c可知香豆素本身的熒光強度很弱;由曲線a可知Hb本身沒有熒光;由曲線c和d可知,當無Hb存在時, H2O2可以氧化香豆素, 但反應進行很慢; 由曲線b和c可知, 體系在456 nm處的熒光強度基本不變, 所以香豆素與Hb基本不反應; 由曲線e可知, Hb對H2O2氧化香豆素的反應具有催化作用, 香豆素-H2O2-Hb體系的熒光強度明顯增強, 最大發射波長為456 nm, 最大激發波長為330 nm。
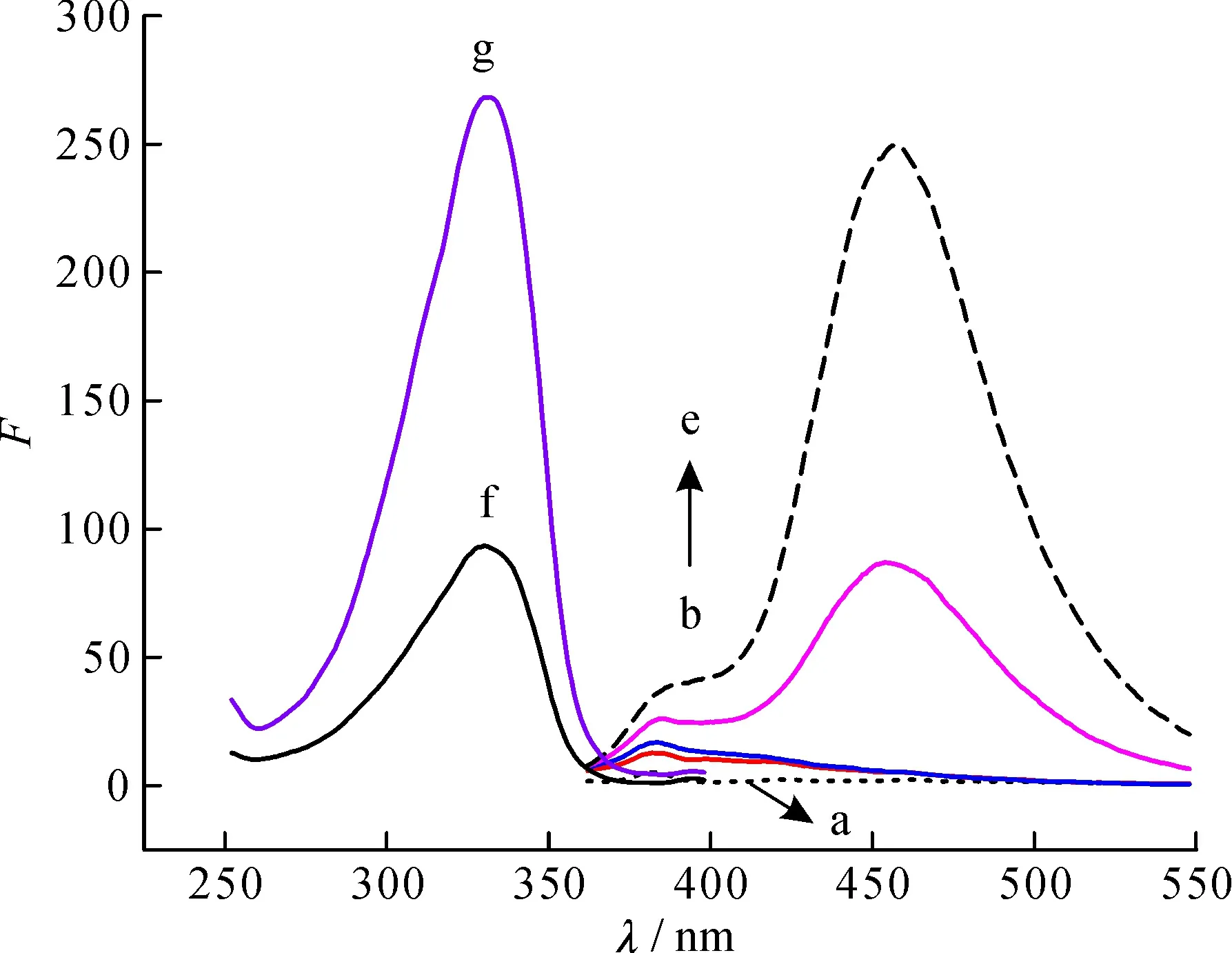
圖1 體系的熒光光譜Fig.1 Fluorescence spectra of the system 發射光譜:a—Hb; b—香豆素+Hb; c—香豆素; d—香豆素+H2O2; e—香豆素+H2O2+Hb;激發光譜:f—香豆素+H2O2; g—香豆素+H2O2+Hb
2.2實驗條件優化
2.2.1緩沖溶液的選擇比較了不同pH值的NaOH-H2SO4、HAc-NaAc和B-R 3種緩沖液對體系ΔF值的影響。由實驗結果可知,在pH 3.5的NaOH-H2SO4緩沖液中,ΔF值最大,反應的靈敏度最高。所以選擇pH 3.5的NaOH-H2SO4緩沖液為反應介質。對NaOH-H2SO4緩沖液的用量進行了考察,結果表明:當緩沖液用量為0~2.5 mL時,體系的ΔF值隨緩沖液用量的增加而逐漸增大;當用量大于2.5 mL時,體系的ΔF值達到最大并基本趨于穩定,故實驗選擇加入pH 3.5的NaOH-H2SO4緩沖溶液3.0 mL。
2.2.2溫度的選擇由溫度對反應ΔF值的影響可知, 在12~45 ℃,體系的ΔF值隨溫度的升高而增大, 當溫度大于45 ℃后(45~60 ℃), ΔF值達到最大并穩定。因為Hb是一種蛋白質,所以溫度過高易使Hb失活,也易使H2O2分解,因此選擇在50 ℃進行反應。
2.2.3酶催化時間的選擇研究了酶催化時間對反應體系ΔF值的影響:在10~50 min,體系的ΔF值隨時間的增加而增大,當反應時間為50 min時,ΔF值達到最大,繼續延長反應時間ΔF值保持穩定,所以選擇反應進行60 min時進行測定。
2.2.4香豆素用量實驗表明:當香豆素的用量在0.5~1.8 mL之間時,ΔF值隨香豆素用量的增加而增大;用量大于1.8 mL后,體系的ΔF值隨著香豆素用量的增加而減小,所以選擇ΔF值最大時所對應的香豆素用量1.8 mL。
2.2.5Hb用量Hb在反應中作催化劑,其用量對體系ΔF值的影響較明顯。當Hb用量為1.0 mL時,催化效果最明顯,ΔF值達到最大值,所以在反應中加入Hb 1.0 mL。
2.3共存物質的影響
當H2O2濃度為3.94×10-5mol/L、相對誤差≤± 5%時,干擾物質的允許倍數為:Mg2+(2 000);SO42-(1 000); Zn2+(500); K+(200); Al3+(100); Ca2+、 Na+、 Sr2+、 Co2+、 Pb2+、 NH4+、 NO3-、 葡萄糖、 SO32-、 尿素(20); Mn2+(10); Vc、 Ni2+(5); CO32-(2); Cu2+、NO2-、 EDTA(1); C2O42-(0.5); Fe3+(0.05)。
2.4工作曲線及檢出限
在上述選定的實驗條件下,繪制不同濃度H2O2與對應ΔF值的標準曲線。由所得標準曲線可知,H2O2濃度在3.940×10-7~7.880×10-5mol/L范圍內與體系的ΔF值存在良好的線性關系。線性回歸方程為:ΔF=6.094×106c+2.780(c為H2O2的濃度, 單位為mol/L),相關系數r=0.998 5。平行測定13次試劑空白的標準偏差S為0.025 3,由此計算得到檢出限為1.25×10-8mol/L(DL=3S/K)。與已經報道的以牛血紅蛋白為催化劑的相關文獻[14-16]相比,本方法檢出限低、靈敏度高(表1)。
2.5樣品測定
在桂林市雁山區采集新鮮雨水,然后對雨水樣品進行預處理。首先將雨水靜置10 min,然后用濾紙過濾,取濾液進行樣品測定。取雨水樣品1.0 mL按實驗方法進行測定,同時做加標回收實驗(取雨水1.0 mL, 加H2O2標準工作液0.5 mL),結果如表2所示。
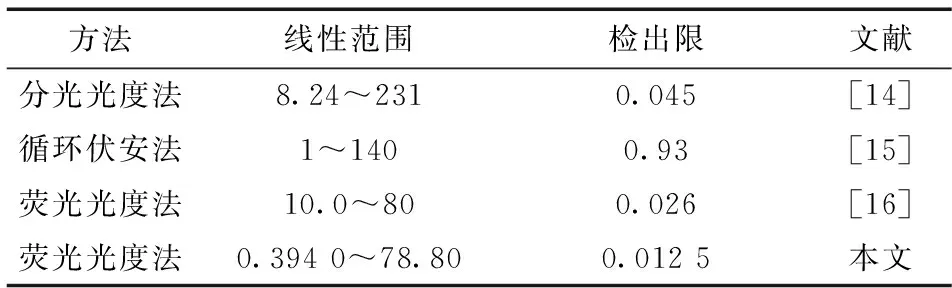
表1 測定H2O2的方法比較Table 1 Comparison of some assays for H2O2 determination μmol/L
另取標示量為3%的醫用雙氧水消毒液(廣東南國藥業有限公司)1 mL,逐級稀釋10 000倍作為待測液。取0.5 mL 待測液按實驗方法進行測定并做加標回收(表2)。

表2 樣品分析結果及回收率(n=5)Table 2 Analytical results of samples and recovery(n=5)
3結論
以牛血紅蛋白為模擬酶,催化H2O2氧化香豆素生成熒光產物7-羥基香豆素,體系的熒光強度增強,據此建立了一種靈敏的測定痕量H2O2的新方法。方法的檢出限為1.25×10-8mol/L,測定H2O2的線性范圍是3.940×10-7~7.880×10-5mol/L。該方法可用于雨水及消毒液中H2O2含量的測定。
參考文獻:
[1]黃佳,常青,江國棟,等. 分光光度法間接快速測定過氧化氫——基于納米α-FeOOH/GO的類似過氧化物酶的催化作用[J]. 理化檢驗: 化學分冊, 2014, 50(4): 417-420.
[2]Luo W, Li Y S, Yuan J, et al. Ultrasensitive fluorometric determination of hydrogen peroxide and glucose by using multiferroic BiFeO3nanoparticles as a catalyst[J]. Talanta, 2010, 81(3): 901-907.
[3]Gao Y, Wang G N, Huang H, et al. Fluorometric method for the determination of hydrogen peroxide and glucose with Fe3O4as catalyst[J]. Talanta, 2011, 85(2): 1075-1080.
[4]Tarvin M, McCord B, Mount K, et al. Analysis of hydrogen peroxide field samples by HPLC/FD and HPLC/ED in DC mode[J]. Forensic Science International, 2011, 209(1): 166-172.
[5]Hu H C, Jin H J, Chai X S. Rapid determination of hydrogen peroxide in pulp bleaching effluents by headspace gas chromatography[J]. Journal of Chromatography A, 2012, 1235:182-184.
[6]Yang C Y, Zhang Z J. Flow injection determination of hydrogen peroxide using diperiodatoargentate- and diperiodatonickelate-luminol chemiluminescence[J]. International Journal of Environmental Analytical Chemistry, 2012, 92(5): 523-533.
[7]Yamashiro N, Uchida S, Satoh Y, et al. Determination of hydrogen peroxide in water by chemiluminescence detection, (I) flow injection type hydrogen peroxide detection system[J]. Journal of Nuclear Science and Technolology, 2004, 41(9): 890-897.
[8]Palanisamy S, Karuppiah C, Chen S M, et al. Direct electrochemistry of myoglobin at silver nanoparticles/myoglobin biocomposite: Application for hydrogen peroxide sensing[J]. Sensors and Actuators B: Chemical, 2014, 202: 177-184.
[9]Wang Y H, Yu C M, Pan Z Q, et al. A gold electrode modified with hemoglobin and the chitosan@Fe3O4nanocomposite particles for direct electrochemistry of hydrogen peroxide[J]. Microchim Acta, 2013, 180(7-8): 659-667.
[10]蔣治良, 湯亞芳,梁愛惠, 等. (Au)核(Ag)殼納米微粒-火焰原子吸收光譜法測定過氧化氫[J]. 光譜學與光譜分析, 2009, 29(7): 1990-1992.
[11]Sang Y, Zhang L, Li Y F, et al. A visual detection of hydrogen peroxide on the basis of Fenton reaction with gold nanoparticles[J]. Analytica Chimica Acta, 2010, 659(1): 224-228.
[12]Ouyang H X,Huang S W, Jiang Z L. Enzyme catalytic resonance scattering spectral detection of trace hydrogen peroxide using guaiacol as substrate[J]. Bulletin Chemical Society of Ethiopia, 2011, 25(2): 161-168.
[13]蘇敬東. 滴定法測定百合干中過氧化氫殘留研究[J]. 甘肅科技縱橫,2011,40(3):56-57.
[14]唐寧莉, 蒙華毅, 李欣, 等. 牛血紅蛋白催化分光光度法測定過氧化氫[J]. 理化檢驗:化學分冊, 2014, 50(2): 191-194.
[15]Xuan J, Jia X D, Jiang L P, et al. Gold nanoparticle-assembled capsules and their application as hydrogen peroxide biosensor based on hemoglobin[J]. Bioelectrochemistry, 2012, 84:32-37.
[16]Xu C L, Zhang Z J. Fluorescence determination of hydrogen peroxide using hemoglobin as a mimetic enzyme of peroxidase[J]. Analytical Sciences, 2001, 17(12): 1449-1451.
文章編號:1674-9057(2016)02-0333-04
doi:10.3969/j.issn.1674-9057.2016.02.023
收稿日期:2015-03-24
基金項目:國家自然科學基金項目( 21165008)
作者簡介:單雅琦(1989— ),女,碩士,分析化學專業。
通訊作者:唐寧莉,教授,ysshiyanshi@163.com。
中圖分類號:O657.3
文獻標志碼:A
Fluorometric determination of hydrogen peroxide by bovine hemoglobin catalytic coumarin system
SHAN Ya-qi, CHEN Yong-ning, ZHANG Rong-hui, TANG Ning-li
(College of Chemistry and Bioengineering,Guilin University of Technology,Guilin 541004,China)
Abstract:In pH 3.5 NaOH-H2SO4 buffer solution, with bovine hemoglobin as catalyst, coumarin was oxidized to produce 7-hydroxycoumarin by hydrogen peroxide, which had strong fluorescence in acid solution. At the length of maximum emission 456 nm, the increased value of fluorescence intensity(ΔF)was linear to the concentration of hydrogen peroxide in the range of 3.940×10-7- 7.880×10-5mol/L, with a correlation coefficient of 0.998 5 and a detection limit of 1.25×10-8mol/L. Based on this, a simple and highly sensitive fluorometric method was proposed for the determination of trace H2O2. This new fluorometric method can be applied to the analysis of H2O2 in rainwater and disinfectant fluid samples with satisfactory results.
Key words:hydrogen peroxide;bovine hemoglobin;coumarin;fluorometry
引文格式:單雅琦,陳永寧,張容琿,等.牛血紅蛋白催化香豆素體系熒光光度法測定過氧化氫[J].桂林理工大學學報,2016,36(2):333-336.

