不同化學(xué)發(fā)光分析系統(tǒng)在皮質(zhì)醇檢測中的性能評價與比較*
陳 翊,李穎能,陳煥輝,林 濤,湯勇才
(1.廣東省廣州市婦女兒童醫(yī)療中心中心實驗室 510120;2.廣東省廣州市第一人民醫(yī)院檢驗科 510180)
?
不同化學(xué)發(fā)光分析系統(tǒng)在皮質(zhì)醇檢測中的性能評價與比較*
陳翊1,李穎能2,陳煥輝1,林濤1,湯勇才2
(1.廣東省廣州市婦女兒童醫(yī)療中心中心實驗室510120;2.廣東省廣州市第一人民醫(yī)院檢驗科510180)
摘要:目的比較貝克曼Access 2 Immunoassay System化學(xué)發(fā)光免疫分析系統(tǒng)及羅氏COBAS E 411電化學(xué)發(fā)光免疫分析系統(tǒng)對皮質(zhì)醇的分析性能與檢測結(jié)果相關(guān)性。方法按照ISO15189中方法評估貝克曼及羅氏分析系統(tǒng)對皮質(zhì)醇檢測的精密度、功能靈敏度、參考范圍、方法學(xué)、陽性符合率、陰性符合率。結(jié)果貝克曼與羅氏分析系統(tǒng)在皮質(zhì)醇檢測中精密度良好,功能靈敏度符合各自廠商設(shè)定的臨床檢測的下限,實驗室自建參考范圍后,將兩分析系統(tǒng)對皮質(zhì)醇的測定值進(jìn)行線性回歸分析,二者間相關(guān)性良好,線性回歸系數(shù)r2=0.977,陽性符合率、陰性符合率均為100%。結(jié)論兩分析系統(tǒng)對于皮質(zhì)醇的分析性能優(yōu)異,均可滿足臨床檢驗需求。經(jīng)過方法學(xué)比對,二者相關(guān)性良好,能夠通過回歸方程對二者間測定值進(jìn)行引證。
關(guān)鍵詞:皮質(zhì)醇;化學(xué)發(fā)光免疫分析;電化學(xué)發(fā)光免疫分析;性能評價
近年來,化學(xué)發(fā)光免疫法越來越多地被應(yīng)用于人體激素的測定,作為一種靈敏度非常高的化學(xué)發(fā)光測定技術(shù)和高特異性免疫反應(yīng)技術(shù)相結(jié)合的新型標(biāo)記免疫測定技術(shù),該方法有著廣闊的應(yīng)用前景。但在實際臨床檢測的應(yīng)用中,不同檢測系統(tǒng)的測定結(jié)果存在差異。如何評估化學(xué)發(fā)光免疫法的測定結(jié)果,推動檢測標(biāo)準(zhǔn)化,并達(dá)到實驗室間的檢驗結(jié)果互認(rèn),尚需進(jìn)一步研究。本課題組以皮質(zhì)醇為對象,通過對現(xiàn)階段化學(xué)發(fā)光免疫法應(yīng)用最廣泛的2種方法(化學(xué)發(fā)光免疫法和電化學(xué)發(fā)光免疫法)進(jìn)行方法學(xué)評價,探討化學(xué)發(fā)光免疫法不同檢測儀器間結(jié)果的相關(guān)性。皮質(zhì)醇是體內(nèi)循環(huán)系統(tǒng)中的一種高豐度甾類化合物,其主要用于血壓維持、抗過敏反應(yīng),以及糖類、蛋白質(zhì)、脂肪的新陳代謝調(diào)節(jié)等[1]。皮質(zhì)醇是一種主要由腎上腺皮質(zhì)合成和分泌的糖皮質(zhì)激素,在促腎上腺皮質(zhì)激素(ACTH)的作用下,腎上腺增加對皮質(zhì)醇的分泌,而高濃度的皮質(zhì)醇會抑制ACTH的合成,從而使皮質(zhì)醇濃度維持恒定[2]。因此,血液中皮質(zhì)醇水平常用于診斷腎上腺相關(guān)疾病,如阿狄森癥和庫欣綜合征等[3-4]。臨床上皮質(zhì)醇的檢驗主要通過免疫法進(jìn)行。其中,化學(xué)發(fā)光免疫法和電化學(xué)發(fā)光免疫法同時具備化學(xué)發(fā)光法靈敏度及免疫法高特異性的優(yōu)點(diǎn),在皮質(zhì)醇的定量測定中應(yīng)用廣泛。本文按照臨床實驗室標(biāo)準(zhǔn)化協(xié)會(CLSI)的EP12-A2文件及ISO15189醫(yī)學(xué)檢驗實驗室認(rèn)可的要求[5-6],對本實驗室貝克曼Access 2 Immunoassay System(化學(xué)發(fā)光免疫法)與羅氏COBAS E 411(電化學(xué)發(fā)光免疫法)檢測系統(tǒng)的皮質(zhì)醇檢測結(jié)果進(jìn)行比對,并對二者結(jié)果進(jìn)行評估,現(xiàn)報道如下。
1資料與方法
1.1一般資料樣本來自廣州市第一人民醫(yī)院2015年3~6月門診、住院患者血清,年齡5~73歲。血清樣本按照相應(yīng)檢測需求進(jìn)行收集,樣本無溶血與脂血,待測血清樣本保存于-20 ℃。
1.2儀器與試劑貝克曼Access 2 Immunoassay System分析儀(化學(xué)發(fā)光免疫法),羅氏COBAS E 411分析儀(電化學(xué)發(fā)光免疫法),皮質(zhì)醇檢測試劑盒、校準(zhǔn)品、質(zhì)控品均為各自儀器配套試劑。
1.3方法
1.3.1樣本檢測所有測試均嚴(yán)格按照相應(yīng)儀器和試劑操作規(guī)程進(jìn)行,保證測試時儀器校準(zhǔn)合格,質(zhì)控在控。
1.3.2精密度試驗收集臨床皮質(zhì)醇樣本,配制成皮質(zhì)醇高、低值兩濃度樣本。將兩樣本當(dāng)日內(nèi)各重復(fù)檢測20次,計算測定值結(jié)果均值、標(biāo)準(zhǔn)偏差及變異系數(shù)(CV),得出批內(nèi)重復(fù)性。將兩樣本每天測定1次,連續(xù)測定20 d,計算測定值結(jié)果均值、標(biāo)準(zhǔn)偏差及CV,得出批間重復(fù)性。
1.3.3功能靈敏度驗證以空白樣本對低值質(zhì)控進(jìn)行稀釋,稀釋最終濃度為各自宣稱檢出限附近(貝克曼0.4 μg/dL和羅氏0.018 μg/dL)。利用兩分析系統(tǒng)分別對上述濃度皮質(zhì)醇樣本進(jìn)行測定,每天測定1次,連續(xù)測定10 d,計算各分析系統(tǒng)對上述樣本測定結(jié)果的均值、標(biāo)準(zhǔn)偏差及CV。
1.3.4參考范圍建立選取120例健康人血清臨床樣本(早晨10:00前取血),分別以貝克曼和羅氏免疫分析儀進(jìn)行檢測,并根據(jù)檢測結(jié)果進(jìn)行參考范圍建立。
1.3.5方法學(xué)比對選取40例能夠均勻覆蓋皮質(zhì)醇檢測范圍的臨床樣本,利用貝克曼Access 2 Immunoassay System分析系統(tǒng)和羅氏COBAS E 411分析系統(tǒng)分別檢測上述樣本,并對兩分析系統(tǒng)的測定值相關(guān)性進(jìn)行比對分析。
1.3.6陰性符合率與陽性符合率結(jié)合實驗室自建的參考范圍及40例臨床樣本的檢測結(jié)果,統(tǒng)計兩分析系統(tǒng)對皮質(zhì)醇檢測的陰性符合率與陽性符合率。
2結(jié)果
2.1精密度評價貝克曼和羅氏分析系統(tǒng)對皮質(zhì)醇測定的精密度通過批內(nèi)精密度和批間精密度呈現(xiàn),見表1。貝克曼和羅氏分析系統(tǒng)對皮質(zhì)醇測定的批間、批內(nèi)CV均小于10%,具備良好的精密度,符合臨床檢驗要求。
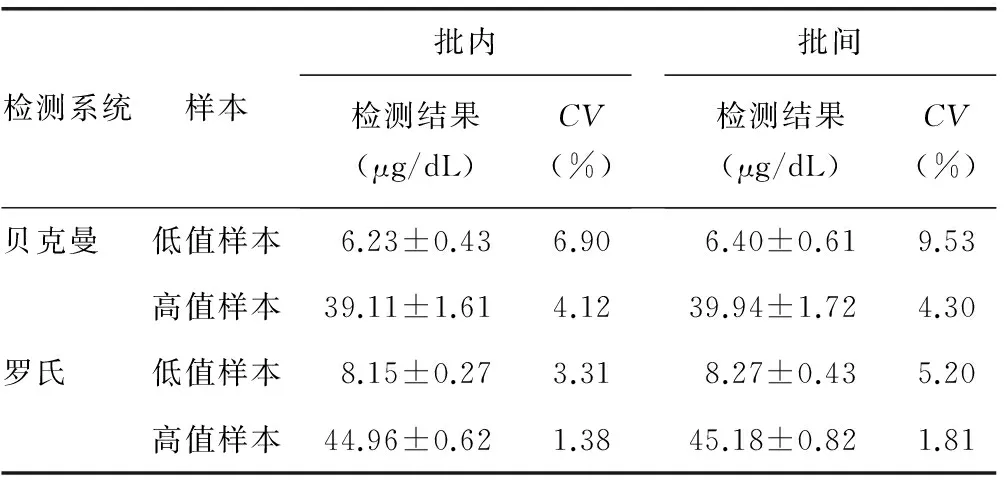
表1 貝克曼和羅氏分析系統(tǒng)檢測皮質(zhì)醇的精密度
2.2功能靈敏度評估本文測定貝克曼與羅氏分析系統(tǒng)在皮質(zhì)醇測定中的功能靈敏度,用于評估二者功能靈敏度的差異。利用皮質(zhì)醇低值質(zhì)控品分別配制檢出限(貝克曼0.4 μg/dL和羅氏0.018 μg/dL)附近的濃度樣本0.50 μg/dL和0.05 μg/dL,以兩分析系統(tǒng)每日分別測定1次,連續(xù)測定10 d。貝克曼分析系統(tǒng)的檢測結(jié)果為(0.55±0.07)μg/dL,CV為12.9%,羅氏分析系統(tǒng)的檢測結(jié)果為(0.052±0.009)μg/dL,CV為17.3%,兩分析系統(tǒng)對于各自宣稱皮質(zhì)醇檢出限附近濃度的樣本檢測結(jié)果CV<20%,表明二者宣稱檢測限能夠作為臨床檢測的下限。
2.3參考范圍確認(rèn)兩分析系統(tǒng)各自的宣稱參考范圍分別為6.7~22.6 μg/dL(貝克曼)和6.2~19.4 μg/dL(羅氏),考慮到本實驗室所處地區(qū)、人群及操作差異,應(yīng)建立實驗室內(nèi)部參考范圍以輔助臨床判斷。根據(jù)C28-A3文件[7],分別采用兩分析系統(tǒng)對120例健康人血清樣本(早晨10:00前取血)進(jìn)行皮質(zhì)醇測定,評估本實驗室內(nèi)各檢測系統(tǒng)的參考范圍,貝克曼與羅氏分析系統(tǒng)說明書建議的參考范圍分別為6.7~22.6、6.2~19.4 μg/dL,本實驗室自建參考范圍分別為6.5~21.3、7.1~24.4 μg/dL。
2.4方法學(xué)比對利用兩分析系統(tǒng)對均勻分布于檢測區(qū)間的40例臨床血清樣本進(jìn)行測試,將測定值結(jié)果進(jìn)行線性回歸,如圖1所示。兩分析系統(tǒng)比對回歸方程為Y=1.08X+1.84(其中X為貝克曼測定值結(jié)果,Y為羅氏測定值結(jié)果),線性回歸系數(shù)r2=0.977。上述結(jié)果表明,二系統(tǒng)測試結(jié)果存在偏差(斜率k=1.08),但二者相關(guān)性良好。利用二分析系統(tǒng)進(jìn)行臨床判斷時,應(yīng)考慮到二者間測定值差異。
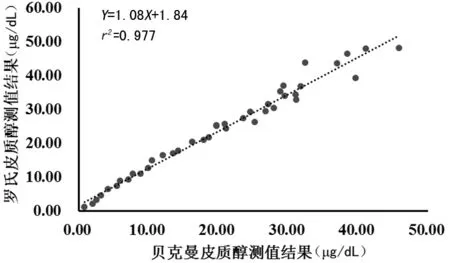
圖1 貝克曼與羅氏分析系統(tǒng)測定皮質(zhì)醇結(jié)果的線性回歸分析
2.5陽性符合率和陰性符合率按照本實驗室自建的臨床參考范圍,對上述40例臨床樣本的測試結(jié)果進(jìn)行陽性符合率和陰性符合率分析,對比分析二者的檢測結(jié)果,確認(rèn)其陰性符合率和陽性符合率均為100%。兩分析系統(tǒng)對皮質(zhì)醇的檢測結(jié)果表明,兩者對臨床判斷的一致性較好。
3討論
化學(xué)發(fā)光免疫法在臨床檢驗中的應(yīng)用日益增多,建立相應(yīng)的評估方法,推動實驗標(biāo)準(zhǔn)化,使檢驗結(jié)果更具溯源性,有著重要的意義。另一方面,根據(jù)CLSI的EP12-A2文件及ISO15189醫(yī)學(xué)檢驗實驗室認(rèn)可的規(guī)定,臨床檢驗科室應(yīng)對分析試劑及配套檢測儀器的主要分析性能(如精密度、功能靈敏度、方法學(xué)、符合率等)進(jìn)行評估,以確保測定值的準(zhǔn)確性。
化學(xué)發(fā)光免疫法和電化學(xué)發(fā)光免疫法結(jié)合發(fā)光系統(tǒng)高靈敏檢測以及免疫法高特異性的優(yōu)點(diǎn),易于實現(xiàn)高通量、自動化分析,且具備優(yōu)異的分析性能,受到臨床檢驗科室的青睞。但在實際工作中,實驗室人員發(fā)現(xiàn)兩者的測定結(jié)果會有差異,如何對結(jié)果進(jìn)行解讀,是本次試驗的出發(fā)點(diǎn)。
本文對實驗室內(nèi)貝克曼Access2ImmunoassaySystem化學(xué)發(fā)光免疫分析系統(tǒng)和羅氏COBASE411電化學(xué)發(fā)光免疫分析系統(tǒng)的皮質(zhì)醇定量檢測分析性能進(jìn)行評估。由于發(fā)光原理的區(qū)別,這兩套檢測系統(tǒng)在試劑、儀器設(shè)計方面均存在顯著區(qū)別,因而二者測定值結(jié)果可能存在系統(tǒng)性差異。試驗結(jié)果表明,兩分析系統(tǒng)均具備良好的精密度,其批間與批內(nèi)CV均小于10%,符合CLSI的EP5-A2標(biāo)準(zhǔn)[8]。兩分析系統(tǒng)的功能靈敏度均滿足皮質(zhì)醇臨床檢測的要求。為了進(jìn)一步比較兩分析系統(tǒng)間測定值準(zhǔn)確性,實驗室自建參考范圍,并對40例臨床樣本進(jìn)行檢測結(jié)果的方法學(xué)比對,以及陽性符合率、陰性符合率分析,數(shù)據(jù)表明兩分析系統(tǒng)對皮質(zhì)醇的檢測結(jié)果相關(guān)性好,線性相關(guān)系數(shù)r2=0.977,測定值略有偏差(線
性回歸方程Y=1.08X+1.84,其中X與Y分別代表貝克曼與羅氏皮質(zhì)醇測定值結(jié)果),但此測定值偏差并不影響臨床判斷,二者的陽性符合率、陰性符合率均為100%。
綜上所述,本次研究遵循ISO15189實驗室認(rèn)可要求,建立了化學(xué)發(fā)光免疫法不同檢測系統(tǒng)間的性能評價方法,應(yīng)用貝克曼和羅氏化學(xué)發(fā)光免疫分析系統(tǒng)對皮質(zhì)醇的分析性能進(jìn)行評估,兩分析系統(tǒng)均滿足臨床檢驗性能要求,并且系統(tǒng)間的測值相關(guān)性良好,但相互引證時需考慮二者間存在的系統(tǒng)性測定值偏差,在臨床判斷時需結(jié)合各自參考范圍進(jìn)行分析。
參考文獻(xiàn)
[1]Foster LB,Dunn RT.Single-antibody technique for radioimmunoassay of cortisol in unextracted serum or plasma[J].Clin Chem,1974,20(3):365-368.
[2]Beisel WR,Diraimondo VC,Chao PY,et al.The influence of plasma protein binding on the extra-adrenal metabolism of cortisol in normal,hyperthyroid and hypothyroid subjects[J].Metabolism,1964,13(10):942-951.
[3]Newell-Price J,Trainer P,Besser M,et al.The diagnosis and differential diagnosis of Cushing′s syndrome and pseudo-Cushing′s states[J].Endocr Rev,1998,19(5):647-672.
[4]Schein RM,Sprung CL,Marcial E,et al.Plasma cortisol levels in patients with septic shock[J].Crit Care Med,1990,18(3):259-263.
[5]CLSI.EP12-A2 User protocol for evaluation of qualitative test performance;Approved guideline[S].2nd ed.Wayne,PA:CLSI,2008.
[6]李金明,申子瑜.正確認(rèn)識臨床實驗室認(rèn)可與提高檢驗質(zhì)量之間的關(guān)系[J].中華檢驗醫(yī)學(xué)雜志,2007,30(2):136-139.
[7]CLSI.C28-A3 Defining,establishing,and verifying reference intervals in the clinical laboratory;Approved guidelines[S].3rd ed.Wayne,PA:CLSI,2008.
[8]CLSI.EP5-A2 Evaluation of precision performance of quantative measurement methods;Approved guideline[S].2nd ed.Wayne,PA:CLSI,2004.
* 基金項目:廣東省廣州市科技計劃項目(2014Y2-00031)。
作者簡介:陳翊,女,副主任檢驗技師,主要從事臨床檢驗研究。
DOI:10.3969/j.issn.1673-4130.2016.14.019
文獻(xiàn)標(biāo)識碼:A
文章編號:1673-4130(2016)14-1949-03
(收稿日期:2016-01-12修回日期:2016-03-18)
Performance evaluation and comparison of different chemiluminescence immunoassay systems in detection of cortisol*
CHENYi1,LIYingneng2,CHENHuanhui1,LINTao1,TANGYongcai2
(1.CentralLaboratory,GuangzhouMunicipalWomenandChildren′sMedicalCenter,Guangzhou,Guangdong510120,China;2.DepartmentofClinicalLaboratory,GuangzhouMunicipalFirstPeople′sHospital,Guangzhou,Guangdong510180,China)
Abstract:ObjectiveTo compare the analytical performance and results correlation of cortisol detection by the Beckman Access 2 Immunoassay System chemiluminescence system and the Roche COBAS E 411 electrochemical luminescence system.MethodsThe precision,functional sensitivity,reference range,positive coincidence rate and negative coincidence rate of both Beckman Access 2 Immunoassay System and Roche COBAS E 411 systems for detecting cortisol were evaluated according to the method of ISO15198.ResultsBoth Beckman Access 2 Immunoassay System and Roche COBAS E 411 system exhibited better precision,the functional sensitivity conformed to the lower limit of clinical detection set by the manufacturers,after establishing the reference range of cortisol by the laboratory,the cortisol values detected by these two systems were performed the linear regression analysis,the results indicated that the correlation between them was good,the linear regression coefficient r2=0.977,and the positive and negative coincidence rates were 100%.ConclusionThe two analytical systems have excellent performance for cortisol,which all meet the clinical detection requirements.The methodological comparison shows good correlation between them,and the detection results could be cited between these two systems by the regression equation.
Key words:cortisol;chemoluminescence;electrochemical luminescence;performance evaluation

