硫鐵礦還原磷石膏反應熱力學分析*
羅蜀峰,付全軍,馬先林,陳 偉,張志業,王辛龍,楊 林,盛 勇(.中化云龍有限公司,云南昆明65504;.中化化肥有限公司成都研發中心;.四川大學化學工程學院)
環境·健康·安全
硫鐵礦還原磷石膏反應熱力學分析*
羅蜀峰1,付全軍2,馬先林1,陳偉2,張志業3,王辛龍3,楊林3,盛勇2
(1.中化云龍有限公司,云南昆明655204;2.中化化肥有限公司成都研發中心;3.四川大學化學工程學院)
采用HSC Chemistry熱力學軟件對硫鐵礦還原磷石膏工藝進行了相關計算,探索了反應分解溫度、不同溫度下物相組成,并與相同條件下的硫鐵礦還原磷石膏實驗結果進行了比較。XRD分析結果表明,硫鐵礦還原分解磷石膏的主要產物為Ca2Fe2O5和CaO,熱力學計算結果與實驗結果一致,表明采用化學熱力學平衡分析方法可作為硫鐵礦還原磷石膏反應特性研究的指導性方法。
磷石膏;硫鐵礦;HSC Chemistry;熱力學分析
磷石膏是濕法磷酸生產過程中采用硫酸與磷礦反應產生的固體廢棄物,其主要成分為CaSO4·xH2O (x=0.5或2),該過程發生的主要反應方程式為[1]:

目前,中國磷肥產量超過世界產量的40%,磷肥行業的快速發展打破了磷肥不足受制于人的不利局面,但副產物磷石膏巨大的產排量,已成為該行業持續發展的主要瓶頸。中國每年的磷石膏產量超過7 500萬t,但綜合利用率不到25%,大量的閑置堆存不僅給企業帶來巨大壓力,同時給周圍環境帶來不利影響[2]。因此,不論從宏觀的戰略發展要求,或是具體到環境保護、企業經濟效益、可持續發展,對磷石膏的綜合處理、綜合利用、變廢為寶是目前最為迫切的任務。
中國擁有非常豐富的硫鐵礦資源,儲量超過20億t[3],且利用價值較高、硫質量分數大于35%的硫鐵礦儲量超過2億t。硫鐵礦作為主要原料生產的硫酸約占整個硫酸總量的40%~50%,但隨著硫磺制酸的大量投產,使得國內硫鐵礦制酸企業面臨巨大挑戰;同時,硫鐵礦制酸副產大量鐵氧化物,由于雜質含量較高,利用率較低,不能為企業創造明顯的經濟效益。因此,硫鐵礦綜合利用成為硫鐵礦行業研究的新方向。
采用硫鐵礦還原磷石膏工藝,利用硫鐵礦中低價態的硫還原磷石膏中高價態的硫,得到的SO2氣體可與氧氣轉化吸收得到硫酸[4]。該工藝不僅利用了硫鐵礦中的硫資源,同時回收了磷石膏中的硫資源,生產得到的硫酸再返回到磷礦萃取工段,實現硫資源循環利用,同時還能副產硫酸。本文采用HSCChemistry熱力學軟件[5],對硫鐵礦還原磷石膏的分解過程進行計算,從熱力學角度對硫鐵礦和磷石膏的分解進行探討,同時對還原過程進行研究,得出硫鐵礦還原磷石膏的最有利條件。
1 計算基礎
HSC熱力學軟件在本文中主要依據的熱力學數據有[6]:、及摩爾等壓熱容與溫度的關系Cp,m=a+bT+cT2。在本文相關計算過程中此軟件的計算依據主要為:
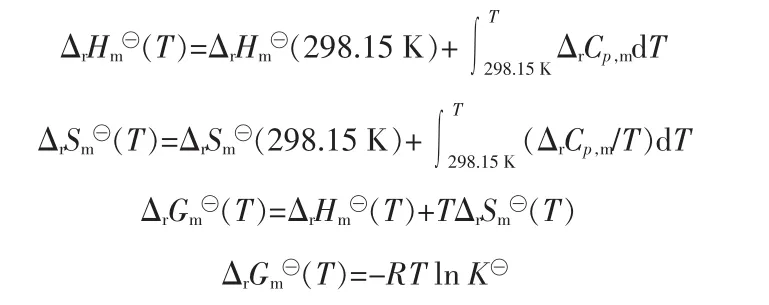
其中:ΔrCp,m=∑νBCp,m(B)
反應系統為敞開系統,在體系反應溫度下,簡化計算過程,同時又能真實描述反應過程熱力學狀態參數,計算時可將氣體視作理想氣體,單位以mol計。無特別注明時反應均在常壓下進行。
2 熱力學計算及分析
本工藝采用硫鐵礦還原磷石膏,其中硫鐵礦中主要成分為FeS2,磷石膏中主要成分為CaSO4,采用的氣氛主要是惰性氣氛N2,反應產生S2和SO2,由于加熱熱源采用煤炭燃燒加熱,且為保證還原性環境,所以還含有一定量的CO2和少量的CO。
該過程中發生的主要反應為原料自身的分解反應和過程中的氧化還原反應[7]。
原料自身可能發生的分解反應:

硫鐵礦自身分解過程中產生的為硫和鐵不同比例的混合物。其中理論計算主要成分為FeS和Fe0.877S,由于兩個物質在該體系下的化學性質相似,故下一步計算主要采用FeS進行計算。
整個反應過程中發生的主要氧化還原反應如下:
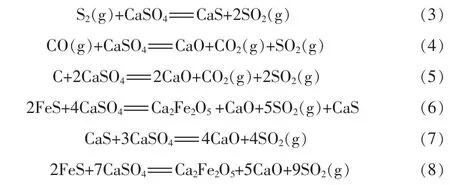
2.1溫度對反應ΔG的影響
圖1中反應1和反應2為判斷硫鐵礦和磷石膏在1 200℃內是否發生分解。通過比較吉布斯自由能與溫度的關系發現,反應1硫鐵礦會發生分解反應,在溫度超過800℃后,硫鐵礦分解產生硫和鐵不同比例的混合物,同時產生硫磺蒸氣;然而硫酸鈣在1 200℃條件內吉布斯自由能恒大于零,在該溫度范圍內性質較為穩定,不會發生分解。

圖1 不同溫度下各反應吉布斯自由能隨溫度的變化曲線
反應3為氣固反應,目前已公開采用S2作為還原劑來還原磷石膏,根據以上計算,其反應的起始分解溫度為880℃,得到的產物分別為硫化鈣固體和SO2氣體。氣相部分直接用于生產硫酸,固相得到的CaS與硫酸鈣繼續發生反應(反應7),氣相可用于生產硫酸,得到CaO渣可代替石灰作為工業原料。
反應4和反應5主要是由于本反應采用煤炭燃燒供熱,在還原性環境中,氣相中會攜帶少量未反應的碳和少量的CO氣體。兩個組分都能與硫酸鈣發生反應,反應起始分解溫度分別為925℃和850℃,得到氧化鈣固體和SO2、CO2氣體。由于在氣相中占比例非常小,不作為主反應考慮。
反應6、7和8為高溫段主要發生的氧化還原反應,其中反應8相當于反應6和反應7疊加之后的總反應,起始分解溫度分別為1 065、1 180、1 115℃。但是比較反應起始分解溫度可以發現,反應8的起始分解溫度為1 115℃,明顯低于反應 7中的1 180℃[8-9]。根據Naoto Mihara等[10]的研究結果發現,硫酸鈣分解過程中若加入一定量的Fe2O3能夠降低硫酸鈣的分解溫度,其原因是由于反應過程中形成了鐵酸鈣共晶混合物,該混合物會降低CaSO4的熔點和分解溫度。
通過以上分析發現,比較硫鐵礦還原磷石膏制備硫酸工藝和硫磺還原磷石膏工藝發現,采用硫磺還原磷石膏的反應起始分解溫度需要達到1 180℃,而本工藝為1 115℃,溫度降低65℃,能夠降低反應能耗,降低生產成本。
2.2不同溫度條件下組分分析
由于硫鐵礦在低溫下會發生分解,故計算FeS2在1 200℃內不同溫度階段的主要存在形式并判斷在該溫度下的穩定性。FeS2在1 200℃內理論分解曲線見圖2。由圖2中的組分含量隨溫度的變化曲線可以得出,FeS2分解的最初產物為 Fe0.877S和硫磺(S2),隨著溫度升高逐漸產生FeS,當溫度超過900℃之后,Fe0.877S會進一步分解形成FeS和S2。以上計算主要說明,溫度在1 200℃以內,硫鐵礦分解產生的Fe0.877S和FeS,在惰性環境中是能夠穩定存在的,且隨著溫度升高Fe0.877S會進一步脫硫形成FeS,故高溫段反應主要采用FeS進行計算。

圖2 FeS2在1 200℃內理論分解曲線
由于S2為氣相,其與硫酸鈣反應為氣固相反應,所需要的條件較為苛刻,在實際生產中,可以忽略反應產生的S2對該反應體系的影響,而計算中S2會參與反應。
反應8作為硫鐵礦還原磷石膏的主反應方程式,根據其中的物料比例設定加入物料的物質的量,計算在不同溫度下的主要組分含量,得到400~1 200℃范圍內的分布圖,見圖3[5]。從圖3不同溫度下的組分分布來看,在400℃之前整個體系不發生反應,隨著溫度升高,硫鐵礦分解產生Fe0.877S、FeS 和S2。當超過800℃之后,首先是S2含量下降,由于其與硫酸鈣反應產生CaS;當達到1 000℃以上時,Fe0.877S、FeS與硫酸鈣發生反應,此階段CaS含量明顯增加,同時開始產生少量的Ca2Fe2O5,反應6的還原過程中既會得到硫化鈣也能得到Ca2Fe2O5的結論得到了證實;超過1 100℃之后,之前產生的CaS含量逐漸降低,說明達到該溫度后CaS與CaSO4發生反應(反應7),得到氣相為SO2,可用于生產硫酸,得到固相為Ca2Fe2O5和CaO的混合物,可作為水泥熟料使用。
2.3理論計算與實際反應實驗結果XRD分析
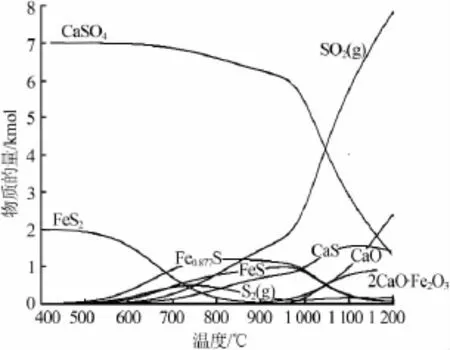
圖3 FeS2與CaSO4反應分解曲線
為了進一步驗證該計算過程與實際反應結論一致,設計兩個實驗證明該計算過程具有一定的可靠性。
設計實驗一:氮氣氣氛中加熱硫鐵礦,研究在800℃下硫鐵礦的分解情況,證明該過程中的分解產物與理論計算結果一致。采用XRD分析反應殘渣的主要組分,得到的主要結果如圖4所示。

圖4 硫鐵礦在N2氣氛中分解殘渣XRD分析譜圖
圖4中XRD分析結果顯示,固體殘渣中主要成分為Fe1-xS,與理論計算中得到的Fe0.877S和FeS產物一致。說明在800℃下,硫鐵礦分解形成的固相產物為Fe1-xS,其中x的值可能為0.123或者0,同時該溫度條件下其比較穩定,不會與磷石膏中的硫酸鈣發生反應,隨著溫度繼續升高,該產物能夠還原磷石膏中的硫酸鈣,實現脫硫過程。
設計實驗二:氮氣氣氛中加熱,按照硫鐵礦與磷石膏理論有效成分的物質的量比[n(FeS2)∶n(CaSO4)]為2∶7進行配料,研究在1 150℃條件下硫鐵礦還原磷石膏的分解情況,證明該過程中的分解產物與理論計算結果一致。采用XRD分析反應殘渣的主要組分[4],得到的主要結果如圖5所示。
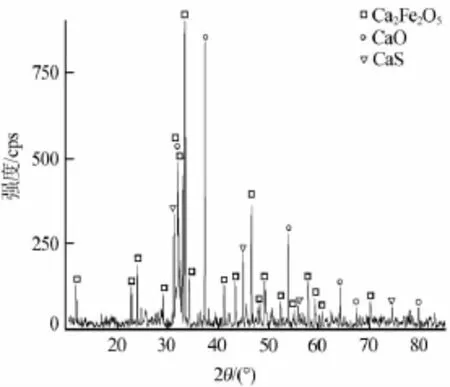
圖5 硫鐵礦在N2氣氛中還原分解磷石膏殘渣XRD分析譜圖
圖5中XRD分析結果顯示,在該溫度條件下反應得到的殘渣主要成分為Ca2Fe2O5、CaO和CaS[10]。由于添加原料硫鐵礦和磷石膏的物質的量比為2∶7,若忽略硫鐵礦分解的硫磺與硫酸鈣發生反應的部分,殘渣中不會存在過量的CaS。根據結果分析,殘渣中的CaS質量分數約為5.0%,經計算可以確定在該反應過程中,硫鐵礦分解產生的硫磺約有10%~15%與硫酸鈣發生氧化還原反應。根據GB 175—2007《通用硅酸鹽水泥》規定,水泥熟料中SO3質量分數需低于3.5%,由于該部分殘渣總S質量分數大于4%,不能作為水泥熟料使用,因此需調整物料比例,提高磷石膏所占比例,降低殘渣中的總S含量。
調整硫鐵礦和磷石膏的物質的量比,提高磷石膏所占比例,其他反應條件與之前一致。經物相分析,得到反應殘渣的XRD譜圖,結果如圖6所示。
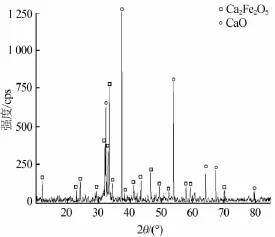
圖6 物料物質的量比調整后還原殘渣XRD分析譜圖
圖6中XRD分析結果顯示,調整物料比例后得到的殘渣經XRD分析后,殘渣中僅檢測到Ca2Fe2O5和CaO兩種物質,說明調整物料比例后,原料中帶入的硫鐵礦正好能夠完全還原磷石膏中的硫酸鈣。為了確定殘渣中含有的硫酸鈣和硫化鈣是否滿足水泥標準,采用化學分析方法確定殘渣中雜質的含量,主要分析結果如表1所示。

表1 硫鐵礦還原磷石膏殘渣化學分析結果 %
根據表1可知,殘渣化學分析結果滿足GB 175—2007規定的w(MgO)≤5.0%,w(SO3)≤3.5%。將其作為水泥熟料添加到水泥中,不會影響水泥的基本性能,同時,特別適用于添加到高鐵水泥中。
3 結論
理論計算與實驗結果的物相組成完全一致,反應溫度達到1 150℃時,產物主要為Ca2Fe2O5和CaO兩種,由于計算過程中計算了S2參與還原反應,故計算結果中CaS含量較高。實際實驗結果中硫鐵礦分解產生的S2僅是部分參與反應,其余部分隨惰性氣氛帶走,考慮該部分參與反應的S2后,調整物料比例得到的殘渣完全滿足水泥熟料要求。
采用硫鐵礦還原磷石膏,不僅解決了磷石膏處理難的問題,同時為硫鐵礦的利用提供了新的方向,得到的SO2氣相直接用于生產硫酸,實現硫資源循環利用,固相殘渣可作為水泥熟料。該工藝無任何三廢排放,是一條既經濟又環保的工藝路線。
[1]Ma Liping,Ning Ping,Zheng Shaocong,et al.Reaction mechanism and kinetic analysis of the decomposition of phosphogypsum via a solid-statereaction[J].Ind.Eng.Chem.Res.,2010,49(8):3597-3602.
[2]王辛龍,張志業,楊守明,等.硫磺分解磷石膏制硫酸技術的研究進展[C]∥第二十二屆全國磷復肥行業年會資料匯編.成都:中國磷復肥工業協會,2015:207-215.
[3]李振飛,文書明,周興龍,等.我國硫鐵礦加工業現狀及硫鐵礦燒渣利用綜述[J].國外金屬礦選礦,2006(6):10-12.
[4]Kutsovskaya M L,Hepworth M T,McGaa J R.Recovery of lime,sulfur,and iron from gypsum and pyrite wastes[J].Ind.Eng.Chem. Res.,1996,35:1736-1746.
[5]Yang Xiushan,Zhang Zhiye,Wang Xinlong,et al.Thermodynamic study of phosphogypsum decomposition by sulfur[J].J.Chem.Thermodynamics,2013,57:39-45.
[6]任雪嬌,夏舉佩,張召述.磷石膏還原分解反應熱力學分析[J].環境工程學報,2013,7(3):1128-1132.
[7]張茜,劉少文,吳元欣.磷石膏制酸新工藝熱力學分析[J].化學工程,2007,35(10):72-74.
[8]Ma Liping,Niu Xuekui,Hou Juan,et al.Reaction mechanism and influence factors analysis for calcium sulfide generation in the process of phosphogypsum decomposition[J].Thermochimica Acta,2011,526:163-168.
[9]肖海平,周俊虎,劉建忠,等.CaSO4與CaS在N2氣氛下反應動力學[J].化工學報,2005,56(7):1322-1326.
[10]Naoto Mihara,Dalibor Kuchar,Yoshihiro Kojima,et al.Reductive decomposition of waste gypsum with SiO2,Al2O3,and Fe2O3additives[J].Journal of Material Cycles and Waste Management,2007,9(1):21-26.
聯系方式:luoshufeng@sinochem.com
Thermodynamic analysis of reductive reaction of phosphogypsum with pyrite
Luo Shufeng1,Fu Quanjun2,Ma Xianlin1,Chen Wei2,Zhang Zhiye3,Wang Xinlong3,Yang Lin3,Sheng Yong2
(1.Sinochem Yunlong Co.,Ltd.,Kunming 655204,China;2.Sinofert Chengdu Research&Development Center;3.College of Chemical Engineering,Sichuan University)
Thermodynamic calculation software HSC Chemistry was used to analyze the reductive reaction of phosphogypsum as a kind of pollution from phosphorus chemical industry with pyrite.The decomposition temperature and phase composition at different temperatures were explored,and the results were compared with that of reductive reaction of phosphogypsum with pyrite.XRD results of the reductive reaction of phosphogypsum showed the products were Ca2Fe2O5and CaO,and it was consistent with analog computation.It concluded that chemical thermodynamic equilibrium analysis could be used to study the reductive reaction characteristics of phosphogypsum with pyrite.
phosphogypsum;pyrite;HSC Chemistry;thermodynamic calculation
TQ132.32
A
1006-4990(2016)04-0057-04
國家高技術研究發展計劃資助項目(863計劃)(No.2011AA06A106)。
2015-10-24
羅蜀峰(1972—),男,碩士研究生,中級工程師,研究方向為磷化工資源綜合利用。

