重度腺病毒肺炎患兒預后不良相關危險因素
鄭申健,胡俊,汪珍珍,付文龍,劉賀臨
(1 武漢科技大學附屬孝感醫院 孝感市中心醫院,湖北 孝感 432000; 2 重慶醫科大學附屬兒童醫院,重慶 401122)
?
·論著·
重度腺病毒肺炎患兒預后不良相關危險因素
鄭申健1,胡俊1,汪珍珍1,付文龍2,劉賀臨1
(1 武漢科技大學附屬孝感醫院 孝感市中心醫院,湖北 孝感432000; 2 重慶醫科大學附屬兒童醫院,重慶401122)
目的了解重度腺病毒肺炎(SAP)患兒預后不良的相關危險因素,為臨床診療及預后判斷提供指導。方法采用回顧性分析方法,對2012年1月—2014年1月重慶醫科大學附屬兒童醫院兒科病房確診的91例SAP住院患兒的臨床資料進行統計分析。結果91例SAP住院患兒,預后不良23例(25.27%)。SAP患兒預后不良危險因素單因素分析結果顯示,發病年齡、患先心病等嚴重基礎疾病、機械通氣治療、發生急性呼吸窘迫綜合癥(ARDS)、有肺不張等嚴重影像學改變、出現2個及2個以上肺外并發癥與SAP預后不良密切相關(均P<0.05)。多因素分析結果顯示:患先心病等嚴重基礎疾病、出現2個及2個以上肺外并發癥是SAP預后不良的獨立危險因素(均P<0.05)。結論患有先心病等嚴重基礎疾病、出現2個及2個以上肺外并發癥是SAP預后不良的獨立危險因素,在臨床診治過程中應積極進行干預,改善預后。
兒童; 重度; 腺病毒肺炎; 預后不良; 危險因素
[Chin J Infect Control,2016,15(8):587-591]
隨著醫療技術水平的提高,病原學檢測手段逐漸增多,越來越多的呼吸道感染性疾病最終可以獲得病原學診斷,給醫務工作者提供了極大的幫助。隨著呼吸道免疫熒光、病毒血清學檢測等技術日趨成熟,小兒腺病毒肺炎確診病例也逐年增加,對重度腺病毒肺炎(severe adenovirus pneumonia, SAP)的認識水平較前明顯提高。對SAP預后不良的患兒進行研究,分析危險因素,以期為疾病的早期診斷、治療、干預,以及降低病死率提供幫助。
1 對象與方法
1.1研究對象選取重慶醫科大學附屬兒童醫院兒科病房2012年1月—2014年1月確診的91例SAP住院患兒。
1.2診斷標準所有患兒入院后均行鼻咽部脫落細胞直接免疫熒光技術測定腺病毒抗原,若抗原陽性,參照第7版《諸福棠實用兒科學》[1]腺病毒肺炎的診斷標準。若同時符合世界衛生組織(WHO)推薦重度、極重度肺炎診斷標準[2]即診斷為重度肺炎和極重度肺炎,標準如下:(1)2個月~5歲兒童出現胸壁吸氣性凹陷或鼻翼扇動或呻吟之一表現者,提示有低氧血癥,診斷為重度肺炎;(2)若出現中心性紫紺、嚴重呼吸窘迫、拒食或脫水征、意識障礙(嗜睡、昏迷、驚厥)之一表現者診斷為極重度肺炎。SAP預后不良判定標準:患兒住院期間內死亡,或因嚴重并發癥、后遺癥患兒家屬要求放棄治療。所有患兒根據病情使用GE Light Speed 64排VCT掃描儀進行胸部CT平掃,且至少1次/人。發生以下1種或1種以上影像學改變即判定為嚴重影像學改變:(1)肺部節段實變;(2) 三葉以上肺葉受累;(3)胸腔積液、胸膜改變;(4)肺不張。
1.3研究方法
1.3.1腺病毒檢測方法標本制作:入院當天專科資深護士用一次性吸痰管插入患兒鼻腔深部7~8 cm 處,到達咽部以下位置,用吸痰管誘導吸取約2 mL分泌物。將分泌物置于10~15 mL離心管中,加入PBS 4~8 mL,置于漩渦振蕩器中震蕩5 min,在離心機中300~500 r/min離心30 min,再次加入PBS 4~8 mL,置入離心機中離心洗滌,取出沉淀物加入0.1~0.2 mL稀釋后的PBS溶液混勻。用微量吸管吸取上述液體約25 μL 滴至7孔玻片;室溫空氣下干燥后用4℃丙酮固定10 min。結果觀察:在制作好的標本上分別加入采用熒光標記的呼吸道合胞病毒,腺病毒,流感病毒A型、B型,副流感病毒I型、II型、III型七項病毒的單克隆抗體試劑(美國Chemicon公司生產),在37℃恒溫箱中放置30 min,取出標本,然后用洗滌液洗片3次,風干后應用封閉液封片,并在熒光顯微鏡(IX-7免疫熒光鏡,日本Olympus公司生產)下讀片。陽性細胞在鏡下可見細胞核和/或細胞漿內呈黃綠色熒光;陰性細胞無熒光,背景為淡藍色(參照試劑盒提供的陽性及陰性對比照片進行判定)。
1.3.2臨床資料采用回顧性調查方法,收集研究對象的臨床資料并填寫調查表,調查內容包括:性別,發病年齡,持續發熱是否超過1周,是否有先天性心臟病、先天性氣道發育異常等嚴重基礎疾病,是否需要機械通氣治療,胸部CT影像學改變,各系統相關并發癥,是否使用糖皮質激素,是否使用丙種球蛋白免疫支持治療,以及最終預后等相關信息。
1.4統計分析應用SPSS 17.0軟件進行統計分析,單因素分析計數資料用率表示,并采用χ2檢驗;多因素分析采用二分類的logistic分析,P≤0.05 為差異有統計學意義。
2 結果
2.1一般情況共收集91例SAP患兒,其中男性52例(57.14%),女性39例(42.86%);患兒年齡2個月~5歲,平均年齡(2.1±0.2)歲,其中2個月~1歲患兒56例(61.54%),1~5歲患兒35例(38.46%);有先天性心臟病(先心病)等嚴重基礎疾病患兒31例(34.07%),機械通氣患兒82例(90.11%),使用丙種球蛋白患兒84例(92.31%),使用腎上腺糖皮質激素患兒78例(85.71%),預后不良患兒23例(25.27%)。
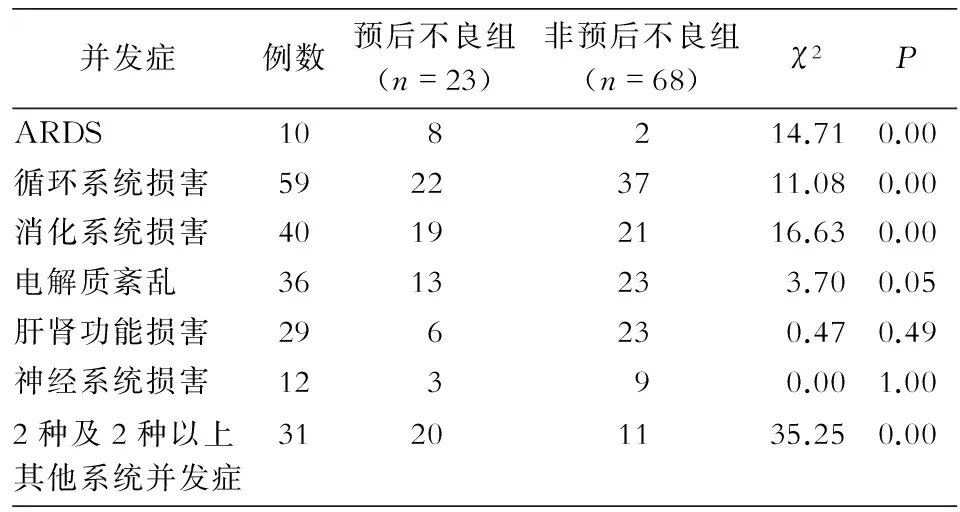
2.2并發癥所有研究對象均出現肺內并發癥,其中出現急性呼吸窘迫綜合征(ARDS)10例(10.99%);循環系統并發癥主要為:心肌損害、心力衰竭、心律失常,共59例(64.84%);消化系統并發癥主要為:腹瀉、消化道出血,共40例(43.96%);電解質紊亂并發癥為:高鈉血癥、低鈉血癥、高鉀血癥和低鉀血癥,共36例(39.56%);神經系統并發癥主要為:熱性驚厥、中毒性腦病和病毒性腦炎,共12例(13.19%);肝腎功能損害并發癥共29例(31.87%);其中有2種及2種以上肺外并發癥者31例(34.07%)。見表1。
表1預后不良與非預后不良組患兒并發癥比較
Table 1Comparison of complications between poor prognosis group and non-poor prognosis group
并發癥例數預后不良組(n=23)非預后不良組(n=68)χ2PARDS108214.710.00循環系統損害59223711.080.00消化系統損害40192116.630.00電解質紊亂3613233.700.05肝腎功能損害296230.470.49神經系統損害12390.001.002種及2種以上其他系統并發癥31201135.250.00
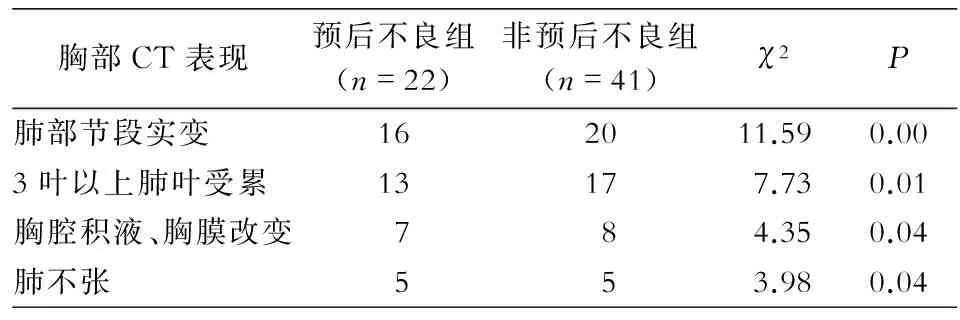
2.3影像學63例SAP患兒共計出現91例次嚴重肺部影像學改變,其中預后不良組22例出現41例次,非預后不良組41例出現50例次。嚴重影像學改變包括肺部節段實變36例次,三葉以上肺葉受累30例次,胸腔積液、胸膜改變15例次,肺不張10例次。詳見表2。
表2 預后不良組與非預后不良組影像學改變比較(例次)
Table 2Comparison of radiological changes between poor prognosis group and non-poor prognosis group (No. of cases)
胸部CT表現預后不良組(n=22)非預后不良組(n=41)χ2P肺部節段實變162011.590.003葉以上肺葉受累13177.730.01胸腔積液、胸膜改變784.350.04肺不張553.980.04
2.4單因素分析結果顯示,發病年齡、患先心病等嚴重基礎疾病、機械通氣治療、發生ARDS、有肺不張等嚴重影像學改變、出現2個及2個以上肺外并發癥與SAP預后不良相關(均P<0.05)。見表3。
2.5多因素分析結果顯示:患先心病等嚴重基礎疾病、出現2個及2個以上肺外并發癥是SAP預后不良的獨立危險因素(均P<0.05)。見表4。

表3 SAP患兒預后不良的發生率及危險因素單因素分析

表4 SAP患兒預后不良相關危險因素的logistic回歸分析
3 討論
腺病毒是一種無外殼的雙鏈DNA病毒,能感染人的腺病毒有A—G共7個組,其中最常見的致病型為1~8型,其中4型及7型最容易出現重癥。腺病毒主要通過空氣飛沫傳播,嬰幼兒、老年人,以及免疫力功能低下者較易感染并容易發展為重度肺炎,嚴重時危及生命[3]。不同地區腺病毒肺炎感染率存在較大區別。徐雷等[4]研究報道,齊魯地區腺病毒肺炎在住院肺炎患兒中約占10%,而在重癥肺炎患兒中占11.9%;余春梅等[5]研究表明,重慶地區SAP在嬰幼兒重癥肺炎中占19.3%;而北京兒童醫院劉秀云等[6]報道腺病毒引起嬰兒重癥肺炎的比率高達32.2%,是目前所知的報道比率最高的地區。以上資料均表明腺病毒肺炎在嬰幼兒肺炎中占據較高比例,尤其是嬰幼兒重癥肺炎。
目前,腺病毒檢測技術主要有病毒分類培養、聚合酶鏈反應、免疫技術、酶聯免疫吸附測定法,以及其他如基因芯片技術等,其中直接免疫熒光技術被普遍推薦[7],據報道其特異性可達86%,敏感性達95%,而且用時短,設備技術要求較低,在普通基層醫院即可開展[8]。本研究選用直接免疫熒光技術作為腺病毒感染的判定標準,不足之處是未能進行腺病毒分型檢測,未能提供更準確的病原學結果。
本研究嚴格按照WHO重度肺炎診斷標準選取2個月~5歲兒童作為研究對象,其平均年齡為(2.1±0.2)歲,參照劉愛良等[9]研究分析的結論,選取1歲作為分界點,單因素χ2檢驗分析提示,年齡≤1歲與發生SAP預后不良密切相關(P<0.05)。考慮原因有:≤1歲的嬰兒吞噬細胞(主要為中性粒細胞)功能發育不完善,加上自身的解剖結構,如皮膚、黏膜發育不成熟,保護能力較弱,容易成為病毒侵犯的對象;其次,≤1歲嬰兒時期,淋巴細胞的功能發育不成熟,病毒感染后產生特異性抗體均較低下,自6個月以后隨著年齡增大來自母體提供的IgG水平降低,此階段抵抗力較低,清除病毒的能力也較差,一旦有外來病原菌入侵,就容易出現重癥表現[1];再者,1歲左右嬰幼兒正處于對外界環境的適應期,此階段嬰兒正處于學步或剛剛能夠獨立行走狀態,對外面陌生世界充滿好奇,會經常主動要求出入廣場、超市等人口密集場所,接觸病原菌的機會也較多,而腺病毒主要傳播途徑即是通過飛沫、空氣傳播,所以此年齡段嬰幼兒容易發生感染。因此,我們應盡量減少≤1歲嬰幼兒到人口密集、空氣不流通的公共場所的機會,盡可能地切斷腺病毒感染的傳播途徑,降低感染率。
先天性心臟病是兒童最常見的一種先天性發育異常疾病,年齡越小發病率越高,并且未經治療的各種先心病嬰兒中約60%于1歲內死亡[1]。先天性氣道發育異常,如氣管軟化、狹窄等疾病,隨著影像學技術和纖維支氣管鏡的成熟應用,也越來越常見。本組91例SAP患兒中,有31例(34.07%)患兒合并有先天性心臟病和先天性氣管發育異常,其中15例(48.39%)最終出現預后不良。統計分析顯示,患嚴重基礎疾病是SAP預后不良的一個獨立危險因素,與杜芳等[10]研究結論吻合。先心病患兒,尤其是左向右分流的先心病患兒,可能長期存在慢性心功能不全,在發生肺部感染時,心肺負荷增加,極易出現呼吸衰竭、心力衰竭,而最終死亡。所以,當有先心病等嚴重基礎疾病的患兒發生SAP時,我們應提高警惕,嚴密觀察疾病的進展,在積極救治的同時,時刻與家屬做好溝通工作,謹防預后不良事件的發生。
ARDS是一種具有復雜病理和發病機制的異質性綜合征,是急性肺損傷的嚴重階段,其主要病理生理變化過程包括肺泡毛細血管通透性增加、肺順應性降低、通氣/血流比失調、肺內分流增加等階段,最后可導致臨床上頑固的低氧血癥,甚至通過機械通氣輔助呼吸也難以糾正。兒童ARDS的病死率與當前各地的兒科重癥監護病房(PICU)技術水平密切相關。據統計,最高住院病死率可達80%以上[11],ARDS的出現也經常預示著預后不良。本研究中,發生ARDS者10例(10.99%),其中8例最終出現預后不良。單因素χ2檢驗分析結果顯示,ARDS與重度SAP預后不良密切相關。我們應高度重視SAP患兒呼吸系統自身的病情進展,時刻監測血氣分析,警惕ARDS的發生。一旦有呼吸衰竭表現,即應早期評估,及時行機械通氣治療,盡早糾正低氧血癥,阻止疾病進展。早期干預可以改善預后并提高存活率,最大限度地減少多器官功能衰竭、死亡的發生[12]。
本研究結果提示,患有2種及2種以上肺外并發癥也是預后不良的獨立危險因素。重癥SAP除引起呼吸系統本身的損害外,還可以引起循環系統、消化系統等較為常見的肺外并發癥。SAP患兒發生多系統并發癥可能與患兒自身免疫功能及臟器功能發育不完善相關,同時出現多系統并發癥也常預示著病毒血癥的發生。腺病毒既可造成細胞溶解性感染,使感染細胞發生溶解、壞死,功能完全喪失;也可發生細胞轉化性感染,使細胞的增生能力大大增強,功能受到損害;甚至有可能導致病毒核酸與細胞基因組DNA的整合,干擾細胞的正常基因表達或通過其他機制破壞細胞增殖的調控而形成腫瘤[1]。上述發病機制決定了SAP容易導致最終的預后不良。
本組91例SAP患兒,82例(90.11%)使用過機械通氣進行治療,考慮與SAP患兒呼吸系統本身損害嚴重相關。影像學顯示,39.56%的SAP患兒出現肺部的節段實變,32.97%的SAP患兒可出現三葉以上肺葉受累,嚴重的影像學改變預示著大部分患兒需要進行機械通氣的輔助治療。單因素分析結果顯示,機械通氣與SAP預后不良相關,機械通氣的正確使用很大程度上影響著SAP的預后。因此,醫務工作者應不停學習,不斷摸索,掌握最新的理念與技術,如機械通氣的使用時機、小潮氣通氣量肺保護策略、允許性高碳酸血癥策略等,保持與時俱進,最大限度地降低SAP預后不良的發生率。
本組SAP患兒常規行高分辨率胸部CT檢查,至少1人次/例,根據嚴重影像學判斷標準確定影像學改變,結果顯示,嚴重的影像學改變與SAP預后不良密切相關。其中肺部節段實變、三葉以上肺葉受累最為常見,約占所有SAP的72.53%,可見SAP患兒肺部損害的嚴重性及多態性。嚴重影像學改變考慮可能與腺病毒感染肺炎的發病機制有關:腺病毒肺炎在肺泡上可出現肺泡出血性肺水腫,導致氣道狹窄,分泌物增多,而嬰幼兒咳嗽反射較弱,無法及時排出氣道分泌物。當病變累及細支氣管、支氣管時即可形成肺部節段性實變、肺不張等病理改變。及時的胸部CT檢查,不僅可以盡早了解疾病的嚴重程度,同時對后期并發癥的隨訪也有著重要價值[13]。
總之,有較嚴重先心病等基礎疾病、出現2個及2個以上其他系統并發癥是重度SAP預后不良的獨立危險因素,我們應早期判斷,早期干預,以期避免不良后果的發生。
[1]吳瑞平,胡亞美,江載芳.諸福棠實用兒科學[M].7版.北京:人民衛生出版社,2002:1191-1194.
[2]中華醫學會兒科學分會呼吸學組. 兒童社區獲得性肺炎管理指南(2013修訂)(上)[J]. 中華兒科雜志, 2013, 51(10):745-752.
[3]全軍傳染病專業委員會,新突發傳染病中西醫臨床救治課. 腺病毒感染診療指南[J]. 解放軍醫學雜志, 2013, 38(7):529-534.
[4]徐雷, 陳蕾, 王沖,等. 兒童重癥肺炎105例臨床特征及高危因素分析[J]. 齊魯醫學雜志, 2012, 27(3):250-252.
[5]余春梅, 楊錫強, 許峰,等. 重慶地區嬰幼兒重癥肺炎呼吸道病毒病原分析[J]. 中華兒科雜志, 2010, 48(2):143-147.
[6]劉秀云, 江載芳. 小兒重癥社區獲得性肺炎31例病原分析[J]. 中國實用兒科雜志, 2005, 20(12):749-750.
[7]吳迪, 胡宇芳, 劉瓊,等. 呼吸道感染患兒咽拭子病毒檢測分析[J]. 中國感染控制雜志, 2015, 14(3):166-169.
[8]金玉霞. 呼吸道病毒檢測方法的進展及意義[J]. 中華醫院感染學雜志, 2013, 23(4):959-960.
[9]劉愛良, 黃英, 楊洋,等. 兒童重癥腺病毒肺炎213例臨床特征分析[J]. 臨床兒科雜志, 2013,31(8):726-729.
[10] 杜芳, 黃英, 舒暢,等. 小兒重癥腺病毒肺炎混合感染及高危因素分析[J]. 中國當代兒科雜志, 2013, 15(5):375-378.
[11] 牛志民, 李艷紅, 姜舜杰,等. 兒童急性呼吸窘迫綜合征預后及其影響因素分析[J]. 中國當代兒科雜志, 2011, 13(7):543-546.
[12] Marraro GA, Chen C, Piga MA, et al. Acute respiratory distress syndrome in the pediatric age: an update on advanced treatment[J]. Chin J Contemp Pediatr, 2014,16(5): 437-447.
[13] 劉成軍, 王華華, 李靜,等. 重癥腺病毒肺炎患兒的臨床和胸部影像學特征分析[J]. 華中科技大學學報:醫學版, 2012, 41(3):379-381.
(本文編輯:孟秀娟)
Risk factors for poor prognosis of severe adenovirus pneumonia in children
ZHENGShen-jian1,HUJun1,WANGZhen-zhen1,FUWen-long2,LIUHe-lin1
(1XiaoganHospitalAffiliatedtoWuhanUniversityofScienceandTechnology,TheCentralHospitalofXiaogan,Xiaogan432000,China; 2ChongqingChildren’sHospital,ChongqingMedicalUniversity,Chongqing401122,China)
ObjectiveTo understand the risk factors for poor prognosis of severe adenovirus pneumonia (SAP) in children, and provide guidance for clinical diagnosis and prognosis.MethodsClinical data of 91 hospitalized children who diagnosed with SAP in Chongqing Children’s Hospital of Chongqing Medical University between January 2012 and January 2014 were analyzed retrospectively.ResultsOf 91 SAP children, 23(25.27%)had poor prognosis. Univariate analysis showed that risk factors for poor prognosis of SAP were age of onset, congenital heart disease and other serious underlying diseases, mechanical ventilation therapy, acute respiratory distress syndrome (ARDS), atelectasis and other serious radiological changes, and emergence of two and more extra-pulmonary complications (allP<0.05). Multivariate regression analysis showed that congenital heart disease and other serious underlying diseases, and emergence of two and more extra-pulmonary complications were independent risk factors for poor prognosis of SAP (allP<0.05).ConclusionCongenital heart disease and other serious underlying diseases, emergence of two and more extra-pulmonary complications are independent risk factors for poor prognosis of SAP, active intervention should be conducted during the process of clinical diagnosis and treatment, so as to improve the prognosis.
child; severe; adenovirus pneumonia; poor prognosis; risk factor
2015-09-12
鄭申健(1978-),男(漢族),湖北省廣水市人,主治醫師,主要從事小兒呼吸系統疾病研究。
劉賀臨E-maill:63686503@qq.com
R725.6
A
1671-9638(2016)08-0587-05
DOI:10.3969/j.issn.1671-9638.2016.08.012

