銅與濃、稀硝酸連續反應演示實驗的再改進
葉永謙 張賢金 吳新建
摘要:針對銅與濃、稀硝酸的反應演示實驗存在現象不夠明顯、裝置過于復雜等不足,從藥品和儀器的選擇兩方面進行探索,設計了一套可用于銅與濃、稀硝酸連續反應的演示裝置,并介紹了實驗的步驟和現象。該演示裝置具有構思巧妙、簡約明了、安全環保等特點。
關鍵詞:銅與硝酸;連續反應;藥品和儀器選擇;演示裝置設計;實驗改進
文章編號:1005–6629(2016)7–0060–03 中圖分類號:G633.8 文獻標識碼:B
銅與濃、稀硝酸反應分別生成紅棕色的二氧化氮氣體和無色的一氧化氮氣體,因氣體均有毒性,且硝酸具有腐蝕性,對于該實驗的改進,一般都是從綠色化、微型化方向進行研究。但是,微型化可能由于演示裝置過于微小或者現象不夠明顯,影響觀察的效果;為了做到銅既和濃硝酸反應,又和稀硝酸反應,并保證安全環保,裝置設計往往過于復雜。本改進實驗通過使用固體與多種液體連續反應制備氣體演示裝置,進行銅與濃、稀硝酸的連續反應,使該實驗操作簡單、現象明顯、安全環保。
1 藥品的選擇
由于實驗產生的氮氧化合物氣體需吸收處理,所用到的硝酸具有腐蝕性,為了達到綠色化要求,本實驗除了使用氫氧化鈉溶液吸收氮氧化合物氣體外,還就銅片的規格、數量,硝酸的濃度進行研究。
1.1 銅片的選擇
實驗室的單質銅一般有銅粉、銅箔和銅片三種,前兩種由于反應太快,一般遇到濃硝酸短時間就全部溶解掉,無法再設計與稀硝酸的反應,且實驗難以控制,瞬間產生大量的有毒氣體無法全部處理。因此,本實驗采用長3cm、寬1cm、厚0.2cm的銅片三塊,保證有足夠的量與濃硝酸反應后再與稀硝酸反應,且反應較溫和,產生有毒氣體氣流平穩有利于吸收和處理。
1.2 硝酸濃度的選擇
濃硝酸與銅反應若要觀察到紅棕色的氣體,必須達到一定濃度,但是濃度太高有可能因反應過于劇烈而無法控制造成危險,產生的有毒氣體也無法及時處理。同時,銅片短時間內全部溶解,無法觀察到其與稀硝酸反應的現象;如果硝酸濃度不夠,則無法觀察到紅棕色氣體[1]。經過對照反應,本實驗最終選擇的硝酸濃度在6 mol·L-1左右,有利于控制反應平穩進行并能觀察到明顯現象。
2 儀器的選擇
2.1 可視化、簡約化角度的選擇
化學學科的演示實驗,不僅要為學生提供正確而有說服力的感性知識,還要激發學生學習化學的興趣,培養學生的觀察能力和思維能力,提高科學素養。為了提高演示實驗的效果,設計時必須關注現象的清晰性和操作的簡練性[2],方便教師在幾分鐘內將實驗目的、實驗原理、儀器藥品、操作步驟、實驗結果等講解清楚。因此,為了使學生在演示實驗過程中既“看得清”又“看得懂”,儀器的選擇要滿足現象可視化、裝置簡約化的要求。佃武杰等在“銅與濃、稀硝酸反應微型實驗設計”[3]一文中的裝置(圖1)設計巧妙,能實現銅與濃、稀硝酸反應,但在課堂演示過程中,可視度方面略顯不足。張澤志等在“銅與硝酸反應的實驗創新設計”[4]一文中的裝置(圖2),能明顯對比銅與濃、稀硝酸反應的差別,但裝置設計過于復雜,不利于學生直觀理解實驗過程。基于以上原因,不宜選用注射器、點滴管、小試管等進行儀器設計,將簡單實驗復雜化。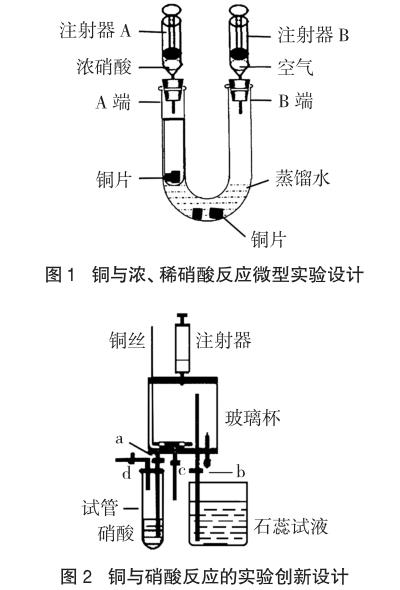
2.2 連續反應角度的選擇
本實驗屬于塊狀固體與液體作用產生難溶性氣體的反應,啟普發生器及其簡易裝置也是選擇的方向之一。但要使銅與濃硝酸反應后繼續與稀硝酸反應,必須在反應一段時間后流出濃硝酸,再注入蒸餾水得到稀硝酸,啟普發生器類裝置無法實
現這個功能。因此,固體與多種液體連續反應制備氣體演示裝置[5]是較為合理的選擇。為了防止反應產生的毒氣吸收不夠完全導致環境污染,在本實驗裝置中改裝后的筒形恒壓漏斗下管口處增加一個倒扣的塑料漏斗,以確保實驗安全。具體實驗裝置如圖3所示。
在上述裝置中,改裝的恒壓漏斗是反應的發生裝置,三角漏斗用于注入濃硝酸和承裝反應后被壓出的液體,n形彎管及外玻璃管用于導出反應產生的氣體,內玻璃管及玻璃活塞1用于控制濃硝酸的流出,玻璃活塞2用于控制氣體的導出,倒扣的塑料漏斗用于防止因氫氧化鈉吸收氮氧氣體不完全而導致毒氣泄漏。
3 實驗步驟與現象
3.1 銅與濃硝酸反應及二氧化氮處理
3.1.1 濃硝酸的配制
往恒壓漏斗中加入銅片后,量取40mL 65%~69%濃硝酸溶解在60mL蒸餾水中稀釋配制成濃度為6 mol·L-1左右的硝酸,從三角漏斗中倒入恒壓漏斗至充滿,關閉彎管玻璃活塞2。
3.1.2 二氧化氮的生成
銅片接觸濃硝酸后,表面立即有氣泡產生,溶液變淺綠色,反應較為緩慢。一段時間后,反應加快,恒壓漏斗上端有紅棕色氣體產生,將溶液壓入三角漏斗中,在液面上滴加適量植物油覆蓋,防止溶液中溶有的二氧化氮氣體逸出。
3.1.3 二氧化氮的吸收
觀察到明顯的紅棕色二氧化氮氣體生成后,打開彎管玻璃活塞2,三角漏斗中的液體下降。控制流速,讓恒壓漏斗中紅棕色氣體形成緩慢氣流全部被氫氧化鈉溶液吸收。
3.2 銅與稀硝酸反應和氮氧化合物氣體處理
3.2.1 稀硝酸的配制
當恒壓漏斗中紅棕色氣體全部被排出后,打開漏斗下方玻璃活塞1,使溶液流出,燒杯中有藍色沉淀生成。溶液流出過程中可能伴有氮氧化合物氣體,由于恒壓漏斗下口浸在氫氧化鈉溶液中且設計有倒扣的漏斗,可以有效吸收該氣體。待溶液流出大約30mL左右,關閉玻璃活塞1,往三角漏斗中加入蒸餾水,打開彎管玻璃活塞2,使蒸餾水順利流入并充滿恒壓漏斗形成濃度為4 mol·L-1左右的稀硝酸。
3.2.2 一氧化氮的生成和檢驗
硝酸被稀釋后,溶液顏色變為淺藍色,銅片表面氣泡繼續產生。一段時間后,恒壓漏斗上部產生無色氣體,并將溶液壓入三角漏斗中。接著,打開玻璃活塞1,使恒壓漏斗中稀硝酸全部流出,隨著空氣的進入,恒壓漏斗中無色氣體立即變為紅棕色。通過以上現象,可以證明銅與稀硝酸反應產生的無色氣體是一氧化氮。
3.2.3 有毒氣體的吸收
當恒壓漏斗中液體全部流出后,關閉玻璃活塞1,打開彎管玻璃活塞2,往三角漏斗中加蒸餾水,將恒壓漏斗中有毒氣體全部排到氫氧化鈉溶液中吸收,實驗完成。
4 設計亮點
通過以上設計,可以明顯地觀察到銅與濃硝酸反應產生紅棕色氣體,與稀硝酸反應產生無色氣體,該無色氣體遇空氣后又變為紅棕色氣體。在有效提高實驗演示的可視化程度的同時,還具有以下亮點。
4.1 構思巧妙
本實驗巧妙地運用濃、稀硝酸產生二氧化氮和一氧化氮的界限進行設計,通過濃硝酸的流出和蒸餾水的加入實現硝酸濃度從6 mol·L-1到4 mol·L-1的變化,從而觀察到明顯的紅棕色氣體和無色氣體,且該無色氣體可再轉化為紅棕色氣體。
4.2 簡約明了
本實驗所用的儀器方便易得,且價格便宜,便于推廣使用。操作步驟簡練,實驗一氣呵成,時間在7分鐘左右,適合課堂上演示,使實驗“看得清”和“看得懂”。
4.3 安全環保
本實驗使用氫氧化鈉處理有毒的氣體,使用大容積外管確保毒氣充分吸收,并使用植物油、倒扣的塑料漏斗防止毒氣外逸。在確保實驗安全的同時,有利于培養學生綠色環保的意識。
參考文獻:
[1]羅宿星,伍遠輝,孫東來.銅與硝酸反應實驗中硝酸濃稀界限的研究[J].實驗室科學,2012,(5):67~69.
[2]沈偉藝.試論如何提高化學課堂演示實驗效果的途徑[J].廈門大學學報(自然科學版),2011,(9):192~194.
[3]張玉征,李先栓.銅與硝酸反應的綠色化設計[J].當代化工,2011,(8):792~797.
[4]張澤志,韓春亮.銅與硝酸反應的實驗創新設計[J].河南教育學院學報(自然科學版),2013,(2):30~31.
[5]葉永謙,張賢金,吳新建,葉燕珠.鋁與水反應演示實驗裝置的設計[J].化學教學,2016,(1):74~76.

