FeM nOx和等離子體對苯的協同降解
陳 睿,王升高,崔麗佳,劉星星,張 維,皮曉強
(武漢工程大學 湖北省等離子體化學與新材料重點實驗室,武漢 430074)
FeM nOx和等離子體對苯的協同降解
陳睿,王升高,崔麗佳,劉星星,張維,皮曉強
(武漢工程大學 湖北省等離子體化學與新材料重點實驗室,武漢430074)
為提高介質阻擋放電對空氣中苯的降解效率,以硫酸錳和過硫酸銨為原料,采用水熱法制備出β-MnO2載體,并用浸漬燒結法制備出FeMnOx復合型催化劑。結合等離子體對模擬空氣中的苯進行了降解研究,分析了β-MnO2和FeMnOx在不同條件下對苯的降解率的影響。結果表明,FeMnOx復合型催化劑與等離子體結合能有效提高模擬空氣中苯的降解率和二氧化碳選擇比;苯的降解率和二氧化碳選擇比隨功率的增加而增加,但隨氣體流速的增加而減少。苯的降解率可達到73.4%,二氧化碳選擇比升至86.5%。
介質阻擋放電;催化;降解
0 引言
苯為揮發性有機化合物[1],在充足陽光下可與氧化劑發生化學反應,產生有毒的光化學煙霧[2]、破壞臭氧層;不僅如此,一旦苯的含量達到一定濃度,通過呼吸道吸入人體,在很短時間內人會產生乏力、頭痛、惡心等癥狀,長期吸入一定量的高濃度苯蒸氣,可損害造血系統和神經系統而發生慢性苯中毒[3]。目前對揮發性有機化合物的降解方法主要有冷凝法、液體吸收法、吸附法、光催化法等[4-11],但這些傳統方法都存在一些缺點。低溫等離子體[12]的電子溫度高于背景氣體溫度,能保證大部分能量被用來產生高能電子、離子和活性自由基,從而促進降解反應的進行。但是,在分解過程中,單一等離子體在放電過程中存在對副產品難以控制,處理不完全等問題[13],調查表明[14-20],采用將低溫等離子體協同不同種類的催化劑的方法,在處理廢氣的時候,其在降低反應能耗跟提高降解率等方面都有著相當不俗的表現[21-22],目前國內外研究者在銅系、錳系、鎳系[23]等催化劑都有相關的研究。
利用硫酸錳和過硫酸銨為基本原料,采用浸漬燒結法制備FeMnOx粉末,比較了β-MnO2和FeMnOx在不同功率和不同氣體流速對苯的降解率的影響,分析了FeMnOx復合催化劑的催化效果。
1 實驗部分
1.1主要實驗試劑
實驗中使用的主要化學試劑如表1所列。
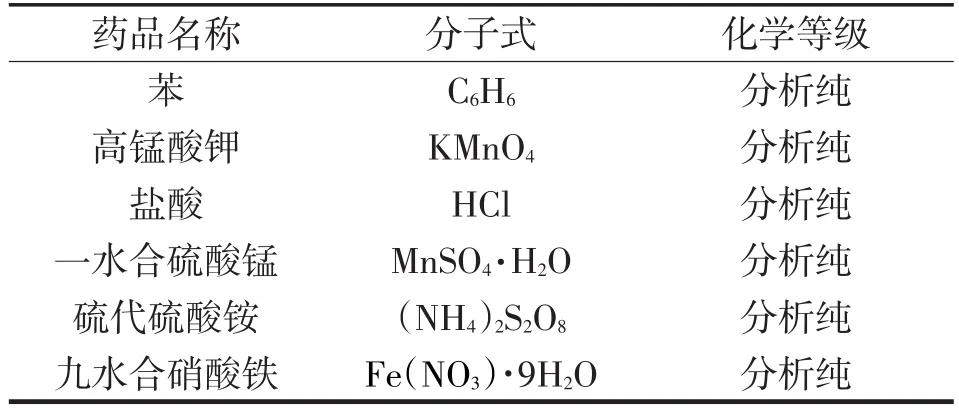
表1 實驗試劑表
1.2主要實驗裝置
實驗中使用的主要實驗裝置如表2所列。

表2 實驗儀器表
1.3β-MnO2的制備
稱取2.7 g MnSO4·H2O、3.7 g(NH4)2S2O8粉末,用40 mL去離子水溶解,磁力攪拌30 min后冷卻至室溫,將溶液轉移至50 mL高壓釜,控制溫度120℃反應48 h后冷卻至室溫。用去離子水過濾洗滌至pH值為7,在真空干燥箱中70℃干燥24 h,得到二氧化錳黑色粉末。
1.4FeMnOx的制備
稱取4.1 g Fe(NO3)·9H2O和2.6 gβ-MnO2,用40 mL去離子水溶解,在90℃下旋轉蒸發,將樣品放入管式爐中并在600℃下焙燒4 h制備出鐵錳復合催化劑。
1.5介質阻擋放電與結合催化劑對苯的降解
實驗裝置[24]由等離子體反應器和分析系統、供氣系統組成。DBD等離子體反應器由具有同心圓結構的雙石英管組成,外層石英管外徑為45 mm,壁厚為2 mm,內石英管外徑為33 mm,壁厚2 mm,采用聚四氟乙烯將雙石英管完全密封。石英管外壁纏有作為放電電極的銅膠紙,放電間隙為5 mm,放電長度為50 mm。最內層直徑6 mm的玻璃管作為催化劑床。
使用的模擬氣體流速為120 mL/min,初始濃度為3 500 mg/L。將所制備的催化劑粉末放入最內層玻璃管中通氣,分別改變功率為20、24、28、32、36 W,測得不同條件下降解后苯的濃度。
1.6苯降解率測量
苯標準溶液的配制:將2 mL分析純苯溶于一定量丙酮中,再把溶液移入100 mL定容瓶中定容。分別將0.1、0.2、0.3、0.4、0.5μL含微量苯的丙酮依次注入氣相色譜儀獲得對應的峰面積,式(1)為色譜峰面積與苯含量的關系。苯降解率的測定通過式(2)進行計算。
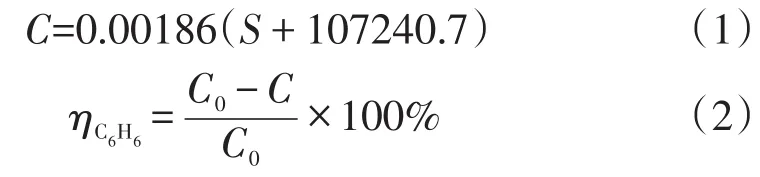
式中:S為檢測樣品的峰面積,C0為苯的起始濃度,mg/L,C為反應后苯的濃度,mg/L,為苯的降解率,%。
以苯的標液量為橫坐標,以峰面積為縱坐標,繪制濃度標準曲線。
1.7碳氧化物的測定
本實驗氣相色譜儀裝配有十通閥和六通閥分析氣體中CO和CO2含量,柱箱溫度為80℃,TCD溫度為80℃。氣體樣品先通過TDX-01填充柱將CO2與其他氣體成分分離并被保留在TDX-01填充柱中,然后其他氣體成分經過5A分子篩填充柱進一步分離,并進入TCD檢測器,而后再切換六通閥使載氣反沖TDX-01填充柱中將CO2帶入TCD檢測器中。通過TCD圖譜中各成分峰面積采用歸一法計算樣品氣體CO和CO2的含量。其計算如式(3):
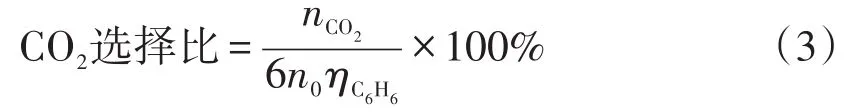
2 結果與討論
圖1為FeMnOx催化劑的XRD圖,通過比對PDF卡片,FeMnOx催化劑中含有兩種晶體,一種是MnO2(JCPDS No.24-0735),另一種是(Mn0.98Fe0.017)2O3(JCPDSNo.24-0507)。說明β-MnO2反應以后得到(Mn0.98Fe0.017)2O3。
圖2為FeMnOx催化劑的SEM照片,由圖可知,粉末的分散性較好,均以納米棒的形式存在,通過氮吸附測得其比表面積為74.5 m2/g,通常來說,催化劑的比表面積越大,催化劑表面的活性基團的分散狀態也就越好,能更好的和氣體分子進行反應。
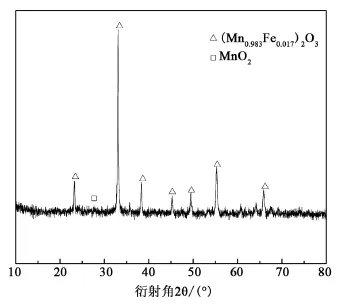
圖1 FeMnOX的衍射圖譜

圖2 FeMnOx的SEM圖
圖3為苯的降解率隨功率的變化。根據Hyun等[25]的理論,隨著功率的增大苯的降解率逐步增加,隨著氣體流速的增大而逐步減小。其主要原因是,當功率增大時,等離子區的電場強度增強,氣體分子運動加劇,分子間作用力增大,苯的降解程度加大;而當流速加快時,氣體分子在放電區域反應的時間相對減少,有機氣體分子與活性粒子間發生碰撞降解程度降低。對比(a)、(b)圖可知,只用單一等離子體對苯的有機氣體進行降解時,苯的降解率為43%~57%;當MnO2和等離子體協同降解時,苯的降解率為60%~70%,可見在MnO2催化劑的作用下,苯的降解率有很大的提高;而(c)中FeMnOx催化降解時,苯的降解率提高到65%~75%。這可能是由于等離子體中活性離子和自由基氣體放電時,一些高能激發粒子向下躍遷產生紫外光,紫外光能更好的激發Fe里面的電子,使電子從價帶躍遷到了導帶,形成具有很強活性的電子空穴對,并誘捕一系列氧化還原反應的進行,提高了對苯的降解率[26-28]。
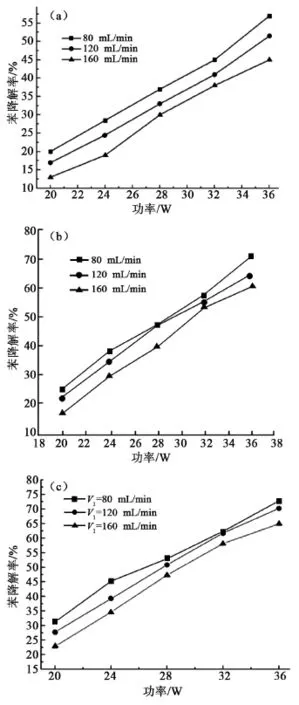
圖3 苯的降解率隨功率的變化曲線圖
圖4為降解產物中CO2的選擇比隨功率的變化,二氧化碳選擇比隨功率的增大而增加,隨氣體流速的增大而減小。其主要原因是,當功率增大時,苯的降解程度加大,降解更完全,一氧化碳轉變成二氧化碳的量增加;而當流速加快時,氣體分子在放電區域反應的時間相對減少,降解程度減弱,反應不完全,一氧化碳的量增加。對比(a)、(b)圖可知,在單一等離子體的處理下,二氧化碳選擇比為38%~55%;在等離子體和MnO2協同催化下,二氧化碳選擇比為45%~75%;而在(c)等離子體和FeMnOx催化降解下,二氧化碳選擇比明顯提高至76%~87%。可能是因為Fe作為金屬粒子,是氧運輸和保存的載體,可以加快活性氧的反應,因此將Fe負載在MnO2上能大大提高氧的存儲能力和釋放轉換能力,同時氧的活性也得以提高,增加了對二氧化碳的選擇性[29-30]。
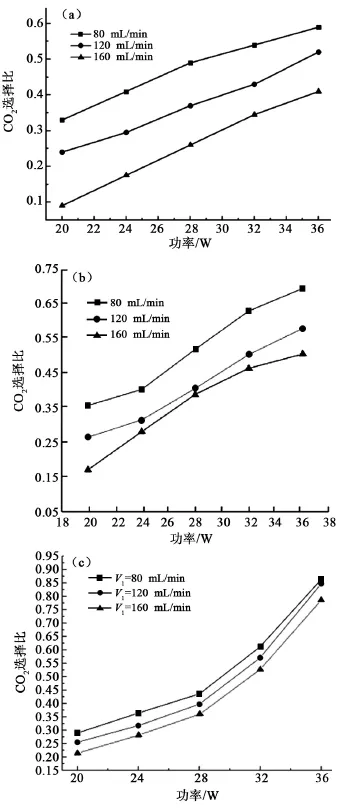
圖4 降解產物中CO2的選擇比隨功率的變化曲線圖
3 結論
利用硫酸錳和過硫酸銨反應,成功制備出β-MnO2,采用浸漬燒結制備鐵錳氧化物催化劑,結合DBD對含苯的有機廢氣進行降解分析發現,苯的降解率和二氧化碳選擇比均隨功率的增加而增加,隨氣體流速的增大而減小。
分析發現,利用浸漬燒結生成的(Mn0.98Fe0.017)2O3催化性能比β-MnO2好,對苯的降解率可達到73.4%,二氧化碳選擇比升至86.5%。
[1]DirectiveC.CouncilDirective1999/30/ECof22April1999 relating to limitvalues forsulphurdioxide,nitrogen dioxide and oxidesofnitrogen,particulatematterand lead inambientair[J]. JournaloftheEuropeanCommunities,1999,50(163):41-60.
[2]Duncan BN,Yoshida Y,Olson JR,etal.Application ofOMI observations toa space-based indicatorofNOxand VOC controlson surfaceozone formation[J].Atmospheric Environment,2010,44(18):2213-2223.
[3]趙琳,肖燕,金潤銘.再生障礙性貧血發病機制研究進展[J].中國實用兒科雜志.2011,26(7):545-547.
[4]岑超平,陳定盛,藍如輝,等.吸收法脫除廢氣的實驗研究[J].環境工程,2007,25(6):40-42.
[5]李湘凌,林崗,周元祥,等.復方液吸收法處理低濃度苯類廢氣[J].合肥工業大學學報,2002,25(5):794-796.
[6]閏勇.有機廢氣中VOC的回收方法[J].化工環保,1997,17 (6):332-335.
[7]Khan F I,GhoshalAK.Removalofvolatileorganic compounds from polluted air[J].Journal of loss prevention in the process industries,2000,13(6):527-545.
[8]GhoshalAK,Manjare SD.Selection ofappropriateadsorption technique for recoveryofVOCs:an analysis[J].Journalof Loss prevention in theProcess Industries,2002,15(6):413-421.
[9]曹耀華,楊紹文,金梅,等.納米二氧化鈦降解有機污染物的試驗研究[J].礦產保護與利用,2002(3):37-40.
[10]孫珮石,王潔,吳獻花,等.生物法凈化處理低濃度揮發性有機及惡臭氣體[J].環境工程,2006,24(3):38-41.
[11]劉媛,王鴦鴦,楊威.淺析揮發性有機廢氣治理技術[J].中國環保產業,2012(11):40-43.
[12]李天鳴,閆光緒,郭紹輝.低溫等離子體放電技術應用研究進展[J].石油技術,2014,14(2):59-64.
[13]TangX,Feng F,Ye L,etal.RemovalofdiluteVOCsinairby post-plasma catalysis over Ag-based composite oxide catalysts[J].CatalysisToday,2013,211:39-43.
[14]倪章松,李國強,高超.介質擋板面放電等離子體流動控制研究進展[J].真空與低溫,2014,20(1):9-16.
[15]ChenW M,Qie L,ShaoQG,etal.Controllable Synthesisof Hollow Bipyramidβ-MnO2and Its High Electrochemical Performance for Lithium Storage[J].ACSappliedmaterials& interfaces,2012,4(6):3047-3053.
[16]ZhangDE,XieQ,Chen AM,etal.Fabricationand characterisation ofMnOOH andβ-MnO2nanorodswith rectangular cross-sections[J].Journal of Experimental Nanoscience,2013,8(1):77-83.
[17]Boppana V BR,Jiao F.Nanostructured MnO2:an efficient and robustwateroxidation catalyst[J].ChemicalCommunications,2011,47(31):8973-8975.
[18]LiY,LiD,Li J,etal.Pretreatmentof cyanided tailingsby catalytic ozonation with Mn2+/O3[J].Journalof EnvironmentalSciences,2015,28:14-21.
[19]CastaoM H,Molina R,Moreno S.Cooperative effectof the Co-Mnmixed oxides for the catalytic oxidation ofVOCs:Influenceof the synthesismethod[J].Applied Catalysis AGeneral,2015(492):48-59.
[20]LiY,LiD,Li J,etal.Pretreatmentof cyanided tailings by catalytic ozonation with Mn2+/O3[J].Journalof EnvironmentalSciences,2015,28:14-21.
[21]Vandenbroucke A M,Morent R,De Geyter N,etal.Nonthermal plasmas fornon-catalytic and catalytic VOC abatement[J].Journalofhazardousmaterials,2011,195:30-54.
[22]KirkpatrickM J,Odic E,ZinolaS,etal.Plasmaassisted heterogeneous catalytic oxidation:HCCIDieselengine investigations[J].Applied Catalysis B:Environmental,2012,117: 1-9.
[23]Chen CY,Liu T,Wang H,etal.Removalofhexane by nonthermal plasma and MnO2/γ-Al2O3combination[J].Chinese JournalofCatalysis,2012,33(6):941-951.
[24]王升高,劉翔,孔垂雄,等.介質阻擋放電結合二氧化錳對空氣中苯的降解[J].武漢工程大學學報,2014,36(7): 48-52.
[25]Hyun-Ha H,Seung-Min O,AtsushiO,etal.Decompotion ofgas-phase benzene using plasma-driven catalyst(PDC)reactorpackedwith Ag/TiO2catalyst[J].Applied CatalysisB: Environmental,2005,56(3):213-220.
[26]寧曉宇,陳紅,耿靜,等.低溫等離子體-催化協同空氣凈化技術研究進展[J].科技導報,2009,27(6):97-101.
[27]都基峻,季學李.低溫等離子體處理氣態有機物[J].污染防治技術,2000,13(1):33-34.
[28]陳礪,區瑞錕,嚴宗誠,等.放電等離子體驅動下甲醛的光催化降解豐[J].華南理工大學學報(自然科學版),2011,39(1)68-73.
[29邱作志,葉代啟.放電等離子體驅動光催化降解甲苯研究[J].工業催化,2008,16(6):69-74.
[30]TangW X,Wu X F,Liu G,etal.Preparation ofhierarchical layer-stackingMn-Cecompositeoxide forcatalytic totaloxidationofVOCs[J].JournalofRareEarths,2015,33:62-69.
SYNERGY OFFeM nOXANDPLASMA FOR THEREMOVAL OFBENZENE
CHEN Rui,WANG Sheng-gao,CUILi-jia,LIU Xing-xing,ZHANGWei,PIXiao-qiang
(Provincial Key Laboratory of Plasma Chem istry and Advanced M aterialsof HubeiProvince,Wuhan Instituteof Technology,Wuhan430074,China)
To improve the degradation capability of the dielectric barrier discharge technology on benzene,using sulfateand ammonium persulphateas raw materials,β-MnO2are prepared by hydrothermalmethod,FeMnOx catalystare prepared by impregnationmethod,and used to degrade the benzene in the simulated air combined w ith plasma.The effects of β-MnO2and FeMnOx on the different conditionswas evaluated.The result indicates that the degradation ratio of benzene and the selectivity of carbon dioxide are improved when the plasma degradation andmanganese dioxide catalytic degradation are simultaneously used,the degradation efficiency of benzene and the selectivity of carbon dioxide are both improved w ith the increasing of power,butdecreasew ith the increasing of gas velocity.The degradation ratio of benzene increases to 73.4%and the selectivity of carbon dioxide growsup to 86.5%.
dielectric barrier discharge;catalysis;degradation
O53
A
1006-7086(2016)03-0173-05
10.3969/j.issn.1006-7086.2016.03.011
2016-01-04
國家自然科學基金(No.51272187和No.51442003)、湖北省自然科學基金(No.2013CFA012和No.2015CFB229)及湖北省科技廳(No.2015BAA093)
陳睿,(1993-),男,湖北武漢人,碩士研究生,主要從事等離子體技術與應用。E-mail:2334156911@qq.com。

