Acetobacter sp.馴化選育及固定化生產3-羥基丙酸
李俊,宗紅,諸葛斌*,陸信曜,方慧英,宋健,董卓麗
1(江南大學 生物工程學院,工業生物技術教育部重點實驗室,工業微生物研究中心,江蘇 無錫,214122)2(江南大學 化學與材料工程學院,江蘇 無錫,214122)
?
Acetobactersp.馴化選育及固定化生產3-羥基丙酸
李俊1,宗紅1,諸葛斌1*,陸信曜1,方慧英1,宋健2,董卓麗1
1(江南大學 生物工程學院,工業生物技術教育部重點實驗室,工業微生物研究中心,江蘇 無錫,214122)2(江南大學 化學與材料工程學院,江蘇 無錫,214122)
3-羥基丙酸作為最有價值的平臺化合物之一,其自身及諸多衍生化合物被廣泛應用于材料、紡織、食品工業及生物醫藥領域。利用Acetobactersp. 生物催化1,3-丙二醇(1,3-PDO)合成3-羥基丙酸(3-hydroxypropionic acid,3-HP)的性能,通過梯度增加培養基中1,3-PDO濃度馴化選育Acetobactersp.,有效提高了該菌對底物的耐受性;同時利用固定化細胞的方法提高菌株對底物的耐受性和3-HP轉化率,當包埋材料為30 g/L海藻酸鈉和聚乙烯醇混合物、顆粒粒徑2 mm,添加0.1 mmol/L Fe2+時,固定化細胞表現出最大的催化活性。10 g/L(CDW)固定化細胞可催化70 g/L 1,3-PDO為66.95 g/L 3-HP,催化水平是靜息細胞的1.32倍,且固定化細胞經50 g/L底物循環利用5次后,3-HP摩爾轉化率仍保持80.65%。固定化的醋酸菌類生物催化劑為工業上3-HP的實際生產提供了一種新可能。
馴化;固定化細胞;底物耐受性;3-羥基丙酸;Acetobactersp.
3-羥基丙酸(3-hydroxypropionic acid,3-HP)是乳酸的同分異構體,非手性的結構使其具有更活潑的化學特性[1],作為一種高附加值的新型三碳平臺化合物,3-HP及其諸多高附加值的衍生物在食品、材料、紡織和醫藥等眾多領域被廣泛應用[2-3]。同時3-HP被美國能源部列為當前12種最具開發潛力的生物化工產品之一,位列其中第3位[4]。
目前,高效工業化合成途徑的缺乏是3-HP仍未被規模化生產的主要原因。相比現有的化學合成法,微生物法合成3-HP具有反應條件溫和、副產物少、操作簡便等優點,是當下的研究熱點。其中,生物轉化法過程簡單、轉化率高,是極具潛力的一種3-HP生物合成途徑[5]。已有的報道中,3-HP可由底物丙烯酸經Candidarugose[6],Byssochlamyssp.[7],Rhodococcuserythropolis[8]催化獲得,然而丙烯酸和丙酸類底物本身對功能微生物的生長和活性有抑制作用,為此有必要尋找更多新的催化底物和催化合成路徑。本研究室前期已篩選獲得了1株以1,3-丙二醇(1,3-PDO)為底物高效轉化合成3-HP的菌株Acetobactersp.,該菌株在最適條件下可將10 g/L 1,3-PDO轉化為11.65 g/L 3-HP,摩爾轉化率高達98.4%;然而,當1,3-PDO濃度提高到50 g/L時,菌體受底物抑制明顯,靜息細胞重復催化3次后摩爾轉化率僅為12.4%[9]。因此,提高菌株底物耐受性、消除底物的抑制作用對生物催化法高效合成3-HP具有重要的實際意義。
本研究以Acetobactersp. 為研究對象,通過連續底物脅迫實驗提高菌株對1,3-PDO的耐受性,同時利用固定化細胞技術進一步提高Acetobactersp. 的底物耐受性,并實現可重復利用生產,為工業化合成3-HP提供一種新方法。
1 材料與方法
1.1菌種和試劑
Acetobactersp. 為本研究室篩選獲得;標準品1,3-PDO、3-HP為色譜純,分別購于阿拉丁(上海)有限公司、Tokyo Chemical Industry公司,其他試劑均為分析純。
1.2培養基及培養方法
種子培養基(g/L):甘油12,蔗糖8,蛋白胨10,MgSO4·7H2O 1,KH2PO41。
發酵培養基(g/L):甘油12,蔗糖8,蛋白胨10,MgSO4·7H2O 1,KH2PO41,L-α-丙氨酸1,丙酸1,FeCl2·H2O 0.1 mmol/L。
以φ=5%接種量將活化種子液接種至裝液量為φ=20%的三角瓶液體培養基中,于30 ℃、200 r/min培養24 h。
1.31,3-PDO生長抑制臨界濃度的確定
制備1,3-PDO終質量濃度分別為20、30、40、50、60、70、80 g/L的固體培養基梯度平板,涂布200 μL種子液后置于30 ℃恒溫箱培養48 h,根據生長情況(單菌落個數),確定1,3-PDO對原始菌株的臨界致死濃度。
1.4菌株的馴化
根據確定的臨界濃度制備梯度平板固體培養基。涂布接種原始菌株后,于30 ℃恒溫培養箱中培養3~5 d后,挑取1,3-PDO濃度高一側的單菌體至液體培養基中,再以此菌體重復上述脅迫培養,多次傳代直至某子代菌株的底物耐受性明顯增強。每代菌株均保菌冷藏備用。
1.5固定化細胞的制備
挑取單菌落于50 mL三角瓶中,30 ℃,200 r/min培養6 h。轉接至500 mL三角瓶中,30 ℃,200 r/min培養20 h。將菌液于4 500 r/min離心30 min,小心倒出上清,生理鹽水重懸后于7 000 r/min再次離心30 min,收獲濃縮菌體細胞。與相應包埋材料溶液充分混勻后,混合液通過蠕動泵抽入接有針頭的橡皮管并緩慢逐滴注入0.05 mol/L CaCl2中,形成均一穩定的球狀顆粒。連接不同尺寸的針頭以改變固定化顆粒的粒徑大小。4 ℃靜置備用。
1.6機械強度和染料浸染實驗
單軸抗壓實驗:在相同制備條件下,取不同材料包埋菌體獲得的固定化顆粒3顆,置于兩載玻片之間,在分析天平上逐漸加力增壓直至顆粒球形結構破裂形變,以天平顯示的最大壓力數值為固定化顆粒的機械強度值。
染料浸染實驗:將固定化細胞顆粒置于一定濃度的結晶紫染料中1 min,再取出浸入純水中1 min以除去表面的染料,顯微切片后在10倍物鏡下顯微成像(Optec BK-FL4),以成像像素(px)為單位測量浸染程度。
2組試驗每次樣品均重復10次并取平均值。
1.73-HP生物催化體系
在100 mL三角瓶中,將菌體終濃度為10 g CDW/L固定化顆粒置于含有適量濃度1,3-PDO的20 mL醋酸緩沖液(0.2 mol/L,pH 7.0)中,30 ℃,200 r/min搖床進行生物轉化。精確取樣,HPLC檢測底物和產物的含量。系統總質量差法定量反應體系體積的變化。
3-HP摩爾轉化率:催化生成的產物3-HP與被催化的底物1,3-PDO的摩爾質量百分比。
1.8檢測方法
1,3-PDO、3-HP的檢測均采用高效液相色譜(Dionex Summit P680)法,色譜柱Bio-Rad Aminex HPX-87H,色譜分析條件:流動相5 mmol/L H2SO4,流速0.6 mL/min,柱溫60 ℃,進樣量10 μL,紫外波長210 nm,示差檢測器溫度35 ℃,采用外標法定量。
2 材料與方法
2.1Acetobactersp. 耐1,3-PDO馴化
按照1.3的實驗方法確定了1,3-PDO抑制Acetobactersp. 生長的臨界濃度為50 g/L,并在此臨界濃度下,經過連續9輪次的脅迫培養獲得了馴化菌株。同條件下培養48 h后,原始菌株和馴化菌株在相同的梯度平板上生長狀況如圖1所示。1,3-PDO濃度隨箭頭方向由零遞增至100 g/L,馴化菌株在超過臨界濃度的平板上仍能夠良好生長,表明其底物耐受性得到提升,能在后續的實際催化應用中耐受更高濃度的1,3-PDO。
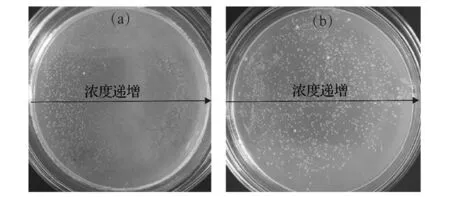
圖1 原始菌株(a)和馴化菌株(b)在梯度平板上的生長Fig.1 Growth conditions of original strain(a) and tamed strain(b) on gradient plate
利用原始菌株與馴化菌株的靜息細胞進行了催化性能對比實驗,結果如圖2所示。
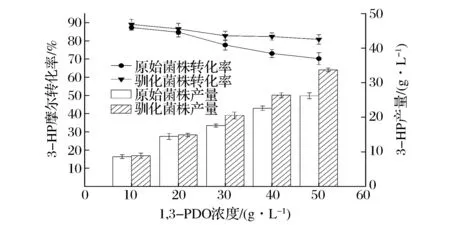
圖2 原始菌株與馴化菌株的催化性能Fig.2 Biocatalytic properties of original strain and tamed strain
當1,3-PDO質量濃度為10~20 g/L時,原始菌株和馴化菌株催化性能相當。但是隨著1,3-PDO濃度的逐漸增加,原始菌株的3-HP產量和轉化率均低于馴化菌株。當底物質量濃度達到50 g/L時,馴化菌株的3-HP產量可達33.7 g/L,而原始菌株的產量僅為26.9 g/L。綜上,通過菌株的馴化培養不僅提升了Acetobactersp. 的自身底物耐受性,3-HP催化性能也有所提升,馴化菌株更適用于高濃度1,3-PDO時的轉化生產。
2.2細胞固定化
2.2.1包埋材料
分別以終質量濃度均為30 g/L的海藻酸鈉(SA)、聚乙烯醇(PVA)及兩者的混合物(SA+PVA)為包埋材料,制備固定化顆粒并考察各自催化性能。結果如圖3所示,單一材料SA制備的固定化顆粒其染料浸染程度值為170 px,較PVA高28.57%,表明SA優于PVA的傳質能力;而由PVA包埋的菌體顆粒機械強度則比SA高16.31%。固定化顆粒良好的傳質性能有利于催化的進行,這與SA組的3-HP摩爾轉化率達到最高值86.70%相符合。此外,利用兩種材料的混合物包埋Acetobactersp. 時,雖然其3-HP摩爾轉化率比單一材料SA略有降低,但混合材料較SA和PVA的機械強度有了明顯提高(分別提高51.49%和30.24%),染料浸染程度也比單一材料分別提高11.84%和43.80%,因此,我們選擇終質量濃度為30 g/L的SA和PVA混合物作為Acetobactersp. 的包埋材料。
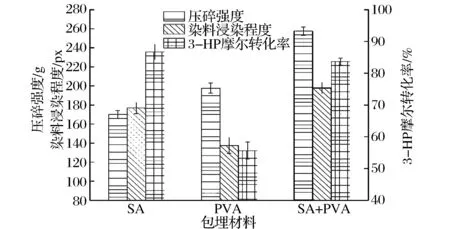
圖3 不同包埋材料制備固定化細胞的物理性能和生物催化效率Fig.3 Physical properties and bioconversion efficiency of immobilized cells in different embedding materials
2.2.2金屬離子
如圖4(a)所示,催化體系中添加0.1 mmol/L Ca2+,Mg2+,Fe2+分別使固定化細胞的3-HP摩爾轉化率增加了7.0%,5.2%和8.0%,而添加EDTA則使3-HP摩爾轉化率降低36.8%。主導1,3-PDO氧化反應的功能酶為Acetobactersp. 細胞質膜上的PQQ依賴型醇脫氫酶(PQQ-ADHs)[10],已有研究表明,這些脫氫酶中的Ca2+或Mg2+是核心組分之一,能夠與PQQ活性位點結合,在脫氫酶結構成形中起到重要作用[11]。此外,PQQ自身的組成亞基就含有[2Fe-2S]簇和細胞色素c等必需成分[12-13],因此添加Fe2+對這一催化過程有利。而EDTA則會引起金屬螯合效應,明顯地抑制了Acetobactersp. 的3-HP生物合成性能,這也從側面驗證了上述金屬離子在此催化過程中的重要性。
2.2.3粒徑大小
不同粒徑大小的固定化顆粒的催化性能結果如圖4(b)所示,3-HP的轉化率隨著顆粒直徑的增加而逐漸降低,顆粒直徑為1 mm 時轉化率最高,為86.4%;而顆粒直徑為5 mm時,3-HP轉化率降低13.4%。這可能與Acetobactersp. 作為生物催化劑氧化1,3-PDO屬于嚴格好氧過程有關,O2在這一過程作為最終電子受體是影響反應的關鍵因素,接受來自膜上脫氫酶氧化呼吸鏈的電子,與H+結合生成水,完成3-HP的合成[14]。然而,球形顆粒的比表面積與其粒徑成反比,粒徑的減小顯然有利于O2和物質的傳遞,從而促進固定化細胞更高效的生物催化。另外,考慮到固定化顆粒制備的難度,我們選擇2 mm為后續實驗的最適粒徑大小。
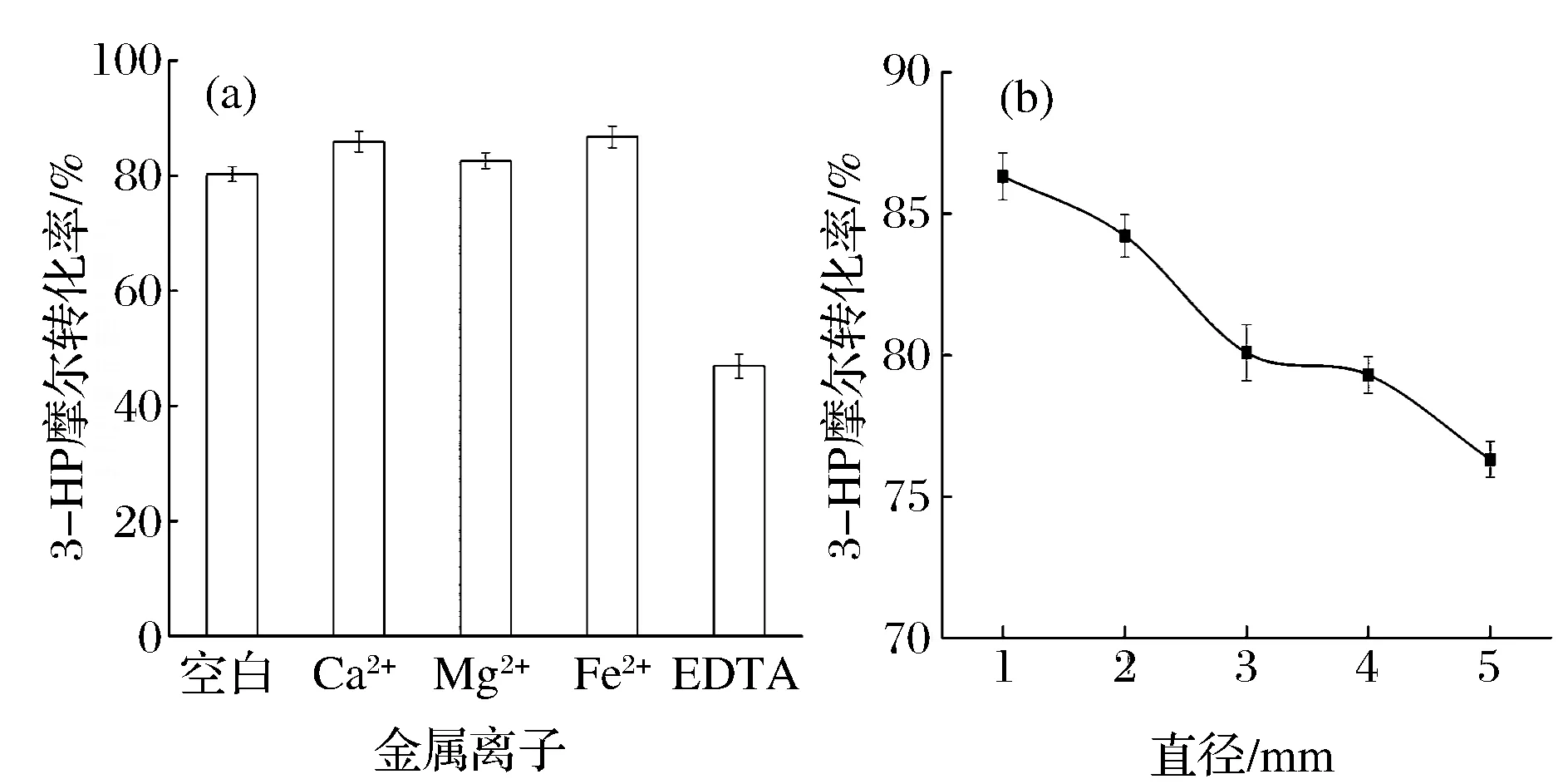
圖4 金屬離子和粒徑大小對固定化細胞催化性能的影響Fig.4 Influences of metal ions and biocapsules diameter on catalytic efficiency of immobilized cells
2.3固定化細胞的性能
2.3.1固定化細胞的底物耐受性
分別利用靜息細胞和固定化細胞對不同濃度的1,3-PDO進行催化,結果如圖5所示。在10、20 g/L的低1,3-PDO濃度下,靜息細胞較固定化細胞有更高的轉化性能,這可能與固定化細胞的傳質性能有關。而當底物濃度進一步增大后,靜息細胞的底物抑制作用明顯,催化性能降低,而固定化細胞則在70 g/L的高底物濃度下依舊保持80.27%的摩爾轉化率,是同等濃度下靜息細胞催化水平的1.32倍。由此可見,細胞的固定化可有效提升Acetobactersp. 在高濃度底物下的催化性能。
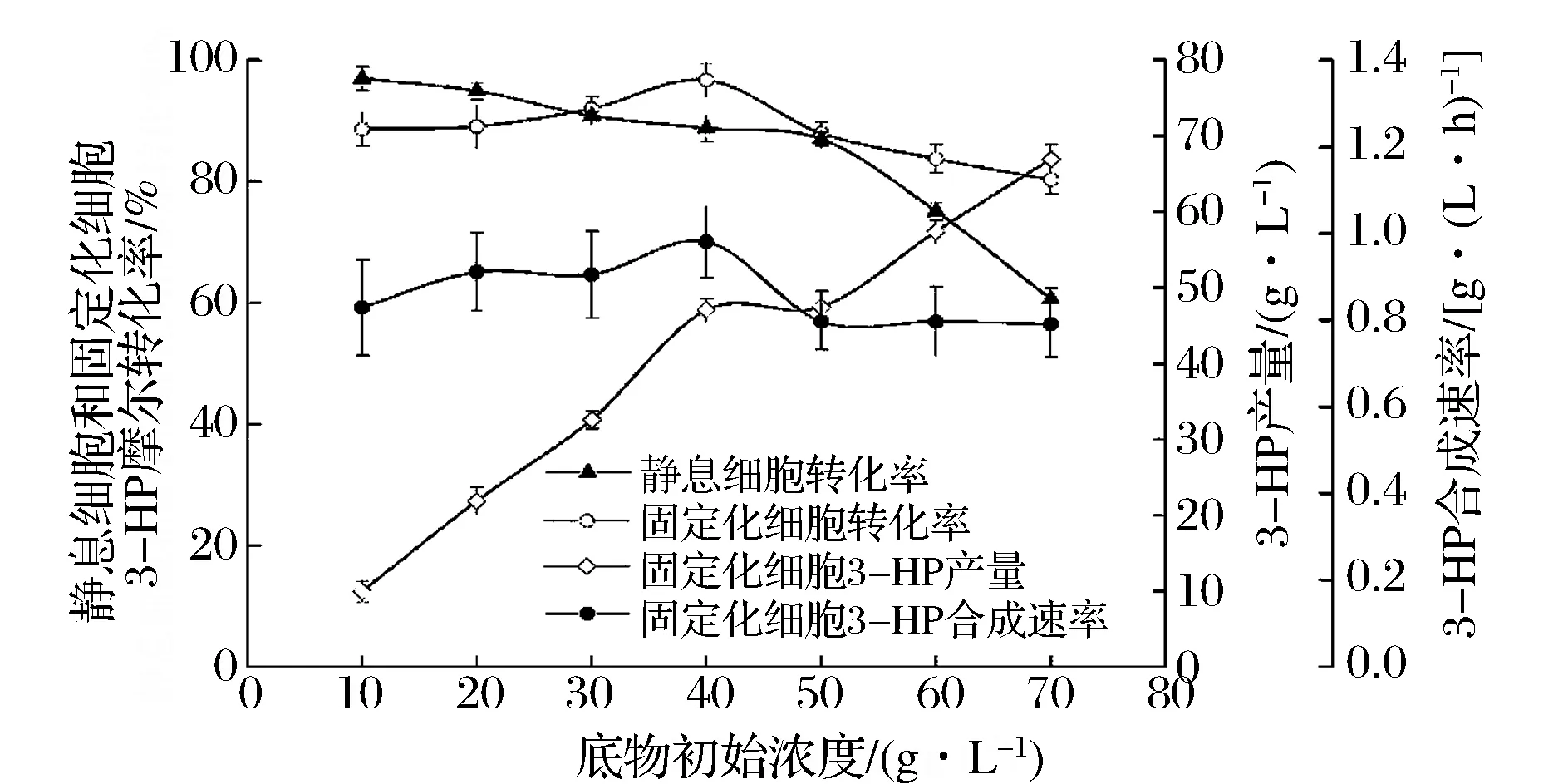
圖5 不同底物初試濃度下靜息細胞和固定化細胞的催化性能Fig.5 Catalytic characteristics of resting cells and immobilized cells at different initial substrate concentrations
2.3.2熱穩定性和pH穩定性
通過包埋法獲得的固定化細胞Acetobactersp.具有良好的操作穩定性。在不同溫度下固定化細胞催化性能隨貯存時間的變化情況如圖6(a)所示。在4 ℃貯存超過100 h后仍保持3-HP摩爾轉化率為82.2%,在20 ℃和30 ℃下長期貯存也能保持較高的催化性能,而在37 ℃貯存40 h后則急劇下降。固定化細胞在不同pH的醋酸緩沖液(pH 3.0,4.0,5.0和6.0)和Tris-HCl緩沖液(pH 7.0,8.0和9.0)中相對轉化率如圖6(b)所示。以pH 7.0的最高轉化率為對照,當pH > 7.0時,固定化細胞經過60 h的催化仍保持83.69%的相對轉化率,而pH低至3.0時也高達85.85%,說明固定化后的細胞具有良好的pH穩定性。
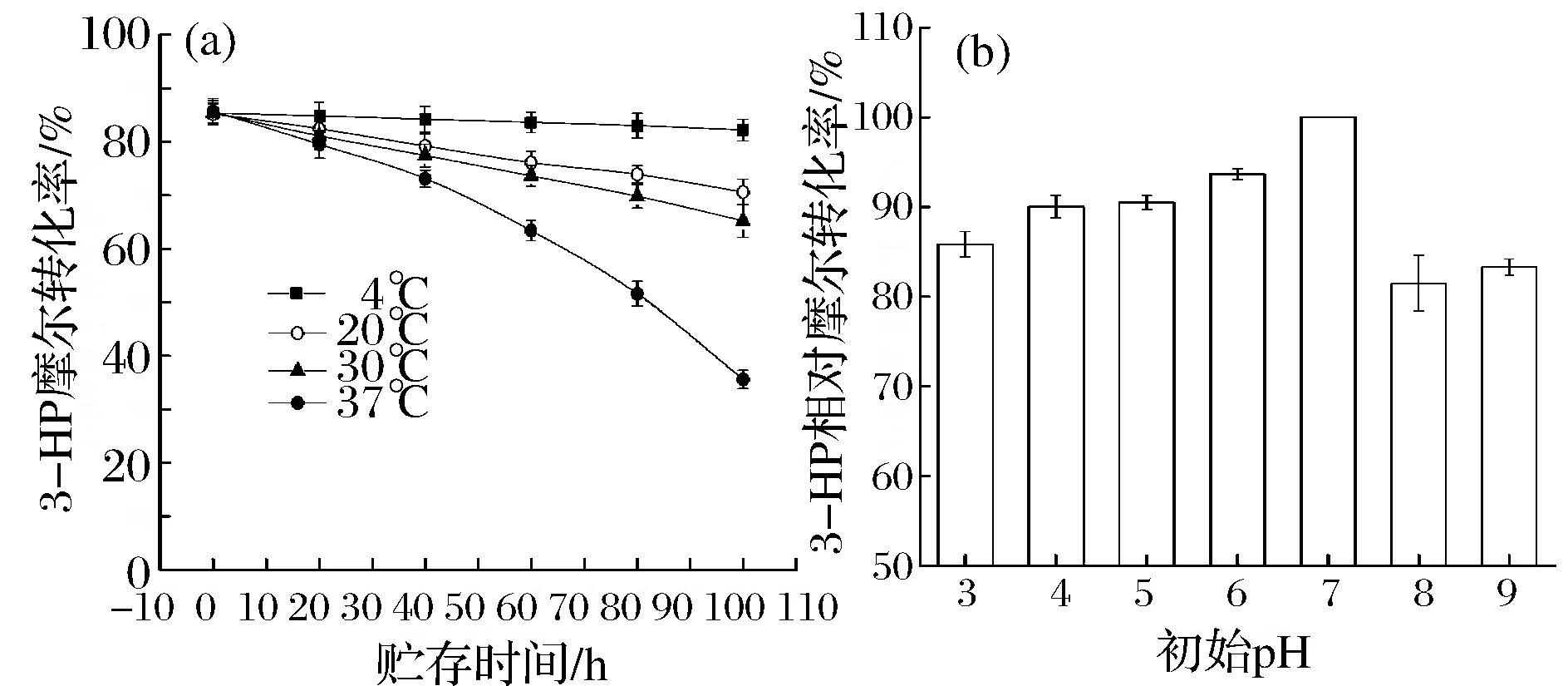
圖6 固定化細胞熱穩定性(a)和pH穩定性(b)Fig.6 Thermal stability (a) and pH stability (b) of immobilized cells
2.3.3重復利用性
在1,3-PDO濃度為50 g/L的反應體系中,在最適反應條件(30 ℃,pH 7.0,200 r/min)下連續催化60 h作為一個批次,收集固定化細胞置于生理鹽水中除去殘留底物產物后,重新添加50 g/L 1,3-PDO進行下一批次催化,結果如圖7所示。
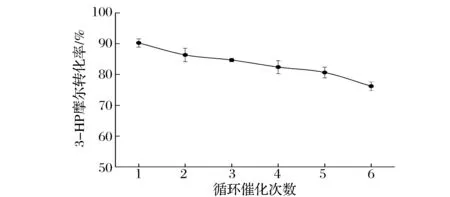
圖7 固定化細胞的重復利用Fig.7 Recycling utilization of immobilized cells
固定化顆粒的3-HP摩爾轉化率隨批次增加而緩慢降低,但經過5輪(300 h)連續催化仍達到80.65%,表明固定化細胞能夠很好地保持Acetobactersp. 的催化活性,可循環利用性好,為實際生產合成3-HP提供了重要參考。
3 結論
本文利用Acetobactersp. 的生物催化性能,通過在培養基中添加高濃度的底物1,3-PDO進行連續脅馴化培養,獲得了底物耐受性及3-HP轉化性能均有增強的馴化菌株。同時利用細胞固定化技術進一步提升生物催化反應的底物耐受濃度。當包埋材料SA和PVA終濃度為30 g/L、顆粒粒徑2 mm,并添加0.1 mmol/L Fe2+時,固定化細胞表現出最大的催化活性。70 g/L 1,3-PDO經固定化細胞催化轉化為66.95 g/L3-HP,摩爾轉化率為靜息細胞的1.32倍。此外,固定化顆粒具有良好的熱穩定性和pH穩定性,高濃度底物循環利用5次后,3-HP摩爾轉化率仍保持80.65%。本研究通過馴化選育和細胞固定化的方法有效提高了Acetobactersp. 對底物1,3-PDO的耐受性,為生物催化法工業化生產3-HP提供了一種可能。
[1]CORMA A,IBORRA S,VELTY A.Chemical routes for the transformation of biomass into chemicals[J].Chemical Reviews,2007,107(6):2 411-2 502.
[2]BROWN S F.Bioplastic fantastic[J].Fortune,2003,148(2):92-97.
[3]KUMAR V,ASHOK S,PARK S.Recent advances in biological production of 3-hydroxypropionic acid[J].Biotechnology Advances,2013,31(6):945-961.
[4]WERPY T,PETERSEN G,ADEN A,et al.Top value added chemicals from biomass Volume I: Results of screening for potential candidates from sugars and synthesis gas[M].Washington D.C.:Energy Efficiency and Renewable Energy,2004:1-31.
[5]JIANG Xin-ling,MENG Xin,XIAN Mo.Biosynthetic pathways for 3-hydroxypropionic acid production[J].Applied Microbiology Biotechnology,2009,82(6):995-1 003.
[6]ZHOU Feng-li,ZHANG Ru-bing,ZHANG Yong-guang,et al.Cloning and transcription analysis of theCandidarugosapropionyl-CoA dehydrogenase gene and its expression inPichiapastoris[J].Journal of Basic Microbiology,2012,52(3):360-367.
[7]TAKAMIZAWA K,HORITSU H,ICHIKAWA T,et al.β-hydroxypropionic acid production byByssochlamyssp. grown on acrylic acid[J].Applied Microbiology and Biotechnology,1993,40(2):196-200.
[8]LEE S H,PARK S J,PARK O J,et al.Production of 3-hydroxypropionic acid from acrylic acid by newly isolatedRhodococcuserythropolisLG12[J].Journal of Microbiology and Biotechnology,2009,19(5):474-481.
[9]吳金鑫,諸葛斌,宗紅,等.高效催化合成3-羥基丙酸的菌株特性研究[J].應用與環境生物學報,2014,20(5):804-808.
[10]TOYAMA H,MATHEWS F S,ADACHI O,et al.Quinohemoprotein alcohol dehydrogenases:structure,function,and physiology[J].Archives of Biochemistry and Biophysics,2004,428(1):10-21.
[11]COZIER G E,ANTHONYC.Structure of the quinoprotein glucose dehydrogenase ofEscherichiacolimodelled on that of methanol dehydrogenase fromMethylobacteriumextorquens[J].Biochemical Journal,1995,312(3):679-685.
[12]ADACHI O,MOONMANGMEE D,TOYAMA H,et al.New developments in oxidative fermentation[J].Applied Microbiology and Biotechnology,2003,60(6):643-653.
[13]GOMEZ-MANZO S,GONZALEZ-VALDEZ A A,ORIA-HERNANDEZ J,et al.The active (ADHa) and inactive (ADHi) forms of the PQQ-alcohol dehydrogenase fromGluconacetobacterdiazotrophicusdiffer in their respective oligomeric structures and redox state of their corresponding prosthetic groups[J].FMES Microbiology Letters,2012,328(2):106-113.
[14]YAKUSHI T,MATSUSHITAK.Alcohol dehydrogenase of acetic acid bacteria: structure,mode of action,and applications in biotechnology[J].Applied Microbiology Biotechnology,2010,86(5):1 257-1 265.
Domestication and immobilization ofAcetobactersp.for 3-hydroxypropionic acid bioproduction
LI Jun1,ZONG Hong1,ZHUGE Bin1*,LU Xin-yao1,FANG Hui-ying1,SONG Jian2,DONG Zhuo-li1
1(Key Laboratory of Industrial Biotechnology, Ministry of Education, Laboratory of Industrial Microorganisms,School of Biotechnology, Jiangnan University, Wuxi 214122, China)2(School of Chemical and Material Engineering, Jiangnan University, Wuxi 214122, China)
As one of the important chemical platform organics, 3-hydroxypropionic acid (3-HP) and a plenty of its derivatives were widely utilized in the fields of materials, textile, food and biomedicine. Based on the property of 3-HP synthesis from 1,3-propanediol(1,3-PDO) oxidation using biocatalystAcetobactersp., the substrate tolerance of domesticated strain was effectively promoted via gradient addition of 1,3-PDO in plate culture medium. Whole cell immobilization was also used for adaption of high concentration substrate and elevation of 3-HP conversion efficiency. Biocapsules with 2 mm diameter were embedded by 30 g/L compound of sodium alginate and polyvinyl alcohol. Then the maximum catalytic activity of immobilized cells was obtained after addition of 0.1 mmol/L Fe2+invitro. Under the reaction condition of 10 g/L (CDW) cell concentration, pH 7.0 and 30 ℃, 3-HP molar conversion of immobilized cells was 1.32 fold higher than that of resting cells and reach maximum production of 66.95 g/L 3-HP converted from 70 g/L 1,3-PDO. After 5 times of recycle use, immobilized cells biotransformed 50 g/L 1,3-PDO continuously over 300 h and maintained a 3-HP molar conversion of 80.65%. A new alternative method for industrial 3-HP production was provided when acetic acid bacteria were used as immobilized biocatalysts.
domestication; immobilized cells; substrate tolerance; 3-hydroxypropionic acid;Acetobactersp.
10.13995/j.cnki.11-1802/ts.201609007
碩士研究生(諸葛斌教授為通訊作者,E-mail:Bzhuge@163.com)。
江蘇省青年自然科學基金(BK20140134);國家自然科學基金(31570052)
2016-01-26,改回日期:2016-04-03

