白術內酯Ⅰ對慢性萎縮性胃炎大鼠胃黏膜保護作用
河北北方學院附屬第一醫院消化內科
李 多 于永強 高會斌 劉德清△(張家口 075000)
?
白術內酯Ⅰ對慢性萎縮性胃炎大鼠胃黏膜保護作用
河北北方學院附屬第一醫院消化內科
李多于永強高會斌劉德清△(張家口 075000)
提要目的:探討白術內酯Ⅰ對慢性萎縮性胃炎(CAG)大鼠胃黏膜保護機制。方法: 實驗動物隨機分為空白對照組、模型組、白術內酯Ⅰ組(10、20、40 mg/kg), 采用脫氧膽酸鈉和熱鹽水交替灌胃、結合饑飽失常方法制備CAG大鼠模型, 治療8周后, 采用ELISA法檢測白細胞介素-8(IL-8)含量、Western blot法檢測熱休克蛋白70(HSP 70)、核轉錄因子-k B(NF-kB)和環氧合酶-2(COX-2)蛋白表達。結果: 與空白對照組對比, 模型組HSP70蛋白表達降低(P<0.01), IL-8含量(P<0.01)增加、NF-κB和COX-2蛋白表達升高(P<0.01); 與模型組對比, 白術內酯Ⅰ高、中、低3個劑量組提高HSP70蛋白表達, 降低IL-8含量、NF-κB和COX-2蛋白表達(P<0.05), 以白術內酯Ⅰ組(40 mg/kg)作用顯著。結論: 白術內酯Ⅰ對CAG大鼠的保護作用是通過抗炎作用。
白術內酯Ⅰ;慢性萎縮性胃炎;白細胞介素-8;熱休克蛋白70;核轉錄因子-kB;環氧合酶-2
慢性萎縮性胃炎(CAG)是消化系統多發病, 是一種以胃黏膜廣泛性或局部性固有腺體萎縮、黏膜層變薄、黏膜肌層變厚為主要病理改變的慢性胃炎, 并且常伴有炎性反應、腸上皮化生以及不典型增生。[1]CAG于1978年被世界衛生組織列為胃癌前狀態。CAG是一個多階段、多病因、多基因逐漸變異積累的過程。 它常與幽門螺桿菌感染、煙酒、飲食、十二指腸反流等致病因素有關。中醫藥在治療CAG中也起到積極的作用, 有文獻報道, 胃炎Ⅰ號[2]、復方中藥安胃湯[3]等在治療CAG中效果明顯。枳術寬中也是治療胃腸道疾病常用藥, 其君藥為白術, 白術為菊科植物白術(Atractylodes macrocephala Koidz)的干燥根, 主產于浙江、湖北等省。其性味甘、苦、溫, 具有健脾益氣、燥濕利水、止汗、安胎的功效, 其有效成分單體白術內酯Ⅰ調節胃腸道功能和促進營養物質吸收的功效, 具有抗炎[4]、抗腫瘤、增強免疫力作用。[5-6]CAG研究結果顯示, CAG模型中白介素-8[7]、(IL-8)、熱休克蛋白70[8](HSP 70)、核轉錄因子-kB[9](NF-kB)和環氧合酶-2[10](COX-2)蛋白在疾病進展中有重要作用。IL-8可促使NF-kB表達并發生活化, 導致炎癥級聯反應, 胃黏膜受損, 慢慢形成CAG。而在細胞核內NF-K B可增加COX-2的合成。 而HSP70競爭性抑制N-kB活化,阻斷IL-8的過量生成, 中斷IL-8與NF-kB的炎癥級聯反應,[11]保護胃黏膜, 阻止CAG發生。因此, 本實驗探討白術內酯Ⅰ對CAG大鼠模型體內IL-8、HSP70、NF-kB、COX-2的影響, 為臨床工作提供理論基礎。
1 材料和方法
1.1材料實驗動物為8周齡SPF級SD大鼠, 由河北北方學院動物中心提供, 共70只, 雌雄對半, 體質量180~200 g。在實驗過程中, 分籠飼養, 室溫18℃~25℃, 濕度50%~60%, 空氣新鮮, 自由攝食、飲水, 通風良好, 符合實驗動物倫理學原則。 白術內酯Ⅰ對照品(批號111687), 購于中國生物制品藥品鑒定所; 脫氧膽酸鈉, IL-8 Elisa試劑盒(批號131209), 兔抗鼠HSP多克隆抗體(批號bs-1105R)、兔抗鼠NF-kB多克隆抗體(批號bs-1361R)、兔抗鼠COX-2多克隆抗體(批號bs-0081R), Goat Anti- rabbit Ig G/HRP(批號bs-0295G-HRP), BCA蛋白濃度測定試劑盒(批號140821), 預染寬范圍蛋白質分子量標準條帶(批號111687), DAB顯色劑(批號ZLI-9017)購于北京博奧森生物技術有限公司。
1.2方法
1.2.1CAG模型的建立:選用50只SD大鼠, 隨機分為空白對照組10只, 造模組40只, 參考相關文獻[12]大鼠先以0.2%的脫氧膽酸鈉溶液灌胃, 1.5 mL/只·d-1, 間隔時間為5 h, 再用 50℃熱鹽水灌胃, 2 mL/只·d-1, 并且加用饑飽失常(即2 d喂食, 足量, 1 d停食)的方法, 隨機剖殺, 光鏡下胃黏膜病理學檢查, 確認模型成功, 持續造模共8周。模型成功后, 隨機分為模型組, 白術內酯Ⅰ高、中、低3個劑量組, 每組10只,動物如有死亡, 及時補充。 空白對照組大鼠給予相應等量的蒸餾水, 正常喂養, 自由活動飲水。
1.2.2模型鑒定標準:參照《中藥新藥臨床研
究指導原則》(2002) CAG的病理診斷標準[13]: 固有腺體萎縮, 黏膜肌層增厚, 可有腸上皮或假幽門腺上皮化生, 固有膜驗證, 可有淋巴濾泡形成。
1.2.3給藥:白術內酯Ⅰ溶液的配制: 各治療組從第 9 周始每日上午8點分別灌胃給藥, 空白對照組和模型組給予等體積的生理鹽水。按照大鼠與人體表面積比例系數換算,[14]白術內酯Ⅰ高劑量組40 mg/kg, 白術內酯Ⅰ中劑量組20 mg/kg, 白術內酯Ⅰ低劑量組10 mg/kg, 每天稱大鼠體質量1次, 依據大鼠末次體質量調整給藥劑量, 給藥時間8周。
1.3IL-8的測定采集大鼠空腹動脈血5 mL, 及時分離血清, 取上清液, 置于-20℃冰箱備用。采用ELISA試劑盒進行檢查, 嚴格按照IL-8試劑盒說明書步驟操作, 繪制標準曲線得出IL-8含量。
1.4HSP70、NF-kB、COX-2檢測大鼠處死后, 取全胃胃竇黏膜組織, 放入-80℃。 提取組織中總蛋白:將剪刀剪碎組織塊, 加入400 μL裂解液于勻漿器中進行勻漿。然后置于冰上裂解30 min后, 移入離心管中, 4℃12 000 r/min 離心5 min, 取上清液分裝, 放置-20℃保存。 采用BCA法測蛋白含量, 每孔蛋白上樣量為 25 μg, 將1份蛋白與4份5×上樣緩沖液混勻, 100℃煮沸5 min, 離心上樣;SDS-PAGE電泳, 轉膜, 封閉, 然后分別與兔多克隆一抗HSP70 (1︰200), NF-kB (1︰200), COX-2 (1︰200) 4℃孵育過夜, 沖洗辣根過氧化酶標記二抗(1︰1500)室溫孵育1 h, 沖洗, DAB顯色, 以GAPDH為內參照, 用凝膠分析軟件Qantity one對蛋白條帶灰度值進行分析。
2 結果
2.1白術內酯Ⅰ降低CAG模型大鼠血清IL-8含量與空白對照組比較, 模型組血清IL-8含量升高, 差異具有非常顯著性(P<0.01),說明CAG模型大鼠血清中IL-8含量有明顯升高。 與模型組比較, 白術內酯Ⅰ高、中、低3個劑量組中血清IL-8含量顯著下降(P<0.05), 且隨著劑量的增高血清IL-8含量顯著下降(P<0.01),說明白術內酯Ⅰ降低CAG模型大鼠血清IL-8含量,并與白術內酯Ⅰ劑量的高低有關。詳見表1。
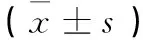

分組例數 劑量(mg/kg)IL-8(pg/mL)空白對照組106.67±0.25模型組1021.92±1.06**白術內酯Ⅰ低劑量組101017.47±1.34△白術內酯Ⅰ中劑量組102013.01±1.12△△白術內酯Ⅰ高劑量組10409.18±0.98△△
注:與空白對照組比較,** P<0.01;與模型組比較,△ P<0.05, △△ P<0.01
2.2白術內酯Ⅰ對CAG模型大鼠蛋白表達影響與空白對照組比較, 模型組HSP70蛋白表達減少, NF-kB、COX-2蛋白表達升高, 差異具有非常顯著性(P<0.01),說明CAG模型大鼠HSP70蛋白表達明顯下降, NF-kB、COX-2蛋白表達明顯升高。與模型組比較, 白術內酯Ⅰ3個劑量組中HSP70蛋白表達顯著增加, NF-kB、COX-2蛋白表達顯著下降(P<0.05), 說明白術內酯Ⅰ提高CAG模型大鼠HSP70蛋白表達, 降低CAG模型大鼠NF-kB、COX-2蛋白表達。詳見表2。
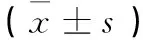

分組例數劑量(mg/kg) HSP70NF-κBCOX-2空白對照組102.20±0.010.23±0.040.43±0.09模型組101.10±0.08**0.76±0.05**1.23±0.09**白術內酯Ⅰ低劑量組10101.39±0.07△0.65±0.07△1.03±0.07△白術內酯Ⅰ中劑量組10201.57±0.06△△0.52±0.07△△0.83±0.09△△白術內酯Ⅰ高劑量組10401.86±0.08△△0.41±0.06△△0.63±0.08△△
注:與空白對照組比較,** P<0.01;與模型組比較,△ P<0.05, △△ P<0.01
3 討論
IL-8是一種糖蛋白, 定位于人染色體4q12-21, 由3個內含子和4個外顯子組成, 包括69、72和77個氨基酸3種形式, 其中72個氨基酸是活性形式, 長5.2 kb。 研究表明, 炎癥參與某些腫瘤病理學發展過程。炎癥細胞可分泌大量細胞因子與細胞外基質形成新微環境, 還可以形成炎性細胞因子網絡, 促進腫瘤的發生, 細胞遷移和侵襲。CAG發展為胃癌與幽門螺旋桿菌感染密切相關。幽門螺旋桿菌感染引起胃黏膜慢性炎癥, 釋放大量IL-8、NF-κB等炎性因子, IL-8、NF-κB持續高表達, 抑制肌體免疫應答、導致胃黏膜細胞惡變等; 同時高表達的炎性因子通過不同作用機制促進胃癌的形成與發展。[15]文獻報道, IL-8在胃癌腫瘤組織、血清中高表達。 付浩等[16]研究發現, IL-8蛋白陽性表達率在正常胃黏膜-癌前狀態-胃癌的發生過程中逐漸升高。本實驗結果顯示, 與空白對照組比較, 模型組血清IL-8含量升高, 具有顯著差異;說明CAG模型大鼠血清中IL-8含量明顯升高。與模型組比較, 白術內酯Ⅰ組血清IL-8含量顯著下降, 說明白術內酯Ⅰ降低CAG模型大鼠血清IL-8含量。
HSP70是應激反應蛋白并在生物進化過程中高度保守, 是細胞內分子伴侶, 當組織遇到各種不良刺激時 它能結合未折疊或新生蛋白, 輔助或穩定其形成正確空間構象; 調節細胞免疫系統, 維持調節蛋白整體性; 還可以結合變性蛋白, 使結合蛋白降解。有研究發現, 在如胃潰瘍、慢性胃炎等胃黏膜病變損傷修復中, 誘導HSP70表達可增強胃黏膜細胞的抵抗力, 保護胃黏膜細胞。有研究表明, 誘導HSP70表達增加能減輕肝切除、急、慢性胃潰瘍、慢性結腸炎等疾病的組織損傷, 增強細胞抵抗力。[17]目前HSP70在慢性萎縮性胃炎中的作用機制可能為HSP70可增強細胞的應激反應狀態, 調節增殖與凋亡的動態平衡, 減少突變, 另外研究發現幽門螺桿菌感染可能通過抑制HSP70表達, 獲得免疫逃避, 而長期定植。本實驗結果顯示, 與空白對照組比較, 模型組HSP70蛋白表達減少, 具有顯著差異;說明CAG模型大鼠HSP70蛋白表達明顯下降。與模型組比較, 白術內酯Ⅰ組HSP70蛋白表達顯著增加, 說明白術內酯Ⅰ提高CAG模型大鼠HSP70蛋白表達。
NF-κB是一種多向性細胞核轉錄因子, 以無活性的形式存在, 無調節基因轉錄功能, 只有被激活時, NF-κB進入細胞核發揮重要作用。大量文獻報道, NF-κB參與肌體的炎癥反應、免疫應答, 調控細胞增殖、凋亡相關基因, 調控腫瘤細胞生長。NF-κB與COX-2的關系也非常密切。[18]COX-2則是一種胞裝蛋白, 與炎癥、腫瘤等病理過程相關。COX-2可通過AKT信號轉導通路激活細胞NF-κB, COX-2選擇性抑制劑, 可抑制NF-κB活性, 抑制腫瘤增殖, COX-2在腫瘤形成中的作用機制可能為催化致癌物質的形成, 催化前列腺素, 調節細胞生長分化, 增加細胞與胞外基質的黏附力等。本實驗結果顯示, 與空白對照組比較, 模型組NF-κB蛋白表達升高, 具有顯著差異;說明CAG模型大鼠NF-κB、COX-2蛋白表達明顯升高。與模型組比較, 白術內酯Ⅰ組NF-κB、COX-2蛋白表達顯著下降, 說明白術內酯Ⅰ降低CAG模型大鼠NF-κB、COX-2蛋白表達。
其中在炎癥反應中IL-8可促使NF-κB表達并發生活化, 兩者相互影響, 導致炎癥級聯反應, 胃黏膜在這種長期炎癥作用下受損, 慢慢形成CAG。此外, 在細胞核內NF-κB可增加前列腺素合成限速酶COX-2的合成。而HSP70競爭性抑制NF-κB活化, 阻斷IL-8的過量生成, 中斷IL-8與NF-κB的炎癥級聯反應,[11]保護胃黏膜, 阻止CAG發生。本實驗結果表明, 白術內酯Ⅰ可能通過抑制IL-8的釋放、降低NF-κB和COX-2的合成、提高HSP70的合成, 切斷炎癥因素對胃黏膜的損傷, 對CAG起到治療作用, 為臨床用藥提供實驗數據和理論依據。
[1]鐵玲玲, 姜樹民. 姜樹民以癰論治慢性萎縮性胃炎[J]. 實用中醫內科雜志,2014,28(11): 10-11
[2]韋玉娜, 張靜, 王文杰,等. 胃炎Ⅰ號對慢性萎縮性胃炎PCNA、Bcl-2和Bax表達的影響[J]. 世界華人消化雜志,2015,23(6): 944-948
[3]林壽寧, 韋維, 黃貴華,等. 復方中藥安胃湯對慢性萎縮性胃炎大鼠模型TFF mRNA表達的影響[J]. 世界華人消化雜志,2011,19(1): 68-73
[4]熊蘊珠. 白術內酯Ⅰ對MyD88+人卵巢癌細胞分泌的免疫抑制因子TGF-β1、IL-17A、IL-10和IL-4的影響[D].成都:成都中醫藥大學.2014.42-43
[5]高小玲, 汪保英, 尹素改,等. 白術內酯對IEC-6細胞及食管癌細胞ECA9706增殖能力的影響[J]. 中華中醫藥雜志,2015,30(3): 921-923
[6]王嫦鶴, 耿慶光, 王雨軒. 白術內酯Ⅰ對免疫性肝損傷的保護作用[J]. 中國中藥雜志,2012,37(12): 1 809-1 813
[7]Li ZW, Wu Y, Sun Y, et al. Inflammatory cytokine gene polymorphisms increase the risk of atrophic gastritis and intestinal metaplasia[J]. World J Gastroenterol,2010,16(14): 1 788-1 794
[8]周嘉鶴, 傅志泉, 鄧建平,等. 健脾和胃化瘀中藥對慢性萎縮性胃炎患者胃黏膜熱休克蛋白70表達的影響[J]. 中國中西醫結合雜志,2015, 33(4): 406-410
[9]Lin HY, Zhao Y, Yu J N,et al. Effects of traditional Chinese medicine Wei-Wei-Kang-Granule on the expression of EGFR and NF-KB in chronic atrophic gastritis rats[J]. Afr J Tradit Complement Altern Med,2012,9(1): 1-7
[10]Ock CY, Kim EH, Choi DJ,et al. 8-Hydroxydeoxyguanosine: not mere biomarker for oxidative stress, but remedy for oxidative stress-implicated gastrointestinal diseases[J]. World J Gastroenterol,2012, 18(4): 302-308
[11]Wang L, Liu Y, Jin H,et al. Electrical stimulation induced Hsp70 response in C2C12 cells[J]. Exerc Immunol Rev,2010,16(5):1 686-1 697
[12]李紅平, 毛萬姬, 鄒學正. 丹白麥門冬湯對慢性萎縮性胃炎大鼠胃黏膜病理形態學的影響[J]. 陜西中醫, 2007, 28(2): 243-245
[13]鄭筱萸. 中藥新藥臨床研究指導原則[S]. 北京: 中國醫藥科技出版社, 2002. 124
[14]苗明三. 實驗動物和動物實驗技術[M]. 北京: 中國中醫藥出版社, 2003.142
[15]Munoz A and Costa M. Nutritionally mediated oxidative stress and inflammation[J]. Oxid Med Cell Longev, 2013(12):610 950
[16]付浩, 王旭光, 富偉能,等. IL-8基因在幽門螺桿菌相關性胃疾病中的表達[J]. 中國醫科大學學報,2009, 38(1): 26-27
[17]Takahashi T, Otaka M, Odashima M,et al. Correlation of heat shock protein expression to gender difference in development of stress-induced gastric mucosal injury in rats[J]. J Clin Biochem Nutr, 2010,47: 64-73
[18]Terzuoli E, Meini S, Cucchi P,et al.Antagonism of bradykinin B2 receptor prevents inflammatory responses in human endothelial cells by quenching the NF-kB pathway activation[J]. PLoS One, 2014, 9:e 84 358
(2016-02-29收稿)
Protection of Atractylenolide I for Gastric Mucosa of Chronic Atrophic Gastritis Rats
Digestive System Department of No. 1 Affiliated Hospital, Hebei North University
LIDuoYUYong-qiangGAOHui-binLIUDe-qing(Zhangjiakou 075000)
Objective: to explore the protective mechanism of Atractylenolide I for gastric mucosa of chronic atrophic gastritis (GAC) rats. Methods: The laboratory animals were randomly divided into control group, model group and Atractylenolide I group (10, 20, 40 mg/kg). The models were established by alternate intragastric administration with sodium deoxycholate and hot saline, which was combined with irregular diet. 8 weeks later, ELISA was taken to detect IL-8 content, and Western blot to detect HSP 70, NF-κB and COX-2 expressions. Results: Compared to control group, HSP 70 of model group decreased (P<0.01), IL-8 increased (P<0.01), , NF-κB and COX-2 increased (P<0.01); compared to model group, low, medium and high dose groups of Atractylenolide I increased HSP 70 expression, decreased IL-8, NF-κB and COX-2 (P<0.05), especially significantly in the high dose group (40 mg/kg) . Conclusion: Atractylenolide I may provide protection for CAG rats through anti-inflammatory action.
Atractylenolide I; chronic atrophic gastritis (GAC); IL-8 (interleukin-8); HSP 70 (heat shock protein 70); NF-κB (nuclear factor-κB); COX-2
R285.5
A
1007-5615(2016)03-0005-04
△河北省康保縣人民醫院內科(康保 076650)

