BSA與羥磷灰石相互吸附的FTIR-ATR光譜
葉 青 胡 仁 周劍章 葉藝文 許朝曦 林昌健 林種玉,*(廈門大學化學化工學院化學系,固體表面物理化學國家重點實驗室,福建廈門6005;浙江師范大學初陽學院,浙江金華004;廈門阿爾特系統工程有限公司,福建廈門6005)
BSA與羥磷灰石相互吸附的FTIR-ATR光譜
葉青2胡仁1周劍章1葉藝文1許朝曦3林昌健1林種玉1,*
(1廈門大學化學化工學院化學系,固體表面物理化學國家重點實驗室,福建廈門361005;2浙江師范大學初陽學院,浙江金華321004;3廈門阿爾特系統工程有限公司,福建廈門361005)
采用傅里葉變換紅外衰減全反射(FTIR-ATR)光譜法對牛血清白蛋白(BSA)在羥磷灰石(HA) [Ca10(OH)2(PO4)6]表面不同時間的相互吸附作用進行了表征。在BSA溶液作用下,羥磷灰石表面的Ca2+、PO43-和OH-離子初始的溶解和再沉淀使得BSA與HA相互作用層層疊加,在HA表面形成從表層到次表層分子都包含有吸附的BSA的覆蓋層,從而加深兩者之間的相互作用。經紅外差譜法處理過的相關ATR數據表明,BSA與HA之間的相互作用是快速的,并隨時間變化進一步加強;來自HA上PO43-的P=O基團對蛋白質肽鍵的酰胺II帶(―CNH)、多肽鏈的甲基(―CH3)和亞甲基(―CH2)上氫的吸附作用要比P―O快速而且強烈。Ca2+在該吸附過程中起了極其重要的作用,其快速與蛋白質肽鍵的羰基氧發生作用,并誘導該蛋白質二級結構由β-折疊向α-螺旋和β-轉角構象轉變;伴隨著這一構象變化,蛋白質多肽鏈上大多數肽鍵的―C=O和H―N―活性基團從鏈間氫鍵交聯中釋放出來,帶動眾多的氫分別參與同HA表面的Ca2+、PO43-和OH-離子的相互吸附作用,并牢牢地結合于HA表面;這對硬組織的再生起著重要作用,促進了HA的生物礦化過程。
生物材料;蛋白質吸附作用;多肽;紅外光譜;FTIR-ATR;生物礦化作用
O646
doi:10.3866/PKU.WHXB201511301
1 引言
蛋白質的吸附作用有強吸附和弱吸附1,強吸附作用對各種生物過程產生著重要的影響,首先是對植入材料的生物反應的影響。相關作用的研究普遍側重于測定各種生物材料表面吸附蛋白質的二級結構構象情況2-8。作為生物活性陶瓷的羥磷灰石與蛋白質之間的相互吸附作用過程也已有諸多的報道6-10,但相關過程的分子作用機制以及吸附的蛋白質是以何種分子構象為主乃存在爭議,還有待進一步探討。本文在前期工作10的基礎上,采用傅里葉變換紅外衰減全反射(FTIR-ATR)光譜法進一步考察了牛血清白蛋白在HA表面的吸附作用,揭示它們之間在各不同時間的相互作用機理。FTIR-ATR光譜法直接提供了吸附于HA表面的蛋白質的相關信息,但應該注意的一個重要問題是,由于ATR反射光透過深度(紅外漸消場在酰胺I和酰胺II帶區間的貫穿深度大約是400-600 nm)超過HA修飾層的厚度(約為20-40 nm),而進入BSA溶液中,該檢測所得到的是表面吸附的和非吸附的蛋白質的混合光譜11。因此必須利用紅外差譜方法2,11減去那部分非吸附的蛋白質的貢獻,才能得到準確的吸附于HA表面的蛋白質信息。此方法提供了可信賴的而且重現性較好的差減結果12。另外,由于水在1643 cm-1處有較強的羥基彎曲振動吸收,在一定程度上干擾了蛋白質酰胺I帶而影響觀察其吸收情況。本實驗采用重水(D2O)代替水溶液。
2 實驗方法
2.1主要試劑
BSA(0903,99.0%)為上海生物工程有限公司生產的生化試劑。
2.2樣品制備
鍺晶體表面羥磷灰石的修飾按照文獻9,10報道的方法進行。將幾何尺寸為50 mm×10 mm×3 mm的ATR鍺晶體側立浸泡于沸騰的飽和Ca(OH)2溶液40 min,再用20%的H3PO4溶液(pH 2.0-2.4)于90°C繼續浸泡30 min,之后將該晶體用去離子水沖洗2次在室溫下晾干。牛血清白蛋白用0.9% NaCl重水溶液配制成濃度為40 mg?mL-1的BSA溶液。
2.3FTIR-ATR檢測
使用美國Nicolet 740 SX FT-IR光譜儀,MCTB檢測器,衰減全反射附件。反射光束由鍺晶體45°斜面入射,在晶體內產生多次的衰減全反射再經聚焦反射到達檢測器檢測。先測定鍺晶體表面空白HA;之后往液池(帶有HA修飾層的鍺晶)中注入1 mL新鮮的BSA溶液,從0 min開始每隔1 min掃描收集數據至10 min,然后至15、30、60 min以及5、24和30h。掃描波長范圍:4000-625cm-1,分辨率為4 cm-1,增益為1,掃描次數為128。為了檢驗測定結果的重現性,確保檢測質量,該實驗重復做3次。實驗所測得的數據是HA表面吸附的和非吸附的BSA的混合光譜。為了獲得準確的吸附于HA表面的BSA的信息,利用紅外差譜法,調節各個差減因子(FCR)扣除那部分非吸附的蛋白質的吸收。
3 結果與討論
3.1羥磷灰石及其對BSA的吸附作用
3.1.1鍺晶體表面羥磷灰石修飾層
圖1曲線1示出修飾于鍺晶體表面羥磷灰石[Ca10(OH)2(PO4)6]的FTIR-ATR光譜圖;與HA透射譜帶101100-1000 cm-1區間出現的各吸收帶頻率相比較基本上接近,說明鍺晶體表面的修飾層的確為HA,這樣該修飾層含有Ca2+、PO34-和OH-羥磷灰石離子。其中1098和1026 cm-1吸收帶均與HA的PO基團振動有關13,可分別歸屬于P=O和P―O的伸縮振動帶。1656 cm-1的吸收為HA分子的O―H基團的彎曲振動帶(該吸收帶弱,并不影響觀察蛋白質酰胺I帶的吸收情況)。
圖1曲線2和3分別為HA與BSA作用1 min和30 h的FTIR-ATR光譜圖。譜線2和3上的蛋白質酰胺I帶(1652,1649 cm-1)、酰胺II帶(1548,1563 cm-1)以及蛋白質多肽鏈上的亞甲基(1459和1455 cm-1)和甲基(1445和1443 cm-1)的C―H彎曲振動帶13-15的吸收實際上均為HA表面吸附的和非吸附的BSA的混合吸收光譜。作用1 min的P=O譜帶由空白時的1098 cm-1紅移至1094 cm-1,但作用了30 h該譜帶還是在1094 cm-1處;而空白HA的P―O基團及其與BSA分別作用1 min和30 h的吸收均在1026 cm-1處。說明曲線2和3所示的1094與1026 cm-1的吸收應該分別來自HA分子中參與吸附和未參與吸附蛋白質的P=O與P―O各基團的混合吸收帶。很可能由于參與吸附作用的PO(P=O與P―O)各基團含量較少,分別被還未參與吸附的各PO基團(含量多)的吸收所掩蓋,因而看不出譜帶的紅移。1208 cm-1處的吸收歸屬于重水O―D的彎曲振動帶。
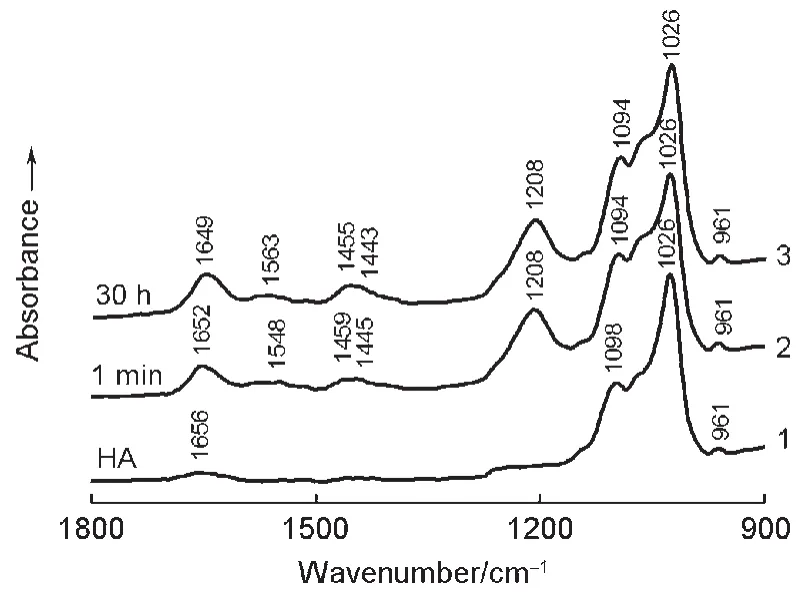
圖1 鍺晶體表面HA修飾層及其與BSA作用不同時間的FTIR-ATR光譜Fig.1 FTIR-ATR spectra of HAcoated on Ge crystal and reacted with BSAfor different time
3.1.2羥磷灰石修飾層的溶解與再沉淀
圖2示出修飾于鍺晶體表面的空白HA(曲線1)及其分別與BSA相互作用5 min,0.5 h,24 h和30 h的FTIR-ATR光譜圖。由曲線2可以看出:加入BSA溶液的最初5 min,HA的P―O基團吸收帶比曲線1明顯減弱。說明加入BSA(NaCl/D2O)溶液后,HA修飾層與BSA發生了相互吸附作用;與此同時,BSA溶液中的Na+和Cl-很可能與涂層表面羥磷灰石離子進行離子交換6,16使部分Ca2+、與OH-溶解進入BSA溶液中;溶液中的蛋白質很容易吸附(結合)溶解出的PO34-基團,因此促使PO34-基團的進一步溶解(注意:這里PO34-基團進入溶液中的位置應該超出ATR反射光的透過深度),因此ATR檢測到的各PO基團的吸收強度減弱。基團含有3個P―O鍵和1個P=O鍵(空白HA的P―O吸收帶明顯比P=O強),所以在最初5 min,隨著PO34-基團的溶解,1026 cm-1處的P―O基團吸收帶強度減弱要比P=O明顯得多。文獻6報道在初始的相同時間段里,含有白蛋白的鹽溶液從磷酸鈣涂層釋放出的PO34-基團比空白鹽溶液所釋放的要多得多(前者約為后者的2.5倍多)。顯然,蛋白質的吸附作用是影響HA修飾層溶解的重要因素6,17。
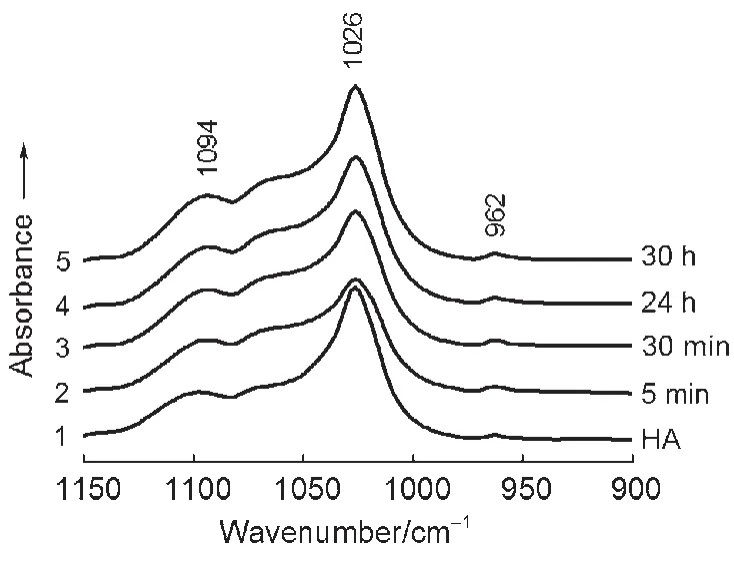
圖2 HA修飾層及其與BSA作用不同時間的FTIR-ATR光譜Fig.2 FTIR-ATR spectra of HAcoating and reacted with BSAfor different time
隨后吸附于HA涂層表面的生物大分子繼續吸附溶液中的HA離子,使溶液中的Ca2+、和OH-離子快速沉淀下來。于是涂層上PO各基團吸收帶逐漸增強(圖2曲線3-5)。這部分被吸附而覆蓋于蛋白質表面的HA離子緊接著又與溶液中的BSA發生吸附作用。HA表面的Ca2+、PO34-和OH-離子的這種初始的溶解和再沉淀9,18,19使得BSA與HA相互作用層層疊加,在HA修飾層形成從表層到次表層分子都包含有吸附的BSA覆蓋層9,從而加深兩者之間的相互作用。
3.1.3羥磷灰石(PO43-基團)對BSA的吸附作用
為了得到準確的參與吸附蛋白質的PO各基團的信息,利用IR差譜法扣除那部分還未參與吸附蛋白質的PO各基團的吸收。圖3曲線1是與BSA作用1 min的HA扣除空白HA譜線的差減結果。該曲線較為準確地展示出作用1 min時參與吸附蛋白質的PO各基團的信息。譜線上HA的PO各基團由于參與吸附蛋白質,P=O基團的吸收由原來的1098 cm-1紅移至1091和1064 cm-1,而P―O由1026紅移至1015 cm-1。僅僅作用1 min時間,PO各吸收帶就出現明顯紅移,充分表明HA對BSA的作用是快速的化學吸附。圖3曲線2-5分別是與BSA作用30 min、60 min、5 h和30 h的HA減去空白HA的紅外光譜差譜。各曲線分別清楚地展示出參與吸附蛋白質的P=O基團的紅移:由1090和1063 cm-1(30 min)分別至1089和1063 cm-1(60 min、5 h和30 h)以及P―O基團由1013 cm-1(30 min)→1010 cm-1(60 min)→1009 cm-1(5 h)→1007 cm-1(30 h)。而且這些吸收帶強度隨時間變化明顯增強;1063和1089 cm-1譜帶增強尤為明顯,表明P=O基團與蛋白質的相互吸附作用要比P―O基團快速而且強烈。PO各基團很可能是與蛋白質多肽的―CH3、―CH2和肽鍵的―C―N―H基團的氫發生吸附作用。從PO的價鍵結構特征分析:P―O單鍵為σ鍵而P=O雙鍵除含有σ鍵外還含有π鍵。由于π鍵在化學性能上比σ鍵更活潑,更容易接受―CH和―CNH上的氫原子,因此含有π鍵的P=O基團與氫的相互作用要比P―O更加迅速而強烈。這與紅外光譜檢測分析結果完全一致。P=O基團對蛋白質的作用有強吸附(1063 cm-1)和弱吸附(1089 cm-1)兩種情況,其強吸附作用比弱吸附要快速得多。
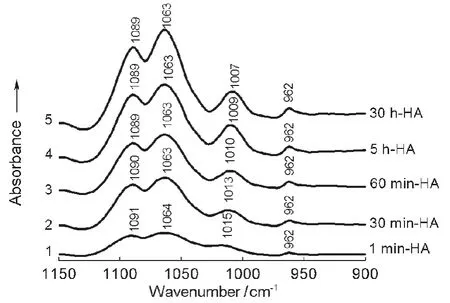
圖3 與BSA作用不同時間的HA的FTIR-ATR光譜差譜Fig.3 FTIR-ATR subtraction results of HA reacted with BSAfor different time
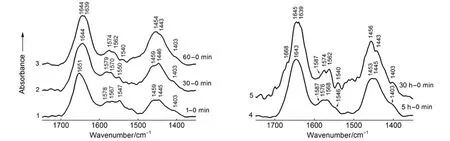
圖4 與HA作用不同時間的BSA的FTIR-ATR光譜差譜Fig.4 FTIR-ATR difference spectra of BSAreacted with HAfor different time
3.2牛血清白蛋白在HA上的吸附作用
圖4曲線1-5分別為與HA作用1 min、30 min、60 min、5 h和30 h的BSA減去與HA作用0 min的BSA光譜差譜。這里0 min譜線是經過128次掃描,歷時64 s獲得的,該譜線是HA表面吸附和非吸附的BSA混合光譜,但非吸附的占據大多數。減去該譜線時,雖然減去了一小部分初始吸附的BSA,但非吸附的BSA卻全被扣除。而各譜線都同樣扣除那一小部分初始吸附的BSA,并不影響各吸附的BSA譜線之間的對比分析結果。由于扣除了非吸附的BSA吸收的干擾,曲線1展示出與HA作用1 min后吸附于HA表面的蛋白質吸收帶。1651 cm-1的吸收歸屬于肽鍵的酰胺I帶C=O伸縮振動,說明該蛋白質的二級結構是以α-螺旋構象(這是蛋白質中含量最豐富的二級結構,體系中該譜帶的中心位置應于1653 cm-1附近)成分為主3,20,21,應該還包含有β-折疊構象(這是蛋白質中第二種最常見的二級結構)成分所對應的振動吸收子帶;該譜帶的中心大約位于1632 cm-1附近,在此與α-螺旋構象所對應的振動吸收子帶重疊在一起2,3,12,21。1459和1445 cm-1的吸收分別為多肽的―CH2和―CH3的C―H彎曲振動帶。曲線1-3示出在重水中(1-60 min)譜帶1540-1579 cm-1的吸收均處在肽鍵酰胺II帶的范圍內13-15,21(酰胺II帶在酰胺質子氫-氘交換后,產生大的紅移,移至1450 cm-1附近),說明由于該酰胺質子處于內埋或強的氫鍵作用而不容易交換,使氫-氘交換作用不完全21。
值得注意的是,圖4曲線2示出BSA與HA作用30 min后,位于1579、1570和1550 cm-1的酰胺II帶的吸收比作用1 min的各對應吸收帶都有1-3 cm-1的藍移。該譜帶來自酰胺II帶的N―H彎曲振動和C―N伸縮振動強偶合產生的吸收帶13,14,21,譜帶的藍移說明N―H和C―N的鍵力有所增強。文獻21,22表明,當有金屬離子存在時,歸屬于蛋白質二級結構β-折疊的酰胺II帶的吸收發生4-6 cm-1的藍移(酰胺I帶有1 cm-1的位移);并進一步指出,由于金屬離子的影響,使得蛋白質(尤其是1634 cm-1處的β-折疊構象)有很大一部分的氫鍵作用發生了變化。因此可以推斷體系中吸附的BSA的β-折疊的多肽鏈間氫鍵交聯已經發生了變化。這里肽鍵的―C―N―H基團中C―N和N―H鍵力增強,說明體系中沒參與相鄰鏈間肽鍵(―N―H和O=C―)的氫鍵交聯作用的―N―H含量增加了(可以確定沒參與氫鍵作用的O=C―含量也隨之增加);因為β-折疊中所有的肽鍵都參與了多肽鏈間氫鍵的交聯作用23,這就是說原來β-折疊中相鄰肽鏈間的氫鍵在Ca2+的作用下發生了斷裂,轉而由各自肽鏈結構的―N―H和O=C―形成5→1或4→1(肽單元)鏈內氫鍵的α-螺旋或β-轉角23等的構象。由于Ca2+極易與蛋白質結合并誘導該蛋白質二級結構向α-螺旋轉變24-29;又由于α-螺旋構象的規則性引起該螺旋折疊中的協同作用,一旦體系中形成鏈內第一圈α-螺旋,隨后逐個殘基的加入(即螺圈的形成)就會變得更加容易而迅速23。因此曲線2酰胺II帶的藍移說明體系中有一部分蛋白質二級結構由β-折疊轉變為α-螺旋。在這種情況下,由于沒參與氫鍵交聯的―C=O基團含量增加,酰胺I帶理應藍移;但曲線2的酰胺I帶卻由原來的1651 cm-1紅移至1644 cm-1。文獻30指出:來自肽鏈側鏈帶負電荷的羧基氧和肽鍵上不帶電荷的羰基氧都能很好地結合于Ca2+上,因此酰胺I帶的紅移應該是Ca2+與α-螺旋中沒參加氫鍵交聯作用的羰基氧發生了吸附作用,并進一步形成配位鍵3,15,30,使得C=O鍵力削弱,酰胺I帶紅移2,15,31。EDS檢測出空白HA表面的Ca/P比值為1.259,說明該修飾層表面Ca2+的含量較高,能與較多酰胺I帶的氧發生作用。這里酰胺I帶的頻率位置主要取決于兩方面的因素:一是當肽鏈由β-折疊轉變為α-螺旋時,由于沒參與氫鍵交聯作用的羰基氧含量增多,C=O鍵力增強而引起譜帶藍移;二是Ca2+與羰基氧的絡合作用削弱C=O鍵力,而導致該譜帶紅移。由于后者的作用更為強烈,兩者疊加的結果是C=O鍵力削弱引起譜帶紅移。之前發表的論文,由于體系中Pt(IV)32以及Au(III)33的含量很少,因此金屬離子對羰基氧的作用所引起C=O鍵力的削弱程度比起由于肽鏈構象變化而釋放出相當大一部分的羰基氧所引起的C=O鍵力增強,前者的作用顯得微不足道(基本上可以忽略);凈結果自然是C=O鍵力增強,導致譜帶藍移。因此判斷蛋白質二級結構構象時,在金屬離子含量較多的情況下,應該考慮到其與羰基氧的作用對C=O鍵力的影響。曲線2的1644 cm-1的吸收應該是吸附于HA表面的BSA中已經參與和還未參與同Ca2+作用的α-螺旋的C=O混合吸收帶。
圖4曲線3示出與HA作用60 min的BSA酰胺I帶有一部分由原來的1644 cm-1紅移至1639 cm-1處,而且酰胺II帶各吸收也比作用30 min時的有明顯紅移,說明此時BSA與HA之間的相互作用進一步增強。
圖4曲線4示出與HA作用5 h的BSA的酰胺I帶由1644 cm-1紅移至1643 cm-1,其原來的1639 cm-1的吸收應該被包在1643 cm-1譜帶中。酰胺II帶比作用60 min的各有2-6 cm-1的藍移,說明此時肽鏈β-折疊的鏈間氫鍵在Ca2+的作用下繼續斷裂而轉變為α-螺旋構象(與曲線2的情況相似)。
作用30 h的BSA(圖4曲線5)在1587 cm-1處的肩峰和1403 cm-1的吸收分別來自肽鏈側鏈及其C端的離子化羧基()的反對稱和對稱伸縮振動吸收帶13,15,34-36,該吸收比作用5 h的明顯增強,說明隨作用時間延長,吸附于HA表面的羧基陰離子的量進一步增加。Ca2+應該是通過強大的靜電作用力將羧基陰離子吸引到HA表面,兩者之間靠離子鍵維系15,21,34,35。羧基陰離子比酰胺I帶更容易與Ca2+發生配位作用24,25,36,形成配位羧基后,其反對稱伸縮振動譜帶由原來的1587 cm-1藍移至1605 cm-1附近34,36;由于含量少(該紅外吸收大約只占酰胺I帶的10%-30%35,37),被強的酰胺Ⅰ帶所掩蓋21。1668 cm-1處出現的新峰來自β-轉角構象的羰基吸收20,21,38,這是由各自肽鏈上肽鍵的―C=O與H―N―基團之間形成4→1的分子內氫鍵的又一種環形構象23。此外還可清楚地看到歸屬于α-螺旋構象的酰胺I帶分裂為1645和1639 cm-1兩個吸收峰(隨后將對此作詳細分析);該吸收帶整體的強度隨時間變化明顯增強,說明有更多α-螺旋的羰基氧參與了同Ca2+的相互作用。曲線5的酰胺II帶(1574、1562和1540 cm-1)以及1-5各條曲線的CH2(1459-1453 cm-1)和CH3(1446-1443 cm-1)的C―H彎曲振動吸收帶也都隨時間延長而增強,CH2吸收帶的增強尤為明顯(曲線5,1456 cm-1);說明隨著越來越多酰胺I帶與Ca2+的作用,帶動更多肽鍵和碳氫鍵上的氫參與了同HA表面的PO和OH基團的吸附作用,并且牢牢地結合于HA表面。在這一吸附過程中,酰胺II帶始終保持在正常的范圍內;酰胺質子的氘代作用難于在Ca2+負載的狀態下進行,暗示Ca2與肽鍵的結合相當緊密和堅實。進一步表明體系中的BSA與HA具有很強的相互作用能力。
圖5曲線1-7示出與HA作用30 h的BSA分別扣除與HA作用0、1、2、3、5、10、15 min的BSA的光譜差譜。這里主要觀察從0、1、2、3、5、10、15 min至30 h各不同時間段酰胺I帶的吸收情況。其中1668 cm-1(來自β-轉角構象的羰基吸收,其含量明顯比較少)和1639 cm-1(主要來自與Ca2+發生作用的α-螺旋的酰胺I帶)兩處的吸收頻率并不隨各不同的時間段而變化,吸收強度也沒有明顯的改變;而1649 cm-1的吸收頻率和強度卻隨各不同的時間段而變化。此時(已經作用了30 h),體系中絕大多數的Ca2+都參加了與羧基陰離子和α-螺旋的羰基氧的配位作用,已經達到了化學平衡;而肽鏈的α-螺旋還在形成。Chittur20指出,溶液中蛋白質α-螺旋的吸收發生在較低的波數,大約在1650-1655 cm-1附近;而在重水中該吸收會降得更低。因此,1649 cm-1的吸收應該主要來自這部分還沒與Ca2+發生絡合作用的α-螺旋的C=O吸收帶的貢獻。從曲線1至7(時間段朝后靠),該吸收呈增長趨勢并由1645 cm-1(曲線1-4)→1646 cm-1(曲線5)→1648 cm-1(曲線6)→1649 cm-1(曲線7)呈現藍移;表明隨著時間段朝后推移,體系中沒與Ca2+發生作用的α-螺旋的―C=O含量逐漸增多。這為該體系吸附的蛋白質二級結構構象變化趨勢是由β-折疊轉變為α-螺旋(和一小部分β-轉角)提供了進一步的證據。
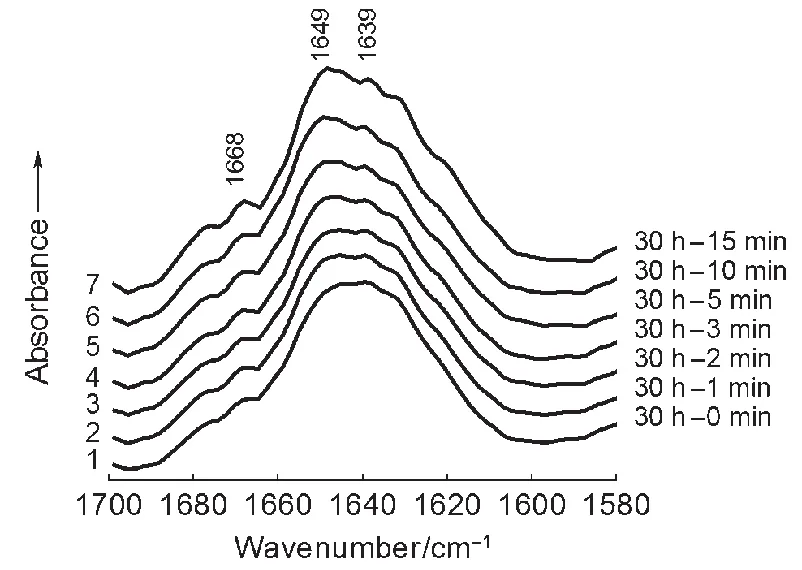
圖5 系列與HA作用30 h的BSA的FTIR-ATR光譜差譜Fig.5 FTIR-ATR subtraction results of BSA reacted with HAfor 30 h
3.3α-螺旋構象促進蛋白質與HA之間的相互作用
Moulton等1觀察到吸附于TiO2表面免疫球蛋白的酰胺I帶(1636 cm-1)和酰胺II帶(1545 cm-1)在加入磷酸鹽緩沖液后兩譜帶吸收明顯減弱,而且酰胺I帶由1636 cm-1藍移至1651 cm-1。這是由于原先吸附于TiO2表面的酰胺I帶(1636 cm-1)是以β-折疊構象成分為主而其中還含有一部分α-螺旋構象成分所對應的振動吸收子帶。當加入磷酸鹽緩沖劑后,PO各基團參與了同TiO2表面該蛋白質酰胺I帶的競爭吸附作用;取代了吸附于該表面酰胺I帶中絕大部分的β-折疊(弱吸附)組分,導致1636 cm-1譜帶消失只剩下α-螺旋組分所對應的吸收帶(1651 cm-1)。充分說明α-螺旋構象的蛋白質具有很強的吸附能力,能牢牢地結合于TiO2生物材料表面。
β-折疊構象中所有肽鍵的―N―H和O=C―基團都參加了多肽鏈間的氫鍵交聯作用;而α-螺旋和β-轉角分別只有20%和25%的肽鍵參加鏈內的氫鍵交聯。當BSA蛋白質二級結構構象由β-折疊轉變為α-螺旋和β-轉角時,其肽鏈上分別有相當多的―N―H和O=C―活性基團從鏈間氫鍵作用中釋放出來參與同HA作用;而且隨著肽鏈由伸展的折疊片向螺旋圈卷曲而引起該鏈及其側鏈上各化學官能團的空間位置發生變化這一動態過程,帶動更多的羧基陰離子、肽鍵以及大量的氫共同參與對HA的吸附作用,大大提高該蛋白質對HA的親合性。另外,由于α-螺旋0.54 nm的螺距與Ca2+在HA六方晶系中(001晶面)的0.545 nm原子間點陣間距十分接近39,這一有意義的構象特征十分有利于蛋白質調節其自身與Ca2+的相互作用24,40,41。看來吸附的蛋白質的α-螺旋構象,其規律性間距的羰基氧和側鏈羧基陰離子與處于這種點陣結構的Ca2+形成了高度的互補。這應該是蛋白質能牢固地吸附并結合于HA表面的重要原因。體系中BSA正是通過肽鏈α-螺旋表面大量的活性基團與HA之間的這種強的化學吸附作用來傳遞并調節細胞活性物質對HA界面的基本反應42,43,這對促進硬組織的再生起著十分重要的作用8,44-46。
4 結論
IR實驗結果表明:吸附于HA表面的BSA在Ca2+的誘導作用下,其蛋白質二級結構由β-折疊轉變為α-螺旋和一小部分β-轉角的圈形構象,從而大大提高了蛋白質對HA生物材料的吸附活性,使蛋白質能牢牢地吸附并結合于HA表面。這樣有利于細胞活性物質與HA界面的相互作用,從而引起和促進了生物礦化過程。
References
(1)Moulton,S.E.;Barisci,J.N.;McQuillan,A.J.;Wallace,G.G. Colloid.Surf.A:Physicochem.Eng.Asp.2003,220,159.doi: 10.1016/S0927-7757(03)00078-5
(2)Lenk,T.J.;Ratner,B.D.;Gendreau,R.M.;Chittur,K.K. J.Biomed.Mater.Res.1989,23,549.
(3)Shen,Y.H.;Yang,Z.L.;Wu,J.G.Acta Phys.-Chim.Sin. 1999,15(12),1064.[沈玉華,楊展瀾,吳瑾光.物理化學學報,1999,15(12),1064.]doi:10.3866/PKU.WHXB19991203
(4)Shen,Y.H.;Yang,Z.L.;Wu,J.G.1999,35(4),431.[沈玉華,楊展瀾,吳瑾光.北京大學學報(自然科學版),1999,35(4), 431.]
(5)Elangovan,S.;Margolis,H.C.;Oppenheim,F.G.;Beniash,E. Langmuir 2007,23(22),11200.doi:10.1021/la7013978
(6)Ong,J.L.;Chittur,K.K.;Lucas,L.C.J.Biomed.Mater.Res. 1994,28,1337.
(7)Yang,Q.;Zhang,Y.Y.;Liu,M.L.;Ye,M.;Zhang,Y.Q.;Yao, S.Z.Analytica Chimica Acta 2007,597,58.doi:10.1016/j. aca.2007.06.025
(8)Zeng,H.T.;Chittur,K.K.;Lacefield,W.R.Biomaterials 1999,20,377.doi:10.1016/S0142-9612(98)00184-7
(9)Feng,B.;Chen,J.Y.;Zhang,X.D.Biomaterials 2002,23 (12),2499.doi:10.1016/S0142-9612(01)00384-2
(10)Ye,Q.;Hu,R.;Lin,Z.Y.;Lin,C.J.Chem.J.Chin.Univ.2006, 27(8),1552.[葉青,胡仁,林種玉,林昌健.高等學校化學學報,2006,27(8),1552.]
(11)Yan,Y.L.;Jin,Z.C.Applications of Fourier Transform Infrared Spectrometry in Researches ofAgriculture,Food and Biology.In Modern Fourier-Transform Infrared Spectrometry and Its Applications(Part II);1st ed.;Wu,J.G.Ed.;Literature of Science and Technology Press:Beijing,1994;pp 177-180. [嚴衍祿,金澤宸.傅里葉變換光譜在農業、食品和生物學研究中的應用;近代傅里葉變換紅外光譜技術及應用(下卷).吳瑾光主編.北京:科學技術文獻出版社,1994:177-180.]
(12)Maruyama,T.;Katoh,S.;Nakajima,M.;Nabetani,H.;Abbott, T.P.;Shono,A.;Satoh,K.J.Membr.Sci.2001,192,201.doi: 10.1016/S0376-7388(01)00502-6
(13)Bellamy,L.J.The Infra-red Spectra of Complex Molecules, 3rd ed.;Chapman and Hall:London,1975;pp 14-26,107-125,183-202,386.
(14)Silverstein,R.M.;Bassler,G.C.;Morrill,T.C.Infrared spectrometry.In Spectrometric Identification of Organic Compounds,5th ed.;Sawicki,D.,Stiefel,J.Eds.;Wiley:New York,1991;pp 103,123.
(15)Rao,C.N.R.Chemical applications of Infrared Spectroscopy. 1st ed.;Academic Press Inc.:New York,1963;pp 131-138, 255-262,480-495.
(16)Driessens,F.C.M.;van Dijk,J.W.E.;Borggreven,J.M.P.M. Calcif.Tissue Res.1978,26,127.doi:10.1007/BF02013247
(17)Clark,G.C.F.;Williams,D.F.J.Biomed.Mater.Res.1982, 16(2),125.
(18)Ong,J.L.;Lucas,L.C.Biomaterials.1998,19(4-5), 455.doi:10.1016/S0142-9612(97)00224-X
(19)Margolis,H.C.;Moreno,E.C.Calcif.Tissue Int.1992,50(2), 137.doi:10.1007/BF00298791
(20)Chittur,K.K.Biomaterials 1998,19(4-5),357.doi:10.1016/ S0142-9612(97)00223-8
(21)Zhou,J.M.;Shi,N.Applications of Fourier Transform Infrared Spectrometry in Biochemistry.In Modern Fouriertransform Infrared Spectrometry and Its Applications(Part II), 1st ed.;Wu,J.G.Ed.;Literature of Science and Technology Press:Beijing,1994;pp 193-212.[周筠梅,施鼐.傅里葉變換紅外光譜在生物化學中的應用;近代傅里葉變換紅外光譜技術及應用(下卷).吳瑾光主編.北京:科學技術文獻出版社,1994:193-212.]
(22)Alvarez,J.;Haris,P.I.;Lee,D.C.;Chapman,D.Biochimica Et Biophysica Acta 1987,916(1),5.doi:10.1016/0167-4838 (87)90204-4
(23)Xu,C.F.Proteins.In Biochemistry(Book One),2nd ed.;Shen, T.;Wang,J.Y.Eds.;Higher Education Press:Beijing,1990; pp 146-150.[徐長法.生物化學(上冊).沈同,王鏡巖主編.北京:高等教育出版社,1990:146-150.]
(24)Hauschka,P.V.Haemostasis 1986,16(3-4),258.
(25)Prestrelski,S.J.;Byler,D.M.;Thompson,M.P.Biochemistry 1991,30(36),8797.doi:10.1021/bi00100a010
(26)Fronticelli,C.;Bucci,E.;Shamoo,A.E.Biophys.Chem.1984, 19(3),255.doi:10.1016/0301-4622(84)87007-6
(27)Inesi,G.Annu.Rev.Physiol.1985,47,573.doi:10.1146/ annurev.ph.47.030185.003041
(28)Wu,G.R.;Gao,Z.Y.;Dong,A.C.;Yu,S.N.Int.J.Biol. Macromol.2012,50(4),1011.
(29)Zhao,Y.W.;Yang,H.Y.;Meng,K.J.;Yu,S.N.Int.J.Biol. Macromol.2014,64,453.doi:10.1016/j.ijbiomac.2013.12.036
(30)Yu,M.M.Hormones.In Biochemistry(Book One),2nd ed.; Shen,T.,Wang,J.Y.Eds.;Higher Education Press:Beijing, 1990;pp 447-455.[俞梅敏.生物化學(上冊).沈同,王鏡巖主編.北京:高等教育出版社,1990:447-455.]
(31)Morrissey,B.W.;Stromberg,R.R.J.Colloid.Interface Sci. 1974,46(1),152.doi:10.1016/0021-9797(74)90036-8
(32)Lin,Z.Y.;Xue,R.;Ye,Y.W.;Zheng,J.H.;Xu,Z.L.BMC Biotechnol.2009,9,62.doi:10.1186/1472-6750-9-62
(33)Lin,Z.Y.;Ye,Y.W.;Li,Q.L.;Xu,Z.L.;Wang,M.BMC Biotechnol.2011,11,98.doi:10.1186/1472-6750-11-98
(34)Zhou,W.J.;Wang,Y.Applications of Infrared Spectrometry in Basic Researches of Inorganic and Coordination Chemistry.In Modern Fourier-transform Infrared Spectrometry and Its Applications(Part II),1st ed.;Wu,J.G.Ed.;Literature of Science and Technology Press:Beijing,1994;pp 292-296.[周維金,王毅.紅外光譜法在無機和配位化學基礎研究中的應用;近代傅里葉變換紅外光譜技術及應用(下卷).吳瑾光主編.北京:科學技術文獻版社,1994:292-296.]
(35)Barth,A.Prog.Biophys.Mol.Biol.2000,74(3-5),141.doi: 10.1016/S0079-6107(00)00021-3
(36)Farkas,V.;Vass,E.;Hanssens,I.;Majer,Z.;Hollosi,M. Bioorg.Med.Chem.2005,13(17),5310.doi:10.1016/j. bmc.2005.06.040
(37)Rahmelow,K.;Hübner,W.;Ackermann,T.Anal.Biochem. 1998,257(1),1.doi:10.1006/abio.1997.2502
(38)Shai,Y.Biochim.Biophys.Acta-Biomembr.2013,1828(10), 2306.
(39)Kay,M.I.;Young,R.A.;Posner,A.S.Nature 1964,204, 1050.doi:10.1038/2041050a0
(40)Hauschka,P.V.;Carr,S.A.Biochemistry 1982,21(10), 2538.doi:10.1021/bi00539a038
(41)Hauschka,P.V.Osteocalcin and Its Functional Domains.In The Chemistry and Biology of Mineralized Tissues;Butler,W. T.Ed.;EBSCO Media:Birmingham,1985;pp 149-158.
(42)Horbett,T.A.ProteinAdsorption on Biomaterials.In Biomaterials:Interface Phenomena and Applications;Cooper, S.L.,Peppas,N.A.Eds.;American Chemical Society: Washington DC,1982;pp 233-244.
(43)Davies,J.E.The importance and Measurement of Surface Charge Species in Cell Behavior at the Biomaterial Interface. In Surface Characterization of Biomaterials;Ratner,B.D. Ed.;Elsevier:Amsterdam,1988;pp 219-222.
(44)Ono,I.;Gunji,H.;Kaneko,F.;Saito,T.;Kuboki,Y. J.Craniofac.Surg.1995,6(3),238.doi:10.1097/00001665-199505000-00011
(45)El-Ghannam,A.;Ducheyne,P.;Shapiro,I.M.Trans 21st Annual Meeting of Society for Biomaterials 1995,46.
(46)Gungormus,M.;Fong,H.;Kim,I.W.;Evans,J.S.;Tamerler, C.;Sarikaya,M.Biomacromolecules 2008,9(3),966.doi: 10.1021/bm701037x
FTIR-ATR Spectrometry of BSA Adsorption on Hydroxyapatite
YE Qing2HU Ren1ZHOU Jian-Zhang1YE Yi-Wen1XU Zhao-Xi3LIN Chang-Jian1LIN Zhong-Yu1,*
(1State Key Laboratory of Physical Chemistry of Solid Surfaces,Department of Chemistry,College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,Fujian Province,P.R.China;2Chuyang Honors College,Zhejiang Normal University,Jinhua 321004,Zhejiang Province,P.R.China;3Xiamen AERTE System Engineering CO.,LTD,Xiamen 361005,Fujian Province,P.R.China)
The microcosmic process of bovine serum albumin(BSA)adsorbing onto hydroxyapatite(HA)for different time intervals was investigated by Fourier transform infrared attenuated total internal reflectance(FTIRATR)spectrometry.The initial dissolution and re-precipitation of PO43-,Ca2+,and OH-ions from the HAcoating led to the occurrence of the coating including adsorbed BSAon the HA from surface-to subsurface-molecular layers and to in-depth interaction between BSAand HA.The subtraction results gained in the adsorption regions of HAand BSAreveal that the binding of P=O,from the phosphate(PO43-),tothehydrogenof amide II,methyl and methene of the BSA appears to be considerably more rapid and stronger than that of the P―O group.In addition,it is very likely that Ca2+plays an important role in the interaction of BSAwith HA.It appears that the binding of Ca2+to the carbonyl-oxygen of the peptide bond in BSAcaused a significant,molecular,conformationalrearrangement of polypeptide backbones from β-pleated sheet to helical circles of α-helix and β-turn.This change appears to have been followed by much hydrogen of polypeptides being driven to bind PO43-and OH-effectively and much―C=O and H―N―groups of the peptide bond being freed from inter-chain hydrogenbonding to act on Ca2+and combine strongly with the HAsurface.This might reasonably be expected to promote hard tissue regeneration.BSA seems to be activated by the inductive effect of Ca2+via the molecular rearrangement of polypeptide backbones from pleated sheet to helical circles and in turn reacts strongly on the HA,resulting in profound effects on the course of biomineralization.
Biomaterial;Protein adsorption;Polypeptide;IR spectroscopy;FTIR-ATR;Biomineralization
July 2,2015;Revised:November 26,2015;Published on Web:November 30,2015.*Corresponding author.Email:stzylin@xmu.edu.cn;Tel:+86-592-2185956.
The project was supported by the National Natural Science Foundation of China(51571169).
國家自然科學基金(51571169)資助項目
?Editorial office ofActa Physico-Chimica Sinica

