阿瑞匹坦預防化療引起惡心嘔吐的療效及安全性
蘇 丹,趙水喜,曹京旭
?
阿瑞匹坦預防化療引起惡心嘔吐的療效及安全性
蘇 丹,趙水喜,曹京旭
目的 觀察阿瑞匹坦對減輕化療所致惡心嘔吐的療效及安全性。方法 將80例接受含順鉑化療患者隨機分為觀察組和對照組, 觀察組采用阿瑞匹坦與昂丹司瓊、地塞米松聯合止吐, 對照組采用帕洛諾司瓊與昂丹司瓊、地塞米松聯合止吐, 觀察兩組療效及不良反應。結果 觀察組嘔吐的完全緩解率和惡心控制率分別為80%和77.5%,優于對照組的47.5%和37.5%,皆有統計學意義(P<0.01)。兩組中出現最多的不良反應主要有便秘、腹瀉、呃逆、食欲減退、疲乏、失眠、轉氨酶升高等, 均為輕度。結論 阿瑞匹坦對化療所致惡心嘔吐有明顯的預防作用,且不良反應輕,具有臨床應用前景。
阿瑞匹坦 ;化療;嘔吐
化療引起的惡心嘔吐(chemotherapy-induced nausea and vomiting,CINV)是最常見的化療不良反應之一,據統計有70%~80% 的化療患者有惡心嘔吐的經歷[1]。如不能有效控制,可產生一系列的相關并發癥,如脫水、電解質紊亂、營養不良,嚴重者可因消化道黏膜損傷而發生出血、感染甚至死亡。因此,預防或減輕CINV對生活質量的維護、延續治療極其重要[2,3]。NK-1受體阻滯藥阿瑞匹坦于2013-10在中國上市,本研究通過對阿瑞匹坦與長效5HT3受體拮抗藥帕洛諾司瓊預防CINV的療效、不良反應的比較,為臨床提供依據。
1 對象和方法
1.1 對象 我科2013-11至2015-06收治的肺癌患者80例,男40例,女40例,年齡38~69歲,平均(55.21±7.67)歲。入選標準:年齡>18歲,經病理學或細胞學確診,ECOG<2分,既往未接受過化療,化療前心肝腎功能及血常規無異常。排除標準:合并消化道疾病、使用阿片類藥物或有顱腦轉移瘤等可能出現非化療原因導致嘔吐的患者。80例均使用含高致吐化療藥順鉑的化療方案,順鉑劑量70 mg/m2,第1天。按隨機數字表法分為觀察組和對照組各40例,兩組患者年齡、性別、化療方案、病程等方面比較,差異無統計學意義(P<0.05) 。1.2 方法 (1)對照組:鹽酸帕洛諾司瓊注射液 0. 25 mg 靜脈滴入,1次/d,第1天。地塞米松注射液 10 mg 壺入, 1次/d,第1天;5 mg 壺入, 1次/d,第2~4天。鹽酸昂丹司瓊注射液 8 mg 靜脈滴入, 2次/d, 第1~4天。(2)觀察組:阿瑞匹坦膠囊 125 mg口服,1次/d,第1天;80 mg 口服, 1次/d,第2~3天。地塞米松注射液 7.5 mg 壺入, 1次/d, 第1天;3.75 mg 壺入, 1次/d, 第2~4天。鹽酸昂丹司瓊注射液 8 mg 靜脈滴入, 2次/d, 第1~4天。
1.3 判定標準
1.3.1 惡心嚴重程度標準 惡心嚴重程度分級標準按照視覺模擬量表VAS評定[4]。在紙上面劃一條10 cm的橫線,橫線的一端為0,表示無惡心;另一端為10,表示惡心極其嚴重;中間部分表示不同程度的惡心癥狀。無明顯惡心為VAS評分<2.5 cm,無明顯惡心例數/總例數為惡心完全控制率。
1.3.2 止吐療效評定標準 止吐療效評定標準采用中國抗癌協會癌癥康復與姑息治療專業委員會制定的標準[5]:完全緩解(CR),24 h內無嘔吐;部分緩解(PR),24 h嘔吐1~2 次;輕度緩解(MR),24 h嘔吐3~5次;無效(F),24 h嘔吐6次以上。連續觀察120 h。完全緩解例數/總例數×100%為完全緩解率。
1.3.4 不良反應 按照美國癌癥研究所( NCI) 化療毒性分級標準(CTC3.0版)[6]進行觀察和判斷,記錄兩個方案從治療開始到治療結束2 周的不良反應發生情況。
1.4 統計學處理 采用SPSS 21. 0 統計分析軟件對組中數據進行計算,率的比較采用χ2檢驗,P<0.01為差異有統計學意義。
2 結 果
在總觀察期(順鉑使用后0~120 h),急性期(順鉑使用后0~24 h),延遲期(順鉑使用后25~120 h)對阿瑞匹坦膠囊進行了評價。由表1、2可見,在總觀察期,觀察組預防嘔吐的完全緩解率和惡心控制率改善,皆有統計學意義(P<0.01)。延遲期體現出明顯差異,具有統計學意義(P<0.01)。急性期預防嘔吐的完全緩解率亦有差異,但是沒有統計學意義。由表3可見,兩組中出現最多的不良反應主要有便秘、腹瀉、呃逆、食欲減退、疲乏、失眠、轉氨酶升高等, 均為輕度,兩組差別不大。
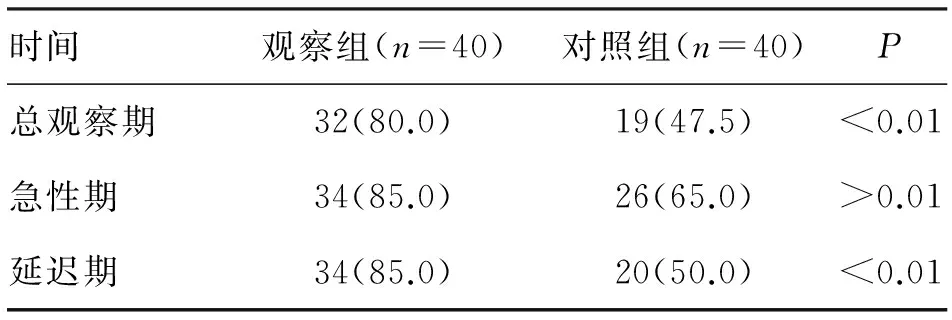
表1 兩組方案預防嘔吐的完全緩解率對比 (n;%)
注:觀察組指阿瑞匹坦膠囊+地塞米松+昂丹司瓊。對照組指鹽酸帕洛諾司瓊+地塞米松+昂丹司瓊
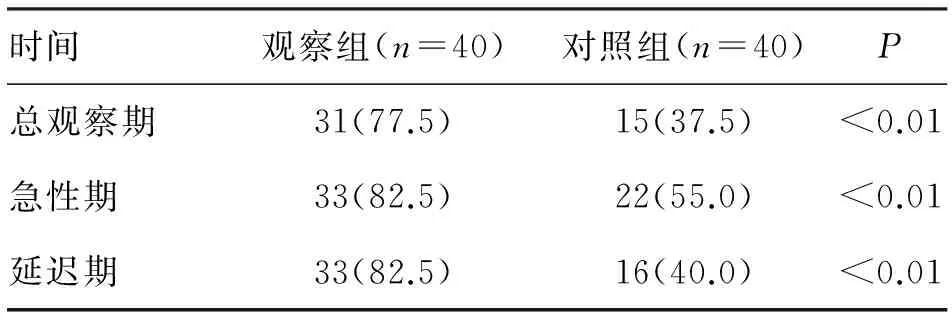
表2 兩組方案預防惡心的完全控制率對比 (n;%)
注:觀察組指阿瑞匹坦膠囊+地塞米松+昂丹司瓊。對照組指鹽酸帕洛諾司瓊+地塞米松+昂丹司瓊
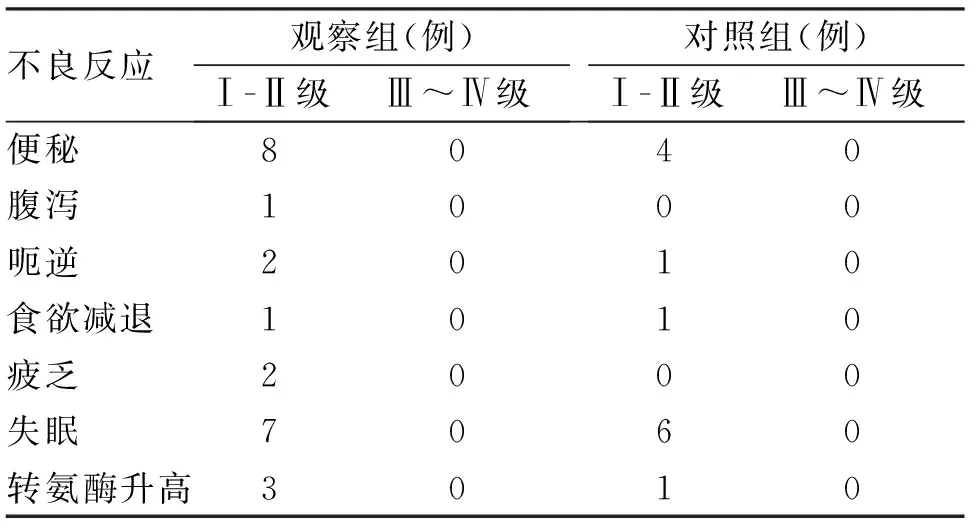
表3 兩組方案最常見的臨床不良反應
注:觀察組指阿瑞匹坦膠囊+地塞米松+昂丹司瓊。對照組指鹽酸帕洛諾司瓊+地塞米松+昂丹司瓊
3 討 論
3.1 CINV的機制及NK-1、5HT3的藥理作用 CINV分為兩個不同的階段存在不同的機制[7]。CINV的急性期階段主要由5HT和5HT3受體系統引起,體內90%的5-HT存在于整個胃腸道的嗜鉻細胞中,5HT3受體也在外周神經系統體內分布于交感與副交感節后神經元和纖維中、腸神經系統的感覺神經元中,在中樞神經系統高度集中于最后區和孤束核的迷走神經傳入纖維末梢。5-HT通過5HT3受體介導外周和中樞神經系統化療嘔吐反射[8]。延遲期階段P物質和NK1受體系統對CINV影響更大[7]。P物質主要由神經細胞和胃腸道等周圍組織器官中,通過與G蛋白偶聯的神經激肽受體結合而發揮生物作用。P物質與5-HT共存于嗜鉻細胞以及腦干孤束核和最后區[9]。5HT3受體拮抗藥及NK-1受體拮抗藥通過選擇性結合其相應抗體進而阻斷嘔吐過程的發生。
3.2 療效、不良反應分析 順鉑在ASCO、MASCC、NCCN的化療指南上被定義為高致吐性化療藥,推薦NK-1受體阻滯藥+5HT3受體阻滯藥+糖皮質激素作為標準止吐方案[10-12]。瑞匹坦是第一個NK-1受體拮抗藥,在國外已廣泛應用于臨床實踐預防CINV,中國上市后尚未有任何數據公布。
國外接受含順鉑的抗腫瘤化療方案中進行的2項隨機對照研究匯總中[13],完全緩解率在總觀察期、急性期、延遲期方面,阿瑞匹坦組對比觀察組分別為60%vs45%(P<0.01),82%vs70%(P<0.01),64%vs47%(P<0.01)。完全緩解率在總觀察期、急性期、延遲期方面,惡心控制率在總觀察期、急性期、延遲期方面,阿瑞匹坦組對比觀察組分別為72%vs65%(P<0.05),91%vs85%(P<0.05),74%vs67%(P<0.05)。本研究中觀察組較對照組在總觀察期及延遲期阿瑞匹坦組嘔吐完全控制率皆明顯提高,惡心控制率也明顯提高,有統計學意義。這與國外文獻報道的結論一致,結果明顯好于國外試驗數據,這可能與連續、多次使用昂丹司瓊配合止吐相關。而在急性期嘔吐控制率兩組相比卻沒有差異,提示瑞匹坦主要對延遲期起關鍵作用。
國外試驗中阿瑞匹坦組顯著高于對照組的不良反應包括:呃逆(4.6%)、ALT升高(2.8%)、消化不良(2.6%)、便秘(2.4%)、頭痛(2.0%)和食欲減退(2.0%)。本組試驗中失眠和便秘在兩組的發生概率都較高,這與糖皮質激素的使用相關。其余不良反應發生較少。因樣本量較少,還需繼續觀察。
綜上所述,阿瑞匹坦能有效預防急性和延遲性化療所致惡心嘔吐,可作為高致吐藥物化療中預防治療惡心嘔吐的首選藥物之一,安全性好值得臨床推廣。為患者順利治療、改善生活質量及提高療效打下基礎。
[1] Ettinger D S,Bierman P J,Bradbury B,etal. Antiemesis[J]. J Natl Compr Canc Netw,2007,5(1):12-33.
[2] Richardson J L, Marks G, Levine A .The influence of symptoms of disease and side effects of treatment on compliance with cancer therapy[J]. J Clin Oncol,1988,6(11):1746-1752.
[3] Bloechl-Daum B, Deuson R R, Mavros P,etal.Delayed nausea and vomiting continue to reduce patients’ quality of life after highly and moderately emetogenic chemotherapy despite antiemetic treatment[J].J Clin Oncol,2006,24(27):4472-4478.
[4] Martin A R, Pearson J D, Cai B,etal. Assessing the impact of chemotherapy-induced nausea and vomiting on patients’ daily lives: a modified version of the Functional Living Index-Emesis (FLIE) with 5-day recall[J]. Support Care Cancer,2003,11:522-527.
[5] 中國抗癌協會癌癥康復與姑息治療專業委員會. 腫瘤治療相關嘔吐防治指南[M].北京: 中國協和醫科大學出版社,2009: 20-42.
[6] Saito M,Aogi K,Sekine L,etal.Palonosetron plus dexamethasone versus granisetron plus dexamethasone for prevention of nausea and vomiting during chemotherapy: a double-blind, double-dummy, randomised, comparative phase III trial[J]. Lancet Oncol,2009,10(2):115-124.
[7] Cubeddu L X. Serotonin mechanisms in chemotherapy- induced emesis in cancer patients[J].Oncology,1996, 1:18-25 .
[8] Wolf H. Preclinical and clinical pharmacology of the 5- HT3 receptor antagonists[J].Scand J Rheumatol Suppl,2000,113:37-45.
[9] 張曉靜,張 頻.腫瘤化療所致惡心嘔吐的發生機制和藥物治療的研究進展[J].癌癥進展,2006,4(4):348-354.
[10] Roila F, Herrstedt J, Aapro M,etal. Guideline update for MASCC and ESMO in the prevention of chemotherapy- and radiotherapy-induced nausea and vomiting: results of the Perugia consensus conference[J]. Ann Oncol, 2010,21(5):232-243.
[11] Basch E, Prestrud A A, Hesketh P J,etal. Antiemetic American Society Clinical Oncology clinical practice guideline update[J].J Clin Oncol, 2011,29:4189-4198.
[12] NCCN Clinical Practice Guidelines in Oncology version 1 2014. Antiemesis[M]. National Comprehensive Cancer Network (NCCN),2014.
[13] Warr D G,Grunberg S M,Gralla R J,etal. The oral NK(1) antagonist aprepitant for the prevention of acute and delayed chemotherapy-induced nausea andvomiting:Pooled data from 2 randomised, double-blind, placebo controlled trials[J].Eur J Cancer,2013,41(9):1278-1285.
(2016-02-23收稿 2016-06-18修回)
(責任編輯 梁秋野)
Efficacy and safety of aprepitant in patients with nausea and vomiting caused by chemotherapy
SU Dan, ZHAO Shuixi, and CAO Jingxu.
Department of Oncology, the General Hospital of Chinese People’s Armed Police Force, Beijing 100039, China
Objective To observe the curative effect and adverse reaction of aprepitant in alleviating nausea and vomiting caused by chemotherapy. Methods 80 patients with cisplatin chemotherapy were randomly divided into study group and control group. The study group used aprepitant combined with the ondansetron hydrochloride, dexamethasone. The control group received palonosetron hydrochlorid combined with ondansetron hydrochloride, and dexamethasone. The curative effect and adverse reactions in the two groups were observed. Results In the study group, complete remission rate and nausea vomiting control rates were 80% and 77.5% respectively, compared with 47.5% and 37.5% in the control group, there was statistically significant difference (P<0.01). In the two groups, the most adverse reactions mainly included constipation, diarrhea, hiccups, anorexia, fatigue, insomnia, transaminase and elevation, were mild. Conclusions Aprepitant has obvious preventive effect on chemotherapy induced nausea and vomiting, and has clinical application prospects.
aprepitant;chemotherapy;vomiting
蘇 丹,本科學歷,主治醫師。
100039 北京,武警總醫院腫瘤一科
趙水喜,E-mail:zhaoshuixi@sina.com
R734.2

