化風丹血清藥物化學的初步研究Δ
向文英,楊 武,梅朝葉,王永林,李勇軍,黃 勇#(.貴州省藥物制劑重點實驗室,貴陽 55000;2.貴州醫科大學藥學院,貴陽 55000;3.國家苗藥工程技術研究中心,貴陽 55000;.民族藥與中藥開發應用教育部工程研究中心,貴陽 55000)
化風丹血清藥物化學的初步研究Δ
向文英1,2,3*,楊武1,2,梅朝葉1,2,王永林1,李勇軍4,黃勇1#(1.貴州省藥物制劑重點實驗室,貴陽550004;2.貴州醫科大學藥學院,貴陽550004;3.國家苗藥工程技術研究中心,貴陽550004;4.民族藥與中藥開發應用教育部工程研究中心,貴陽550004)
目的:對化風丹血清藥物化學進行研究,初步探討其藥效物質基礎。方法:采用超高效液相色譜-飛行時間質譜聯用法,同時建立化風丹提取物以及大鼠ig化風丹(6 g/kg)、藥母(1.37 g/kg)、藥母陰性樣品(5.73 g/kg)提取物后含藥血清的指紋圖譜,分別在正、負離子檢測模式下通過比較化風丹和含藥血清的指紋圖譜,初步鑒定化風丹在大鼠血中移行成分及其代謝產物。結果:在負離子模式下含藥血清中共發現8個藥源性成分(其中3個為原型成分,5個可能為代謝產物),有6個來自藥母;在正離子模式下含藥血清中共發現9個藥源性成分(其中2個為原型成分,7個可能為代謝產物),有6個來自藥母。結論:初步確定了化風丹的入血成分,其入血成分主要來自藥母。
血清藥物化學;化風丹;藥母;指紋圖譜;含藥血清;移行成分;大鼠
化風丹是由牛膽水、白附子、生半夏、生南星、生川烏、郁金、紫蘇葉、僵蠶、天麻等21味藥材組成的復方中藥制劑。方中以獨特發酵工藝制成的藥母(含牛膽水、白附子、生半夏、生南星、生川烏、郁金6味藥材)作為君藥,具有息風鎮痙、活血止痛之功效;天麻、全蝎、僵蠶、白附子等作為臣藥,具有化痰息風,以增強藥母平肝、息風、鎮痙的功效。該藥多用于風痰閉阻、中風偏癱、癲癇、面神經麻痹等癥的治療,是受國務院保護的四大名藥之一[1]。
傳統中藥多為口服給藥,其有效物質必須以血液為介質輸送到靶點,因而給藥后的含藥血清才是真正起作用的“制劑”,血清中含有的成分才是中藥的體內直接作用物質[2]。化風丹為復方純中藥制劑,在中藥組方配伍中君藥是針對病因病機與體質的,是起主要治療作用的藥物;輔藥的作用是協助與加強主藥的功效。而拆方研究也是根據中醫藥理論中復方的組成原則,以達到精簡方劑、增效減毒的目的。因為中藥復方是中醫臨床的基本形式,但是中藥復方成分復雜,很難明確其起治療作用的部位或成分,所以進行中藥復方拆方研究有助于提高中藥質量、指導臨床用藥[3]。目前,國內外對化風丹的藥效物質基礎及其藥理作用機制研究相對薄弱,已成為化風丹深層次開發利用的技術瓶頸,因此,明確化風丹的藥效物質及作用機制具有重要意義,并可對指導臨床合理用藥提供重要依據。本文通過對化風丹進行血清藥物化學研究,為探討化風丹的藥效物質成分奠定實驗基礎。
1 材料
1.1儀器
Agilent 1290 Infinity超高效液相色譜-飛行時間質譜聯用(UPLC-Q-TOF/MS)儀,包括自動進樣器、柱溫箱、DAD二極管陣列檢測器、二元泵(美國Agilent公司);EL204電子分析天平(上海梅特勒-托利多儀器有限公司);Allegra64R低溫高速離心機(美國Beckman公司)。
1.2藥品與試劑
化風丹(批號:20150601,規格:0.12 g/丸)、藥母(褐黑色固體)和由除藥母外其他藥材制成的粉末狀藥母陰性樣品(遵義廖元和堂藥業有限公司,批號:20150401);乙腈(德國默克股份兩合公司,色譜純);甲醇(天津歐密科化學試劑有限公司,色譜純);水為蒸餾水,其余試劑均為分析純。
1.3動物
健康SD成年大鼠,SPF級,♂,體質量(300±20g,購自重慶騰鑫生物技術有限公司[許可證號:SCXK(渝)2012-0008]。
2 方法與結果
2.1溶液的制備
稱取研碎的化風丹成品、藥母和藥母陰性樣品各50g,加入12倍量50%甲醇,回流提取2h,過濾,重復提取3次,合并濾液,旋蒸回收甲醇至無醇味,并濃縮制備成含生藥量均為0.6g/ml的提取藥液,冷藏備用。
2.2空白血清和含藥血清的制備
取健康SD大鼠40只,隨機分為空白組、化風丹組、藥母組和藥母陰性樣品組,每組10只。大鼠禁食不禁水12 h后,根據文獻[4]和前期預實驗結果,化風丹組大鼠ig化風丹提取物6 g/kg,藥母組大鼠ig藥母提取物1.37g/kg,藥母陰性樣品組大鼠ig藥母陰性樣品提取物5.73g/kg,空白組大鼠ig等體積蒸餾水,每天給藥2次,連續給藥3d。末次給藥后1.5 h于股動脈取血,37℃水浴至上層有黃色液體析出后取出,以離心半徑為8cm、5000r/min離心10min,分離血清。同組大鼠血清合并以消除個體差異,然后置于-20℃條件下保存,備用。
2.3血清藥品預處理
取大鼠含藥血清和空白血清各1ml,分別加入4ml甲醇,渦旋2min、超聲10min后以離心半徑為8cm、15 000r/min低溫離心10min,取上清液,37℃氮氣吹干。再加入2ml甲醇于吹干樣品中,按上述處理方法二次沉淀蛋白,取上清液于37℃ 氮氣吹干后,加入200μl甲醇復溶,渦旋2min,超聲10min,再次低溫離心10min。取上清液,即為含藥血清樣品和空白血清樣品,供血清藥物化學研究用。
2.4分析條件
2.4.1色譜條件色譜柱:Agilent Eclipse Plus C18(100mm×2.1 mm,1.8μm);流動相:0.1%甲酸水(A)-0.1%甲酸乙腈(B)(梯度洗脫:0~7min,10%B~25%B;7~10 min,25%B~45%B;10~15min,45%B~65%B;15~18min,65%B~100%B);流速:0.30ml/min;柱溫:40.0℃;進樣量:2μl。
2.4.2質譜條件電噴霧離子源,掃描方式為正、負離子掃描(ESI-、ESI+,m/z:100~1 000);毛細管電壓為4.5kV;錐孔電壓為150V;離子源溫度為110℃;霧化氣(N2)壓力為1.2 bar,流速為8.0 L/min,溫度為200℃;準確質量測定采用甲酸鈉校正標準液,校正模式選用Enhanced Quadratic。數據分析采用Metabolite Detect軟件,運用此軟件將空白血清色譜圖從含藥血清色譜圖扣除,得到其差異圖譜。
2.5血清指紋圖譜共有峰的標定
取“2.2”項下含藥血清樣品6份,按“2.3”項下方法處理后分別進行UPLC-Q-TOF/MS分析。通過對6份來自不同大鼠的含藥血清的指紋圖譜進行分析,在大鼠血清中共標定出9個共有峰(A1~A9),結果見圖1。
2.6方法學考察
2.6.1重復性取“2.2”項下化風丹含藥血清樣品5份,血清樣品按“2.3”項下方法處理后分別進行測定。以A7號峰為參照峰,記錄各峰的保留時間和峰面積,并計算各峰的相對保留時間和相對峰面積。結果,A1~A9號峰相對保留時間的RSD均在1%(n=5)以內,其相對峰面積的RSD均在10%(n=5)以內,表明該方法的重復性較好。
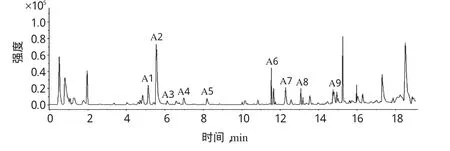
圖1 正離子檢測模式下標定的血清樣品共有峰Fig 1 Common peak of serum samples under positive ion mode
2.6.2精密度取“2.2”項下化風丹含藥血清混合樣品1份,按“2.3”項下處理后分析方法分別進行測定。以A7號峰為參照峰,記錄各峰的保留時間和峰面積,并計算各峰的相對保留時間和相對峰面積。結果,A1~A9號峰相對保留時間的RSD均在1%(n=5)以內,其相對峰面積的RSD均在10%(n=5)以內,表明精密度較好。
2.6.3穩定性取“2.2”項下化風丹含藥血清混合樣品1份,按“2.3”項下方法處理后進樣,分別考察放置0、3、6、9、12 h后樣品的穩定性。以A7號峰為參照峰,記錄各峰的保留時間和峰面積,并計算各峰的相對保留時間和相對峰面積。結果,A1~A9號峰相對保留時間的RSD均在1%(n=5)以內,其相對峰面積的RSD均在10%(n=5)以內,表明樣品在12h內穩定。
2.7正、負離子檢測模式下化學成分及血清樣品分析
2.7.1正離子檢測模式下取離心后化風丹提取物以及按“2.3”項下處理后的各血清樣品,分別按“2.4”項下條件進行UPLC-Q-TOF/MS分析。通過化風丹成品提取物溶液的正離子色譜圖和參考文獻[5-9],得到化風丹提取液正離子檢測模式下質譜信息。與化風丹提取物樣品液保留時間比較,化風丹含藥血清色譜圖中8、9號色譜峰所表征的成分為原型入血成分。與藥母含藥血清、藥母陰性樣品含藥血清色譜圖比較,認定9個血中移行成分中2、4、6、7、8、9號色譜峰所表征的成分來自于君藥藥母;1號色譜峰所表征的成分來自于藥母陰性樣品;而2、4、6號色譜峰所表征的成分在藥母和藥母陰性樣品中都有貢獻。結果表明藥母和藥母陰性樣品對化風丹在體內的直接作用物質均有貢獻。色譜圖詳見圖2、質譜信息見表1。
2.7.2負離子檢測模式下取離心后化風丹提取物以及按“2.3”項下處理后的各血清樣品,分別按“2.4”項下條件進行UPLC-Q-TOF/MS分析。通過化風丹成品提取物溶液的負離子色譜圖和參考文獻[10-11],得到化風丹提取液負離子檢測模式下質譜信息。與化風丹提取物樣品保留時間比較,化風丹含藥血清色譜圖中6、7、8號色譜峰所表征的成分為原型入血成分。與藥母含藥血清、藥母陰性樣品含藥血清與空白血清差異圖譜相比較,認定8個血中移行成分中2、3、5、6、7、8號色譜峰所表征的成分來自于君藥藥母;1號色譜峰所表征的成分來自于藥母陰性樣品;而2、3號色譜峰所表征的成分在藥母和藥母陰性樣品中都有貢獻。除了3個入血原型成分外,其他5個色譜峰所表征的成分可能為大鼠口服藥物提取樣品液后其在體內轉化的代謝產物或機體對藥物產生的應激成分。色譜圖詳見圖3、質譜信息見表2。
3 討論
UPLC是高效液相色譜分析方法中的一種突破性分析方法,具有對復雜樣品的超高分離能力、超高分析速度和超高分析靈敏度,極大地提高了分析工作的效率和質量;而Q-TOFMS是高分辨串聯質譜,能夠精確分析相對分子質量以及可能的分子式與結構[12]。而本研究采用UPLC與Q-TOF/MS聯用建立了一種高效、準確、快速地分析復雜中藥體系化學成分的方法,充分合理地將液相色譜強大的分離能力和質譜的高分辨特點運用在復方中藥體系中。在該方法的分析條件下,18 min內就能將化合物分離完畢。在15 min前有機相的洗脫梯度是在65%以下,梯度比例轉換緩慢;在15~18 min,有機相的洗脫梯度由65%至100%,梯度比例轉換較快,導致色譜圖中基線存在向上飄移的現象,但這對實驗結果不會產生太大影響。
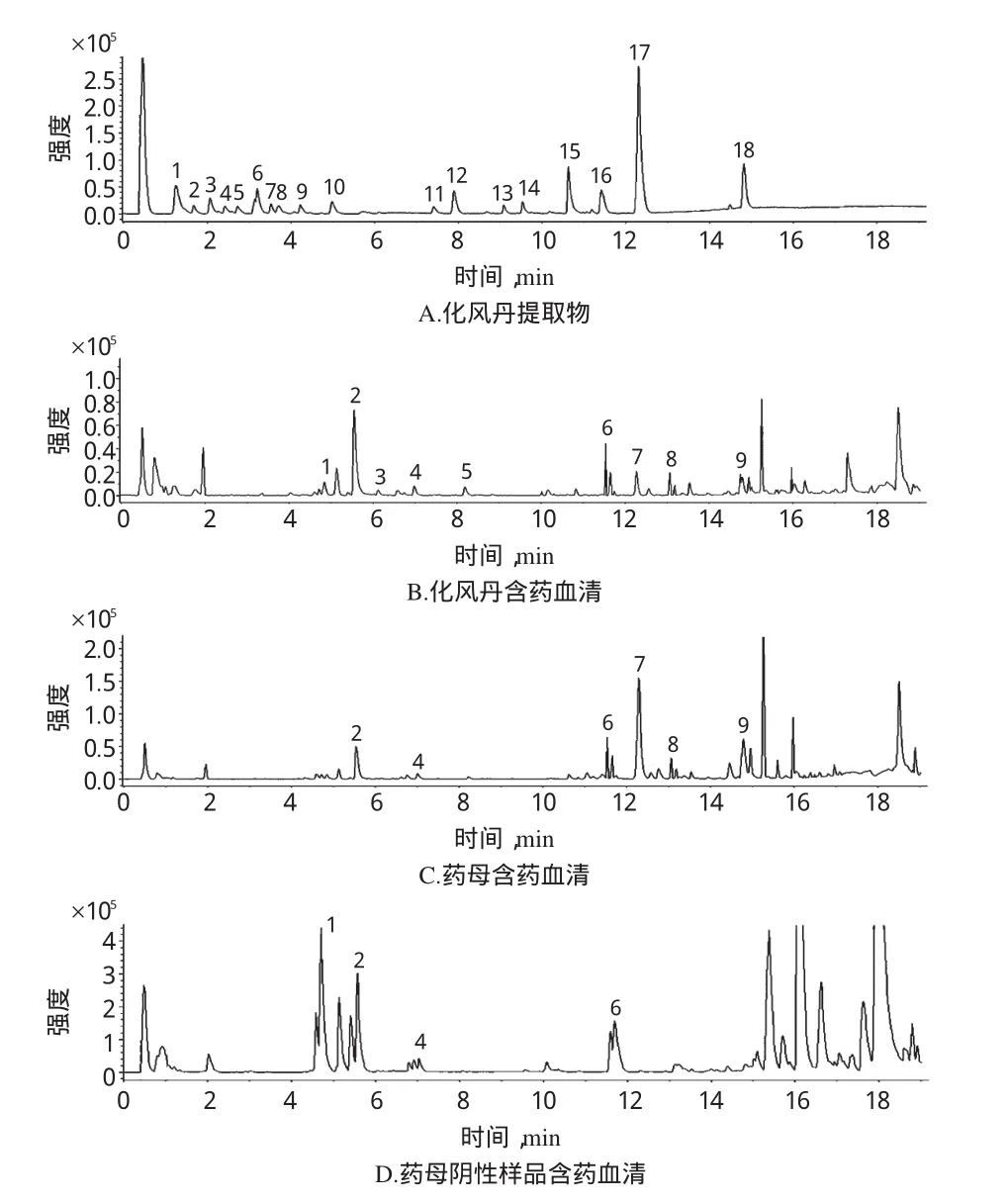
圖2 化風丹提取物及血清樣品液正離子檢測模式色譜圖Fig 2 The positive ion mode chromatogram of Huafengdan extract and drug-cuntaining serum
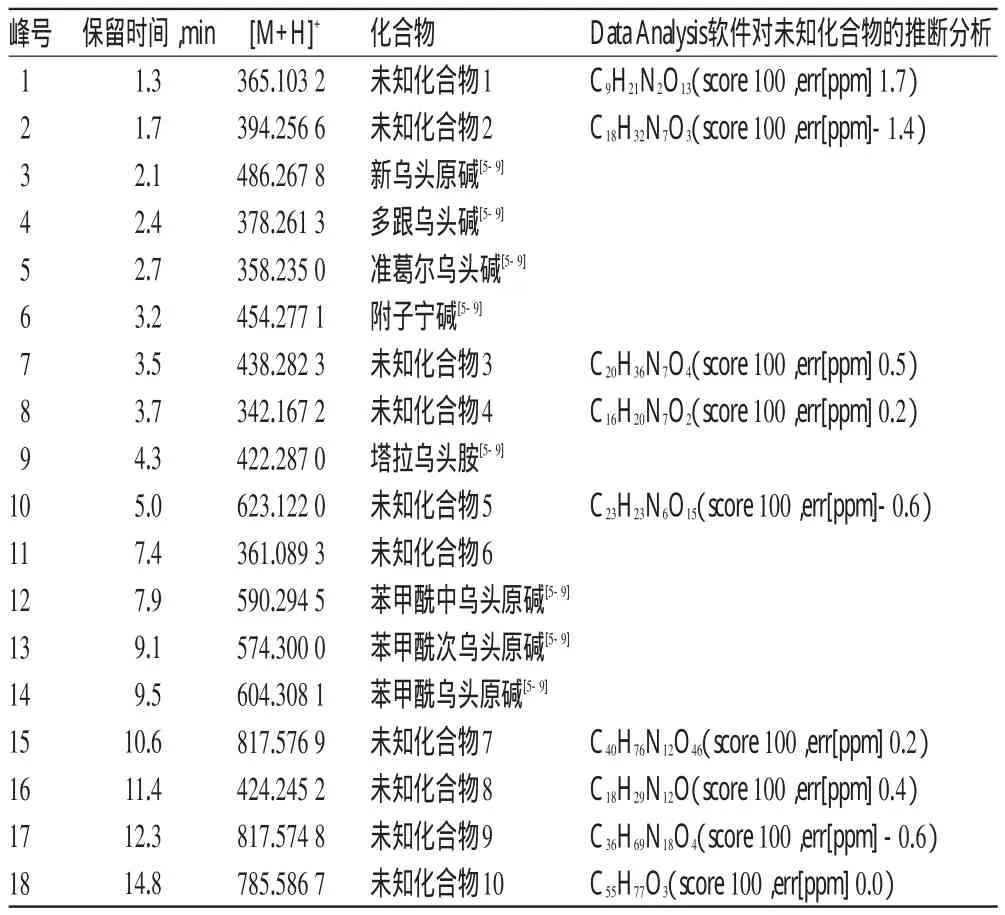
表1 化風丹提取物樣品液正離子檢測模式色譜峰歸屬表Tab 1 The positive ion mode chromatogram peak of Huafengdan extract
化風丹為純中藥復方制劑,因其所含化學成分復雜難以區分且各成分含量差異大,難以對含藥血清中化合物進行認定以及標準品難以獲取等原因給其血清分析帶來極大困難[13]。含藥血清中的原型成分和代謝成分最有可能成為化風丹的藥效物質基礎。在本試驗中,筆者采用正、負離子掃描方式對化風丹提取物樣品液進行全掃描,其在正、負離子模式下均有響應且成分較多。正離子模式下多為生物堿,主要由藥母提供;負離子模式下主要由藥母陰性樣品提供,多為黃酮類。從血清樣品分析結果得出,化風丹含藥血清中都有入血成分存在,而且有較多代謝產物產生。且化風丹血清樣品在正、負離子模式下入血原型成分多與君藥藥母入血原型成分相一致,所以化風丹入血原型成分可能主要由君藥藥母貢獻。本次研究將為進一步明確化風丹藥效物質基礎提供科學依據。
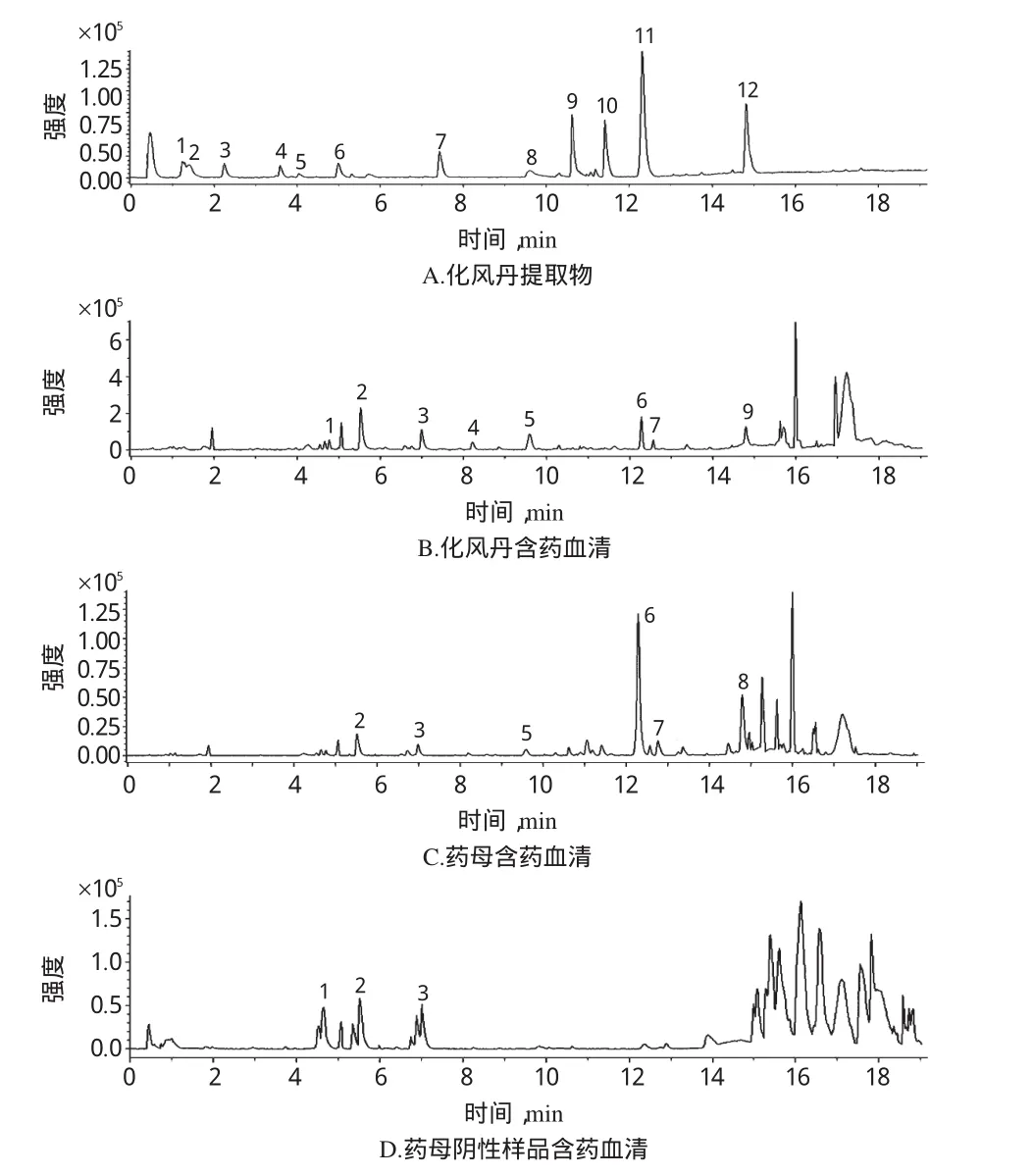
圖3 化風丹提取物及血清樣品液負離子檢測模式色譜圖Fig 3 The negative ion mode chromatogram of Huafengdan extract and drug-cuntaining serum
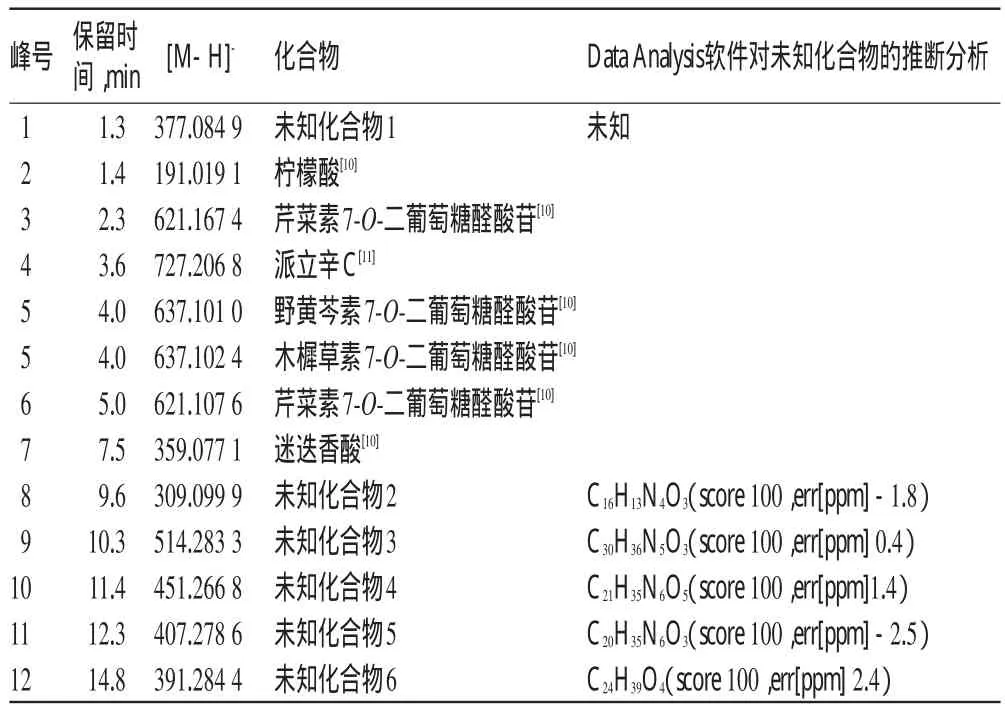
表2 化風丹提取物樣品液負離子檢測模式色譜峰歸屬表Tab 2 The negative ion mode chromatogram peak of Huafengdan extract
[1]營國瓊,張永萍,徐劍,等.化風丹藥母干燥工藝的研究[J].中國民族醫藥雜志,2012,7(7):38.
[2]楊會錦,尹華.中藥血清藥物化學的研究進展[J].中國醫院藥學雜志,2013,33(5):399.
[3]徐彬,陳永剛,吳金虎.中藥復方藥效物質基礎研究的概述[J].醫學綜述,2014,20(1):126.
[4] 朱瓊妮,陸遠富,時京珍,等.含朱砂的萬勝化風丹和氯化汞對大鼠腎轉運體、腎汞蓄積和Kim-1表達的影響[J].中國中藥雜志,2014,39(10):1892.
[5] 王兆基,關錫耀,徐樹棋,等.毒性中藥生川烏質量標準研究[J].中成藥,2006,28(5):651.
[6]程麗麗,許妍妍,張艷軍.中藥川烏多成分同時檢測及藥動學評價研究進展[J].天津中醫藥大學學報,2014,33(1):56.
[7]亞娟.黃花烏頭化學成分研究概況[J].時珍國醫國藥,2006,17(4):638.
[8]郭志勇,呂永磊,許曉嘉,等.炮制對烏頭母根、子根中生物堿類成分的影響與其自身含量差異的比較研究[J].中醫藥學報,2014,42(3):60.
[9]譚漢添.中藥川烏炮制前后的質譜分析[J].醫學信息,2010,23(6):161.
[10]陳永康,趙志剛,孫麗娟.液相色譜-飛行時間質譜法快速鑒定紫蘇葉中的化學成分[J].醫藥導報,2013,32(3):3714.
[11] 王亞男,林生,陳明華,等.天麻水提取物的化學成分研究[J].中國中藥雜志,2012,37(12):1775.
[12] 劉穎坤,喻衛武,白巖.UPLC-ESI-Q-TOF-MS在分析山茱萸化學成分中的應用[J].中國現代應用藥學,2011,28(3):226.
[13]徐述,劉忠良,胡晉紅.藥物腸吸收的實驗研究方法概述[J].中國藥房,2009,20(16):1266.
(編輯:林靜)
Serum Pharmacochemistry Study on Huafengdan
XIANG Wenying1,2,3,YANG Wu1,2,MEI Chaoye1,2,WANG Yonglin1,LI Yongjun4,HUANG Yong1(1.Guizhou Provincial Key Laboratory of Pharmaceutics,Guiyang 550004,China;2.School of Pharmacy,Guizhou Medical University,Guiyang 550004,China;3.National Engineering Research Center of Miao’s Medicines,Guiyang 550004,China;4.Engineering Research Center for the Development and Application of Ethnic Medicine and TCM,Ministry of Education,Guiyang 550004,China)
OBJECTIVE:To study the serum pharmacochemistry of Huafengdan,and to investigate its active component base preliminarily.METHODS:UPLC-Q-TOF/MS was used to establish the fingerprints of Huafengdan and drug-containing serum of rats after intragastric administration of extract of Huafengdan(6 g/kg),Yaomu(1.37 g/kg)and Yaomu negative sample(5.73 g/ kg).The fingerprints of Huafengdan and drug-containing serum were compared under positive and negative ion model,in order to preliminarily indentify the components absorbed into blood and metabolites of Huafengdan.RESULTS:Under negative ion model,8 drug-induced constituents(3 prototype components,5 possible metabolites)were found in drug-containing serum,6 of which were from Yaomu.Under positive ion model,9 drug-induced constituents(2 prototype components,7 possible metabolites)were found in drug-containing serum,6 of which were from Yaomu.CONCLUSIONS:The components absorbed into blood of Huafengdan are confirmed preliminarily and mainly come from Yaomu.
Serum pharmacochemistry;Huafengdan;Yaomu;Fingerprint;Drug-containing serum;Absorbed component;Rats
R285.5
A
1001-0408(2016)28-3911-04
10.6039/j.issn.1001-0408.2016.28.07
國家科技支撐計劃課題(No.2013BAI11B01);貴州省中藥現代化科技產業研究開發專項項目(No.黔科合重G字〔2013〕4001);貴州省高等學校創新能力提升計劃(No.黔教合協同創新字〔2013〕04);貴州省研究生卓越人才計劃項目(No.黔教研合ZYRC字〔2014〕012)
*碩士研究生。研究方向:藥動學。E-mail:852017994@qq.com
教授,碩士生導師,博士。研究方向:中藥活性成分及新藥開發研究。電話:0851-6908899。E-mail:Hujie51619@sina.cn
(2016-01-12
2016-06-15)

