CYP3A5基因型對中國腎移植術后患者體內他克莫司緩釋劑型藥動學參數的影響
陳 攀,傅 茜,李晶潔,孫萍萍,鄧蓉蓉,李 軍,劉曉曼,王洪陽,黃 民,陳 孝,王長希
(中山大學 1.附屬第一醫院藥學部臨床藥學室、2. 附屬第一醫院器官移植中心、3. 臨床藥理研究所,廣東 廣州 510080;4. 中山大學附屬第六醫院生殖醫學中心,廣東 廣州 510655)
?
CYP3A5基因型對中國腎移植術后患者體內他克莫司緩釋劑型藥動學參數的影響
陳 攀1,傅 茜2,李晶潔4,孫萍萍1,鄧蓉蓉1,李 軍2,劉曉曼3,王洪陽2,黃 民3,陳 孝1,王長希2
(中山大學 1.附屬第一醫院藥學部臨床藥學室、2. 附屬第一醫院器官移植中心、3. 臨床藥理研究所,廣東 廣州 510080;4. 中山大學附屬第六醫院生殖醫學中心,廣東 廣州 510655)
目的 研究CYP3A5基因型對中國腎移植術后患者體內他克莫司緩釋劑型藥動學參數的影響。方法 采用化學發光免疫法檢測20例腎移植術后患者在服用緩釋(10例)和普通劑型(10例)他克莫司后的全血濃度;采用聚合酶鏈反應-限制性片段長度多態法檢測服用緩釋劑型他克莫司患者的CYP3A5基因型;緩釋劑型組檢測0~24 h的11個時間點的血藥濃度,而普通劑型檢測0~12 h內的10個時間點的血藥濃度。結果 無劑量校正的緩釋劑型組的AUC0~24 h為普通劑型組AUC0~12 h的1.78倍,有劑量校正的緩釋劑型組的C0為普通劑型的60%,其余藥動學參數差異無顯著性;緩釋劑型中慢代謝型組的Cmax、AUC0~24 h和C0分別為快代謝型組的1.75、1.96、2.49倍(無劑量校正)以及1.80、2.34和2.64倍(有劑量校正);緩釋劑型組的C0與AUC0~24 h的相關性良好。結論 他克莫司普通劑型轉換至緩釋劑型時應該注意上調給藥劑量,同時緩釋劑型應結合CYP3A5的基因型檢測,確保C0值在治療窗范圍內。
他克莫司;緩釋劑型;腎移植;CYP3A5;藥代動力學;基因多態性;免疫抑制劑
他克莫司是目前臨床上最常用的鈣調磷酸酶抑制劑,但該藥存在明顯的個體間及個體內藥動學差異,且治療窗狹窄[1-2]。現有他克莫司劑型包括普通與緩釋2種,給藥頻次分別為1 d 2次與1 d 1次[3]。影響他克莫司血藥濃度的重要因素之一為CYP3A5 6986A>G位點的基因多態性,CYP3A5*1/*1和CYP3A5*1/*3基因型相比CYP3A5*3/*3具有明顯的CYP3A5酶活性,能快速代謝他克莫司,導致其體內濃度相對較低[4]。目前,國內尚無CYP3A5基因多態性對他克莫司緩釋劑型藥動學特征的報道,本實驗在腎移植術后腎功能穩定的患者中比較CYP3A5基因多態性與緩釋劑型這2個因素對他克莫司藥動學特征的影響,為中國腎移植術后患者提供他克莫司用藥參考。
1 對象與方法
1.1 受試對象的選擇 本研究納入2013~2014年于中山大學附屬第一醫院器官移植中心進行腎移植手術的患者,共20例。其中,他克莫司緩釋劑型組與普通劑型組各10例。
1.1.1 入選標準 ① 首次腎移植;② 單一器官移植;③ 年齡18~60歲,性別不限;④ 肝功能正常;⑤ 采用他克莫司+霉酚酸酯+糖皮質激素三聯免疫抑制治療方案。
1.1.2 排除標準 ① 難以控制的嚴重感染(細菌、真菌、病毒感染);② 惡性腫瘤患者、糖尿病患者、人類免疫缺陷病毒攜帶者;③ 多器官移植;④ 術前群體反應性抗體(PRA)>20%;⑤ 慢性腸炎、慢性腹瀉者;⑥ 有嚴重的心肺功能不全、肝硬化病史;⑦ 處于妊娠期或計劃在1年內懷孕者;⑧ 唑類抗真菌類藥物(氟康唑、伊曲康唑等)、五酯片、抗結核藥物等已知與FK506相互作用的藥物。
本研究方案經中山大學附屬第一醫院醫學倫理委員會討論并批準。所有受試者均在入組前簽署知情同意書。
1.2 他克莫司采血時間點選擇與濃度檢測 緩釋劑型的采血時間點為0、0.5、1、1.5、2、3、4、6、9、12、24 h,共11個時間點,而普通劑型的采血時間點為0、0.5、1、1.5、2、3、4、6、9、12 h,共10個時間點。每個時間點采集外周靜脈血2 mL,置于肝素化抗凝真空管中,采用化學發光免疫法檢測他克莫司全血濃度。為便于比較, 對他克莫司的濃度進行劑量校正,校正濃度=全血濃度·體質量·劑量-1。
1.3 CYP3A5基因型檢測 于給藥前1 d,取患者外周靜脈血2 mL,參照Loparev等[5]的碘化鈉-氯仿法提取基因組DNA。CYP3A5*3(6986 A>G)的基因型沿用本實驗室采用的聚合酶鏈反應-限制性片段長度多態(polymerase chain reaction-restriction fragment length polymorphism, PCR-RFLP) 法檢測[6]。
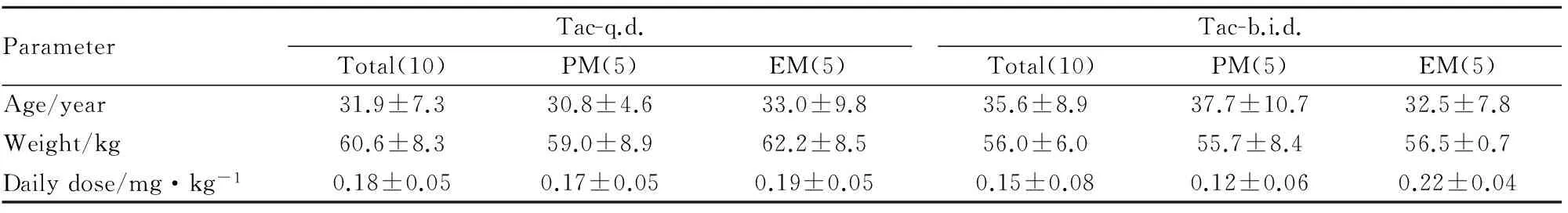
Tab 1 Demographics of enrolled patients and daily dose of tacrolimus
2 結果
2.1 受試患者一般信息與給藥劑量 如Tab 1所示,此次納入實驗的受試者共20例,其中緩釋劑型和普通劑型各10例,均根據CYP3A5 6986A>G的多態性分為快代謝型和慢代謝型組,各5例。各組別之間在年齡、體質量差異均無顯著性。普通劑型組中,快代謝型組的給藥劑量是慢代謝型組的1.8倍(P<0.05)。
2.2 他克莫司緩釋劑型與普通劑型在腎移植術后患者中的藥代動力學參數 Fig 1為腎移植術后患者中分別服用他克莫司緩釋劑型和普通劑型的劑量校正血藥濃度-時間曲線。從Tab 2可以得出,在血藥濃度無劑量校正情況下,緩釋劑型與普通劑型組的Tmax、Cmax和C0差異均沒有顯著性,而緩釋劑型組的AUC0~24 h為普通劑型組AUC0~12 h的1.78倍。在劑量校正情況下,相比緩釋劑型,普通劑型的Tmax與AUC有下降趨勢,但差異無顯著性,同時緩釋劑型的C0為普通劑型的60%。
2.3 他克莫司緩釋劑型在不同CYP3A5基因型腎移植術后患者中的藥代動力學參數 Fig 2為不同CYP3A5基因型的腎移植術后患者服用他克莫司緩釋劑型后的劑量校正血藥濃度-時間曲線。從Tab 3可以看出,在血藥濃度無劑量校正情況下,緩釋劑型的慢代謝型組和快代謝組的Tmax差異無顯著性,而慢代謝組的Cmax、AUC0~24 h和C0相比快代謝型組,分別上調了1.75、1.96和2.49倍。在有劑量校正的情況下,兩組的Tmax差異無顯著性,但慢代謝組的Cmax、AUC0~24 h和C0相比快代謝型組,分別上調了1.80、2.34和2.64倍。
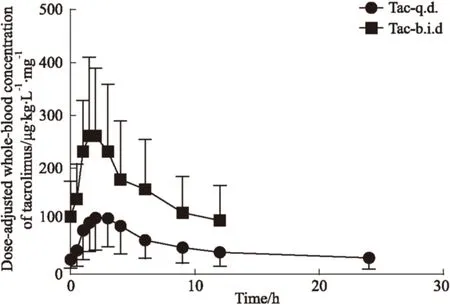
Fig 1 Dose-adjusted ±s whole-blood concentration-time
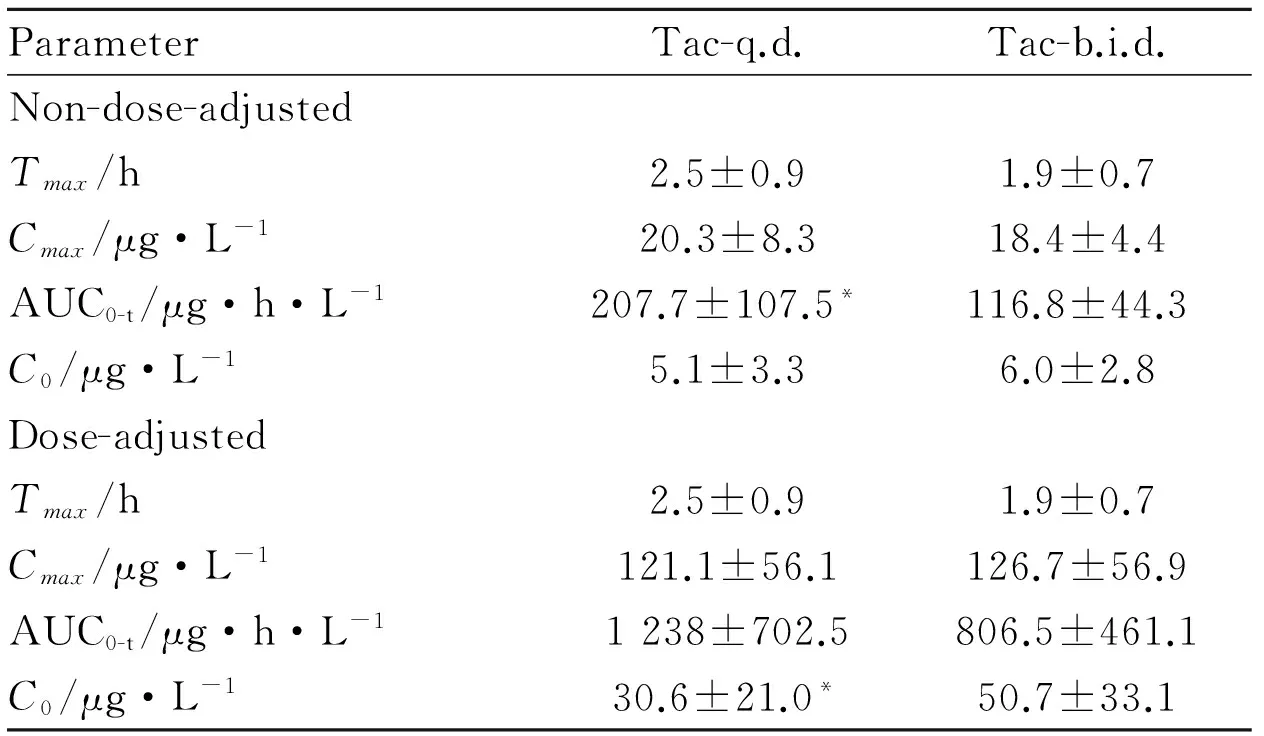
ParameterTac-q.d.Tac-b.i.d.Non-dose-adjustedTmax/h2.5±0.91.9±0.7Cmax/μg·L-120.3±8.318.4±4.4AUC0-t/μg·h·L-1207.7±107.5*116.8±44.3C0/μg·L-15.1±3.36.0±2.8Dose-adjustedTmax/h2.5±0.91.9±0.7Cmax/μg·L-1121.1±56.1126.7±56.9AUC0-t/μg·h·L-11238±702.5806.5±461.1C0/μg·L-130.6±21.0*50.7±33.1
*P<0.05vsTac-b.i.d
2.4 不同CYP3A5基因型的腎移植術后患者口服他克莫司緩釋或普通劑型后的AUC0-t與C0的相關性 由Tab 4可以得出,在血藥濃度無劑量校正情況下,緩釋劑型組的AUC0-t和C0的相關性好于普通劑型組,相關系數分別為0.94和0.78,其中緩釋慢代謝組與快代謝的相關系數差異無顯著性(0.89與0.91)。在劑量校正情況下,普通與緩釋劑型組的AUC0-t和C0均呈現良好的相關性。
3 討論
他克莫司的藥動學個體差異性大,且治療窗相對窄,使得該藥成為臨床上最為常見的需要開展個體化用藥的藥物之一[1,7]。影響他克莫司藥動學的因素較多,包括基因多態性、肝功能、胃腸道功能、飲食、聯合用藥、用藥依從性等[8]。其中,他克莫司緩釋劑型開發的主要目的就是提高患者的用藥依從性,從1 d 2次的給藥頻次改進到1 d 1次,但在相同日劑量情況下,患者服用緩釋與普通劑型后體內的AUC與C0是否一致存在爭論[3]。生產廠家推薦劑型轉換時的劑量比為1 ∶1,而且提出該種劑型轉換對他克莫司的體內暴露水平無影響[9-11]。但近年的一些國外臨床試驗發現相同劑量下,緩釋劑型的C0與AUC下降至普通劑型的25%,因此建議在轉換劑型時應該相應上調緩釋劑型的給藥劑量[12-14]。在本實驗中,我們發現在中國腎移植術后患者中,緩釋劑型的劑量校正C0值相比普通劑型下降占比為0.4,同時分析發現C0與AUC0-t的相關性良好。因此,建議患者將普通劑型轉換為緩釋劑型服用的時候,應該注意相應上調給藥劑量,并在轉換期間密切監測C0濃度。
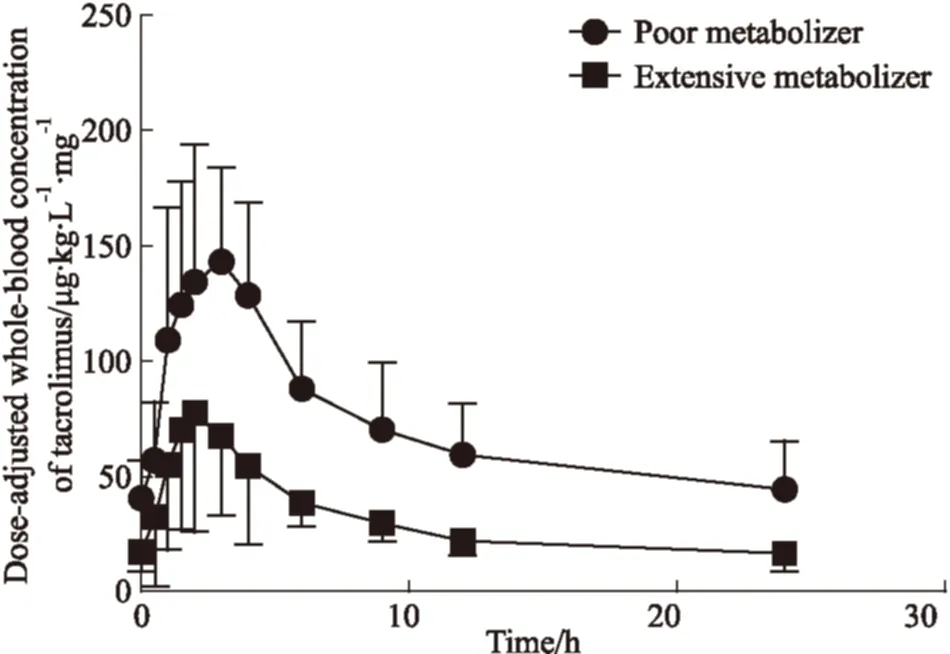
Fig 2 Dose-adjusted ±s whole-blood concentration-time curves
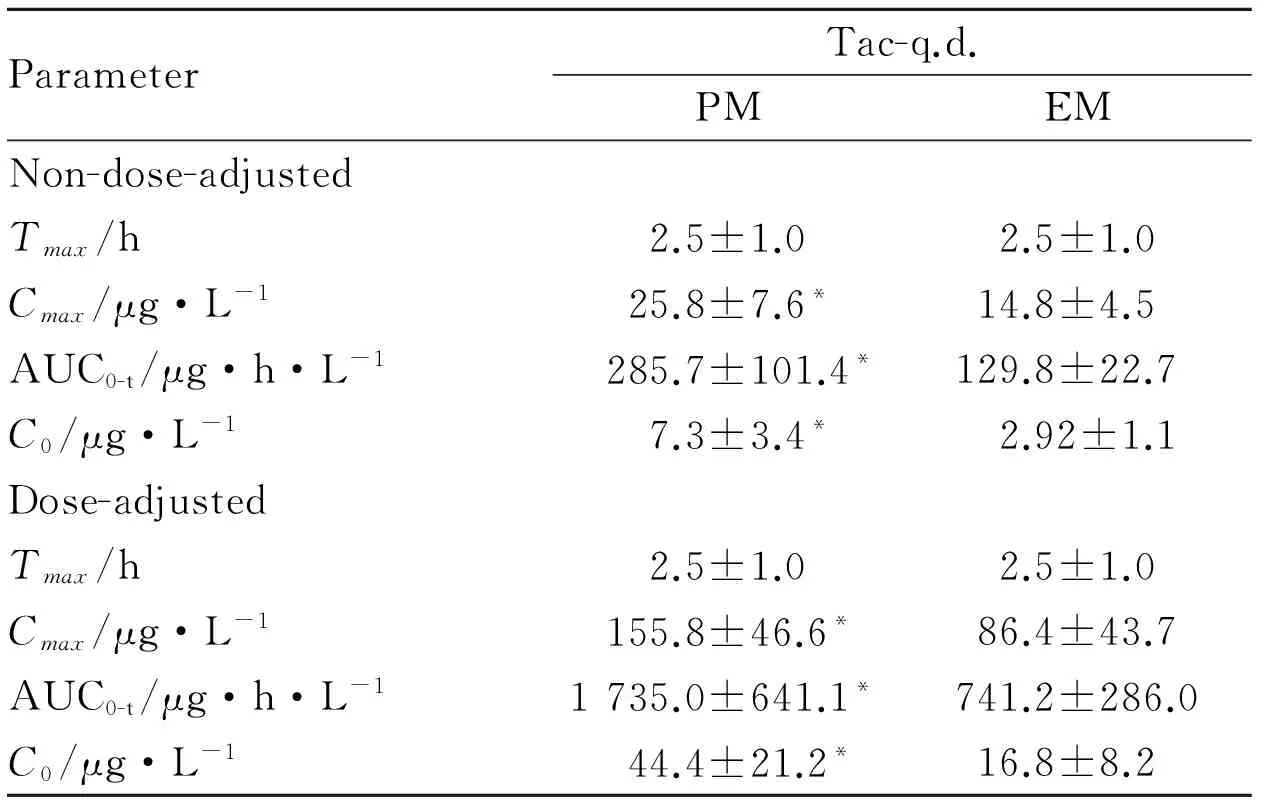
ParameterTac-q.d.PMEMNon-dose-adjustedTmax/h2.5±1.02.5±1.0Cmax/μg·L-125.8±7.6*14.8±4.5AUC0-t/μg·h·L-1285.7±101.4*129.8±22.7C0/μg·L-17.3±3.4*2.92±1.1Dose-adjustedTmax/h2.5±1.02.5±1.0Cmax/μg·L-1155.8±46.6*86.4±43.7AUC0-t/μg·h·L-11735.0±641.1*741.2±286.0C0/μg·L-144.4±21.2*16.8±8.2
*P<0.05vsEM
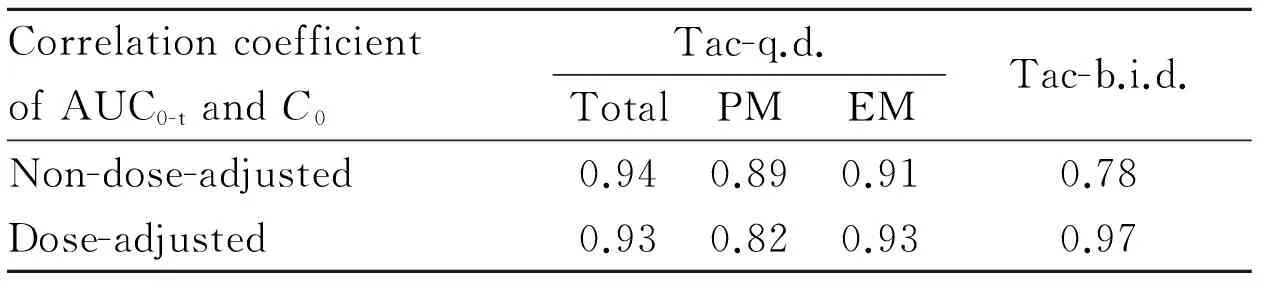
Tab 4 Linear relationship between AUC0-t
CYP3A5 6986A>G位點的多態性在很大程度上影響了他克莫司給藥劑量的制定,在免疫抑制劑的個體化給藥過程中,患者通常需要在移植術前采血檢測其CYP3A5的基因型來確定初始給藥劑量。目前,國內尚無CYP3A5的基因型對緩釋型他克莫司藥動學行為的影響研究。本實驗發現無論劑量有無校正,其藥動學特征的相對趨勢沒有改變,均體現為慢代謝型組的Cmax、AUC0-t和C0值高于快代謝組。此外,有研究提出相比普通劑型,緩釋劑型他克莫司主要延緩腸道的吸收程度,因此,緩釋劑型更大程度上會受到腸道CYP3A5的影響[3,15],這提示患者在應用緩釋劑型他克莫司時,更需要根據CYP3A5的基因型制定給藥劑量。
鑒于本實驗的樣本量相對較少,雖然有看到一些藥動學參數的改變趨勢,但統計分析差異并無顯著性,因此,仍需在后續研究中擴大樣本量。同時,除CYP3A5外,ABCB1的基因多態性也為報道較多的能夠影響他克莫司的因素[4],因此,后續研究也應該納入ABCB1的基因型分析,從而更好制定緩釋劑型他克莫司的個體化給藥劑量。
綜上所述,本實驗表明緩釋劑型他克莫司相比普通劑型,更適合采用C0作為治療藥物的監測指標。此外,在將普通劑型轉換至緩釋劑型的時候,應該注意上調他克莫司給藥劑量,同時結合CYP3A5的基因型檢測,確保C0在治療窗范圍內。
(致謝:本研究在中山大學附屬第一醫院器官移植二區完成血樣及臨床數據收集,在中山大學附屬第一醫院藥學部及中山大學臨床藥理研究所實驗室完成血藥濃度及基因型檢測工作,數據統計分析得到來自中山大學附屬第六醫院的李晶潔幫助,感謝上述人員對本研究給予支持和幫助。)
[1] Schiff J, Cole E, Cantarovich M.Therapeutic monitoring of calcineurin inhibitors for the nephrologist[J].ClinJAmSocNephrol, 2007, 2(2): 374-84.
[2] 陳長仁, 何發忠, 周宏灝, 等.精準醫學的基礎研究與臨床轉化[J].中國藥理學通報, 2015,31(12):1629-32.
[2] Chen C R, He F Z, Zhou H H, et al, Basic research and clinical translation of precision medicine[J].ChinPharmacolBull, 2015,31(12): 1629-32.
[3] Barraclough K A, Isbel N M, Johnson D W,et al.Once-versus twice-daily tacrolimus: are the formulations truly equivalent?[J].Drugs, 2011, 71(12):1561-77.
[4] Macphee I A, Fredericks S, Tai T,et al.Tacrolimus pharmacogenetics: polymorphisms associated with expression of cytochrome p450 3A5 and P-glycoprotein correlate with dose requirement[J].Transplantation, 2002, 74(11): 1486-9.
[5] Loparev V N, Cartas M A, Monken C E,et al.An efficient and simple method of DNA extraction from whole blood and cell lines to identify infectious agents[J].JVirolMethods, 1991, 34(1): 105-12.
[6] Wang Y, Wang C, Li J,et al.Effect of genetic polymorphisms of CYP3A5 and MDR1 on cyclosporine concentration during the early stage after renal transplantation in Chinese patients co-treated with diltiazem[J].EurJClinPharmacol, 2009, 65(3):239-47.
[7] 陳 冰, 蔡衛民.群體藥動學在免疫抑制劑合理用藥中的應用[J].中國藥理學通報, 2010,26(2): 159-63.
[7] Chen B, Cai W M. Application of population pharmacokinetics in the rational usage of immunosuppressive drugs[J].ChinPharmacolBull, 2010,26(2): 159-63.
[8] Staatz C E, Tett S E.Clinical pharmacokinetics and pharmacodynamics of tacrolimus in solid organ transplantation[J].ClinPharmacokinet, 2004, 43(10): 623-53.
[9] Alloway R, Steinberg S, Khalil K,et al.Conversion of stable kidney transplant recipients from a twice daily prograf-based regimen to a once daily modified release tacrolimus-based regimen[J].TransplantProc, 2005, 37(2): 867-70.
[10]Alloway R, Steinberg S, Khalil K,et al.Two years postconversion from a prograf-based regimen to a once-daily tacrolimus extended-release formulation in stable kidney transplant recipients[J].Transplantation, 2007,83(12): 1648-51.
[11]Florman S, Alloway R, Kalayoglu M,et al.Conversion of stable liver transplant recipients from a twice-daily prograf-based regimen to a once-daily modified release tacrolimus-based regimen[J].TransplantProc, 2005, 37(2): 1211-3.
[12]Wlodarczyk Z, Squifflet J P,Ostrowski M,et al.Pharmacokinetics for once- versus twice-daily tacrolimus formulations in de novo kidney transplantation: a randomized, open-label trial[J].AmJTransplant, 2009, 9(11): 2505-13.
[13]de Jonge H, Kuypers D R, Verbeke K,et al.Reduced C0concentrations and increased dose requirements in renal allograft recipients converted to the novel once-daily tacrolimus formulation[J].Transplantation, 2010, 90(5): 523-9.
[14]Satoh S, Niioka T, Kagaya H,et al.Pharmacokinetic and CYP3A5 pharmacogenetic differences between once- and twice-daily tacrolimus from the first dosing day to 1 year after renal transplantation[J].Pharmacogenomics, 2014, 15(11): 1495-506.
[15]Niioka T, Satoh S, Kagaya H,et al.Comparison of pharmacokinetics and pharmacogenetics of once- and twice-daily tacrolimus in the early stage after renal transplantation[J].Transplantation, 2012, 94(10): 1013-9.
Impact of CYP3A5 genetic polymorphism on modified releasing tacrolimus pharmacokinetics in Chinese renal transplant recipients
CHEN Pan1, FU Qian2, LI Jing-jie4, SUN Ping-ping1, DENG Rong-rong1,LI Jun2, LIU Xiao-man3, WANG Hong-yang2, HUANG Min3, CHEN Xiao1, WANG Chang-xi2
(1.DeptofPharmacy,theFirstAffiliatedHospitalofSunYat-senUniversity,2.OrganTransplantCenter,theFirstAffiliatedHospitalofSunYat-senUniversity,3.InstituteofClinicalPharmacology,SunYat-senUniversity,Guangzhou510080,China;4.ReproductiveCenter,theSixthAffiliatedHospitalofSunYat-senUniversity,Guangzhou510655,China)
Aim To investigate the impact of CYP3A5 genetic polymorphism on modified releasing tacrolimus pharmacokinetics in Chinese stable renal transplant recipients.Methods Pharmacokinetics of once daily-tacrolimus(tac-q.d.) and twice daily-tacrolimus(tac-b.i.d.) were determined by CLIA, CYP3A5 genotype was measured by PCR-RFLP. Each 10 patients receiving tac-q.d. and tac-b.i.d. respectively were enrolled, and each 5 patients receiving tac-q.d. were matched to poor metabolizer (PM) and extensive metabolizer (EM) group respectively according to CYP3A5 genotypes.Results AUC0~24 hfor tac-q.d. was 1.78 folds higher than AUC0~12 hfor tac-b.i.d., and dose-adjustedC0was 40% lower for tac-q.d. than for tac-b.i.d. There were no significant differences for other parameters between the two groups;Cmax, AUC0~24 handC0were 1.75, 1.96 and 2.49 folds higher for PM than for EM, and dose-adjustedCmax,AUC0~24 handC0were 1.80, 2.34 and 2.64 folds higher for PM than for EM. There were good correlations between AUC0~24 handC0for tac-q.d.Conclusion Conversion from tac-b.i.d. to tac-q.d. results in requirement of increased tacrolimus dose and detection of CYP3A5 genotype, which is necessary for ensuringC0in the range of therapeutic window.
tacrolimus; modified release; renal transplantation; CYP3A5; pharmacokinetics;genetic polymorphism; immunosuppressant
2016-07-12,
2016-08-05
國家自然科學基金資助項目(No 81503156);廣東省自然科學基金博士啟動項目(No 2014A030310096);廣東省公益基金項目(No 2016A020218006)
陳 攀(1985-),男,博士,主管藥師,研究方向:臨床藥學,E-mail:cepa1@163.com;
王長希(1963-),男,博士,主任醫師,教授,研究方向:器官移植,通訊作者,E-mail:13600450862@163.com
時間:2016-10-20 10:29
http://www.cnki.net/kcms/detail/34.1086.R.20161020.1029.042.html
10.3969/j.issn.1001-1978.2016.11.021
A
1001-1978(2016)11-1592-04
R345.99;R392.2;R394.2;R699.2;R969.1;R944.9;R979.5

