體外研究人臍帶血間充質干細胞對大鼠枯否細胞極化的影響
李 亮,彭 瓊,蔡亦紅,戴 夫
?
體外研究人臍帶血間充質干細胞對大鼠枯否細胞極化的影響
李 亮1,彭 瓊1,蔡亦紅2,戴 夫1
目的 采用脂多糖(LPS)誘導大鼠枯否細胞(KCs)發生極化改變,之后用人臍帶血間充質干細胞(huMSCs)與LPS誘導的KCs在Transwell內共培養,以觀察huMSCs對KCs極化偏移的調節作用。方法 實驗分為KCs組、KCs+LPS組、KCs+LPS+MSCs組。對各組的白介素-4(IL-4)、腫瘤壞死因子(TNF-α)、白介素-10(IL-10)、白介素-6(IL-6)等上清因子采用ELISA法進行檢測;誘導型一氧化氮合酶(iNOS)、精氨酸酶-1(Arg-1)、信號傳導與轉錄激活因子3、6(STAT-3、STAT-6)、核因子kappaB(NF-κB)用Western bolt進行檢測,同時用熒光實時定量PCR(qRT-PCR)對以上結果進行驗證。結果 KCs+LPS組促炎因子TNF-α、IL-6分泌增加,KCs+LPS+MSCs組抑炎因子IL-10、IL-4分泌增加;而Western blot檢測表明,KCs+LPS組中iNOS升高,NF-κB p65入核增高;而KCs+LPS+MSCs組高表達Arg-1,同時pSTAT-3、pSTAT-6表達增加。結論 huMSCs能誘導已經發生M1極化的KCs向M2表型偏移,考慮可能與huMSCs分泌細胞因子有關,起到一種免疫調節作用,huMSCs調節巨噬細胞極化的分子機制可能與通過JAK-STAT信號轉導通路有關。
枯否細胞;人間充質干細胞;免疫調節;極化
間充質干細胞(mesenchymal stem cell,MSCs)取材方便,易于體外培養增殖,除了多向分化能力,還具有獨特免疫特性,因此MSCs移植有希望成為很多疾病治療的有效手段。越來越多的研究者認為MSCs分泌的細胞因子和免疫調節對肝臟損傷起主要作用[1]。另外MSCs分泌的細胞因子也具有強大的調節作用。近年來MSCs對巨噬細胞的免疫調節作用的研究也成為熱點。巨噬細胞參與對抗病原體的第一道防線,各組織的巨噬細胞具有相對特異性,肝臟的巨噬細胞稱為KCs,占肝臟非實質細胞的0.35,占生物體所有實質臟器的巨噬細胞總數的0.8~0.9[2],對各種肝臟疾病的發病與轉歸起重要作用。成熟巨噬細胞在不同的微環境中可被誘導分化出不同的表型和功能狀態,稱為巨噬細胞的極化。目前很多研究[3-5]已經證實MSCs能促進巨噬細胞向M2方向極化,所以研究巨噬細胞極化機制對治療各種肝病具有重要意義。目前人臍帶血間充質干細胞(human umbilical cord blood mesenchymal stem cells,huMSCs)和大鼠KCs體外共培養尚無報道,該實驗首先提取大鼠原代KCs,并觀察huMSCs在體外對大鼠KCs偏移極化的影響。
1 材料與方法
1.1 實驗動物及細胞 普通級健康雄性SD大鼠20只,8~10周齡,(200±20) g,購于蘇州工業園區愛爾麥特科技有限公司,室溫下自由進食標準顆粒飼料、衛生飲水,實驗前12 h禁食,6 h前禁水。huMSCs為合肥市濱湖醫院干細胞中心劉尚全教授饋贈。
1.2 主要試劑和儀器 青霉素、鏈霉素、胰酶細胞消化液和谷氨酰胺(上海碧云天生物技術研究公司);胎牛血清(杭州四季青生物工程材料有限公司);Percoll細胞分離液、臺盼藍(美國Sigma公司);APC-CD68抗體(美國eBioscience公司);HEPA Class l00二氧化碳培養箱(美國Termo electron corporation);TSl00倒置顯微鏡(日本Nikon公司);IX51 熒光倒置顯微鏡(日本Olympus公司);AllegraX-30R梯度離心機(美國Beckman Coulter公司);6孔細胞培養板和Transwell(美國Corning公司);PCR試劑盒(美國AXYGEN公司);Revert Aid First Strand cDNA Synthesis Kit (加拿大Fermentas公司);PCR Master Mix和二抗 tetramethylrhodamine goat-anti-rabbit IgG(美國Promega公司);SYBR Premix Ex TaqTMⅡ(日本TaKaRa公司);TRIzol(美國Invitrogen公司);一抗anti-iNOS和anti-STAT6(美國BD Transduction Laboratories公司);anti-Arg 1、anti-NF-κB p65(美國Santa Cruz公司),免疫熒光一抗NF-κB p65抗體(英國Abcam公司);核蛋白提取試劑盒NucBuster Protein Extraction Kit(德國Novagen公司);磷酸化酶/蛋白酶抑制劑 Protease/Phosphatase Inhibitor Cocktail (美國Cell Signaling公司)。
1.3 大鼠原代KCs的提取及鑒定 SD大鼠吸入乙醚麻醉,酒精消毒,放于無菌托盤,打開腹部和胸腔至見到肝、肺、心臟等器官,結扎下腔靜脈,行門靜脈插管,以15 ml/min速度灌注PBS液10 min,0.5 mg/ml濃度的IV型膠原酶20 ml原位灌注10 min,取肝臟并剪碎至1 mm小塊。0.5 mg/ml IV型膠原酶30 ml震蕩消化(37 ℃)。用細胞濾網(200目)濾過,去除未消化的肝臟組織。肝臟細胞懸液300 r/min離心5 min(4 ℃),離心2次,棄上清液除去殘留消化酶,再次1 550 r/min離心5 min(4 ℃),取沉渣重懸,0.30和0.60 percoll密度梯度1 850 r/min離心20 min(20 ℃);取出乳白色細胞層,利用KCs貼壁特性進一步純化,純化后細胞以2×106/孔鋪板,進一步用于后續實驗。臺盼藍染色實驗:細胞提取后,立即以10 μl細胞懸液和90 μl 0.4%臺盼藍充分混勻,2~3 min后,取10 μl至計數板,臺盼藍染色實驗后顯微鏡下觀察計數。吞墨實驗:用培養24 h后的細胞加入經過濾紙多次過濾并高壓滅菌過的墨汁,6 h后顯微鏡下觀察細胞的吞噬能力。可見細胞內充滿大小不一的黑色顆粒,但細胞仍然存活。
1.4 流式細胞術檢測細胞表面標志物 收集KCs,調整細胞濃度為(1~2)×106/ml,取50 μl細胞懸液,加入2 μl FITC-CD68,低速振蕩5 s、混勻,室溫下避光孵育20 min后,加適量PBS洗1次,上流式細胞儀進行檢測。
1.5 huMSCs與 KCs在 Transwell內共培養 將KCs細胞以1×106/ml鋪到Transwell(0.4 μm孔徑)的下層,并加入終濃度為1 μg/ml的LPS,培養18 h后,將huMSCs以1×105/孔鋪到Transwell板的上層,將二者共培養18 h,同時設置正常培養的KCs組及加入LPS誘導的KCs組以及KCs+LPS+MSCs組。huMSCs和KCs共培養時,KCs+LPS組同時加等量DMEM作對照,分別收集各組培養18 h上清液、18 h KCs細胞蛋白、RNA以便進行后續實驗。
1.6 ELISA試劑盒檢測上清液相關細胞因子 收集各組上清液,用ELISA試劑盒分別檢測IL-6、IL-10、IL-4、TNF-α細胞因子的水平。采用終濃度為1 μg/ml的LPS與KCs共培養18 h,再與等量DMEM或者huMSCs 共培養18 h后檢測各組IL-4、IL-6、IL-10細胞因子水平。而TNF-α為Transwell內與huMSCs共培養18 h后,再以終濃度為1 μg/ml的LPS誘導6 h后再檢測。
1.7 Western blot檢測iNOS、Arg-1、STAT3、p-STAT3、STAT6、p-STAT6、NF-κB p65蛋白表達 實驗各組KCs中加入磷酸化酶/蛋白酶抑制劑,加入裂解緩沖液提取總蛋白,并按試劑盒說明提取核蛋白。將提取蛋白按100 μg/孔加樣,置于SDS-PAGE凝膠上電泳分離,在硝酸纖維素膜上進行轉膜、電轉、TBST清洗硝酸纖維素膜3次后移至含有封閉液的平皿中,稀釋一抗(1 ∶500)后孵育2 h,后進行二抗孵育(1 ∶1 000),最后化學發光,顯影,定影,將膠片進行掃描,用凝膠圖象處理系統(Image J)分析目標帶的分子量和凈光密度值。用全蛋白裂解液檢測目的蛋白表達,用GAPDH為內參照;用核蛋白裂解液檢測細胞核內NF-κB p65水平,用Histone為內參照。
1.8 熒光實時定量PCR分析M1/M2相關基因轉錄水平 收集各組的KCs細胞總RNA用逆轉錄試劑盒逆轉錄合成cDNA,設計引物,用SYBR Green PCR mix試劑盒分別檢測IL-10、IL-6、iNOS、Arg-1 mRNA水平,引物見表1。

表1 熒光實時定量PCR所用引物序列
2 結果
2.1 SD大鼠KCs鑒定 剛提取的KCs成圓形或者橢圓形,透光性好,大小均勻,可見微量雜細胞。臺盼藍染色后經細胞計數,細胞活力為(0.931 1±0.009)(n=3)。培養48 h后可見細胞貼壁,變得形狀不規則,部分細胞呈梭形。培養1周后可見大部分細胞形態更加不規則,貼壁牢固,透光性較前略差。臺盼藍染色實驗、吞墨實驗以及流式細胞術鑒定細胞活力及純度,經檢測活力及純度均大于0.92,可用于下一步實驗,結果見圖1。
2.2 各組培養上清液中細胞因子的表達 KCs+LPS組中的KCs經LPS刺激后,促炎因子TNF-α分泌增加,KCs+LPS+MSCs組中的IL-10、IL-4分泌增加。說明KCs+LPS+MSCs組中的KCs高分泌抗炎因子IL-4和IL-10,結果見圖2。
2.3 各組蛋白表達情況 KCs+LPS組高表達iNOS,而KCs+LPS+MSCs組高表達Arg-1,KCs+LPS+MSCs組可誘導STAT3/STAT6磷酸化;而KCs+LPS組可誘導NF-κB p65磷酸化,促進其核轉位,見圖3。通過收集KCs+LPS+MSCs組及KCs+LPS組細胞24 h后的細胞全蛋白裂解液,經Western blot檢測,以正常細胞為陰性對照。實驗結果表明,KCs+LPS+MSCs組高表達Arg-1,低表達iNOS;而KCs+LPS組高表達iNOS,低表達Arg-1,見圖3。
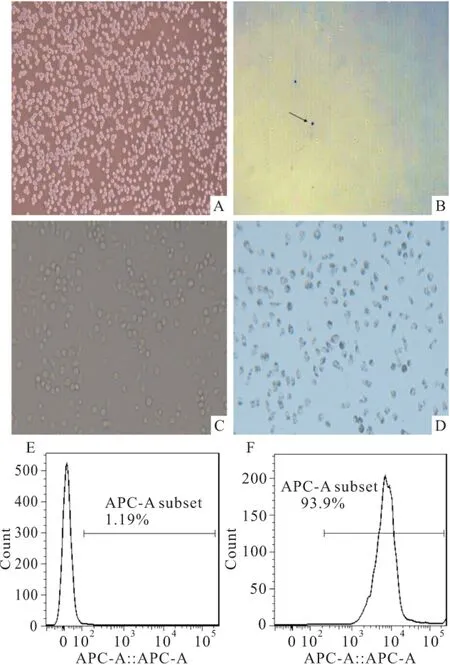
圖1 SD大鼠KCs的鑒定
A:新提取原代細胞培養6 h KCs×100;B:KCs臺盼藍染色圖×100;C:原代培養48 h KCs×200;D: KCs吞墨實驗;E:未經CD68染色的正常細胞作為空白對照組;F:CD68流式抗體染色,經流式細胞儀檢測,分析細胞的純度大于92%(n=3)
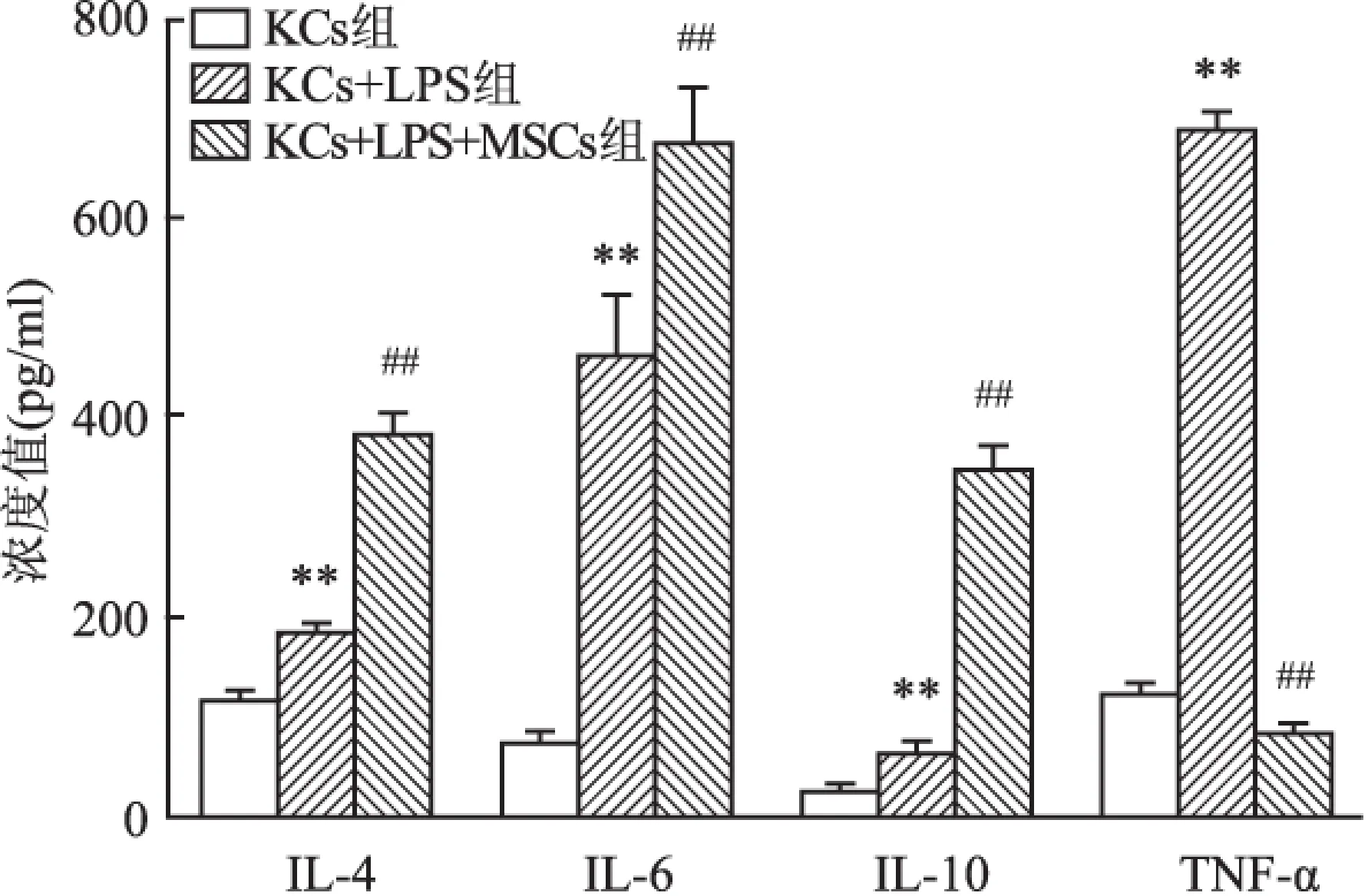
圖2 各組上清液中細胞因子水平 (n=3)
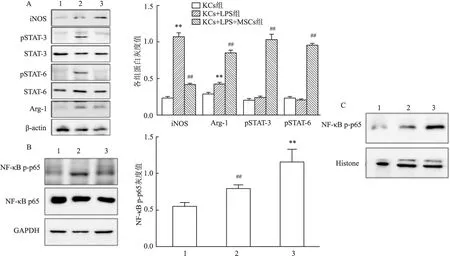
圖3 各組相關細胞因子表達量A:各組收集全細胞裂解液用相應的抗體進行蛋白印跡實驗;用灰度測定法定量分析蛋白印跡結果并進行比較;B:實驗各組收集細胞全蛋白裂解液(檢測NF-κB p65、NF-κB p-p65);各組收集細胞核蛋白裂解液(NF-κB p65);用灰度測定法定量分析核內蛋白印跡NF-κB p-p65結果;C:收集細胞核蛋白裂解液(檢測NF-κB p65);1:KCs組;2:KCs+LPS+MSCs組;3:KCs+LPS組;與KCs組比較: **P<0.01;與KCs+LPS組比較:##P<0.01
2.4 各組iNOS、Arg-1、IL-10、IL-6 mRNA水平 通過熒光實時定量PCR對以上結果中iNOS、Arg-1、IL-10、IL-6 mRNA表達水平進行驗證,結果顯示,KCs+LPS+MSCs組高表達Arg-1、IL-10 mRNA,而KCs+LPS組高表達iNOS mRNA。KCs+LPS組與KCs+LPS+MSCs組IL-6 mRNA水平差異無統計學意義,見圖4。
2.5 huMSCs促進大鼠KCs向M2方向轉化 當用LPS誘導KCs時,KCs高表達TNF-α,并且Westein blot檢測結果顯示iNOS高表達,提示KCs經LPS誘導后可以成功向M1表型轉化。在此基礎上,用huMSCs與極化的KCs共培養,KCs+LPS+MSCs組高表達Arg-1,并且上清液細胞因子IL-10、IL-4濃度明顯增加,提示KCs向M2方向極化。以上結果經熒光實時定量PCR鑒定,提示KCs表型發生改變。為進一步研究表型轉化機制,從胞質蛋白中提取STAT-3、STAT-6、pSTAT-3、pSTAT-6以及在核內和核外提取NF-κB p65。結果顯示,在靜息狀態時,NF-κB p65蛋白主要是位于細胞質內,LPS能刺激NF-κB p65核轉位增加,但與huMSCs共培養時發現其入核減弱,而NF-κB p-p65入核增多,弱化了炎性基因表達,提示其參與了KCs的表型轉化。因此,可以得知MSCs通過分泌細胞因子調節KCs表型轉化。
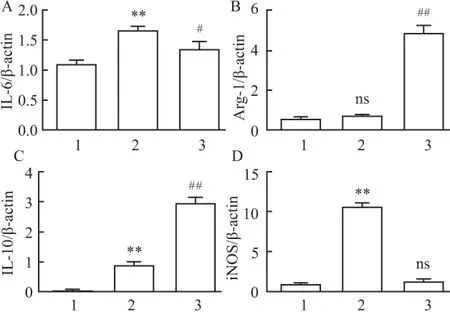
圖4 各組同一時間點收集細胞后提取RNA,應用實時定量PCR分析相關基因的mRNA水平
1:KCs組;2:KCs+LPS組;3: KCs+LPS+MSCs組;與KCs組比較:**P<0.01;與KCs+LPS組比較:#P<0.05,##P<0.01
3 討論
有研究者利用人骨髓MSCs治療豬的爆發性肝衰竭[6],所以利用不同種系的細胞共培養具有可行性。當肝臟發生急性炎癥變化時,MSCs條件培養基能改變白細胞浸潤,通過分泌營養因子減少肝細胞凋亡,增加肝細胞的增殖,進一步發揮對炎癥部位進行修復作用。MSCs可以引起調節性T細胞的增加并減少樹突細胞分泌TNF-α,Th1細胞分泌IFN-α和Th-2細胞分泌IL-4[7]。不論外源性或者內源性MSCs對巨噬細胞的極化起到明顯調節作用。目前,根據巨噬細胞的功能和表型分為經典活化的M1型極化和選擇性活化的M2型極化,經典激活途徑的巨噬細胞通常可以由LPS、干擾素α、腫瘤壞死因子和粒細胞-巨噬細胞集落刺激因子誘導M1方向極化,主要參與體內炎癥反應,有促炎作用,能高分泌IL-1、IL-6、TNF-α,具有高IL-12、IL-23、低IL-10表型。而旁路激活途徑的巨噬細胞具有清除寄生蟲,促進組織修復,促進血管形成及腫瘤發展的作用。具有高IL-10、低IL-12、IL-23表型,高水平清道夫受體,CD206并高表達Arg-1[8],類似于T細胞亞群Th1和Th2亞群在炎癥中的變化。眾所周知,LPS能誘導巨噬細胞向經典的M1型巨噬細胞偏移,但是近年巨噬細胞極化后在乙型病毒性感染所致的肝纖維化中發揮重要作用[9]。M2型巨噬細胞在酒精性肝病中促進肝細胞衰老[10],所以采用huMSCs對LPS已經誘導M1型巨噬細胞進行干預來研究KCs的偏移極化。
本實驗在Transwell內共培養huMSCs和KCs兩種細胞,用huMSCs和經LPS誘導后的KCs共培養證明實驗組IL-10、IL-4分泌增加,體外研究表明MSCs能夠通過分泌IL-10、IL-4部分促進巨噬細胞激活途徑改變,并發現MSCs分泌前列腺素E2與前列腺素E2受體亞型EP4作用后可以增加巨噬細胞IL-10的分泌,熒光實時定量PCR驗證結果提示KCs分泌細胞抗炎因子IL-4、IL-10增加。本實驗中ELISA檢測提示IL-6在實驗組升高,而M2表型的枯否細胞多為IL-6分泌減少,近年來發現MSCs也存在不同表型[11],因此,MSCs不同表型是否對巨噬細胞極化有影響值得進一步研究。從上清液TNF-α以及iNOS表達增加看,經LPS誘導后部分細胞已經發生M1極化,再與huMSCs細胞共培養后,經本實驗驗證,提示可以進一步發生M2極化偏移,這可能反映從炎癥到修復的一個過程,巨噬細胞M1和M2極化代表了一個廣泛的、連續的巨噬細胞功能狀態[12],與不同表型的巨噬細胞在不同炎癥階段發揮不同作用相符。但也有研究[13]表明M2極化的巨噬細胞能促進M1細胞凋亡,調節肝臟炎癥反應。這說明不同表型的巨噬細胞來源及作用和調節機制需要進一步證實和驗證。
目前肝臟疾病中巨噬細胞的個體發生情況仍不清楚,巨噬細胞發生極化的分子機制很復雜,包括多種信號通路參與其中,激活NF-κB和STAT1主要促進M1巨噬細胞極化,而STAT3和STAT6激活促進巨噬細胞M2極化進一步發揮其免疫功能[14]。其中NF-κB信號蛋白的激活對于M1型巨噬細胞偏移極化非常重要。NF-κB家族含有5個成員:p50、p52、p65(RELA)、RELB和REL蛋白,這些蛋白二聚化可引發NF-κB的入核增加,促進炎癥因子表達,同時也參與細胞的生存和凋亡過程。NF-κB檢測結果提示經LPS誘導后,激活M1型巨噬細胞并產生相關炎癥介質如TNF-α升高,iNOS表達增加。在試驗中當LPS刺激后,NF-κB p65入核增多,但與huMSCs共培養時發現其入核減弱,提示其參與了KCs的表型轉化。體外實驗已經明確提示MSCs能誘導巨噬細胞發生M2極化,本研究結果顯示KCs+LPS+MSCs組pSTAT-3、pSTAT-6蛋白合成增加,提示其信號轉導途徑與JAK-STAT信號通路有關。STAT-6是IL-4介導的信號通路主要效應蛋白分子[15],這與本實驗中IL-4升高是一致的,IL-4的升高通過各種途徑進一步促進核內基因表達,介導M2細胞分化成熟[16]。M2型巨噬細胞可以通過Arg-1水解精氨酸,產生鳥氨酸,鳥氨酸是脯氨酸和多肽前體,與纖維化疾病相關。
總的來說,本實驗證明了huMSCs分泌的可溶性因子誘導大鼠KCs向M2表型的轉化,這一過程通過調節巨噬細胞JAK-STAT信號通路實現。但是,由于巨噬細胞極化的分子機制相當復雜,需要進一步實驗驗證。目前明確的是MSCs分泌的細胞因子及免疫調節作用是明確的,對進一步研究huMSCs應用于終末期肝病的治療有明確的意義,同時也說明了MSCs細胞治療具有獨特的免疫優勢,可以用于多種疾病的免疫治療。
[1] Meirelles Lda S,Fontes A M,Covas D T.et al.Mechanisms involved in the therapeutic properties of mesenchymal stem cells[J].Cytokine Growth Factor Rev,2009,20(5-6):419-27.
[2] Liaskou E,Wilson D V,Oo Y H.Innate immune cells in liver inflammation[J].Mediators Inflamm,2012,2012:949157.
[3] Zhang Q Z,Su W R,Shi S H, et al.Human ingiva-derived mesenchymal stem cells elicit polarization of m2 macrophages and enhance cutaneous wound healing[J].Stem Cells,2010,28(10):1856-68.
[4] Kim J,Hematti P.Mesenchymal stem cell-educated macrophages:a novel type of alternatively activated macrophages[J].Exp Hematol,2009,37(12):1445-53.
[5] Dayan V,Yannarelli G,Billia F,et al.Mesenchymal stromal cells mediate a switch to alternatively activated monocytes/macrophages after acute myocardial infarction[J].Basic Res Cardiol,2011,106(6):1299-310.
[6] Li J,Zhang L,Xin J, et al.Immediate intraportal transplantation of human bone marrow mesenchymal stem cells prevents death from fulminant hepatic failure in pigs[J].Hepatology,2012,56(3):1044-52.
[7] Fibbe W E,Nauta A J,Roelofs H. Modulation of immune responses by mesenchymal stem cells[J].Ann N Y Acad Sci,2007,1106:272-8.
[8] Locati M, Mantovani A, Sica A. Macrophage activation and polarization as an adaptive component of innate immunity[J]. Adv Immunol,2013,120:163-84.
[9] Moses T B,Cheng L,Zhang Z,et al.Hepatitis B virus infection and immunopathogenesis in a humanized mouse model: induction of human-specific liver fibrosis and M2-like macrophages[J].PLoS Pathog,2014,10(3):e1004032.
[10] Wan J, Benkdane M, Alons E,et al.M2 Kupffer cells promote hepatocyte senescence an IL-6-dependent protective mechanism against alcoholic liver disease[J].Am J Pathol,2014,184(6):1763-72.
[11] Waterman R S,Tomchuck S L,Henkle S L,et al.A new mesenchymal stem cell (MSCs) paradigm: polarization into a pro-inflammatory MSCs1 or an immunosuppressive MSCs2 phenotype[J].PLoS One,2010,5(4):e10088.
[12] Biswas S K,Mantovani A.Orchestration of metabolism by macrophages[J].Cell Metab,2012,15(4):432-7.
[13] Wan J,Benkdane M,Teixeira-Clerc F,et al.M2 Kupffer cells promote M1 Kupffer cell apoptosis: a protective mechanism against alcoholic and non-alcoholic fatty liver disease[J].Hepatology,2014;59(1):130-42.
[14] Sica A,Mantovani A.Macrophage plasticity and polarization:invivoveritas[J].J Clin Invest,2012,122(3):787-95.
[15] Goenka S,Kaplan M H.Transcriptional regulation by STAT6[J].Immunol Res,2011,50(1):87-96.
[16] Ishii M,Wen H,Corsa C A, et al.Epigenetic regulation of the alternatively activated macrophage phenotype[J].Blood,2009,114(15):3244-54.
Li Liang1,Peng Qiong1,Cai Yihong2,et al
[1DeptofGastroenterology,TheThirdAffiliatedHospitalofAnhuiMedicalUniversity(TheFirstPeople’sHospitalofHefei),Hefei230001;2SchoolofPublicHealth,AnhuiMedicalUniversity,Hefei230032]
The effect of human umbilical cord blood mesenchymal stem cells on the polarization of rat Kupffer cellsinvitro
ObjectiveLPS-stimulatedKupffercells(KCs)andhumanumbilicalcordbloodmesenchymalstemcells(huMSCs)wereco-culturedinTranswelltoobservetheeffectofhuMSCsonthepolarizationofKCs.MethodsDuringthisstudy,themodelofhuMSCsin vitroco-culturingwithKCswasbuilt,andthreegroupswereassigned,whichwereKCsgroup(normalgroup),KCscells+LPSgroup(controlgroup),KCs+LPS+MSCsgroup(experimentalgroup).Amongthethreegroups,IL-4,TNF-α,IL-10,IL-6weredetectedbyELISAwhileinduciblenitricoxidesynthase(iNOS),arginase-1(Arg-1),phosphorylationreactionlevelofsignaltransducerandactivatoroftranscription-3,6(STAT-3,STAT-6)andnuclearfactor-κB(NF-κB)weredetectedbyWesternbolt.Afterthat,qRT-PCTwasadoptedtocheckthepreviousresults.ResultsItwasfoundthatbothTNF-αandIL-6secretionincreasedinthecontrolgroup,whilebothIL-10andIL-4secretionincreasedintheexperimentalgroup.WesternblotdetectionshowedthatthelevelofiNOSincreasedinthecontrolgroup,NF-κBp65increasedinthenucleus,whiletheexperimentalgroupwashighexpressionofArg-1,pSTAT-6,pSTAT-3.ConclusionOurexperiment’sfindingsindicatethathuMSCscaninducealternativeactivationofKCs,andtheactivationpathwaymightbetheJAK-STATpathways.
mesenchymalstemcells;Kupffercells;polarization;signalingpathway
時間:2015-12-30 14:38
http://www.cnki.net/kcms/detail/34.1065.R.20151230.1438.020.html
國家自然科學基金(編號:81101272)
1安徽醫科大學第三附屬醫院(合肥市第一人民醫院)消化內科, 合肥 230001
2安徽醫科大學公共衛生學院, 合肥 230032
李 亮,男,碩士研究生;
戴 夫,男,教授,主任醫師,博士生導師,責任作者,E-mail:hfsdf@sina.com
R 318.06
A
1000-1492(2016)01-0041-06
2015-10-12接收

