全自動化學發(fā)光免疫分析儀檢測肝纖維化指標的方法學性能驗證
黃永攀 韋榮國 覃 政 李 靈 宋波權(quán)
全自動化學發(fā)光免疫分析儀檢測肝纖維化指標的方法學性能驗證
黃永攀①韋榮國①覃 政②李 靈③宋波權(quán)①
目的:對新產(chǎn)業(yè)MAGLUMI全自動化學發(fā)光免疫分析儀檢測肝纖維化指標的方法學性能進行驗證。方法:按照美國臨床實驗室標準化協(xié)會(CLSI)推薦方法測定的生物參考區(qū)間指標,采用MAGLUMI4000化學發(fā)光免疫分析儀對檢測肝纖維化指標透明質(zhì)酸(HA)、層粘連蛋白(LN)、Ⅲ型前膠原氨基端肽(PⅢNP)、Ⅳ型膠原(C Ⅳ)的批內(nèi)和日間精密度、準確度、線性范圍及靈敏度等進行驗證。結(jié)果:MAGLUMI分析儀測定HA、LN、PⅢNP、C Ⅳ批內(nèi)和日間精密度變異系數(shù)(CV)分別為3.01%~4.82%和3.77%~4.69%;相對偏倚(%)為-5.3%~0.2%;測定線性范圍與廠商要求相近;HA、LN、PⅢN-P和C Ⅳ的測定數(shù)值與廠商提供的參考區(qū)間符合,檢測的靈敏度分別為1.30 ng/ml、0.9 ng/ml、0.49 ng/ml和0.54 ng/ml。結(jié)論:MAGLUMI化學發(fā)光免疫分析儀可直接用于對人血清中肝纖維化指標HA、LN、PⅢNP及C Ⅳ的含量進行定量分析,批內(nèi)精密度、日間精密度、準確度、線性范圍、靈敏度以及參考區(qū)間均較好,報告結(jié)果準確可靠。MAGLUMI分析儀是一種較理想的適用于判斷肝纖維化程度的檢測儀,值得推廣應用。
化學發(fā)光免疫分析儀;肝纖維化指標;性能評價
[First-author’s address] Department of Clinical Laboratory, Langdong Hospital of the First People’s Hospital of Nanning, Nanning 530000, China.
肝纖維化是指由各種致病因子所致肝內(nèi)結(jié)締組織異常增生,導致肝內(nèi)彌漫性細胞外基質(zhì)過度沉淀的病理過程,許多慢性肝臟疾病均可引起肝纖維化[1-3]。肝纖維化常見檢查方法有組織病理學檢查、影像學診斷和血清學診斷。組織病理學檢查是判斷慢性肝病是否已導致肝纖維化的“金標準”,而肝活檢是一種創(chuàng)傷性檢查,存在較大疼痛和并發(fā)癥風險,不方便反復取樣檢查,且存在取樣誤差[4-6]。影像學評估以超聲較普遍,但目前影像學技術(shù)不能評估肝纖維化的早期階段,具有一定局限性。血清學診斷具有取樣方便,可隨時多次采血、價格低以及無創(chuàng)傷等優(yōu)勢,利于早期發(fā)現(xiàn),動態(tài)監(jiān)測肝纖維化,是目前應用最廣泛的肝纖維化檢查方法[7]。
肝纖維化標志物包括透明質(zhì)酸(hyaluronic acid,HA)、層粘連蛋白(laminin,LN)、Ⅳ型膠原(C Ⅳ)、Ⅲ型前膠原氨基端肽(N-terminal peptide of procollagen Ⅲ,PⅢNP)及血清甘膽酸(cholyglycine,CG)等[8]。通過對肝纖維化標志物進行血清學檢測,能對慢性肝病纖維化病變發(fā)展程度進行監(jiān)測。為了保證檢驗項目結(jié)果的質(zhì)量,本研究對HA、LN、PⅢNP和C Ⅳ進行檢測,對MAGLUMI化學發(fā)光免疫分析儀的精密度、準確度、線性范圍、靈敏度以及參考區(qū)間等性能進行驗證。
1 資料與方法
1.1標本來源
收集符合肝纖維化指標標本要求的門診或住院患者送檢的標本,并按肝纖維化檢測指標的要求及時分析或處理標本。
1.2儀器和試劑
MAGLUMI 4000全自動化學發(fā)光免疫分析儀(深圳市新產(chǎn)業(yè)生物醫(yī)學工程股份有限公司),檢測試劑,校準品,質(zhì)控品均由深圳市新產(chǎn)業(yè)生物醫(yī)學工程有限公司提供,并嚴格按照儀器及試劑說明書的操作規(guī)程進行。
1.3檢測方法
按照儀器的作業(yè)指導書對儀器進行系統(tǒng)維護保養(yǎng),待常規(guī)室內(nèi)質(zhì)量控制完成后按美國臨床實驗室標準化協(xié)會(clinical and laboratory standards institute,CLSI)推薦方法測定HA、LN、PⅢNP和CⅣ的批內(nèi)和日間精密度、準確度、線性范圍、靈敏度以及生物參考區(qū)間等指標,并進行驗證,且于檢測過程中不定時地插入室內(nèi)質(zhì)控物進行質(zhì)量監(jiān)控,確保整個分析過程中儀器處于質(zhì)量控制的良好狀態(tài)。
1.3.1精密度驗證
批內(nèi)精密度:參照NCCI SEP5-A[11]文件,隨機抽取一盒試劑,按試劑盒說明書規(guī)定檢測,用各自的質(zhì)控品連續(xù)重復測試20次,分別計算其均值±標準差(x-±s)和變異系數(shù)(coefficient variation,CV)值(%)。日間精密度:每日測定1次質(zhì)控品,連續(xù)測定20 d,分別計算x-±s和CV值。
1.3.2準確度驗證
用校準品校準檢測系統(tǒng)后,對定值質(zhì)控品進行HA、LN、PⅢNP和C Ⅳ檢測,檢測結(jié)果與定值質(zhì)控品的靶值進行對照,計算檢測值與靶值的相對偏倚(%),即為公式1:

1.3.3線性范圍驗證
按照美國臨床實驗室標準NCCISEP6-A2[12]文件評價方案,選取高值血清樣本(H)和低值血清樣本(L)各1份,濃度分別接近儀器給定的測量線性范圍的兩側(cè),將樣本H和樣本L按5 H、4 H+L、3 H+2 L、2 H+3 L、H+4 L及5 L的比例混合成6個樣品,每份樣品重復測定3次,計算平均值(x-)。將實測值與理論值相比較驗證線性范圍。
1.3.4靈敏度驗證
分別取10份HA、LN、PⅢ PN-P和C Ⅳ空白液連續(xù)測定3次,取其平均值(x-)作為相應檢測項目的靈敏度。
1.3.5參考區(qū)間驗證
按照NCCIS C28-A2文件[13]要求進行驗證。選擇健康人群標本20份,在MAGLUMI 4000分析儀上進行測定,對結(jié)果進行統(tǒng)計并與儀器說明書提供的參考范圍比較。測定HA、LN、PⅢ PN-P和C Ⅳ項目,要求20個檢測數(shù)據(jù)中只允許有1個數(shù)據(jù)在給定的生物參考區(qū)間之外,否則需要進行檢測項目參考范圍的建立。
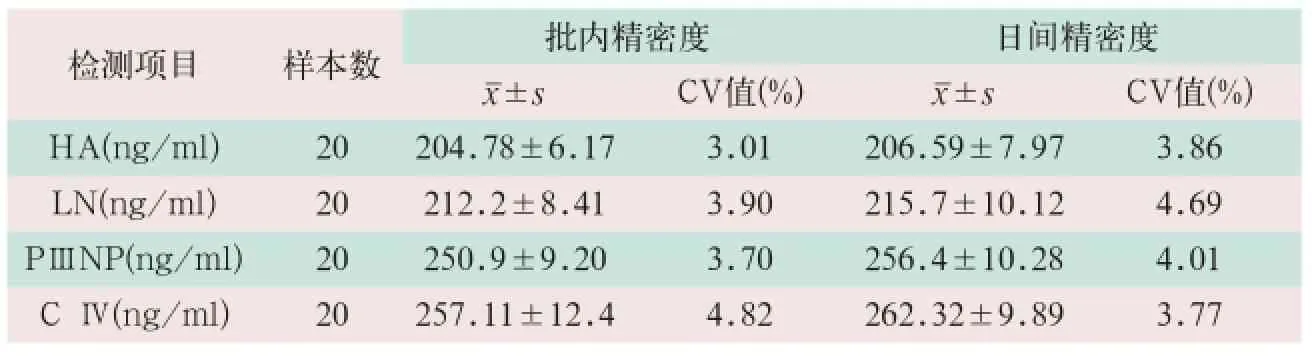
表1 MAGLUMI 4000分析儀測定肝纖4項精密度(%)
2 結(jié)果
2.1精密度
MAGLUMI 4000分析儀檢測HA、LN、PⅢNP和C Ⅳ批內(nèi)精密度分別為3.01%、3.90%、3.70%和1.81%,日間的精密度分別為3.86%、4.69%、4.01%和3.77%,均符合要求,見表1。
2.2準確度
MAGLUMI 4000分析儀檢測HA、LN、PⅢPN-P和C Ⅳ的校正品結(jié)果與靶值的相對偏倚分別為0.09%、-4.4%、0.2%和-5.3%,均在MAGLUMI 4000分析儀允許范圍內(nèi)。
2.3線性范圍
MAGLUMI 4000分析儀檢測HA、LN、PⅢNP和C Ⅳ的線性范圍分別為4.46~1986.99 ng/ml,2.00~999.25 ng/ml,0.50~1983.34 ng/ml和2.00~1990.21 ng/ml,均符合要求。與廠商提供的線性范圍相近,表明廠商提供的線性范圍可靠,可直接用于臨床。
2.4靈敏度
MAGLUMI 4000分析儀檢測HA、LN、PⅢPN-P和C Ⅳ靈敏度分別為1.30 ng/ml、0.9 ng/ml、0.49 ng/ml和0.54 ng/ml,與廠商提供的靈敏度相一致。
2.5參考區(qū)間
MAGLUMI 4000分析儀檢測HA、LN、PⅢNP和C Ⅳ的結(jié)果均與儀器廠商提供的參考區(qū)間符合,儀器廠商提供的參考區(qū)間適合本地區(qū)人群。
3 討論
肝纖維化標志物HA主要由間質(zhì)細胞合成,經(jīng)淋巴循環(huán)入血,由肝臟內(nèi)皮細胞攝取,由特異的HA酶水解,可較準確靈敏地反映肝內(nèi)已生成的纖維量及肝細胞受損狀況,是肝纖維化和肝硬變的敏感指標。LN廣泛分布于基底膜的透明層,緊貼細胞基底部,與C Ⅳ結(jié)合形成基底膜股價,影響細胞的粘附、運動,調(diào)節(jié)細胞生長和分化,并與肝纖維化發(fā)生、腫瘤的浸潤轉(zhuǎn)移等有關(guān)。Ⅲ型前膠原(PC Ⅲ)是PⅢNP的前體,PC Ⅲ分泌到細胞外后,經(jīng)內(nèi)切酶酶切后裂解下來的氨基端多肽形成PⅢNP,PⅢNP在肝纖維化早期即可能升高,血清含量與肝纖維化程度一致。C Ⅳ為構(gòu)成基底膜主要成分,在細胞內(nèi)合成,直接以前膠原形式參與細胞外間質(zhì)的構(gòu)成。正常肝臟C Ⅳ含量極微,肝臟發(fā)生纖維化后,早期即見其增生,且轉(zhuǎn)換率快,最后與持續(xù)沉積的層粘連蛋白形成完整的基底膜。血清C Ⅳ水平升高可較靈敏反映出肝纖維化過程,在肝纖維化時出現(xiàn)最早,是肝纖維化的早期標志之一[7-10]。
肝臟遭到各種致病原侵襲時,引起肝臟損害與炎癥反應,肝組織免疫系統(tǒng)同時被激活,進行組織修復。肝纖維化是指這種組織修復過程過度及失控時,肝組織內(nèi)細胞外基質(zhì)過度增生與異常沉積所致肝臟結(jié)構(gòu)和肝功能異常改變的一種病理過程[14-15]。HA是基質(zhì)成分,可較準確靈敏的反映肝內(nèi)已生成的纖維量及肝細胞受損情況。有資料認為,血清HA動態(tài)檢測較之肝活檢更能完整反映出肝全貌,是肝纖維化和肝硬變的敏感指標,尤其在肝纖維化時,血清HA升高幅度與病變程度相關(guān)。LN為基底膜中特有的非膠原性結(jié)構(gòu)蛋白,與肝纖維化活動程度及門靜脈壓力呈正相關(guān),此外,LN水平越高肝硬化患者的食管靜脈曲張越明顯。正常肝臟間質(zhì)含少量LN,在肝纖維化和肝硬化時,肌成纖維細胞增多,大量合成和分泌膠原、LN等間質(zhì)成分,形成完整的基底膜。PⅢNP反映肝內(nèi)Ⅲ型膠原合成,血清含量與肝纖維化程度一致。持續(xù)PⅢNP升高的慢性活動性肝炎,提示病情可能會惡化并向肝硬化形成發(fā)展,而PⅢNP降至正常可預示病情緩解。C Ⅳ為構(gòu)成基底膜主要成份,反映基底膜膠原更新率,含量增高可較靈敏反映出肝纖維化過程[16-18]。
目前,測定肝纖維化四項血清含量的方法主要有化學發(fā)光法和放射免疫分析法。有研究表明,化學發(fā)光法是檢測血清肝纖維化四項較為特異和準確的方法,其效果明顯優(yōu)于放射免疫分析法[9]。新產(chǎn)業(yè)MAGLUMI化學發(fā)光分析儀,運用先進的直接化學發(fā)光檢測技術(shù),具有準確度高、重復性好、線性范圍廣、孵育時間短、靈敏度高及檢測項目多(如肝纖維化、腫瘤標志物、甲狀腺、性激素、糖代謝、心肌損傷標志物、貧血、骨代謝及傳染病等121個項目)的特點。但不同實驗室之間因條件的差異,如工作人員操作習慣、水質(zhì)、溫度、濕度及電壓穩(wěn)定性等諸多因素存在差異性,因此,每個實驗室都有必要按各自的系統(tǒng)建立和驗證方法學參數(shù),評價MAGLUMI化學發(fā)光分析儀各項性能是否符合要求,檢測結(jié)果是否準確可靠[19]。
精密度是定量測定中最基本的性能指標。本研究結(jié)果顯示,MAGLUMI 4000化學發(fā)光分析儀測定HA、LN、PⅢNP和C Ⅳ批內(nèi)精密度分別為3.01%、3.9%、3.70%和1.81%,均小于廠商說明書給定的允許范圍(<5%),表明該儀器在本室的檢測環(huán)境中系統(tǒng)重復性符合要求,精密度良好,能滿足臨床檢驗質(zhì)量標準。
準確度是通過定值質(zhì)控品或校準品的測定并計算其偏倚(%),若測定結(jié)果在廠商規(guī)定的限值之內(nèi),準確度可被確認。按照NCCLS EP15-A[20]文件和ISO15189文件中對準確度的評價要求,可通過比對定值質(zhì)控品或校正品來對系統(tǒng)的準確度進行驗證。本研究結(jié)果顯示,MAGLUMI 4000化學發(fā)光免疫分析儀檢測HA、LN、PⅢNP和C Ⅳ的校正品結(jié)果與靶值的相對偏倚分別為0.09%、-4.4%、0.2%和-5.3%,均在允許范圍之內(nèi),表明其檢測HA、LN、PⅢ PN-P和C Ⅳ準確度性能符合廠商及實驗室要求。
4 結(jié)語
在確保使用原裝配套試劑的前提下,本研究驗證的HA、LN、PⅢNP和C Ⅳ線性范圍與廠商提供的線性范圍相近,均在廠商提供線性范圍之內(nèi)。按照NCCLSC28-A2[13]文件要求,本研究對HA、LN、PⅢ PN-P和C Ⅳ的正常參考范圍進行了驗證,結(jié)果顯示,MAGLUMI 4000化學發(fā)光分析儀測定本區(qū)健康人群血清中HA、LN、PⅢ PN-P和C Ⅳ的含量均與廠商推薦的參考區(qū)間相符合,可直接引用廠商的參考范圍。新產(chǎn)業(yè)MAGLUMI化學發(fā)光分析儀檢測肝纖維化指標HA、LN、PⅢNP和C Ⅳ的方法性能良好,可滿足要求,能夠為臨床診斷提供準確可靠的結(jié)果。
[1]Lotersztajn S,Julien B,Teixeira-Clerc F,et al. Hepatic fibrosis:molecular mechanisms and drug targets[J].Annu Rev.Pharmacol Toxicol,2005,45:605-628.
[2]Gluud C.Mortality from cirrhosis:lack of progress over the last 35 years[J].Gut,2005,54(11):1523-1526.
[3]Albanis E,F(xiàn)riedman SL.Antifibrotic agents for liver disease[J].Am J Transplant,2006,6(1):12-19.
[4]Afdhal NH,Nunes D.Evaluation of liver fibrosis:a concise review[J].Am J Gastroenterol,2004,99(6):1160-1174.
[5]Thampanitchawong P,Piratvisuth T.Liver biopsy:complications and risk factors[J].World journal of gastroenterology,1999,5(4):301-304.
[6]Regev A,Berho M,Jeffers LJ,et al.Sampling error and intraobserver variation in liver biopsy in patients with chronic HCV infection[J].Am J Gastroenterol,2002,97(10):2614-2618.
[7]劉君,陳娜.肝纖維化血清學指標的臨床意義[J].檢驗醫(yī)學與臨床,2012,9(3):320.
[8]Imbert-Bismut F,Ratziu V,Pieroni L,et al. Biochemical markers of liver fibrosis in patients with hepatitis C virus infection:aprospective study[J].Lancet,2001,357(9262):1069-1075.
[9]周作華,趙紅,黃萍,等.2種方法檢測血清肝纖四項的效果比較[J].現(xiàn)代中西醫(yī)結(jié)合雜志,2012,21(25):2824-2826.
[10]陳小玲,焦曉多,伍勇.肝癌患者血清中透明質(zhì)酸、層粘蛋白、Ⅵ型膠原的測定及臨床意義[J].臨床和實驗醫(yī)學雜志,2010,9(14):1041-1043.
[11]NCCLS.EP5A2:Evaluation of precision peformance of quantitative measurement methods.Approved guideline-second edition[S]. Wayne,PA:NCCLS,2004.
[12]National Committee for Clinical Laboratory Standards.Evaluation of the lineity of quantitative measurerment procedures:A statistical approach'Approve dguideline NCCLS document EP6-A[S].Wayne PA:NCCLS 2003:l-60.
[13]NCCLS.C28-A2:how to define and determine reference intervals in the clinical laboratory. Approved guideline-second edition[S]. Wayne,PA:NCCLS,2000.
[14]Fallowfield JA,Kendall TJ,Iredale J P.Reversal of fibrosis:no longer a pipe dream?[J].Clin liver dis,2006,10(3):481-497.
[15]Popov Y,Schuppan D.Targeting liver fibrosis:strategies for development and validation of antifibrotic therapies[J].Hepatology,2009,50(4):1294-1306.
[16]韓軼,劉立新.肝纖維化血清學診斷指標研究進展[J].中華消化病與影像雜志:電子版,2013,3(4):35-41.
[17]王彩生.肝纖維化的診斷進展[J].臨床肝膽病雜志,2010,26(6):666-668.
[18]劉杰,王吉耀,陸曄.血清纖維化指標對肝纖維化診斷價值的研究[J].中華內(nèi)科雜志,2006,45(6):475-477.
[19]姚偉,劉愛勝,房篤智,等.電化學發(fā)光分析儀檢測貧血指標的方法學性能驗證[J].中國醫(yī)學裝備,2016,13(1):74-77.
[20]NCCLS.EP15-A:User demonstration of performance for precision and accuracy.Approved guideline[S].Wayne,PA:NCCLS,2001.
Research on performance verification methodology for testing hepatic fibrosis indicators by Snibe MAGLUMI chemiluminescence immunoassay analyzer
HUANG Yong-pan, WEI Rong-guo, QIN Zheng, et al// China Medical Equipment,2016,13(11):43-46.
Objective: To detect hepatic fibrosis parameter methodology performance for validation of Snibe MAGLUMI automatic chemiluminescence immunoassay analyzer. Methods: Recommended by the American association of clinical laboratory standardization (CLSI) method, we detected the determination of hyaluronic acid (HA), Laminin (LN), Ⅲ procollagen N-terminal peptide (PⅢ PN-P), Ⅳcollagen (C Ⅳ), and the precision, accuracy, linear range, sensitivity and biological reference range by MAGLUMI analyzer. Results: MAGLUMI determination of HA, LN, PⅢ PN-P, C Ⅳ and precision, and the daytime in this batch variation coefficient were 3.01~4.82% and 3.77~4.69%. Relative bias must lean between -5.3% and 0.2%. The scope of determination of linear range and the manufacturer were similar. The value of HA, LN, PⅢ PN-P, C Ⅳ and reference interval coincidence rate provided by manufacturers were all 100%. And the sensitivities were 1.30ng/ml, 0.9ng/ml, 0.49ng/ml and 0.54ng/ml. Conclusion: MAGLUMI can be used in quantitative analysis of the content of HA, LN, PⅢ PN-P and C Ⅳ directly, which are indicators of liver fibrosis in human serum. Precision, accuracy, linear range, sensitivity and biological reference range show good performance in this methodology. The results of report are accurate and reliable. MAGLUMI is an ideal way to determine the degree of liver fibrosis.
Chemiluminescence immunoassay analyzer; Hepatic fibrosis indicators; Performance evaluation
黃永攀,男,(1976- ),大專,主管技師。南寧市第一人民醫(yī)院埌東醫(yī)院檢驗科,從事臨床檢驗工作。
1672-8270(2016)11-0043-04
R197.39
A
10.3969/J.ISSN.1672-8270.2016.11.013
①南寧市第一人民醫(yī)院埌東醫(yī)院檢驗科 廣西 南寧 530000
②南寧市第一人民醫(yī)院檢驗科 廣西 南寧 530000
③南寧市第一人民醫(yī)院核醫(yī)學科 廣西 南寧 530000
2016-05-10

