復方氨基酸(15AA)雙肽(2)注射液細菌內毒素檢查方法研究
祝清芬,馮巧巧,肖 英,魏 霞(.山東省食品藥品檢驗研究院,濟南 500;.山東省食品藥品監督管理局審評認證中心,濟南 5003)
復方氨基酸(15AA)雙肽(2)注射液細菌內毒素檢查方法研究
祝清芬1*,馮巧巧2,肖 英1,魏 霞1(1.山東省食品藥品檢驗研究院,濟南 250101;2.山東省食品藥品監督管理局審評認證中心,濟南 250013)
目的:為建立復方氨基酸(15AA)雙肽(2)注射液細菌內毒素檢查的標準方法提供參考。方法:按2015年版《中國藥典》(四部)要求確定復方氨基酸(15AA)雙肽(2)注射液的細菌內毒素限值,并分別采用凝膠法與動態濁度法考察樣品對細菌內毒素檢查的干擾情況。結果:樣品調節pH近中性后,采用上述兩種方法在4倍稀釋時對細菌內毒素檢查均無干擾作用。結論:凝膠法與動態濁度法均可用于復方氨基酸(15AA)雙肽(2)注射液的細菌內毒素檢查。由于動態濁度法回收率波動大,建議采用凝膠法。
復方氨基酸(15AA)雙肽(2)注射液;細菌內毒素檢查;干擾試驗;凝膠法;動態濁度法
復方氨基酸(15AA)雙肽(2)注射液是一種腸外營養藥,適用于不能口服或經腸道補給營養以及通過這些途徑補給營養不能滿足需要的患者[1]。該藥臨床上為靜脈給藥,需對其細菌內毒素進行檢查,而以往的該藥細菌內毒素檢查方法研究尚存在不完善之處。故本試驗參照2015年版《中國藥典》(四部)[2]采用凝膠法與動態濁度法對復方氨基酸(15AA)雙肽(2)注射液進行了細菌內毒素檢查方法研究。
1 材料
1.1 儀器
ZH-2型自動漩渦混合器(天津藥典標準儀器廠);TAL-40A型試管恒溫儀(湛江安度斯生物有限公司);BET-48G型細菌內毒素測定儀(天津市天大天發科技有限公司)。
1.2 藥品與試劑
復方氨基酸(15AA)雙肽(2)注射液[青島華仁藥業股份有限公司,批號:B1406001、B1406002、B1406003,規格:500 ml:67 g(氨基酸/雙肽)];凝膠法檢查用鱟試劑(湛江安度斯生物有限公司,批號:1403052,靈敏度:0.06 EU/ml;湛江博康海洋生物有限公司,批號:1301310,靈敏度:0.06 EU/ml);動態濁度法檢查用鱟試劑(湛江安度斯生物有限公司,批號:1307110,靈敏度范圍:10~0.01 EU/ml);細菌內毒素工作標準品(中國食品藥品檢定研究院,批號:150601-201377,規格:70 EU/支);細菌內毒素檢查用水(BET水,湛江安度斯生物有限公司,批號:1406160,規格:5 ml/支)。
2 方法與結果
2.1 樣品細菌內毒素限值(L)確定
該樣品為大容量注射劑,按2015年版《中國藥典》(四部)[2]規定及委托方的要求,其L確定為0.50 EU/ml。
2.2 凝膠法[2-3]
2.2.1 鱟試劑靈敏度復核 按2015年版《中國藥典》(四部)通則1143“細菌內毒素檢查法”項下對于鱟試劑靈敏度復核的要求,分別對兩批鱟試劑進行靈敏度復核。結果,鱟試劑(1403052)的復核靈敏度λc=0.03 EU/ml,鱟試劑(1301310)的復核靈敏度λc=0.125 EU/ml,兩批鱟試劑λc均在0.5λ~2.0λ之間,說明兩批鱟試劑均可用于試驗。
2.2.2 干擾預試驗 目前市售鱟試劑靈敏度一般在0.5~0.03 EU/ml之間,根據最大有效稀釋倍數(MVD)=L/λ(λ指鱟試劑靈敏度),該樣品可采用原液至16倍稀釋液進行試驗。采用批號為B1406001的樣品進行預試驗,結果見表1(注:“-”指凝膠形成陰性,“+”指凝膠形成陽性;“樣品+2λ”指樣品中加入2λ濃度的細菌內毒素標準品)。預試驗結果說明樣品對細菌內毒素檢查具有明顯抑制作用。考慮到其pH呈酸性,故采用1 mol/L氫氧化鈉溶液調節pH至近中性后重新進行預試驗。結果顯示,樣品調節pH近中性后,在2倍稀釋時對試驗存在干擾作用,而在4倍稀釋時即對試驗無干擾作用。
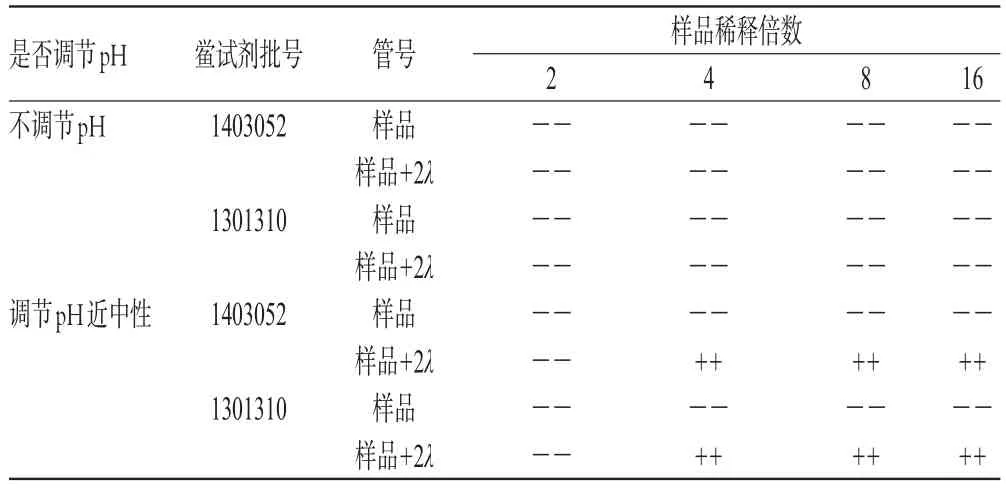
表1 凝膠法細菌內毒素檢查干擾預試驗結果Tab 1 Results of the interference pre-test for bacterial endotoxin test by gel-clot method
2.2.3 干擾試驗 根據預試驗結果,用1 mol/L氫氧化鈉溶液將樣品調節pH近中性后,采用兩批鱟試劑進行干擾試驗,考察4倍稀釋液對細菌內毒素檢查的干擾情況。用BET水將細菌內毒素標準品復溶,并稀釋制成含細菌內毒素2.0λ、1.0λ、0.5 λ、0.25λ 4種濃度的細菌內毒素溶液,即濃度分別為0.125、0.062 5、0.031 25、0.015 6 EU/ml(C液);并制備含有上述4種濃度細菌內毒素的樣品4倍稀釋液(B液)。分別采用上述兩批鱟試劑考察樣品對細菌內毒素檢查的干擾情況,每一濃度平行做4管,同時取BET水(D液)和樣品4倍稀釋液(A液)各做2支陰性對照管。分別計算系列溶液C和B的反應濃度的幾何平均值Es和Et,判斷樣品對細菌內毒素檢查有無干擾作用,結果見表2。試驗結果表明,Es均在0.5 λ~2.0 λ之間,3批樣品Et均在0.5 Es~2.0 Es之間,即調節pH近中性后樣品4倍稀釋液對凝膠法細菌內毒素檢查無干擾作用。
2.3 動態濁度法[2-4]
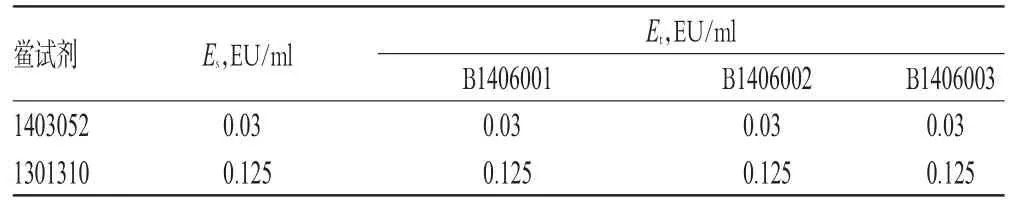
表2 凝膠法細菌內毒素檢查干擾試驗結果Tab 2 Results of the interference test for bacterial endotoxin test by gel-clot method
2.3.1 制備標準曲線 用BET水將細菌內毒素標準品進行倍比稀釋,使最終細菌內毒素濃度分別為2.0、0.5、0.125、0.031 25 EU/ml,各取0.1 ml,分別加入預先加有0.1 ml鱟試劑的反應管內,混合均勻,插入細菌內毒素測定儀進行檢測(檢測波長為405 nm),每一濃度重復4管,同時做陰性對照2管。以細菌內毒素濃度的對數(LgC)為橫坐標、平均反應時間的對數(lgT)為縱坐標,繪制標準曲線(詳見表3)。標準曲線回歸方程為LgT=2.841 71-0.234 17LgC(r=-0.992 1,其絕對值應>0.980),平行管之間的RSD均<10%,陰性對照的反應時間超過標準曲線最低濃度的反應時間,故該標準曲線符合規定。

表3 細菌內毒素標準曲線及可靠性(n=4)Tab 3 Standard curve and reliability of bacterial endotoxin(n=4)
2.3.2 干擾試驗 根據標準曲線細菌內毒素濃度的設置,選擇0.25 EU/ml作為靠近標準曲線中點的內毒素濃度(λm),取批號為B1406001的樣品,調節pH近中性后,分別用BET水將樣品稀釋2、4、8倍,作為供試品溶液(A液);并分別用上述濃度的供試品溶液制備含細菌內毒素濃度為λm(0.25 EU/ml)的溶液(B液)。分別取A、B溶液各0.1 ml,加入預先加有0.1 ml鱟試劑的反應管內,混合均勻,插入細菌內毒素測定儀進行測定,每個濃度重復2管。測定結束后,按標準曲線回歸方程分別計算出A液和B液的細菌內毒素含量,并計算該試驗條件下的回收率,結果見表4。結果表明,樣品稀釋2倍時,平均回收率在50%以下,說明在此稀釋倍數下樣品對細菌內毒素測定有抑制作用。而樣品稀釋4倍及以上時,平均回收率均在50%~200%,符合要求。說明干擾試驗中可選擇樣品4倍稀釋液。另取B1406002、B1406003兩批樣品,調節pH近中性后,分別制備A液和B液(4倍稀釋),依法檢查,平均回收率均在50%~200%,亦符合要求(見表4)。由此表明,樣品在4倍稀釋時對動態濁度法細菌內毒素測定無干擾作用。
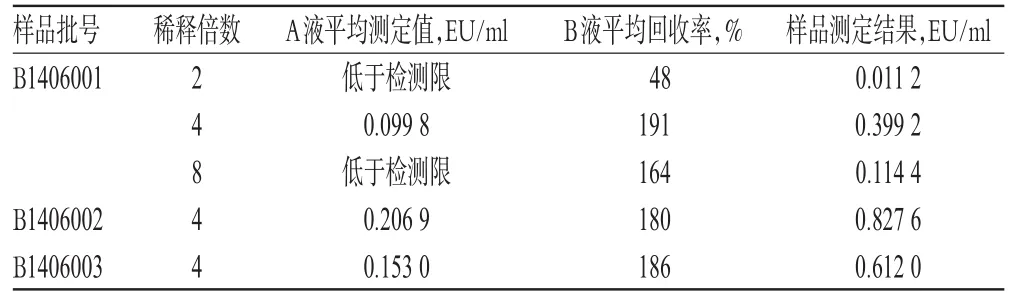
表4 動態濁度法干擾試驗及樣品細菌內毒素測定結果(n=2)Tab 4 Result of interference test and bacterial endotoxin test in samples by kinetic turbidimetric limulus test(n=2)
3 討論
細菌內毒素檢查方法包括凝膠法和光度測定法(定量法),目前后者在檢驗、科研等領域得到了越來越多的應用[5]。動態濁度法是最常用的定量測定方法之一,通過測定反應溶液達到規定濁度所需時間或測定溶液自身的濁度變化率定量測定樣品中細菌內毒素含量。該法操作簡單、快速、靈敏度高、檢測范圍寬。動態濁度法的干擾試驗,以樣品中加入細菌內毒素的回收率進行判斷,若回收率在50%~200%之間,可認為樣品對細菌內毒素測定無干擾[6]。
凝膠法試驗結果表明,復方氨基酸(15AA)雙肽(2)注射液樣品對細菌內毒素檢查有干擾作用,這與相關文獻報道一致[7]。通過進一步探討干擾作用的原因發現,主要與樣品的酸堿性相關。將樣品調節pH近中性后可基本排除干擾,但其2倍稀釋液仍存在干擾,說明這種干擾作用也有其他因素參與。
在動態濁度法試驗中,干擾情況與凝膠法基本相同,復方氨基酸(15AA)雙肽(2)注射液樣品調節pH近中性后,在4倍稀釋時對細菌內毒素測定無干擾作用。但該試驗中發現一個很奇怪的現象,在2倍稀釋時樣品仍存在明顯的抑制作用,但樣品在4倍稀釋時對細菌內毒素測定有一定的增強作用。而試驗過程中也出現過回收率超過200%的情況。同時,樣品中測得的內毒素含量遠遠超出實際值,甚至出現樣品不合格的情況。但通過進一步驗證,采用2015年版《中國藥典》(四部)規定的仲裁法凝膠法進行檢驗,樣品中實際內毒素含量<0.25 EU/ml。出現這種現象的原因仍有待于進一步研究。鑒于此,目前在樣品實際檢驗過程中建議采用凝膠法。
本試驗建立的復方氨基酸(15AA)雙肽(2)注射液細菌內毒素檢查方法如下:取本品,用1 mol/L氫氧化鈉溶液調節pH近中性,然后用BET水稀釋至少4倍后,依照2015年版[《中國藥典》(四部)通則1143進行檢查,本品每1 ml中含內毒素的量應<0.50 EU。
[1] 解曉帥,褚燕琦,白向榮,等.復方氨基酸(15)雙肽(2)注射液臨床用藥調查研究[J].藥學實踐雜志,2014,32(5):58.
[2] 國家藥典委員會.中華人民共和國藥典:四部[S].2015年版.北京:中國醫藥科技出版社,2015:154-157、400-402.
[3] 中國藥品生物制品檢定所.中國藥品檢驗標準操作規范[M].2010年版.北京:中國醫藥科技出版社,2010:310-321.
[4] 魏霞,韓梅,韓瑤,等.血液濾過置換液的細菌內毒素檢查法研究[J].中國藥房,2013,24(29):2 752.
[5] 郭萌,李冠民,黃清泉.細菌內毒素研究進展[J].中國實驗動物學報,2009,17(5):397.
[6] 張娟,祝清芬,范治云.動態濁度法測定人參多糖注射液中細菌內毒素的含量[J].藥學研究,2014,33(6):334.
[7] 陳友愛,李鳴.復方氨基酸(15)雙肽(2)注射液細菌內毒素檢查法建立及方法學研究[J].海峽藥學,2007,19(8):71.
(編輯:周 箐)
Study on the Test Method for Bacterial Endotoxin in Compound Amino Acids(15AA)and Dipeptide(2)Injection
ZHU Qingfen1,FENG Qiaoqiao2,XIAO Ying1,WEI Xia(11.Shandong Institute for Food and Drug Control,Jinan 250101;2.Center for Drug Evaluation&Certification of Shandong FDA,Jinan 250013,China)
OBJECTIVE:To provide reference for establishing the standard method for the bacterial endotoxin test in Compound amino acids(15AA)and dipeptide(2)injection.METHODS:The limit for bacterial endotoxin in Compound amino acids(15AA)and dipeptide(2)injection was designed according to Chinese Pharmacopoeia 2015 edition(four),and both gel-clot method and kinetic turbidimetric limulus test were conducted for detecting the samples'interference to bacterial endotoxin test.RESULTS:After being adjusted to a near neutral pH,samples showed no interfered to bacterial endotoxin in both methods when the sample was diluted to 4 times.CONCLUSIONS:Both gel-clot method and kinetic turbidimetric limulus test can be used for the bacterial endotoxin test in Compound amino acids(15AA)and dipeptide(2)injection.Gel-clot method is recommended due to the large fluctuations of recovery rate in kinetic turbidimetric limulus test.
Compound amino acids(15AA)and dipeptide(2)injection;Bacterial endotoxin test;Interference test;Gel-clot method;Kinetic turbidimetric limulus test
R927
A
1001-0408(2016)33-4742-03
2015-11-30
2016-09-14)
*主任藥師,博士。研究方向:藥理學、毒理學、藥物安全性評價、藥品檢驗。電話:0531-81216599。Email:zhuqingfen73@163.com
DOI 10.6039/j.issn.1001-0408.2016.33.45

