紫甘藍食用色素抑制細胞脂質過氧化活性研究
王忠博,張志斐,姚妍妍,李洋
(華北理工大學藥學院,河北唐山063000)
紫甘藍食用色素抑制細胞脂質過氧化活性研究
王忠博,張志斐,姚妍妍,李洋*
(華北理工大學藥學院,河北唐山063000)
探討紫甘藍食用色素抑制細胞發生脂質過氧化反應的活性。采用H2O2誘導的紅細胞溶血、肝勻漿脂質過氧化反應、肝線粒體腫脹實驗以及羥基自由基評價紫甘藍食用色素抑制細胞脂質過氧化損傷的能力。紫甘藍食用色素能夠顯著抑制紅細胞溶血、降低脂質過氧化反應、減輕線粒體腫脹、清除羥基自由基,均呈一定的量效關系。紫甘藍食用色素在體外能夠抑制細胞脂質過氧化反應,作為天然食用色素開發利用,有廣闊前景。
紫甘藍;天然食用色素;脂質過氧化反應;抗氧化活性
食品中添加的人工合成色素被大量證據證實不僅不能向人體提供營養物質,有些還會危及人類身體健康[1]。隨著全球范圍內消費者日益關注飲食健康,天然色素的應用成為食品行業色素使用的新趨勢。天然色素多來自于動、植物組織以及微生物,不僅對人體無毒害,安全性高,而且部分天然色素具有生理活性,兼有營養保健的作用,如花色苷類色素能夠抗衰老、防治心腦血管疾病[2];葉綠素有拮抗誘變及抗癌作用[3];微生物中南極紅色素有強抗氧化作用[4]等。因此,天然色素的研發愈加受到重視。
紫甘藍(Brassicaoleracea L.var.capitata L.f.rubra)為十字花科、蕓苔屬甘藍種中的一個變種,富含紫紅色色素,顏色鮮艷。紫甘藍適應能力強,產量高,易貯藏,作為食用蔬菜在我國大面積種植,價格低廉,因而紫甘藍色素具備開發成天然食用色素的巨大潛力。有研究表明紫甘藍色素為花色苷類物質[5],揭示了其不僅可作為天然食用色素,更可能具有生理活性。
因此,本文從組織、細胞、細胞器3個方面開展紫甘藍食用色素防護脂質過氧化損傷實驗,以評價其生理活性功能。
1 材料與方法
1.1 材料與試劑
紫甘藍:購自超市。D101大孔吸附樹脂:購自西安藍曉科技有限公司。蘆丁標準品:購自中國藥品生物制品檢定所。抗壞血酸、無水乙醇、雙氧水、十二烷基硫酸鈉、三氯乙酸、硫代巴比妥酸、硫酸亞鐵、水楊酸均為分析純。
1.2 主要儀器
RV8旋轉蒸發儀:艾卡(廣州)儀器設備有限公司;ALPHA 1-2 LD plus冷凍干燥機:德國Christ公司;3K30臺式高速冷凍離心機:德國Sigma公司;TU-1810紫外可見分光光度計:北京普析通用儀器有限責任公司;BT 125D分析天平:德國Sartorius公司。
1.3 試驗方法
1.3.1 紫甘藍食用色素的制備
將新鮮、成熟的紫甘藍剪碎,加入適量含0.1%鹽酸的80%乙醇溶液,室溫浸提4 h,過濾,置旋轉蒸發儀在30℃水浴減壓蒸餾,得濃縮液。將濃縮液加入裝有D101大孔吸附樹脂的色譜柱,吸附飽和后用去離子水洗至洗脫液無色,之后加入含0.1%鹽酸的80%乙醇溶液洗脫至無色,收集洗脫液。將洗脫液濃縮除去乙醇,冷凍干燥處理,得紫甘藍食用色素。
1.3.2 紅細胞和肝勻漿的制備
取KM小鼠,18 g~22 g,摘眼球取血,肝素抗凝全血,將小鼠頸椎脫臼處死,快速取肝臟。血液樣品用10倍體積的磷酸鹽緩沖液(150mmol/LNaCl、8.1mmol/L Na2HPO4、1.9mmol/LNaH2PO4、10mmol/LEDTA,pH 7.4)2 000 r/min、5min離心洗滌3次,去除血漿后得紅細胞,4℃保存并在6 h以內使用[6-7]。
肝臟用冰磷酸鹽緩沖液清洗,濾紙吸干水分后稱重,按1∶9(g/mL)取相應體積的冰磷酸鹽緩沖液于冰浴中將肝組織剪碎,玻璃勻漿器中勻漿,得10%(g/mL)肝勻漿,4℃保存。
1.3.3 對紅細胞保護作用的測定
取1 mL用磷酸鹽緩沖液配制的0.5%(mL/mL)紅細胞懸液,加入不同濃度的紫甘藍食用色素溶液0.1mL(對照組加入0.1mL去離子水)和100mmol/L的H2O2溶液0.1mL,在水浴中37℃恒溫加熱1 h,之后加入4mL磷酸鹽緩沖液并以2 000 r/min離心5min,取上清液在415 nm處測量吸光度,以抗壞血酸作為陽性對照[8]。色素對紅細胞溶血的抑制率計算公式如下:

式中:A415(對照)為空白對照組的吸光度;A415(樣品)為樣品組的吸光度。
按照上述方法,取1mL 0.5%紅細胞懸液和0.1mL 0.1mg/mL紫甘藍食用色素在37℃恒溫加熱1 h,測量415 nm吸光度以檢測色素是否引起紅細胞溶血。
1.3.4 肝勻漿脂質過氧化抑制活性的測定
本實驗通過測量丙二醛的生成量以檢測脂質過氧化程度[9]。取0.2mL 10%肝勻漿和0.1mL不同濃度的紫甘藍食用色素溶液混勻(對照組取0.1mL去離子水),再加入0.1mL的100mmol/LH2O2溶液,37℃水浴加熱1 h,之后加入0.2mL的8.1%十二烷基硫酸鈉溶液,1.5mL的15%三氯乙酸溶液和1.5mL的0.8%硫代巴比妥酸溶液,并將此混合液加熱至95℃保持1 h。冰浴冷卻后3 000 r/min離心10min,取上清液在532 nm處測量吸光度,以蘆丁作為陽性對照。色素對脂質過氧化的抑制率計算公式如下:

式中:A532(對照)空白對照組的吸光度;A532(樣品)樣品組的吸光度。
1.3.5 線粒體腫脹度的測定
將10%肝勻漿在4℃下1 000 r/min離心20min,取上清液在4℃下10 000 r/min離心20min,取沉淀用冰磷酸鹽緩沖液在4℃下10 000 r/min離心20min洗滌1次,沉淀即為肝線粒體,再用冰磷酸鹽緩沖液將沉淀重懸制成懸液,用考馬斯亮藍法測定該懸液的蛋白質濃度(以牛血清白蛋白為標準),再調整成蛋白質濃度為0.5mg/mL的線粒體懸液,4℃保存備用。
取2mL線粒體懸液、0.2mL不同濃度的紫甘藍食用色素溶液、0.2mL的0.5mmol/L FeSO4溶液和0.2mL的0.5mmol/L抗壞血酸溶液混勻,37℃水浴孵育,每隔一段時間在520 nm處測量吸光度。對照組用等體積磷酸鹽緩沖液代替色素溶液、FeSO4溶液和抗壞血酸溶液,損傷組用等體積磷酸鹽緩沖液代替色素溶液,并用蘆丁作為陽性對照。吸光度的降低表明線粒體腫脹度增大[10]。
1.3.6 羥基自由基清除能力的測定
通過Fenton反應產生羥基自由基[11]。取不同濃度的紫甘藍食用色素溶液1mL(對照組加入1mL去離子水),再依次移取1mL 10mmol/LFeSO4溶液、1mL 10mmol/L水楊酸乙醇溶液,之后加1mL 8.8mmol/L H2O2啟動反應,37℃反應0.5 h,在510 nm處測量吸光度,以抗壞血酸作為陽性對照。色素對羥基自由基清除率的計算公式如下:
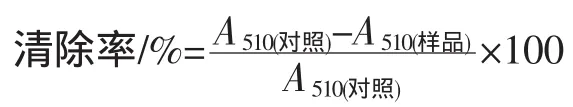
式中:A510(對照)空白對照組的吸光度;A510(樣品)樣品組的吸光度。
1.3.7 數據分析
用GraphPad Prism 6軟件進行單因素方差分析并計算IC50,P<0.05為具有顯著性差異。
2 結果與分析
2.1 對紅細胞的保護作用
血紅蛋白與氧氣運送相關,氧化還原反應非常活躍,是活性氧自由基產生的重要來源。由于含有大量的血紅蛋白,并且在其細胞膜上還有著高濃度的多不飽和脂肪酸,紅細胞被認為是自由基攻擊的主要目標[12]。紅細胞膜受到氧化損傷后會發生溶血現象,因而紅細胞作為一種細胞模型常用于研究生物膜上的氧化損傷。
本試驗先驗證紫甘藍食用色素對紅細胞的破壞作用。色素作用于紅細胞后溶血率為(3.11±0.48)%,這一結果與空白對照組(3.78±0.64)%沒有顯著性差異(P>0.05),由此可知色素對紅細胞無不良影響。
紫甘藍食用色素對H2O2導致的紅細胞溶血的保護作用見圖1。
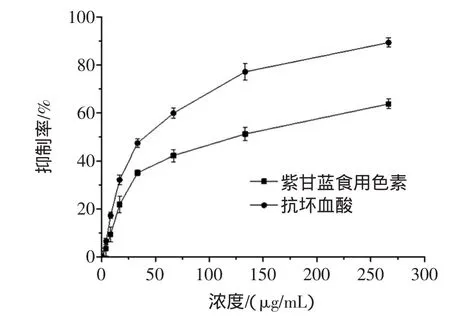
圖1 紫甘藍食用色素對H2O2導致的紅細胞溶血的抑制作用Fig.1 Inhibition of pigm ents from red cabbageagainst H2O2induced erythrocytehem olysis
由圖1可知,在試驗濃度范圍內,色素對紅細胞溶血的抑制作用隨著濃度的增大而增強,能夠顯著抑制H2O2對紅細胞造成的氧化損傷(P<0.05),保護紅細胞結構的完整性,其IC50為109.33μg/mL(抗壞血酸IC50為38.23μg/mL)。
2.2 脂質過氧化抑制活性
脂質過氧化是多不飽和脂肪酸的氧化反應,是生物體內常見的氧化進程。其主產物丙二醛,被廣泛用于脂質過氧化反應的指示物,也用于指示氧化應激反應的發生[13]。因而測定丙二醛的生成量即可表示脂質過氧化反應的程度。紫甘藍食用色素對脂質過氧化的抑制活性見圖2。
與空白對照組相比,H2O2作用肝勻漿1 h后丙二醛的生成量顯著增加(P<0.05),而試驗組中丙二醛的生成量顯著降低(P<0.05),具有量效關系(見圖2),IC50為234.02μg/mL(蘆丁組IC50為98.87μg/mL),表明紫甘藍食用色素對肝勻漿具有顯著的抗脂質過氧化活性。此前有研究顯示紫甘藍色素能夠抑制亞油酸過氧化作用[14],也證實了紫甘藍色素的脂質過氧化抑制能力。
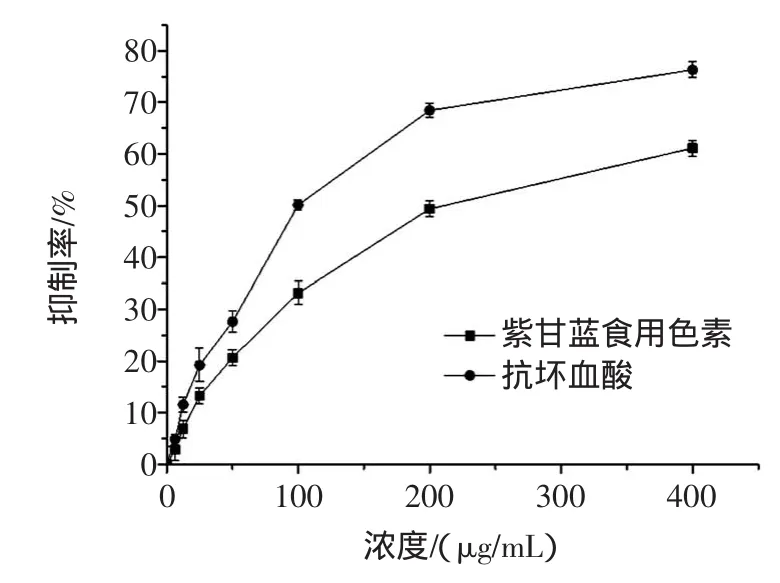
圖2 紫甘藍食用色素對脂質過氧化的抑制活性Fig.2 Inhibitory activity of pigm ents from red cabbage to lipid peroxidation
2.3 對線粒體腫脹的抑制作用
在實驗中,FeSO4與抗壞血酸反應生成H2O2,導致線粒體膜發生脂質過氧化反應造成其結構損傷,膜通透性改變,從而使線粒體發生腫脹[15]。520 nm處的吸光度降低即代表線粒體發生了腫脹,其結構的完整性遭到了破壞,實驗結果如圖3所示。

圖3 紫甘藍食用色素對線粒體腫脹的抑制作用Fig.3 Inhibitory effectof pigm ents from red cabbageon m itochondrialswelling
由圖3可知,與對照組相比,線粒體模型組的吸光度隨著時間推移顯著下降,但在含有紫甘藍食用色素和蘆丁的實驗組中線粒體腫脹程度明顯減弱,表明紫甘藍食用色素能夠抑制氧化損傷造成的線粒體腫脹且抑制能力隨著濃度的增大而增強。在200μg/mL相同終濃度下,紫甘藍食用色素抑制線粒體腫脹的能力要強于蘆丁。
2.4 清除羥基自由基能力
羥基自由基是活性最強的自由基,其在生物體內由氧氣還原成水的過程中不斷產生,是最主要的活性氧自由基,能攻擊并破壞幾乎所有的生物分子,如DNA、蛋白質、磷脂和糖類[16]。由前述實驗結果可知,紫甘藍食用色素能夠抑制H2O2誘導的細胞脂質過氧化反應,因而推測其具有較強清除·OH的能力。結果如圖4所示。
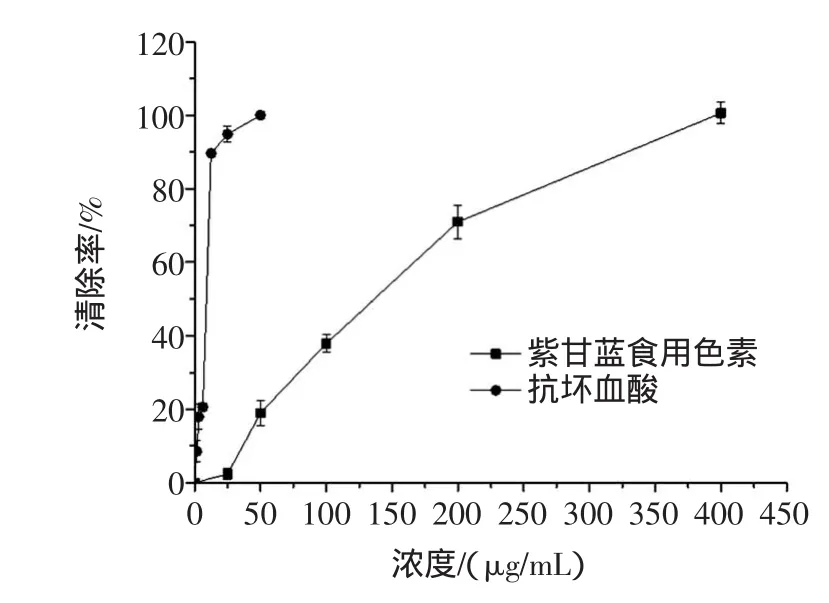
圖4 紫甘藍食用色素對羥基自由基的清除能力Fig.4 Scavenging activity of pigments from red cabbageon hydroxyl radical
由圖4可知,色素清除·OH的能力隨著濃度的增大而增強,400μg/mL時清除率達到98.6%,IC50為111.06μg/mL,大于陽性對照抗壞血酸(IC50為7.65μg/mL)。
3 結論與討論
本研究在細胞器-細胞-組織3個層面上評價紫甘藍食用色素防護細胞脂質過氧化損傷的作用,結果表明紫甘藍食用色素能夠清除·OH,具有顯著的體外抗氧化活性,具有一定的量效關系。
花色苷類物質具有多酚羥基結構,而通常認為酚羥基是抗氧化活性的原因所在,如結構中B環上羥基的數量、位置是其清除活性氧自由基能力的決定因素;C環上3-OH能增強清除自由基的能力;B環上3'、4'鄰二羥基結構能夠極大增強脂質過氧化抑制能力[17]。紫甘藍食用色素屬于矢車菊素花色苷[5],母核結構如圖5,其能夠有效抑制生物體脂質過氧化反應,可能與其母核結構中B環上存在3'、4'鄰二羥基有關,本研究試驗結果與理論相符。
天然色素的需求量越來越大,具有功能作用的花色苷類色素尤其受到關注。開發花色苷類色素,不僅要研究體外活性,其在體內的吸收、代謝及功能作用的發揮情況,更是下一步研究的重點。

圖5 矢車菊素花色苷的基本結構Fig.5 Basic chem icalstructureof cyanidin
[1]海因利希·左林格.色素化學:有機染料和顏料的合成、性能和應用[M].吳祖望,程侶柏,張壯余,譯.北京:化學工業出版社, 2005
[2]趙海田,王振宇,路,等.花色苷類物質降血脂機制研究進展[J].東北農業大學學報,2012,43(3):139-144
[3]王靜,劉昭明,肖凱軍,等.天然食用色素的結構與生理活性分析[J].食品工業科技,2007,28(12):208-212
[4]趙倩,能飛,張梅,等.南極紅色素與3種天然色素還原性和抗氧化性對比研究[J].食品研究與開發,2015,36(2):117-120
[5] Mizgier P,Kucharska A Z,Sokó?-?e towska A,et al.Characterization of phenolic compounds and antioxidantand anti-inflammatory properties of red cabbage and purple carrot extracts[J].Journal of Functional Foods,2016,21:133-146
[6]Yuan XP,Wang J,Yao H Y,etal.Free radical-scavenging capacity and inhibitory activity on rat erythrocyte hemolysis of feruloyl oligosaccharides from wheat bran insoluble dietary fiber[J].LWTFood Scienceand Technology,2005,38(8):877-883
[7] Yang H L,Chen SC,Chang NW,et al.Protection from oxidative damage using Bidens pilosa extracts in normal human erythrocytes [J].Food and Chemical Toxicology,2006,44(9):1513-1521
[8] Tedesco I,Russo M,Russo P,et al.Antioxidant effect of red wine polyphenols on red blood cells[J].The Journal of Nutritional Biochemistry,2000,11(2):114-119
[9] Ohkawa H,Ohishi N,Yagi K.Assay for lipid peroxides in animal tissues by thiobarbituric acid reaction[J].Analytical Biochemistry, 1979,95(2):351-358
[10]Song Y N,Hui J,Kou W,et al.Identification of Inonotus obliquus and analysis of antioxidation and antitumor activitiesof polysaccharides[J].CurrentMicrobiology,2008,57(5):454-462
[11]Wang SY,Jiao H J.Scavenging capacity of berry cropson superoxide radicals,hydrogen peroxide,hydroxyl radicals,and singlet oxygen[J].Journal of Agricultural and Food Chemistry,2000,48(11): 5677-5684
[12]LiY,LiH L,Zhang Y,etal.In vitro antioxidantand anticanceractivitiesof the extract from papermulberry(Broussonetia papyrifera L.)fruit[J].Asian JournalofChemistry,2013,25(10):5453-5456
[13]Janero D R.Malondialdehyde and thiobarbituric acid-reactivity as diagnostic indices of lipid peroxidation and peroxidative tissue injury[J].Free RadicalBiology and Medicine,1990,9(6):515-540
[14]徐亞民,趙曉燕,馬越,等.紫甘藍色素抗氧化能力的研究[J].食品研究與開發,2006,27(11):59-62
[15]Chen Z B,Lv JW,Chen FQ,et al.Studies on telluric hyaluronic acid(TeHA):A novel antioxidant[J].Journal of Molecular Catalysis B:Enzymatic,2008,55(3/4):99-103
[16]Lipinski B.Hydroxyl radical and its scavengers in health and disease[J].OxidativeMedicine and Cellular Longevity,2011,2011:1-9
[17]Heim K E,Tagliaferro A R,Bobilya D J.Flavonoid antioxidants: chemistry,metabolism and structure-activity relationships[J].The JournalofNutritional Biochemistry,2002,13(10):572-584
Inhibitory Activity of the Natural Pigm ents from Red Cabbage to Cellular Lipid Peroxidation
WANGZhong-bo,ZHANGZhi-fei,YAOYan-yan,LIYang*
(SchoolofPharmacy,North China University of Scienceand Technology,Tangshan 063000,Hebei,China)
The objective of thiswork was to study the inhibitory activity of the natural pigments from red cabbage to cellular lipid peroxidation.ThemethodsofH2O2-induced erythrocyte hemolysisand lipid peroxidation of liver homogenate,mitochondrial swelling and scavenging hydroxyl radicalwere used to evaluate the inhibitory activity.The results showed that the natural pigments from red cabbage inhibited erythrocyte hemolysis,lipid peroxidation andmitochondrialswelling significantly andwere scavengersofhydroxyl radical.The inhibitory activity showed a dose-dependent increase in the assays.The naturalpigments from red cabbage could inhibit cellular lipid peroxidation andmightbedeveloped asedible pigmentwith broad prospects.
redcabbage;naturalediblepigment;lipidperoxidation;antioxidantactivity
10.3969/j.issn.1005-6521.2016.24.009
2016-04-14
河北省自然科學基金項目(H2016209319);河北省省級大學生創新創業訓練計劃項目(X2015062)
王忠博(1993—),男(漢),在讀本科,主要從事天然產物生物活性研究。
*通信作者:李洋(1983—),男(漢),講師,博士,主要從事天然產物的化學與生物活性研究。

