篤斯越橘果實花青素提取及穩定性研究
李陽陽,彭瞰看,楊九雙,巨安基,徐永清
(東北農業大學生命科學學院,黑龍江哈爾濱150030)
篤斯越橘果實花青素提取及穩定性研究
李陽陽,彭瞰看,楊九雙,巨安基,徐永清*
(東北農業大學生命科學學院,黑龍江哈爾濱150030)
以篤斯越橘果實為材料,利用超聲波輔助乙醇提取,并采用正交試驗設計,對篤斯越橘果實花青素進行提取,確定其花青素最佳提取條件為:提取溫度40℃,最佳料液比3∶30(g/mL),最佳超聲波功率200W,最佳提取液濃度65%的酸化乙醇。對篤斯越橘果實花青素的穩定性研究結果表明:篤斯越橘果實花青素對pH值敏感;篤斯越橘果實花青素對氧化劑穩定性較差;篤斯越橘果實花青素對還原劑穩定性較強;在pH值為3.0時篤斯越橘果實花青素對Ca2+、Mg2+、Zn2+、Cu2+、Al3+較穩定;篤斯越橘果實花青素弱光穩定性較好,強光穩定性較差。
篤斯越橘;花青素;提取;穩定性
篤斯越橘(Vaccinium uliginosum L.)又稱篤斯、藍莓、黑豆樹,甸果、地果等,杜鵑花科(Ericaceae)越橘屬(Vaccinium L.)落葉灌木,是我國重要的野生資源之一,主要分布在內蒙古、黑龍江、吉林、遼寧等地區[1-2]。篤斯越橘是一種小漿果,果肉細膩,種子極小,它是我國重要的野生漿果資源,具有許多特殊的優良性狀,如抗寒能力極強、花青素含量高等有著很高的營養和保健價值[3-6]。藍莓果實不僅營養豐富,而且含有有機酸、氨基酸、花色苷等獨特的功能性成分[7-10],具有防治心血管疾病、抗癌、抗衰老等多種功效[11-14]。篤斯越橘和越橘是我國面積最大、貯量最多的野生漿果資源[15-16],多生長在人煙稀少,遠離農區的深山中,無化肥和農藥污染,是典型的綠色食品,具有廣闊的開發前景。
鑒于此,本研究以篤斯越橘果實為原材料,探索超聲波輔助法用于從篤斯越橘果實中提取花青素的工藝,提高花青素得率,同時測定pH值、氧化劑、還原劑、金屬離子、光等因素對篤斯越橘果實花青素穩定性的影響,為篤斯越橘果實花青素的生產、保存和應用提供一定的理論依據。
1 材料與方法
1.1 材料與試劑
篤斯越橘果實:采自大興安嶺圖強林場,東北農業大學植物教研室常纓教授鑒定。
乙醇、檸檬酸、鹽酸、氯化鉀、磷酸二氫鈉、氫氧化鈉、雙氧水、抗壞血酸、氯化鈣、氯化鎂、氯化鋅、硫酸銅、氯化鋁(分析純):天津市巴斯夫化工有限公司。
1.2 儀器與設備
超聲波儀:寧波新芝生物科技股份公司;HWS28型電熱恒溫水浴鍋:上海一恒科學儀器有限公司;紫外可見分光光度計:島津有限公司;PB-10型數顯pH計:sartorius公司。
1.3 試驗方法
1.3.1 篤斯越橘果實花青素提取
分別稱取3 g篤斯越橘果實干果研細置于三角瓶中,按表1 L9(34)正交試驗水平表添加浸提液(酸化乙醇),超聲波處理20min而后水浴2 h,過濾保存濾液,濾渣置于原三角瓶中,相同條件水浴1 h再次提取,抽濾,合并兩次濾液。每處理重復3次。

表1 正交試驗因素水平表Table1 Theorthogonalexperiment factors level
1.3.2 篤斯越橘花青素的提取率測定
采用雙波長pH值示差法[17],取待測液1mL,分別加入KCl-HCl緩沖溶液(pH 1.0,0.25mol/L)或NaH2PO4-檸檬酸緩沖溶液(pH3.0,0.20mol/L)9mL,搖勻,轉入光路長為1 cm的比色皿中,靜置。5min后以緩沖溶液為空白對照,518 nm波長處測定光密度(opticaldensity,OD)。
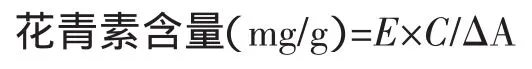
式中:E=(ODpH1.0-ODpH3.0)樣×V/W,V為浸提濾液體積,mL;W為樣品的質量,g;C為標樣濃度,(mg/ mL);ΔA=(ODpH1.0-ODpH3.0)標。因C/ΔA為恒量,故本研究以E值大小衡量花青素的相對提取率。
1.3.3 pH值對篤斯越橘果實花青素穩定性的影響
分別用pH值為1.2、3.2、5.2、7.2、9.2、11.2緩沖溶液稀釋一定量提取液,測定518 nm不同pH值條件下吸光度,并觀察稀釋液顏色變化情況。
1.3.4 氧化劑對篤斯越橘果實花青素穩定性的影響
取一定量提取液,加入30mL 1mmol/L雙氧水溶液稀釋,搖勻靜置,每10分鐘測定吸光度,測定波長518 nm。
1.3.5 還原劑對篤斯越橘果實花青素穩定性的影響
取一定量提取液,分別加入等體積濃度為0.5、1.0、1.5mmol/L抗壞血酸溶液稀釋,測定518 nm吸光度。
1.3.6 金屬離子對篤斯越橘果實花青素穩定性的影響
取一定量提取液,分別加入10mL濃度為0.1%,pH值為3.0 Ca2+、Mg2+、Zn2+、Cu2+、Al3+的溶液稀釋,搖勻后靜置10min,分別測定518 nm溶液的吸光度。
1.3.7 光照對篤斯越橘果實花青素穩定性的影響
取一定量提取液,分別放置于室外自然光、室內自然光、暗室0、2、4、6 d,取樣,測其518 nm吸光度。
2 結果與分析
2.1 篤斯越橘果實花青素提取
對篤斯越橘果實花青素提取研究正交試驗結果的極差分析見表2。
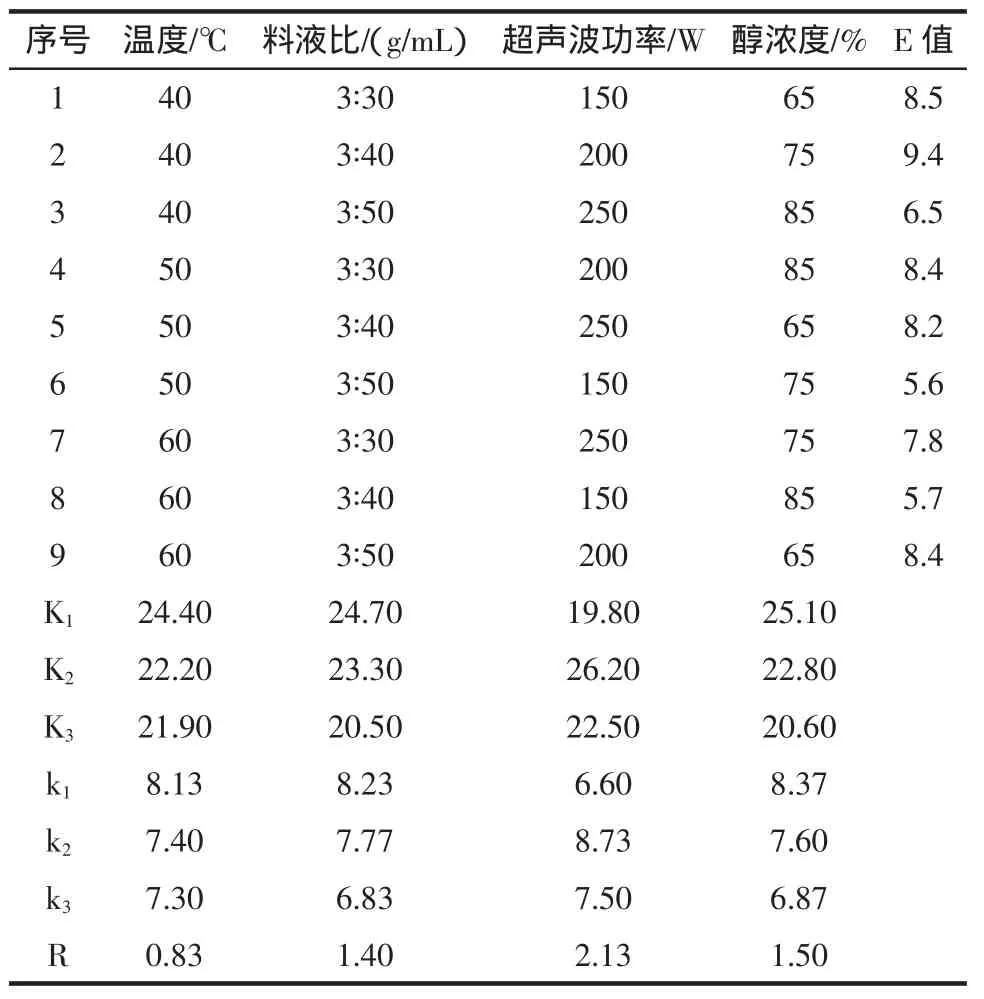
表2 L9(34)正交試驗結果表Table2 The resultsof L9(34)orthogonal test
可以看出:溫度、料液比、超聲波功率、醇濃度這4個因素對篤斯越橘果實花青素含量均有一定影響。影響的主次順序分別為超聲波功率>醇濃度>料液比>溫度;試驗得到最優提取方案為T1V2P2C2組合,即提取溫度40℃,料液比3∶40(g/mL),超聲波功率200W,提取醇濃度75%。
2.2 驗證試驗
從表2正交試驗依據E值獲得最優提取方案為T1V2P2C2組合即提取溫度40℃,料液比3∶40(g/mL),超聲波功率200W,提取醇濃度75%組合,而依據k值最優組合T1V1P2C1組合即提取溫度40℃,料液比3∶30(g/mL),超聲波功率200W,提取醇濃度65%組合;對上述兩組合進行驗證試驗,3次驗證試驗T1V2P2C2組合平均實際E值為9.33,而T1V1P2C1組合平均實際E值為9.41,由此確定最佳的提取組合為T1V1P2C1組合即提取溫度40℃,料液比3∶30(g/mL),超聲波功率200W,提取醇濃度65%,與正交試驗結果吻合。
2.3 pH值對篤斯越橘果實花青素穩定性的影響
pH值對篤斯越橘果實花青素穩定性的影響花見表3。
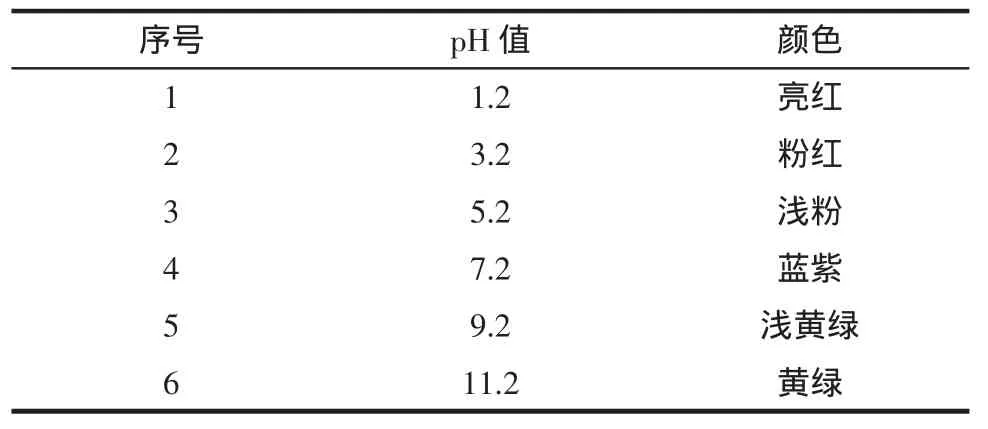
表3 pH值對篤斯越橘果實花青素顏色的影響Table3 Effectsof pH on the color of anthocyanin
花青素受pH值變化影響較大,不同pH值條件下,篤斯越橘花青素溶液呈現肉眼可辨的色澤變化,在酸性條件下呈現紅色至粉色的變化趨勢;中性條件下變成藍紫色,堿性條件下再次轉為黃綠色。
pH值對篤斯越橘果實花青素穩定性的影響花見圖1。
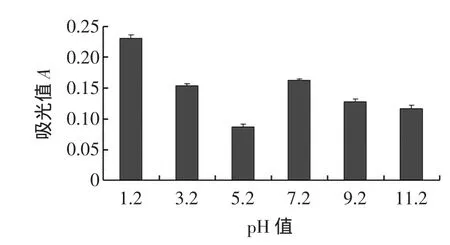
圖1 pH值對篤斯越橘果實花青素穩定性的影響Fig.1 Effectsof pH on the stability ofanthocyanin
處理的吸光值變化幅度較大。pH值為1.2~5.2時,隨pH值的增加吸光值逐漸減小;pH值為7.2吸光值迅速回升,而后下降。pH值對篤斯越橘果實花青素色澤穩定性影響較大,因此在花青素的利用上要考慮制品的pH變化帶來的色澤改變。
2.4 氧化劑H2O2對篤斯越橘果實花青素穩定性的影響
氧化劑H2O2對篤斯越橘果實花青素穩定性的影響見圖2。
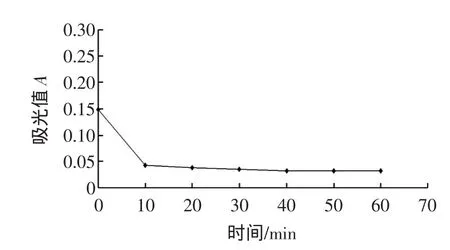
圖2 氧化劑H2O2對篤斯越橘果實花青素穩定性的影響Fig.2 Effectsof oxidantsH2O2on thestability of anthocyanin
篤斯越橘果實花青素提取液中加入1mmol/L雙氧水后,色澤變化明顯,其吸光度也呈現明顯的下降趨勢,這表明提取液對氧化劑的耐受性不強,極易發生直接或間接的氧化反應,導致化學組成變化,原有色澤被破壞,因此在加工利用過程中,應盡量避免與氧化劑的直接接觸。
2.5 抗壞血酸對篤斯越橘果實花青素穩定性的影響抗壞血酸對篤斯越橘果實花青素穩定性的影響見圖3。
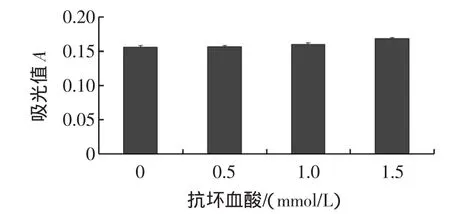
圖3 抗壞血酸對篤斯越橘果實花青素穩定性的影響Fig.3 Effectsof reducing agenton thestability of anthocyanin
不同濃度抗壞血酸引起篤斯越橘果實花青素的吸光值變化并不顯著,顯然還原性環境有利于花青素穩定,由此說明還原劑對篤斯越橘果實花青素穩定性影響不大。
2.6 金屬離子對篤斯越橘果實花青素穩定性的影響
金屬離子對篤斯越橘果實花青素穩定性的影響見圖4。
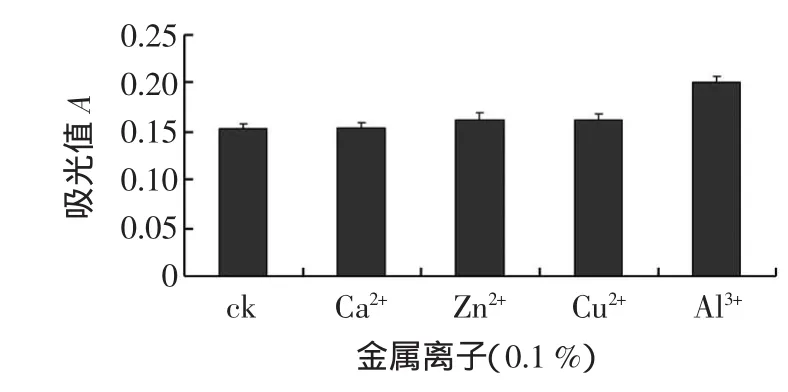
圖4 金屬離子對篤斯越桔果實花青素穩定性的影響Fig.4 Effectsofm etal ion on the stability of anthocyanin
提取物在pH=3.0濃度為0.1%的各試驗金屬離子的溶液中吸光值變化不顯著,由此說明篤斯越橘果實花青素在試驗條件下對Ca2+、Mg2+、Zn2+、Cu2+、Al3+相對穩定。
2.7 光對篤斯越橘果實花青素穩定性的影響
提取液分別放置在室外自然光、室內自然光、暗室3種光照條件6 d后,目測觀察到室內自然光、暗室處理條件下,提取液的顏色無明顯變化,而在室外自然光處理提取液由亮紅色變為亮橙色,顏色變化較為明顯大。光對篤斯越橘果實花青素穩定性的影響見圖5。
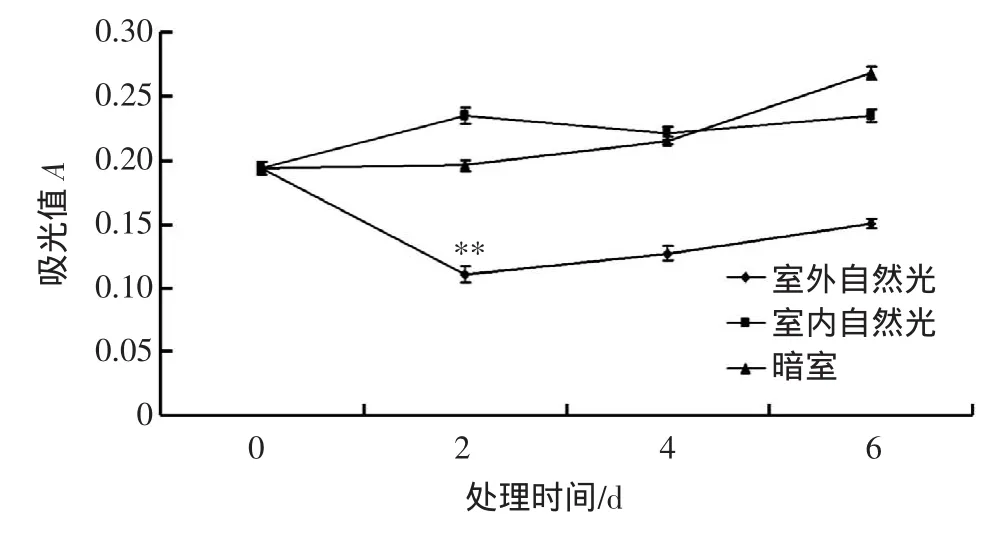
圖5 光對篤斯越橘果實花青素穩定性的影響Fig.5 Effectsof lighton the stability of anthocyanin
提取液吸光值在室外自然光照條件放置兩天即與對照呈現極顯著差異,而室內自然光和暗室條件下放置的樣品吸光值變化差異不顯著。由此可見篤斯越橘果實花青素提取液對較強的光線直射不穩定,成分與色澤均有較顯著的變化,而弱光和避光條件有利于樣品的保存,因此在加工制品的包裝與產品的儲運過程中,應充分考慮光照條件對產品的影響。
3 結論
1)通過利用超聲波輔助,對篤斯越橘果實花青素進行提取,對溫度、料液比、超聲波功率和醇濃度進行正交試驗,確定了最佳提取條件。結果為:最佳提取溫度為40℃,最佳料液比為3∶30(g/mL),最佳超聲波功率為200W,最佳提取液濃度為65%的酸化乙醇。
2)對篤斯越橘果實花青素的穩定性研究結果表明:篤斯越橘果實花青素提取液對pH值敏感;氧化劑H2O2對篤斯越橘果實花青素提取液穩定性影響較大;還原劑抗壞血酸對篤斯越橘果實花青素穩定性影響較小;在pH值為3.0時篤斯越橘果實花青素提取液對Ca2+、Mg2+、Zn2+、Cu2+、Al3+較穩定;篤斯越橘果實花青素提取液對室外自然光照射穩定性較差保存過程中應盡量采取避光措施,以免影響產品品質。
[1]宗長玲,鄧萌,宗成文,等.篤斯越橘研究進展[J].北方園藝,2011 (12):173-176
[2]中國科學院中國植物志編輯委員會.中國植物志 (57卷)[M].北京:科學出版社,1991:156-158
[3]王二雷,林松毅,劉靜波,等.篤斯越橘中花青素含量分析[J].食品科學,2007,28(10):460-463
[4]鄭美香,宗長玲,宋春艷,等.長白山篤斯越橘離體器官再生不定芽的研究[J].延邊大學農學學報,2013,35(4):293-297
[5] 宗長玲,鄧萌,宗成文,等.篤斯越橘研究進展[J].北方園藝,2011 (12):173-176
[6]LIR,WANG P,GUOQQ,etal.Anthocyanin composition and contentof the Vaccinium uliginosum berry[J].Food Chem,2011,125(1): 116-120
[7]OCHMIAN I,OSZMIA N′SKIJ,SKUPIE N′K.Chemical composition,phenolics,and firmnessofsmallblack fruits[J].JAppl Bot Food Qual,2012,83(1):64-69
[8]史經略.藍莓啤酒的研制[J].中國釀造,2009,28(1):180-182
[9]RODRIGUEZ-MATEOSA,CIFUENTES-GOMEZ T,TABATABAEES,etal.Procyanidin,anthocyanin,and chlorogenic acid contents of high-bush and lowbush blueberries[J].JAgr Food Chem,2012, 60(23):5772-5778
[10]陳亮,楊志勇,辛秀蘭,等.藍莓果酒發酵期間抗氧化成分及活性研究[J].中國釀造,2013,32(12):25-28
[11]LACOMBE A,WU V CH,WHITE J,etal.The antimicrobial propertiesof the lowbush blueberry(Vaccinium angustifolium)fractional compo-nents against foodborne pathogens and the conservation of probiotic Lac-tobacillus rhamnosus[J].Food Microbiol,2012,30(1): 124-131
[12]鄭紅巖,高夢,劉建蘭,等.不同品種藍莓果實品質分析[J].食品與發酵工業,2013,39(11):245-249
[13]李影,韓立杰,劉子菱,等.不同種類酵母對藍莓果酒品質的影響[J].食品科技,2014,39(4):73-77
[14]YOUSEFGG,BROWN A F,FUNAKOSHIY,etal.Efficientquantifica-tion of the health-relevant anthocyanin and phenolic acid profiles in com-mercial cultivars and breeding selections of blueberries(Vaccinium spp.)[J].JAgr Food Chem,2013,61(20):4806-4815
[15]李憲平.野生篤斯越橘馴化栽培研究[D].北京:中國農業科學院, 2007:14-15
[16]劉會靈,曹建新.越橘屬植物的研究進展[J].天然產物研究與開發,2009(5):905-911,870
[17]LEE J,DURST R W,WROLSTAD R E.Deter mination of total monomeric anthocyanin pigment content of fruit juices,beverages, natural colorants,and wines by the pH differentialmethod:collaborative study[J].Journal of AOAC international,2005,88(5):1269-1278
Extraction and Determ ination of Stability of Anthocyanin from the Fruit of Vaccinium uliginosum L.
LIYang-yang,PENGKan-kan,YANG Jiu-shuang,JUAn-ji,XU Yong-qing*
(Collegeof Life Science,NortheastAgriculturalUniversity,Harbin 150030,Heilongjiang,China)
This research was aimed to determine the best condition for extracting anthocyanin from fruits of Vaccinium uliginosum L.with orthogonalexperimentaldesign by the ultrasound-assisted ethanolextraction process.Itwas determined that the optimum extraction temperature was 40℃,the optimum material liquid ratio was 3∶30(g/mL),the optimum ultrasonic powerwas 200W and the optimum extraction condition was 65% acidified ethanol.The resultofdetermination ofstability ofanthocyanidin from the fruitof Vaccinium uliginosum L.showed that:anthocyaninwassensitive to pH;oxidanthad larger impacton the stability ofanthocyanin;reducingagenthad littleeffecton the stability ofanthocyanin;when the pH was3.0,anthocyanin from the fruitof Vaccinium uliginosum L.toCa2+,Mg2+,Zn2+,Al3+,Cu2+wasmorestable;ithad better stability on indoornatural lightand dark,and poorstability on outdoornatural light.
Vaccinium uliginosum L.;anthocyanin;extraction;stability
10.3969/j.issn.1005-6521.2016.24.011
2016-09-12
國家基礎科學人才培養基金子課題資助項目(J1210069)作者簡介:李陽陽(1993—),女(漢),學士,研究方向:生物化學與分子生物學。
*通信作者:徐永清(1977—),女,副教授,博士,研究方向:資源植物學與植物次生代謝產物代謝。

