釀酒酵母生產谷胱甘肽合成酶系發酵條件的研究
董永勝,馬蕾,王艷杰
(齊魯工業大學生物工程學院,山東濟南250353)
釀酒酵母生產谷胱甘肽合成酶系發酵條件的研究
董永勝,馬蕾,王艷杰
(齊魯工業大學生物工程學院,山東濟南250353)
研究釀酒酵母NJ-16生產谷胱甘肽合成酶系的發酵條件,確定酵母最適產酶條件為:搖床轉速180 r/min,pH 5.0,培養溫度32℃,培養基中硫酸鎂含量為2 g/L。此條件下,釀酒酵母NJ-16的谷胱甘肽合成酶系的活性為12.5U/g濕菌體。
釀酒酵母;谷胱甘肽合成酶系;發酵條件
谷胱甘肽合成酶系是催化L-谷氨酸、L-半胱氨酸和甘氨酸生成谷胱甘肽(Glutathione,GSH)的酶,由γ-谷氨酰半胱氨酸合成酶(GSH-Ⅰ)和谷胱甘肽合成酶(GSH-Ⅱ)組成[1-2]。谷胱甘肽具有清除自由基、解毒、延緩衰老、預防糖尿病、保護肝臟、抗輻射、提高人體免疫力、抑制艾滋病病毒、防止皮膚老化等功能[3-4],在臨床醫學、運動營養學、食品加工等眾多領域具有重要的應用價值和產業前景[5-6],其工業化生產越來越受到關注。谷胱甘肽作為生物活性物質,已越來越多地應用于食品工業中[7],如在面制品中能起到強化氨基酸的作用,在肉類和海鮮食品中可強化風味并延長保鮮期,在水果蔬菜類飲料中可有效防止食品褐變,還可用于幫助人們排毒的功能食品的生產[8]。
酵母發酵法是生產谷胱甘肽的主要方法,酵母谷胱甘肽合成酶系的活性對谷胱甘肽的產量有決定性的作用,但正常酵母的酶系活性較低,為提高谷胱甘肽產量,常采用各種育種技術進行生產菌株的選育[9-10]。目前對酵母生產谷胱甘肽的發酵條件有較多的研究[11],也對酵母在極端條件下合成谷胱甘肽進行了一些研究[12-13],但對酵母合成谷胱甘肽合成酶系的培養條件研究較少。作者以選育的釀酒酵母NJ-16為出發菌株,以提高酵母谷胱甘肽合成酶系的活性為研究目標,探討酵母高產谷胱甘肽合成酶系的發酵條件,為提高酵母工業化谷胱甘肽產率提供參考。
1 材料與方法
1.1 菌種
釀酒酵母(S.cerevisiae)NJ-16:山東省微生物工程重點實驗室選育。
1.2 培養基
種子培養基(g/L):葡萄糖20,蛋白胨20,酵母膏10,pH 6.0。
發酵培養基(g/L):葡萄糖30,蛋白胨10,酵母膏5,(NH4)2SO45.0,KH2PO45.0,MgSO42.0,pH 5.0。
1.3 酵母培養
從活化斜面上挑取一環菌體接入到種子培養基中,30℃靜置培養24 h。然后將酵母種子培養液以10%的接種量接入到發酵培養基中培養。
1.4 生物量測定
取發酵液25 mL,離心收集菌體,用蒸餾水沖洗3次,離心收集菌體,于70℃烘干至恒重后稱重。
1.5 谷胱甘肽合成酶系活性的測定
將發酵液離心收集細胞,用磷酸緩沖液洗滌菌體,離心收集細胞。取1.0 g濕菌體加入到19.6mL的0.03mol/L、pH7.2的磷酸緩沖液中,再加入0.4mL的甲苯,在35℃下處理2 h。離心收集上清液,即得粗酶液。取10.0mL粗酶液加入到10.0mL反應液中,在37℃、150 r/min下反應1 h,反應液再在沸水浴中保溫10min。離心取上清液,采用HPLC法測定上清液中谷胱甘肽的含量。谷胱甘肽合成酶系活力單位定義:上述反應條件下,每小時轉化生成1mg谷胱甘肽的酶量為1個酶活單位。
反應液組成:40mmol/LL-谷氨酸,20mmol/LL-半胱氨酸,20mmol/L甘氨酸,20mmol/LMgC12,200mmol/L磷酸緩沖液(pH 7.0)。
2 結果與討論
2.1 溫度對酵母合成谷胱甘肽合成酶系的影響
將酵母接種于發酵培養基中,于160 r/min下培養20 h,溫度分別控制在26、28、30、32、34、36、38℃,結果如圖1所示。
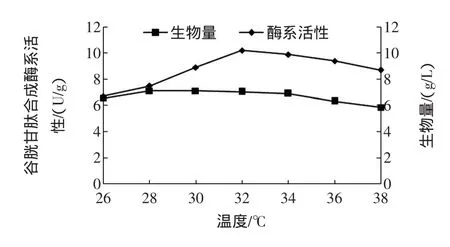
圖1 不同培養溫度下酵母谷胱甘肽合成酶系活性和生物量的變化Fig.1 Changesof theglutathionesynthetasesactivity in the S. cerevisiae cellsand biom asscultured under different tem perature
由圖1可知,發酵溫度對谷胱甘肽合成酶系的活性有明顯影響:隨著溫度的升高酶系活性也隨之升高,32℃時酶系活性達到最高為10.2 U/g濕菌體,比28℃時提高36.0%,說明酵母產酶的溫度高于其生長最適的溫度;在試驗條件下,較高的發酵溫度有利于酶系的合成,如38℃時酶系活性也高于28℃,但卻低于32℃,這是由于較高溫度下酵母代謝相對變慢而引起的,且38℃培養時酵母生物量也比32℃下降了17.7%。因此在釀酒酵母生產谷胱甘肽時,采用較高的培養溫度即可達到較高的生物量,又可提高谷胱甘肽合成酶系的活性,進而提高谷胱甘肽的產量。
2.2 pH對酵母合成谷胱甘肽合成酶系的影響
調發酵培養基的pH值分別為3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0,將酵母接種于不同pH的培養基中,于32℃、160 r/min下分別培養20 h,培養過程中pH的控制通過流加3mol/L的H2SO4或3mol/L的NaOH進行調節,結果如圖2所示。
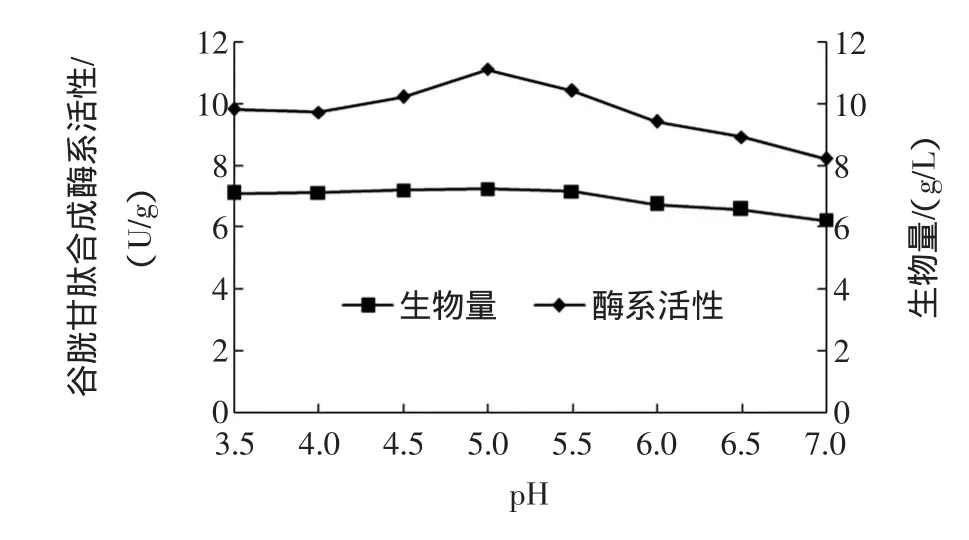
圖2 不同pH下酵母谷胱甘肽合成酶系活性的變化Fig.2 Changesof theglutathione synthetasesactivity in the S. cerevisiae cellsand biomass cultured under differentpH
由圖2可知,pH對酵母谷胱甘肽合成酶系的活性也有明顯影響:酵母在相對較低的pH下培養時酶系活性較高,在pH 5.0時酶系活性達到最高為11.1U/g濕菌體,比pH 7.0時高35.4%,這與釀酒酵母的生長最適pH相同。在pH4.0~5.5之間酵母的生物量變化不大,但在pH 7.0時酵母的生物量與pH 5.0相比下降了14.1%。與圖1相比,恒pH 5.0下酶系活性提高8.8%,這是由于在圖1條件下培養基的初始pH在發酵過程中發生了變化,進而影響到酵母酶系的產率,因此采用恒定pH培養可避免這種影響。
2.3 溶氧對酵母合成谷胱甘肽合成酶系的影響
微生物酶產量與發酵液中的氧含量有直接關系,發酵液中溶氧量與搖床轉速有關。取發酵培養基100mL于500mL三角瓶中接種酵母,于32℃、不同搖床轉速下培養20 h。搖床轉速對酵母谷胱甘肽合成酶系活性的影響如圖3所示。
由圖3可知,隨著轉速增加,酵母的生物量和酶系活性都隨之上升;在轉速160 r/min~200 r/min之間時,酶系活性和生物量都達到相對較高的數值,且基本穩定,因此搖床轉速以160 r/min即可。
2.4 無機鹽對酵母合成谷胱甘肽合成酶系的影響
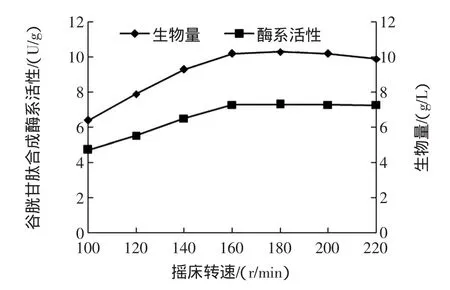
圖3 搖床轉速對酵母合成谷胱甘肽合成酶系和生物量的影響Fig.3 Effectof rotationalspeed on the synthesisof glutathione synthetasesand biom ass
在發酵培養基中分別添加2 g/L的硫酸鈉、氯化鈉、硫酸鉀、氯化鉀以替代硫酸鎂,將酵母于32℃、160 r/min下培養20 h。結果如圖4所示。
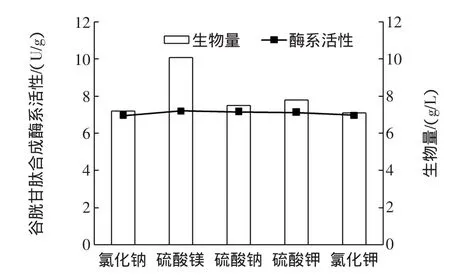
圖4 無機鹽對酵母合成谷胱甘肽合成酶系和生物量的影響Fig.4 Effectof inorganic saltson the synthesisof glutathione synthetasesand biom ass
由圖4可知,不同無機鹽對酵母谷胱甘肽合成酶系活性的影響不同:當培養基中存在硫酸鎂時酶系活性最高;而其他4種鹽存在時,與硫酸鎂相比酶系活性相對下降較多。硫酸鎂使谷胱甘肽合成酶系活性升高的原因是Mg2+為γ—谷氨酰半胱氨酸合成酶和谷胱甘肽合成酶活性中心的輔因子,酶系的合成需要Mg2+的參與。在不同無機鹽下培養酵母時,生物量相對變化不大,說明上述無機鹽對酵母生長的影響較小。因此,在酵母發酵生產谷胱甘肽合成酶系時,應在培養基中添加一定量的硫酸鎂。
2.5 酵母合成谷胱甘肽合成酶系的發酵條件優化
在實際生產中,由于各種因素相互影響,為選出最佳產酶條件,根據單因素對酵母合成谷胱甘肽合成酶系的影響,以培養溫度、pH、轉速和硫酸鎂用量4種因素為影響因子,采用L9(34)正交表進行試驗,試驗結果及分析見表1。
從表中看出:培養溫度、pH、轉速和硫酸鎂用量四因素對酵母谷胱甘肽合成酶系活性的影響順序為:轉速>pH>溫度>硫酸鎂用量,其最佳產酶條件為A2B2C3D2,即轉速為180 r/min、pH為5.0、培養溫度為32℃、硫酸鎂用量為2 g/L。此條件下,酵母谷胱甘肽合成酶系活性最高,驗證試驗其酶系活性為12.5U/g濕菌體。
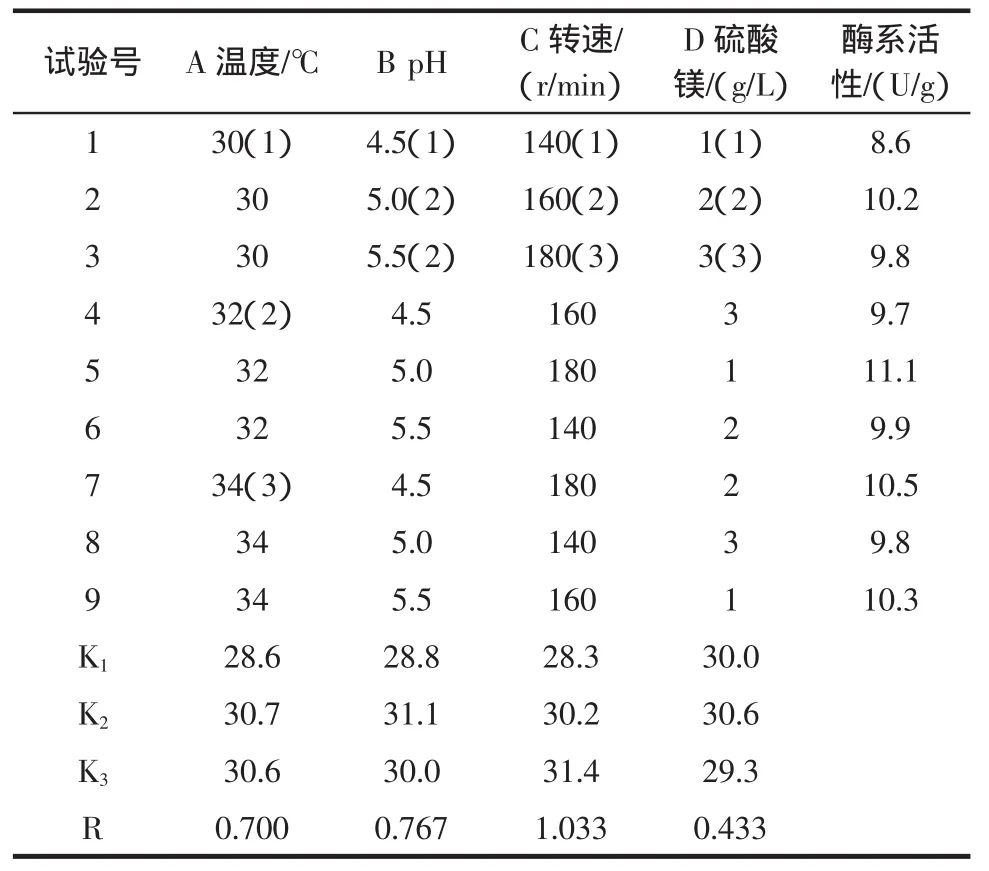
表1 正交表及試驗結果分析Table1 Orthogonal listand the resultanalysisof test
3 結論
釀酒酵母合成谷胱甘肽合成酶系的最適溫度與其生長最適溫度不同,酵母在32℃培養時,酶系活性高于其最適生長溫度;而產酶和生長的最適pH相同,即pH為5.0時,酶系活性最高。釀酒酵母合成谷胱甘肽合成酶系的最佳條件為:搖床轉速為180 r/min,發酵液pH為5.0,發酵溫度為32℃,培養基中硫酸鎂用量為2 g/L,此條件下,酵母谷胱甘肽合成酶系活性可達到12.5U/g濕菌體。本文關于酵母生產谷胱甘肽合成酶系發酵條件的研究,對谷胱甘肽工業化生產具有一定的指導意義。
[1]Wang D Z,Wang C,Wu H,etal.Glutathione production by recombinant Escherichia coli expressing bifunctional glutathione synthetase [J].Journal of Industrial Microbiology&Biotechnology, 2016,43(1):45-53
[2] Hara KY,Kiriyama K,Inagaki A,et al.Improvement of glutathione production bymetabolic engineering the sulfate assimilation pathwayofSaccharomycescerevisiae[J].ApplMicrobiolBiotechnol,2012, 94(5):1313-1319
[3] Ge S,Zhu T,LiY.Expression ofbacterialGshF in Pichiapastoris for glutathione production[J].Appl Environ Microbiol,2012,78(15): 5435-5439
[4]陳志穎,張子健,焦瑞,等.利用啤酒廢酵母擴培物制備富含谷胱甘肽酵母抽提物[J].中國釀造,2015,34(11):61-65
[5]鄭麗雪,劉夢瀅,王立梅,等.不同發酵時期添加金屬離子對釀酒酵母合成谷胱甘肽的影響[J].食品研究與開發,2014,35(6):93-95
[6] 董永勝,馬蕾,王艷杰.提高微生物谷胱甘肽產率措施的探討[J].中國釀造,2016,35(5):6-9
[7]李麗.甘薯中還原型谷胱甘肽的提取及熒光檢測[J].中國食品添加劑,2015(7):162-166
[8] Yanping T,Wen J,Na G,et al.Inhibitory effects of glutathione on dengue virus production[J].BiochemBioph Res Co,2010,397(3): 420-423
[9] 楊建花,李娓,王德正,等.表達雙功能谷胱甘肽合成酶的重組巴斯德畢赤酵母的構建與鑒定[J].工業微生物,2013,43(5):32-36
[10]Vira M U,Taras Y N,Olena G S,et al.GSH2,A gene encodingγglutamylcysteinesynthetase in the methylotrophic yeast Hansenulapolymorpha[J].FEMSYeastResearch,2002,2(3):327-332
[11]劉哲,詹良靜,張新宜,等.高產谷胱甘肽釀酒酵母的選育及發酵工藝的研究[J].微生物學雜志,2013,33(1):25-29
[12]周斌,李清亮,陳娜,等.溫和壓力對面包酵母CICC1447谷胱甘肽合成的影響[J].食品研究與開發,2014,35(9):111-114
[13]鄭麗雪,王斌,朱娉,等.利用低pH處理促進釀酒酵母2-10515生產谷胱甘肽[J].食品研究與開發,2014,35(21):116-118
Study on Fermentation Conditions of Glutathione Synthetases Producted by S.cerevisiae
DONGYong-sheng,MA Lei,WANGYan-jie
(CollegeofBioengineering,Qilu University of Technology,Jinan 250353,Shandong,China)
The fermentation conditions of glutathione synthetasesproducted by S.cerevisiae NJ-16 were researched,and the optimal conditions of enzymes production were determined as follows:rotational speed180 r/ min,pH 5.0,fermentation temperature 32℃,the dosage ofmagnesium sulphate inmedium was 2 g/L.Under these culture conditions,the activity of glutathione synthetasesproducted by S.cerevisiae NJ-16 was 12.5 U/g wetcell.
S.cerevisiae;glutathione synthetases;fermentation condition
10.3969/j.issn.1005-6521.2016.24.036
2016-03-25
董永勝(1964—),男(漢),教授,博士,主要研究方向:食品發酵。

