TiO2--Fe2O3復合材料的制備及對水體中Cu(II)離子的凈化
李銀輝,盧愛黨,韓 健,陳建新,張 娜
(1.河北工業大學 海洋科學與工程學院,天津 300130;2.海水資源高效利用化工技術教育部工程研究中心,天津 300130)
TiO2--Fe2O3復合材料的制備及對水體中Cu(II)離子的凈化
李銀輝1,2,盧愛黨1,2,韓 健1,2,陳建新1,2,張 娜1
(1.河北工業大學 海洋科學與工程學院,天津 300130;2.海水資源高效利用化工技術教育部工程研究中心,天津 300130)
以氯化亞鐵為鐵源,通過水熱合成方法制備了FeOOH,再以FeOOH為基底,鈦酸丁酯為鈦源,通過水熱合方法制備TiO2--Fe2O3復合材料,并利用XRD和SEM對所制備的TiO2--Fe2O3復合材料進行了表征.研究了TiO2--Fe2O3復合材料對水體中Cu(II)離子的吸附性能,考察了Cu(II)離子的初始濃度、Cu(II)離子溶液的pH值、反應時間等條件對TiO2--Fe2O3復合材料吸附性能的影響,并闡述了TiO2--Fe2O3復合材料對Cu II離子的吸附機理.結果表明:TiO2--Fe2O3復合材料是1種有效的Cu(II)離子吸附劑,對Cu(II)離子能快速吸附并達到吸附平衡.同時 TiO2--Fe2O3復合材料中含有具有磁性的 -Fe2O3,通過外加磁場,可以達到快速回收的目的,無需高速離心分離粉末,能節約能耗,降低分離成本,因此可作為1種有前景的功能分離材料應用于重金屬離子廢水的處理.
TiO2--Fe2O3;Cu(II)離子;初始濃度;pH值;反應時間;吸附性能
0 引言
工業廢水中的重金屬在水體中不能被微生物降解,直接危害水體的生態環境,并能沿食物鏈進入人體,在人體內與蛋白質及各種酶發生作用、富集造成人體中毒,危害人體健康.重金屬污染問題已引起環境科學領域及相關部門的廣泛關注[1].其中,過多的銅離子進入人體內可出現惡心、嘔吐、上腹疼痛、急性溶血和腎小管變形等中毒現象,易對人體內的臟器造成負擔,特別是肝和膽,當這2種器官出現問題后,維持人體內的新陳代謝就會出現紊亂,嚴重時可出現肝硬化,肝腹水.因此,對水體中銅離子的處理對保護水體生態環境和人體健康具有重要的實際意義.
傳統治理重金屬污染的方法包括離子交換法[2]、化學沉淀法[3]、膜分離法[4]、吸附法[5,9]和電解法[10]等.從經濟有效的觀點來看,吸附法被公認為最有前景和廣泛使用的方法,它具有吸附劑廉價易得、能耗低、不產生二次污染、對設備要求不高的優點.常用的吸附材料有活性炭、生物質、金屬氧化物、粉煤灰、蒙脫土和沸石等[11-16].由于重金屬離子能在金屬氧化物表面發生物理和化學吸附,能達到較好的吸附效果.因此,利用復合材料研究其對銅離子的吸附性能.
1 實驗部分
1.1 實驗藥品
CuO(自制), 氯化亞鐵(FeCl2·4H2O,分析純,天津市大茂化學試劑廠),氨水(NH3·H2O,25%~28%,分析純,天津市風船化學試劑科技有限公司),鈦酸丁酯(CH3CH23O4Ti,化學純,天津市光復精細化工研究所),硫酸銅(CuSO4·5H2O,分析純,天津市風船化學試劑科技有限公司),硝酸(HNO3,分析純,天津市福晨化學試劑廠),氫氧化鈉(NaOH,分析純,天津市福晨化學試劑廠).
1.2 TiO2--Fe2O3復合材料的制備
1)羥基氧化鐵的制備:將50 mg的CuO納米球采用超聲分散法分散到70 m L去離子水中,然后向上述溶液中加入50 mg FeCl2,將混合溶液在聚四氟高壓反應釜中170℃保持一定時間,冷卻至室溫后,沉淀用氨水和去離子水(體積比為1∶1)的混合液洗滌3次,再用去離子水和乙醇交替洗滌3次,80℃干燥10h,即可得到羥基氧化鐵粉末;2)磁性復合材料的制備:利用1)所制備的羥基氧化鐵為載體,同時作為制備三氧化二鐵的原料,將一定量鈦酸丁酯在室溫下溶解在100 m L無水乙醇(蒸餾水)中,按比例將一定量的FeOOH粉體加入到溶解好的鈦酸丁酯溶液中,超聲分散5 m in,將上述混合液轉移到反應釜中,在聚四氟高壓反應釜中180℃保持12 h,冷卻至室溫后,沉淀用乙醇或蒸餾水洗滌,烘干即得復合材料.其中.
1.3 Cu(Ⅱ)離子標準溶液的配制
準確稱取CuSO45H2O 0.390 1g,用一定量的蒸餾水溶解,倒入l00m L容量瓶中,用蒸餾水稀釋至刻度,搖勻.即配制成濃度為1 g/L的銅離子標準溶液.
1.4 重金屬吸附實驗
分別取25 m L的已知濃度的含銅離子廢水,置于50 m L小瓶中,加入一定量的復合材料,用硝酸和氫氧化鈉控制反應體系的pH值,磁力攪拌反應一定時間后過濾,采用原子吸收分光光度計(AAS)測定濾液中殘余的重金屬離子含量,由反應前后的Cu(II)離子濃度變化,計算復合材料對離子的吸附率和吸附容量.
重金屬離子的吸附率和吸附容量分別按式 (1)和式 (2)計算

式中:E為吸附劑對重金屬離子的吸附率;q為吸附劑對重金屬離子的吸附容量;C0為重金屬離子的初始濃度,g/m L;Ci為重金屬離子的殘余濃度,g/m L;m為吸附劑質量,g;V為溶液體積,m L.
2 結果與討論
2.1 TiO2--Fe2O3復合材料的表征
由圖1可以看出,利用氯化亞鐵合成的氧化鐵為羥基氧化鐵,如圖1b所示,然后以鈦酸丁酯為鈦源,再經過180℃水熱合成12 h后,FeOOH發生了晶型的改變,從原來的纖鐵礦(PDF#08-0098)變為(PDF#39-1346),如圖1a所示,復合材料中二氧化鈦呈銳鈦礦型結構.
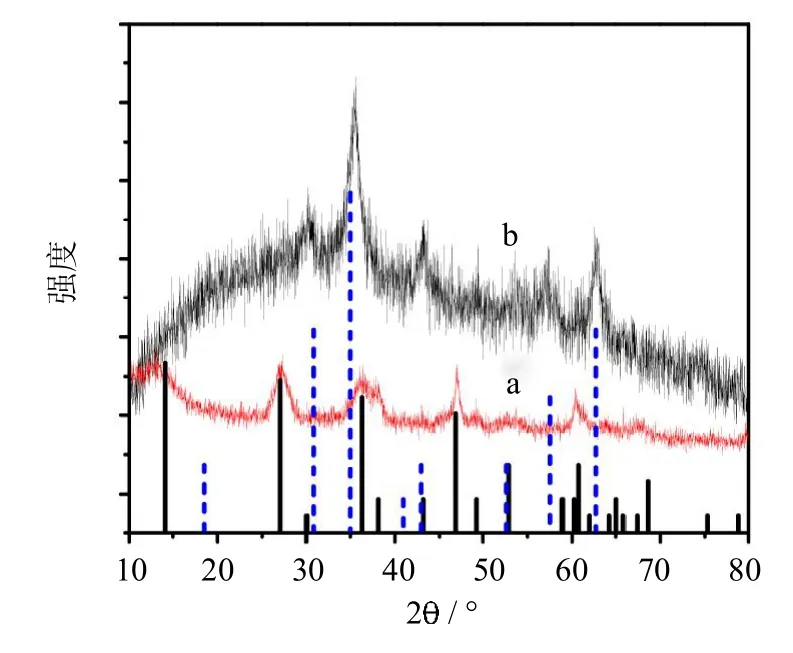
圖1 TiO2--Fe2O3復合材料和FeOOH的XRD衍射圖Fig.1 The XRD patternsof TiO2--Fe2O3compositesand FeOOH

圖2 TiO2--Fe2O3復合材料的SEM照片Fig.2 The SEMimageof TiO2--Fe2O3composites
2.2 Cu(II)離子初始濃度對TiO2--Fe2O3復合材料吸附率的影響
采用pH=4.0的緩沖溶液配制濃度分別為5mg/L,10mg/L,15mg/L,20 mg/L,25 mg/L的Cu(II)離子,分別取上述溶液25m L置于樣品瓶中,加入復合材料,超聲分散2m in后放入25℃恒溫水浴中進行吸附實驗,并定時取樣.測得吸附率曲線如圖3所示,由圖3可知,不同初始濃度下復合材料對Cu(II)離子的吸附效果不同,在初始濃度為5mg/L時吸附效果最好,能達到80%左右,且吸附過程均為快速吸附,在前10min吸附率已達到最大值.
2.3 TiO2--Fe2O3復合材料對Cu(II)離子的吸附容量

圖3 不同Cu(II)離子初始濃度的吸附率的測定Fig.3 Effectof initialCu(II)ions concentration on ion removal from aqueoussolution by TiO2--Fe2O3composites
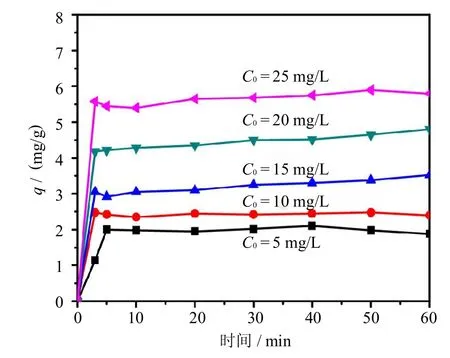
圖4 Cu(II)離子初始濃度對TiO2--Fe2O3復合材料的吸附容量的影響Fig.4 Effectof Cu(II)ions initialconcentration to adsorption capacity by TiO2--Fe2O3composites
2.4 pH值對TiO2--Fe2O3復合材料吸附性能的影響
取25m L(C Cu II=10mg/L)模擬廢水共6份,加入復合材料,用稀的氫氧化鈉溶液和稀的硝酸溶液調節溶液pH值,在室溫下攪拌1 h后過濾,測定濾液中Cu(II)離子的殘余濃度,測定結果如圖5所示.
由圖5可知,廢水中Cu(II)離子的去除率隨著吸附時間增加而增大,且基本上在前1h即達到最大,說明吸附的過程屬于快速吸附.在較低pH值時,隨著時間的延長吸附率略有降低,原因是部分被吸附的Cu(II)離子解吸附,pH越高,這種現象越不明顯,直到pH>6時,無解吸的現象.復合材料在不同pH值條件下對水中Cu(II)離子的吸附實驗,結果表明,在3 h內即可達到吸附平衡.
2.5 TiO2--Fe2O3復合材料對Cu(II)的等溫吸附
TiO2--Fe2O3復合材料對 Cu(II)離子的吸附等溫線如圖6所示.由圖6中曲線的趨勢可知,TiO2-Fe2O3復合材料對Cu(II)離子的吸附等溫線符合吸附等溫形式II型[17].吸附等溫形式II型可用BET公式進行描述,表示吸附劑上有多層溶質分子被吸附,而各層的吸附均符合Langmuir單分子層吸附.
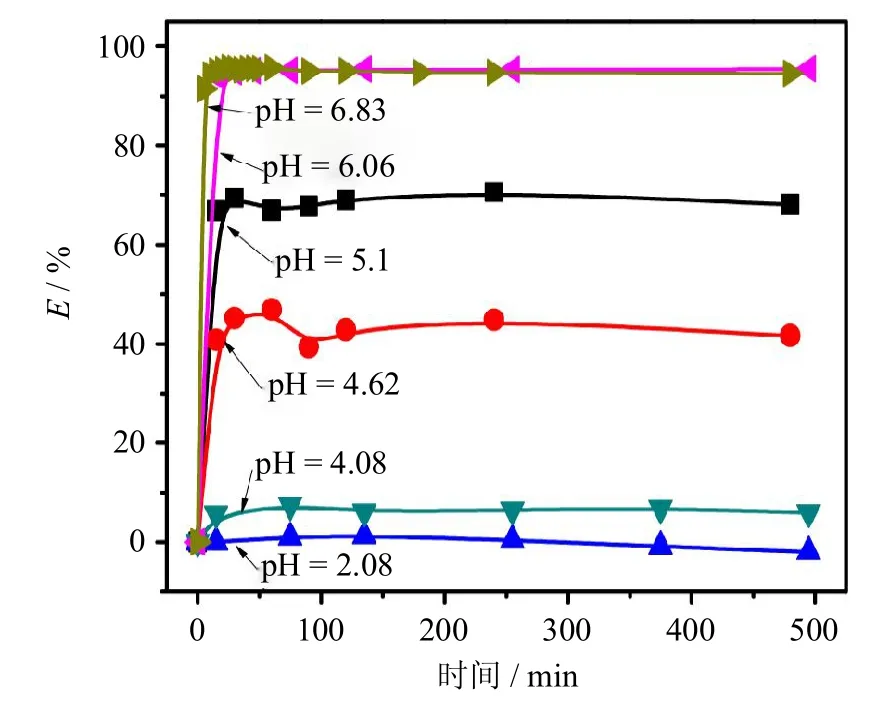
圖5 不同pH值條件下反應時間對吸附率的影響.Fig.5 Plotsof absorption vs time for the absorbentwith
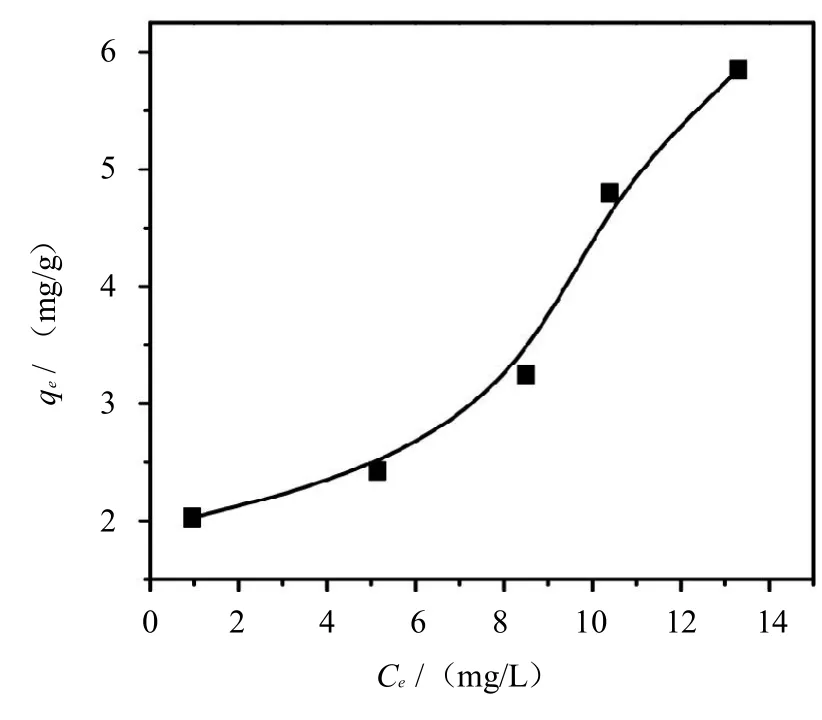
圖6 Ti-Fe2O3-10對Cu(II)離子的吸附等溫線Fig.6 Adsorption isotherms for Cu(II)ions removal by TiO2--Fe2O3composites
3 結論
利用TiO2--Fe2O3復合材料研究了其對水體中銅離子的吸附性能,結果表明:
1)TiO2--Fe2O3復合材料對Cu(II)離子具有良好的吸附性能,加入相同量的TiO2--Fe2O3復合材料,隨著Cu(II)離子初始濃度的升高,TiO2--Fe2O3復合材料對Cu(II)離子的吸附容量增加,且TiO2--Fe2O3復合材料能快速的吸附Cu(II)離子.在其他條件相同,反應時間不同的情況下,隨著反應時間的延長,TiO2--Fe2O3復合材料對Cu(II)離子的吸附率逐漸增加,當達到最大值時,TiO2--Fe2O3復合材料對Cu(II)離子的吸附率略有減小,可能是由于少量Cu(II)離子發生解吸造成的.
2)在其他條件相同,不同pH值的情況下,當pH>6時,TiO2--Fe2O3復合材料對Cu(II)離子的吸附率最高.
3)TiO2--Fe2O3復合材料對Cu(II)離子的吸附為多層溶質分子吸附,各層的吸附則符合Langmuir單分子層吸附.
總之,這種復合材料作為吸附劑應用于水體中重金屬離子的除去具有良好的效果,是一種有應用前景的功能材料.
[1]Mercier L,Pinnavaia T J.Access inmesoporousmaterials:Advantagesofauniform pore structure in the design of aheavymetal ion adsorbent for environmental remediation[J].Advanced Materials,1997,9(6):500-503.
[2]Oehmen A,VergelD,Fradinho J,etal.Mercury removal from waterstreams through the ionexchangemembranebioreactorconcept[J].Journal of hazardousmaterials,2014,264(2):65-70.
[3]Wang G,Chang Q,Han X,etal.RemovalofCr(VI)from aqueoussolutionby flocculantwith thecapacity of reductionand chelation[J].Journal of hazardousmaterials,2013,248(6):115-121.
[4]Zhong Y J,You S J,Wang X H,etal.Synthesis of carbonaceous nanowiremembrane for removing heavymetal ions and high water flux[J].Chem ical Engineering Journal,2013,226(15):217-226.
[5]Liu A M,HidajatK,Kaw iS,etal.A new classof hybridmesoporousmaterialswith functionalized organicmonolayers for selective adsorption of heavymetal ions[J].Chem icalCommunications,2000,13(13):1145-1146.
[6]U nlüN,Ersoz M.Adsorption characteristics of heavy metal ions onto a low cost biopolymeric sorbent from aqueous solutions[J].Journal of HazardousMaterials,2006,136(2):272-280.
[7]楊文瀾.殼聚糖聯合堿改性粉煤灰對重金屬離子的吸附特性 [J].環境工程學報,2009,3(12):2281-2284.
[8]Tofighy M A,MohammadiT.Adsorptionofdivalentheavymetalions from waterusing carbonnanotubesheets[J].JournalofHazardousMaterials,2011,185(1):140-147.
[9]Tuzen M,SaygiK O,Usta C,etal.Pseudomonasaeruginosa immobilizedmultiwalled carbon nanotubesasbiosorbent forheavymetal ions[J].Bioresource Technology,2008,99(6):1563-1570.
[10]袁紹軍,姜斌.電解法凈化含重金屬離子廢水的試驗研究 [J].化學工業與工程,2003,20(1):7-10.
[11]KobyaM,DemirbasE,Senturk E,etal.Adsorption of heavymetal ions from aqueoussolutionsby activated carbon prepared from apricotstone [J].Bioresource technology,2005,96(13):1518-1521.
[12]ShiJ,Luo H,Xiao D,etal.Bio-sorbents from cassavawastebiomassand itsperformance in removalof Pb2+from aqueoussolution[J].Journal of Applied Polymer Science,2014,131(2):39780(1-7).
[13]Li X,Si Z,Lei Y,etal.Hierarchically structured Fe3O4microspheres:morphology control and their application in wastewater treatment[J].CrystEng Comm,2011,13(2):642-648.
[14]王春峰,李健生,王連軍,等.粉煤灰合成NaA型沸石對重金屬離子的吸附動力學 [J].中國環境科學,2009,29(1):36-41.
[15]程愛民,田艷,韓冰,等.聚氨酯/蒙脫土納米復合材料的制備與性能研究 [J].高分子學報,2003(4):591-594.
[16]Anbia M,Kargosha K,Khoshbooei S.Heavymetal ions removal from aqueousmedia bymodifiedmagneticmesoporous silica MCM-48[J].Chem ical Engineering Research and Design,2015,93:779-788.
[17]Liu B,Yao Z,Zhou Z,etal.Kineticsand thermodynamicsof theadsorptionofcopper(II)onto chelating resin[J].Chinese JPro Eng,2009,9(5),865-870.
[責任編輯 田 豐 夏紅梅]
Preparation of TiO2--Fe2O3compositesand theirapplication in the treatmentof Cu(II)ions from wastewater
LIYinhui1,2,LU Aidang1,2,HAN Jian1,2,CHEN Jianxin1,2,ZHANG Na1
(1.School of Marine Science and Engineering,Hebei University of Technology,Tianjin 300130,China;2.Engineering Research Centerof Seawater Utilization Technology,Tianjin 300130,China)
Using ferrous chlorideas the iron source,FeOOH were prepared by hydrothermalsynthesis,using FeOOH as the substrate and tetrabutyl titanate as a titanium source,TiO2--Fe2O3compositematerialswere prepared through a hydrothermalsynthesis,as-prepared TiO2--Fe2O3compositeswere characterized by XRD and SEM,at the same time,the study on the adsorption properties of TiO2--Fe2O3composites towards Cu(II)ions from wastewaterwas investigated, the effectof the initialconcentration of Cu(II)ions,pH value,the reaction time on theadsorption propertiesof TiO2--Fe2O3compositeswere researched,and the adsorptionmechanism of TiO2--Fe2O3compositematerial towards Cu(II) ionswere described.The results showed that TiO2--Fe2O3composites isan effective adsorbent forCu(II)ionsand can rapidly adsorb and achieve adsorption equilibrium,because TiO2--Fe2O3composite containing -Fe2O3magnetic can achieve rapid recovery if itexerts amagnetic field without the high-speed centrifugation powder.Hence,it can greatly save energy and reduce costof separation.A ll in all,the composites can be used asa prom ising functionalmaterials for separation of heavymetals ions inwastewater treatment.
TiO2--Fe2O3;Cu(II)ions;initialconcentration;pH value;reaction time;adsorption performance
X703;TQ028.15
A
1007-2373(2016)01-0080-05
10.14081/j.cnki.hgdxb.2016.01.015
2015-04-17
國家自然科學基金(51309074)
李銀輝(1981-),女(漢族),講師,博士生.

