HT22細胞氧糖剝奪再灌注及Grasp65過表達干預后高爾基體的形態(tài)變化及其可能機制研究
王 佳, 熊 炬, 周文勝
?
HT22細胞氧糖剝奪再灌注及Grasp65過表達干預后高爾基體的形態(tài)變化及其可能機制研究
王 佳1, 熊 炬2, 周文勝2
目的 探討HT22細胞氧糖剝奪再灌注及Grasp65過表達干預后高爾基體的形態(tài)變化及其可能機制。方法 利用小鼠海馬神經(jīng)元細胞系HT22為研究對象,HT22細胞經(jīng)氧糖剝奪再灌注損傷及Grasp65過表達干預后,采用MTT法檢測細胞存活率;Hoechest33258熒光染色法評估細胞凋亡;并應(yīng)用細胞免疫熒光技術(shù)觀察高爾基體的形態(tài);應(yīng)用Western blot技術(shù)檢測GM130和GAAP蛋白的表達。結(jié)果 氧糖剝奪再灌注可導致HT22細胞的活性顯著降低(P<0.05),凋亡率顯著增高(P<0.05);并可導致高爾基體形態(tài)的異常,隨著再灌注時間的延長,高爾基體逐漸發(fā)生碎裂,尤其以再灌注12 h和24 h最為明顯;GM130、GAAP的表達水平在氧糖剝奪再灌注后出現(xiàn)下降,特別是在再灌注12 h、24 h后出現(xiàn)了顯著下降(P<0.05)。過表達Grasp65后,HT22細胞在氧糖剝奪再灌注所致高爾基體碎裂出現(xiàn)減少(P<0.05),碎裂程度減輕,同時GM130和GAAP的表達均顯著增加(P<0.05),HT22細胞的存活率大大提高(P<0.05),凋亡率顯著降低(P<0.05)。結(jié)論 缺血再灌注損傷的細胞模型中,同樣發(fā)生了高爾基體的碎裂;過表達Grasp65可以減輕氧糖剝奪再灌注損傷所致的高爾基體碎裂,并可以減少HT22細胞的凋亡,其機制可能與上調(diào)GM130和GAAP的表達有關(guān)。
高爾基體碎裂; 凋亡; 小鼠海馬神經(jīng)元系HT22; Grasp65; GM130
腦梗死是臨床上較為常見的疾病,其發(fā)病率、致殘率及死亡率均高,缺血再灌注損傷是造成腦梗死的重要原因。近年來許多研究發(fā)現(xiàn),在多種神經(jīng)系統(tǒng)疾病如阿爾茨海默病(AD)、帕金森氏病(PD)、肌萎縮側(cè)索硬化(ALS)等病理神經(jīng)元中發(fā)現(xiàn)了高爾基體形態(tài)的改變,甚至碎裂的現(xiàn)象[1~3]。對此現(xiàn)象深入研究發(fā)現(xiàn),高爾基體可能是細胞內(nèi)死亡信號途徑的重要感受者與放大者,在細胞凋亡早期即核染色體DNA還未改變之前,已出現(xiàn)了高爾基體形態(tài)的變化,說明高爾基體在細胞凋亡過程中起重要的早期啟動作用[4]。另外研究表明,在腦缺血再灌注的動物模型中也發(fā)現(xiàn)了高爾基體的碎裂[5]。但是在缺血再灌注損傷的細胞模型中,是否同樣發(fā)生了高爾基體碎裂?通過阻止高爾基體碎裂是否可以減輕神經(jīng)元細胞的凋亡,改善神經(jīng)功能尚不清楚。因此,研究高爾基體凋亡的信號轉(zhuǎn)導機制對神經(jīng)元凋亡的影響十分重要。
Grasp65是一類重要的高爾基體相關(guān)蛋白,對維持高爾基體的形態(tài)和功能具有重要作用,如參與細胞分裂間期高爾基體解聚、裂解以及細胞凋亡中的高爾基體碎裂[6,7]。既往有多項研究表明轉(zhuǎn)染Grasp65和表達Grasp65突變體可減少高爾基體碎裂[4,8]。本研究利用小鼠海馬神經(jīng)元細胞系HT22建立缺血再灌注損傷的細胞模型,探討HT22細胞氧糖剝奪再灌注及Grasp65過表達干預后高爾基體的形態(tài)變化及其可能機制。
1 材料與方法
1.1 材料 小鼠海馬神經(jīng)元細胞系HT22(本研究所保存);胎牛血清(Gemini公司);高糖DMEM培養(yǎng)基和無糖DMEM培養(yǎng)基(Kccell公司);Hoechest33258(Sigma公司);MTT(Sigma公司);pcDNA3.1-Grasp65 過表達載體(本研究所構(gòu)建與保存);Lipofectamin3000轉(zhuǎn)染試劑(Invitrogen公司);GM130抗體(Abcam公司);GAAP抗體(Santa cruz公司);β-tubulin抗體(聯(lián)科生物);β-actin抗體(Proteintech公司);二抗和熒光二抗(Proteintech公司);ECL超敏發(fā)光液和PVDF膜(Millipore公司);DAPI(碧云天生物有限公司)。
1.2 方 法
1.2.1 細胞培養(yǎng)、分組及氧糖剝奪再灌注(OGD/R)損傷模型建立 用含有10%胎牛血清的高糖DMEM完全培養(yǎng)基,在5%CO2、37 ℃恒溫恒濕培養(yǎng)箱培養(yǎng)HT22細胞。待細胞融合至80%~90%即可傳代,取細胞形態(tài)良好、對數(shù)增殖期培養(yǎng)的細胞用于后續(xù)實驗。實驗分為模型組(OGD/R組)、空載模型組(pcDNA3.1+OGD/R組)、Grasp65過表達干預組(Grasp65+OGD/R組),每組再按再灌注時間點不同分為6 h、12 h、24 h 3個亞組。參照文獻[9]建立HT22細胞OGD/R損傷模型:首先用無糖DMEM培養(yǎng)基沖洗細胞3次,替換掉完全培養(yǎng)基,放置于含1%O2、5%CO2、94%N2的三氣培養(yǎng)箱中缺氧缺糖培養(yǎng)6 h,然后將培養(yǎng)基替換為完全培養(yǎng)基,放置于37 ℃、5%CO2常規(guī)培養(yǎng)箱中復氧培養(yǎng),分別繼續(xù)培養(yǎng)6 h、12 h、24 h。
1.2.2 MTT檢測細胞存活率 各組HT22細胞加入100 L溶解于DMEM的MTT溶液(0.5 mg/ml),在培養(yǎng)箱中孵育4 h,棄掉培養(yǎng)液,加入100 L DMSO溶液,37 ℃振蕩10 min,用酶標儀檢測細胞在490 nm處的吸光度(A)值。用每組A值與空白對照組A值的比值來計算細胞存活率,實驗重復4次,最后取平均值。
1.2.3 Hoechst 33258檢測細胞凋亡率 各組HT22細胞加入Hoechest 33258溶液(5 μg/ml),37 ℃孵育10 min。抗熒光淬滅劑封片,避光,熒光顯微鏡觀察拍片。隨機選取3個高倍視野,計算每個視野細胞凋亡率(凋亡細胞數(shù)/總細胞數(shù)×100%)。
1.2.4 Western blot檢測GM130、GAAP的蛋白表達 收集各組HT22細胞,使用蛋白提取試劑盒提取總蛋白,測量其蛋白濃度。蛋白變性后進行SDS-聚丙烯酰胺凝膠電泳,用半干轉(zhuǎn)移法將凝膠電泳分離的蛋白分子轉(zhuǎn)移到 PVDF膜上。5%牛血清白蛋白室溫封閉1 h,加入相應(yīng)一抗,抗GM130(1∶1000)、GAAP(1∶100)、β-actin(1∶4000),4 ℃孵育過夜。用TBST洗3次,每次10 min。加入相應(yīng)二抗37 ℃孵育1 h,TBST漂洗4次,ECL顯影和采圖。Quantity one軟件分析各條帶吸光度值,計算相對表達量。實驗重復3次,取均值做統(tǒng)計學分析。
1.2.5 細胞免疫熒光觀察高爾基體(用GM130標記)的形態(tài)變化 各組HT22細胞經(jīng)4%多聚甲醛室溫固定后,經(jīng)0.5% tritonX-100通透30 min,用兔源GM130單抗(1∶100)和小鼠源β-tubulin單抗(1∶200)4 ℃孵育過夜,PBS洗,F(xiàn)ITC山羊抗兔和Alex Fuor 595山羊抗小鼠熒光二抗室溫孵育1 h,PBS洗,用含DAPI的封片劑封片,奧林巴斯熒光倒置顯微鏡電腦采像。
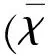
2 結(jié) 果
2.1 氧糖剝奪再灌注及Grasp65過表達干預對HT22細胞活性的影響 模型組、空載模型組和Grasp65過表達干預組HT22細胞經(jīng)氧糖剝奪6 h再灌注6 h、12 h、24 h后,HT22細胞活性顯著降低,與正常組比較有統(tǒng)計學差異(P<0.05);Grasp65過表達干預組與模型組相比,HT22細胞存活率有所上升,其中再灌注6 h、12 h細胞活性有顯著差異(P<0.05),24 h細胞活性無明顯差異(P>0.05);空載模型組與模型組比較無統(tǒng)計學意義(P>0.05)(見表1)。
2.2 氧糖剝奪再灌注及Grasp65過表達干預對HT22細胞凋亡的影響 正常組細胞核形狀正常,呈圓形,顯淡藍色熒光,其核內(nèi)染色質(zhì)均勻分布,無明顯凋亡細胞;模型組細胞隨著再灌注時間的延長,逐漸可見部分細胞胞體縮小,胞漿濃縮,染色質(zhì)分布不均,再灌注12 h、24 h細胞核致密濃染,顯亮藍色,細胞核碎裂呈碎片狀,再灌注24 h可見凋亡細胞增多,細胞出現(xiàn)壞死,細胞輪廓不清,已解體;過表達Grasp65后,氧糖剝奪再灌注所致凋亡細胞減少(見圖1A)。模型組、空載模型組和Grasp65過表達干預組HT22細胞經(jīng)氧糖剝奪6 h再灌注6 h、12 h、24 h后,HT22細胞凋亡率顯著上升,與正常組比較有統(tǒng)計學差異(P<0.05);各個時間點Grasp65過表達干預組與模型組相比,HT22細胞凋亡率下降顯著(P<0.05);空載模型組與模型組比較無統(tǒng)計學意義(P>0.05)(見圖1B)。
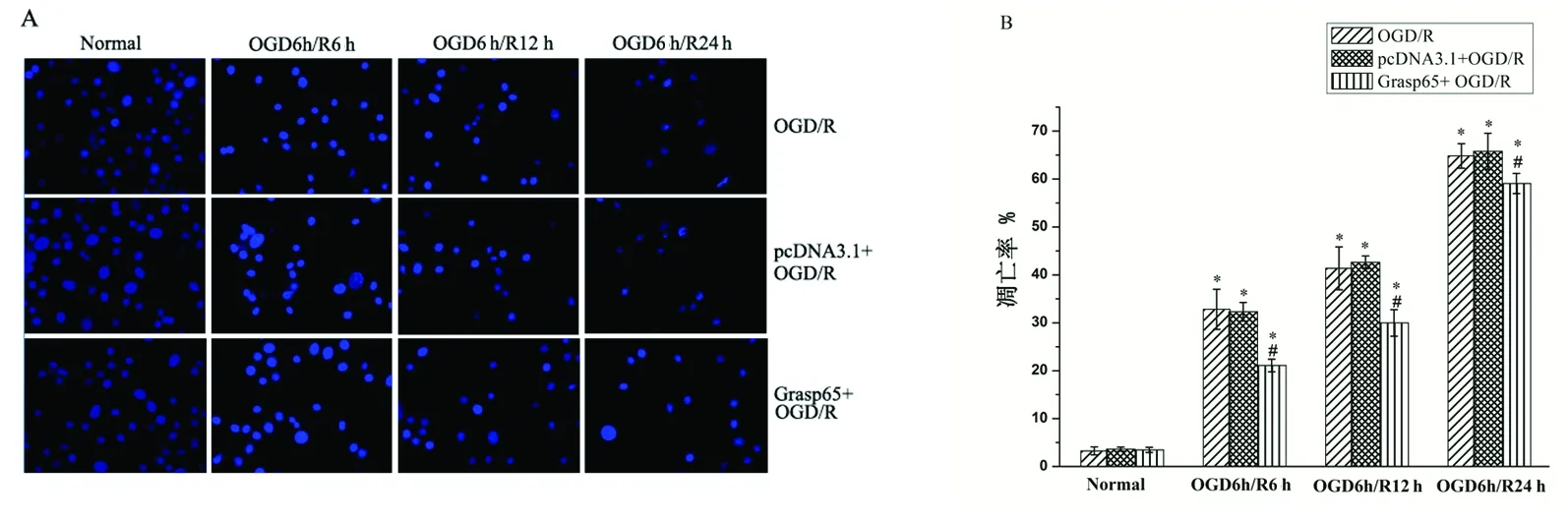
2.3 氧糖剝奪再灌注及Grasp65過表達干預對HT22細胞高爾基體形態(tài)的影響 通過GM130標記高爾基體,β-Tubulin標記細胞微管結(jié)構(gòu),以觀察氧糖剝奪再灌注后高爾基體的形態(tài)變化。免疫熒光結(jié)果顯示,在正常組中,HT22細胞內(nèi)高爾基體結(jié)構(gòu)緊密,聚集于核邊,不分散;氧糖剝奪6 h再灌注6 h后,部分細胞的高爾基體結(jié)構(gòu)較正常組稍松散,可見少量碎裂片段;再灌注12 h、24 h后,大部分細胞內(nèi)高爾基體的正常形態(tài)被破壞,囊膜碎裂明顯,可見明顯的碎裂片段或顆粒廣泛散在細胞內(nèi)(見圖2)。Grasp65過表達干預后,未遭受氧糖剝奪的HT22細胞內(nèi)高爾基體形態(tài)正常,結(jié)構(gòu)緊湊,不分散;氧糖剝奪6 h再灌注6 h、12 h后,高爾基體形態(tài)基本正常,但結(jié)構(gòu)稍顯松散,稍見條形塊狀碎片,與同期模型組比較,高爾基體碎裂程度有所改善;再灌注24 h后,約一半細胞內(nèi)高爾基體出現(xiàn)體積擴大,囊膜結(jié)構(gòu)碎裂成顆粒狀分散在細胞中,但與同期模型組比較,高爾基體碎裂程度也有所減輕(見圖3)。我們發(fā)現(xiàn),空載模型組各時間點高爾基體的碎裂與同期模型組比較均無統(tǒng)計學意義(P>0.05);過表達Grasp65后HT22細胞在氧糖剝奪再灌注6 h后的高爾基體的碎裂較同期模型組有所減少,但差異不具有統(tǒng)計學意義(P>0.05);而在再灌注12 h、24 h后高爾基體的碎裂較同期模型組明顯減少,差異具有統(tǒng)計學意義(P<0.05)(見圖4)。
2.4 氧糖剝奪再灌注及Grasp65過表達干預對HT22細胞GM130、GAAP蛋白表達的影響 與正常組比較,HT22細胞經(jīng)氧糖剝奪6 h再灌注6 h后,細胞內(nèi)GM130和GAAP的表達無明顯變化,差異不具有統(tǒng)計學意義(P>0.05);隨著再灌注時間的延長,GM130和GAAP在再灌注12 h和24 h的表達均較正常組出現(xiàn)了顯著降低,差異具有統(tǒng)計學意義(P<0.05)。Grasp65過表達干預后,氧糖剝奪再灌注6 h、12 h的GM130的表達與正常組基本一致(P>0.05),而24 h的GM130的表達較正常組顯著下降(P<0.05);Grasp65過表達干預后,氧糖剝奪再灌注6 h的GAAP的表達與正常組基本一致(P>0.05),而12 h、24 h的GAAP的表達較正常組顯著下降(P<0.05);Grasp65過表達干預組各時間點GM130和GAAP的表達較同期模型組出現(xiàn)了顯著升高,差異具有統(tǒng)計學意義(P<0.05)(見圖5)。

表1 OGD/R及Grasp65過表達干預對HT22細胞活性的影響
與正常組比較*P<0.05;與模型組比較#P<0.05
A:Hoechst33258凋亡染色(×400);B:各組凋亡率統(tǒng)計分析,與正常組比較*P<0.05;與OGD/R比較#P<0.05
圖1 OGD/R及Grasp65過表達干預對HT22細胞凋亡的影響
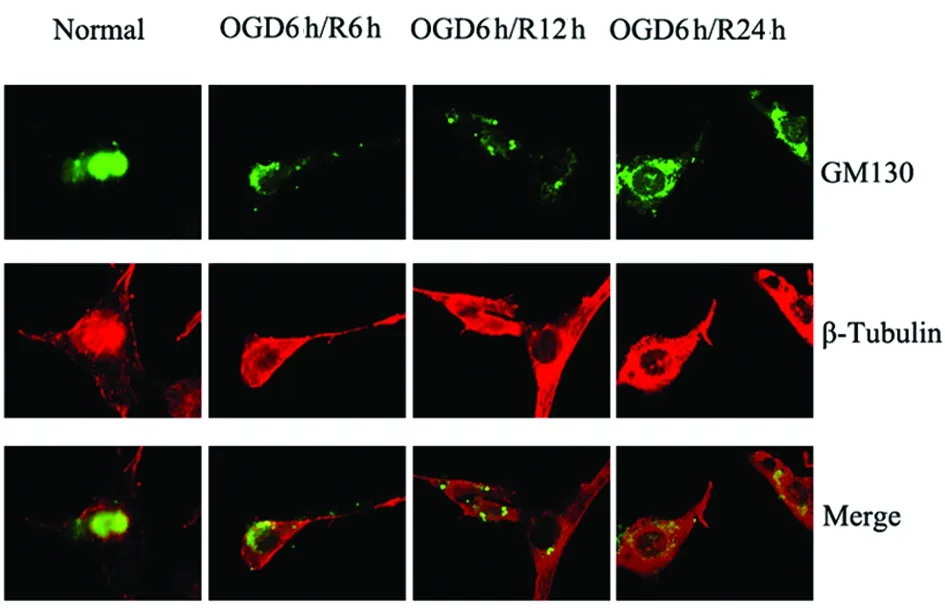
圖2 OGD/R對HT22細胞內(nèi)高爾基體形態(tài)的影響(×400)
圖3 過表達Grasp65后OGD/R對HT22細胞內(nèi)高爾基體形態(tài)的影響(×400)
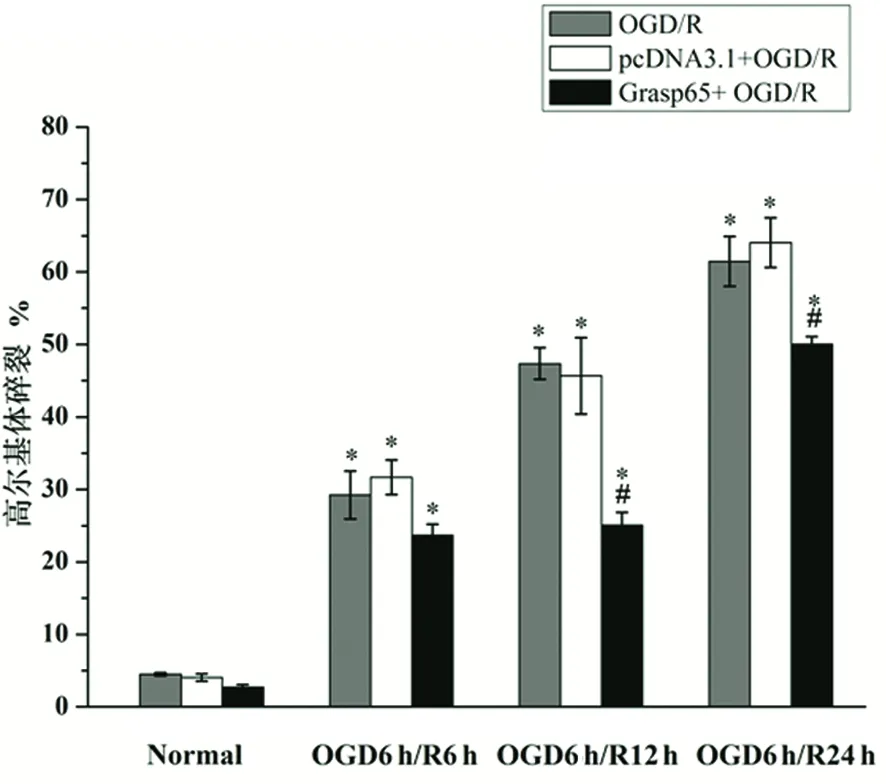
與正常組比較*P<0.05;與OGD/R比較#P<0.05
圖4 OGD/R及Grasp65過表達干預對HT22細胞高爾基體碎裂的統(tǒng)計分析
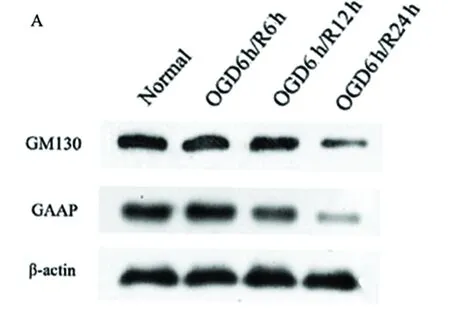
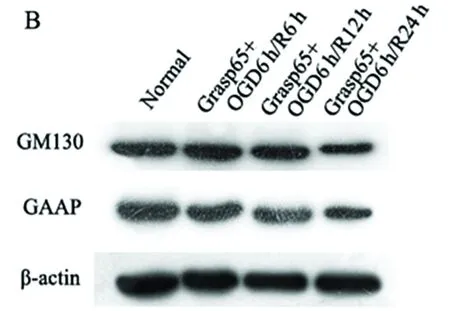
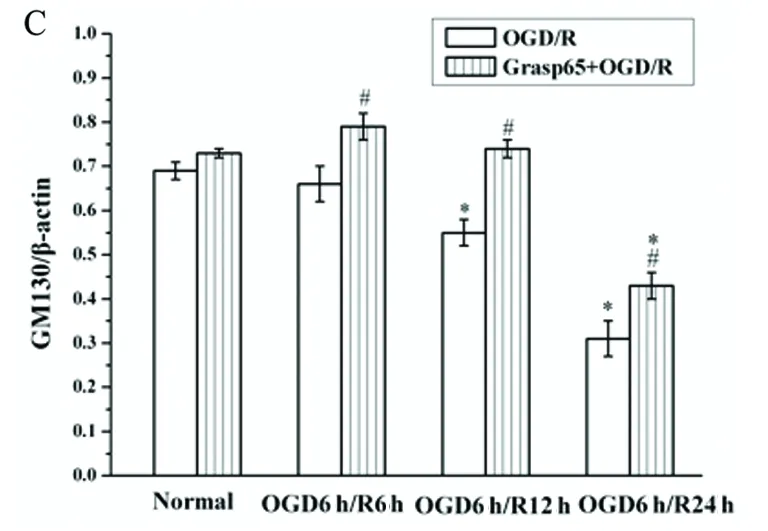
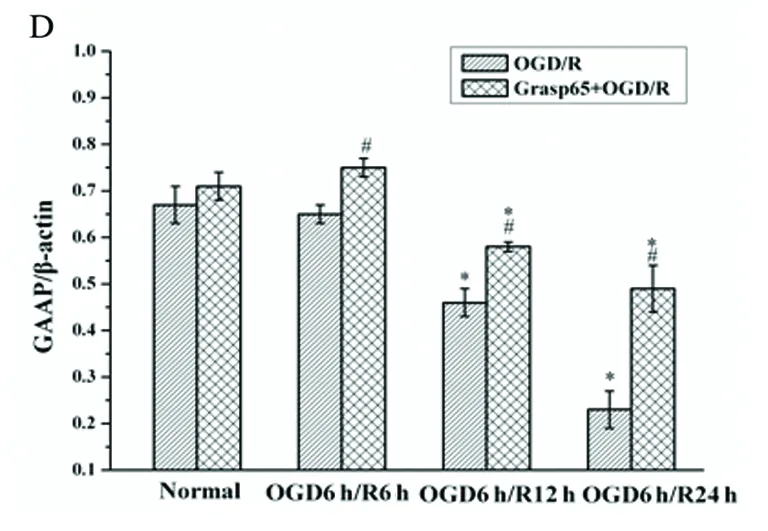
A:Western blot 檢測HT22細胞在OGD/R后各時間點GM130、GAAP的表達;B:Western blot 檢測過表達Grasp65后HT22細胞在OGD/R后各時間點GM130、GAAP的表達;C:GM130表達量變化的統(tǒng)計分析;D:GAAP表達量變化的統(tǒng)計分析;與正常組比較*P<0.05;與OGD/R比較#P<0.05
圖5 OGD/R及Grasp65過表達干預對GM130、GAAP表達的影響
3 討 論
腦缺血后恢復血液再灌注可以減輕部分缺血神經(jīng)元的損傷,但同時也會加重部分缺血細胞的損傷,甚至導致這些細胞的死亡,對中樞神經(jīng)系統(tǒng)功能產(chǎn)生嚴重的影響。因此,從全新的角度探索和研發(fā)新的藥物,促進腦缺血再灌注損傷后神經(jīng)系統(tǒng)功能的改善或恢復,成為近年來研究腦梗死的重點之一。
現(xiàn)在越來越多的研究從細胞器水平來分析神經(jīng)系統(tǒng)疾病的病變過程和病理特點,有證據(jù)表明高爾基體涉及到神經(jīng)系統(tǒng)疾病的發(fā)病機制中[10,11]。本研究利用小鼠海馬神經(jīng)元細胞系HT22建立缺血再灌注損傷的細胞模型,通過對HT22細胞氧糖剝奪6 h再灌注6 h、12 h、24 h后發(fā)現(xiàn),氧糖剝奪再灌注可導致神經(jīng)元細胞的活性顯著降低,凋亡率顯著上升,且隨著再灌注時間的延長,上述損傷表現(xiàn)逐漸加重,這種變化規(guī)則基本符合缺血再灌注損傷的病理生理特點。氧糖剝奪再灌注可導致HT22細胞高爾基體形態(tài)的異常,隨著再灌注時間的延長,高爾基體逐漸發(fā)生碎裂,呈長條狀或顆粒狀,尤其以再灌注12 h和24 h最為明顯。因此,我們認為,與缺血缺氧損傷相比,再灌注損傷對高爾基體的打擊更大,即高爾基體可能不能耐受再灌注損傷的打擊。GM130是維持高爾基體結(jié)構(gòu)和形態(tài)完整的重要蛋白[12]。我們的實驗發(fā)現(xiàn),GM130的表達水平在氧糖剝奪再灌注后出現(xiàn)下降,特別是在再灌注12 h、24 h后,GM130出現(xiàn)顯著的下降,并在這兩個時間點觀察到了大量的HT22細胞內(nèi)高爾基體發(fā)生了嚴重的碎裂。因此,我們有理由相信,氧糖剝奪再灌注所致HT22細胞內(nèi)高爾基體的碎裂可能與GM130表達水平的下降有關(guān)。GAAP是一種定位于高爾基體的抗凋亡蛋白[13]。
本研究發(fā)現(xiàn),在氧糖剝奪再灌注初期,GAAP的表達水平基本沒有變化,而此時高爾基體的形態(tài)基本保持正常,但是從再灌注12 h開始,GAAP的表達水平急劇下降,同時高爾基體發(fā)生了明顯的顆粒狀碎裂。因此,我們推測GAAP蛋白可能僅在氧糖剝奪再灌注早期發(fā)揮了一定的抗凋亡作用,GAAP蛋白表達水平的下降可能也是導致高爾基體碎裂的原因之一。
氧糖剝奪再灌注損傷引起高爾基體的碎裂,有可能對蛋白加工成熟、囊泡運輸以及鈣離子穩(wěn)態(tài)產(chǎn)生影響,從而誘導缺血的神經(jīng)細胞發(fā)生死亡或凋亡。故若能從抑制高爾基體碎裂的角度來保護高爾基體,減少缺血神經(jīng)細胞的凋亡,從而發(fā)揮神經(jīng)保護作用。因此,為了阻止高爾基體的碎裂,我們過表達了高爾基體重組和堆疊蛋白Grasp65,它被證實能在細胞有絲分裂時特異的抑制高爾基體的碎裂[4,14]。轉(zhuǎn)染Grasp65后HT22細胞在氧糖剝奪再灌注所致高爾基體碎裂出現(xiàn)減少,碎裂程度減輕,同時GM130、GAAP的表達顯著增加,最后致使HT22細胞的存活率大大提高,凋亡率顯著降低。提示過表達Grasp65減輕缺血再灌注損傷所致的高爾基體碎裂,可以減少缺血神經(jīng)細胞的凋亡,改善神經(jīng)功能,其機制可能與上調(diào)GM130、GAAP的表達有關(guān)。
[1]Joshi G,Chi Y,Huang Z,et al.Abeta-induced Golgi fragmentation in Alzheimer’s disease enhances Abeta production[J].Proc Natl Acad Sci USA,2014,111(13):1230-1239.
[2]Fujita Y,Ohama E,Takatama M,et al.Fragmentation of Golgi apparatus of nigral neurons with alpha-synuclein-positive inclusions in patients with Parkinson’s disease[J].Acta Neuropathol,2006,112(3):261-265.
[3]Sundaramoorthy V,Sultana JM,Atkin JD.Golgi fragmentation in amyotrophic lateral sclerosis,an overview of possible triggers and consequences[J].Front Neurosci,2015,9:400.
[4]Nakagomi S,Barsoum MJ,Bossy-Wetzel E,et al.A Golgi fragmentation pathway in neurodegeneration[J].Neurobiol Dis,2008,29(2):221-231.
[5]王 燕.丹紅注射液對腦缺血再灌注大鼠高爾基體影響的研究[D].長沙:中南大學,2011.
[6]Jarvela T,Linstedt AD.Isoform-specific tethering links the Golgi ribbon to maintain compartmentalization[J].Mol Biol Cell,2014,25(1):133-144.
[7]Tang D,Yuan H,Wang Y.The role of GRASP65 in Golgi cisternal stacking and cell cycle progression[J].Traffic,2010,11(6): 827-842.
[8]Cervigni RI,Bonavita R,Barretta ML,et al.JNK2 controls fragmentation of the Golgi complex and the G2/M transition through phosphorylation of GRASP65[J].J Cell Sci,2015,128(12):2249-2260.
[9]Lecht S,Rotfeld E,Arien-Zakay H,et al.Neuroprotective effects of nimodipine and nifedipine in the NGF-differentiated PC12 cells exposed to oxygen-glucose deprivation or trophic withdrawal[J].Int J Dev Neurosci,2012,30(6):465-469.
[10]Fan J,Hu Z,Zeng L,et al.Golgi apparatus and neurodegenerative diseases[J].Int J Dev Neurosci,2008,26(6):523-534.
[11]Gonatas NK,Stieber A,Gonatas JO.Fragmentation of the Golgi apparatus in neurodegenerative diseases and cell death[J].J Neurol Sci,2006,246(1/2):21-30.
[12]Shamseldin HE,Bennett AH,Alfadhel M,et al.GOLGA2,encoding a master regulator of golgi apparatus,is mutated in a patient with a neuromuscular disorder[J].Hum Genet,2016,135(2):245-251.
[13]Saraiva N,Prole DL,Carrara G,et al.Human and viral Golgi anti-apoptotic proteins (GAAPs) oligomerize via different mechanisms and monomeric GAAP inhibits apoptosis and modulates calcium[J].J Biol Chem,2013,288(18):13057-13067.
[14]Sutterlin C,Hsu P,Mallabiabarrena A,et al.Fragmentation and dispersal of the pericentriolar Golgi complex is required for entry into mitosis in mammalian cells[J].Cell,2002,109(3):359-369.
Morphological alterations of Golgi apparatus after oxygen-glucose deprivation followed by reperfusion and intervening by over-expressed Grasp65 in HT22 cells and their underlying mechanism
WANGJia,XIONGJu,ZHOUWensheng.
(DepartmentofNeurvousDisease,HunanInstituteofGerontology,HunanProvincialPeople’sHospital,Changsha410016,China)
Objecive To investigate Morphological alterations of Golgi apparatus after oxygen-glucose deprivation followed by reperfusion (OGD/R) and intervening by over-expressed Grasp65 in HT22 cells and their underlying mechanism.Methods Using mouse hippocampal neuronal cell line HT22 as the research object.After OGD/R and intervening by over-expressed Grasp65,using MTT method to detect cell viability and hoechest33258 fluorescence staining method to evaluate cell apoptosis.Morphology of Golgi apparatus were observed with cytochemistry immunofluorescence.The protein expressions of GM130 and GAAP were detected by Western blot.Results HT22 cells activity was significantly decreased (P<0.05) via OGD/R induction and apoptosis rate increased significantly (P<0.05).OGD/R could also lead to abnormal Golgi morphology.Along with the reperfusion time extended,the Golgi apparatus gradually fragmented,it was the most obvious at 12 h and 24 h of reperfusion.The protein expression levels of GM130 and GAAP were decreased significantly at 12 h and 24 h time points after OGD/R (P<0.05).Performing OGD/R treatment after over-expressed Grasp65 in HT22 cells,Golgi fragmentation were significantly decreased (P<0.05) and the degree of fragmentation alleviated.The protein expressions of GM130 and GAAP were significantly increased (P<0.05).HT22 cells survival rate was greatly improved (P<0.05) and apoptosis rate decreased significantly (P<0.05).Conclusions In the cell model of ischemia reperfusion injury,the same happened to fragmentation of the Golgi apparatus.Over-expression of Grasp65 could alleviate OGD/R-induced Golgi fragmentation and reduce HT22 cells apoptosis,possibly related to the up-regulation of the expression of GM130 and GAAP.
Golgi fragmentation; Apoptosis; Mouse hippocampal neuronal cell line HT22; Grasp65; GM130
1003-2754(2016)12-1067-05
2016-08-24;
2016-09-30 基金項目:湖南省自然科學基金(No.14JJ2143);湖南省衛(wèi)計委科研項目(No.B2012-121) 作者單位:(1.湖南省人民醫(yī)院湖南省老年醫(yī)學研究所神經(jīng)疾病研究室,湖南 長沙 410016;2.湖南省人民醫(yī)院馬王堆院區(qū)神經(jīng)內(nèi)科,湖南 長沙 410016) 通訊作者:周文勝,E-mail:zhouwensheng2004@163.com
R743.3
A

