典型煤種快速熱解氣體的逸出特性
陸志峰, 王亦飛, 李季林, 王輔臣, 于廣鎖
(華東理工大學煤氣化及能源化工教育部重點實驗室,上海煤氣化工程技術研究中心,上海 200237)
典型煤種快速熱解氣體的逸出特性
陸志峰, 王亦飛, 李季林, 王輔臣, 于廣鎖
(華東理工大學煤氣化及能源化工教育部重點實驗室,上海煤氣化工程技術研究中心,上海 200237)
為深入認識煤樣的快速熱解行為,捕捉氣體釋放特性,在873~1 273 K條件下基于管式反應器對3種不同煤階的典型煤樣開展熱解實驗研究,借助紅外氣體分析系統記錄在線氣體組成。研究結果表明,熱解溫度的升高,對煤中含氫/含氧官能團的分解有促進作用,當溫度自873 K上升至1 273 K時,H2和CO的釋放量均增加了4~5倍;在實驗范圍的高溫下,煤階對熱解反應有效氣體產物組成的影響較小,在1 273 K時,H2的釋放量幾乎與煤種無關。
煤熱解; 氣體釋放; 紅外氣體分析儀
我國“富煤、缺油、少氣”的能源結構特征決定了煤炭作為我國主體能源的地位較難改變。隨著國民經濟的飛速發展,社會對煤炭資源的供應需求日益增強,以煤直接燃燒為主的煤炭利用方式卻給環境帶來了嚴重污染且資源利用效率較低。為了提高煤炭綜合利用效率并減少燃煤帶來的環境問題,以大規模煤氣化技術為基礎的煤基多聯產技術、整體煤氣化聯合循環發電(IGCC)以及煤炭間接液化技術具有較好的發展前景[1]。
作為煤氣化反應的基礎步驟,煤熱解對于氣化反應影響顯著。煤熱解不僅可以有效利用煤來獲得脫硫焦以及焦油,同時對于獲得高附加值液體及氣體產物有重要意義。研究者們利用不同反應器,包括固定床反應器、流化床反應器、滴管爐反應器、絲網反應器等,對熱解產物釋放特性進行了大量研究。研究主要集中于煤焦比表面積的測定[2-3]、XRD和TEM等手段分析煤焦的微晶結構[4-5]以及紅外光譜法分析熱解前后官能團變化[6-7];對于反應器的選擇,多使用熱重(TGA)及滴管爐(DTF)[8-9]進行煤樣快速升溫熱解實驗。熱重分析由于加熱速率限制與工業裝置實際反應情況(105~106K/s)有較大區別,且每次實驗只能添加少量煤樣,實驗獲取產物有限;滴管爐有很高的升溫速率,然而其反應溫度難以精確控制[10]。
本文通過自行搭建的管式反應器研究煤顆粒落入高溫環境內的熱解反應行為,并使其在反應器中部停留至反應結束,通過在線紅外氣體分析儀對反應器出口氣體組分變化進行實時記錄。實驗考察煤階和熱解條件對于熱解氣體釋放特性的影響,研究了內蒙褐煤(NM)、神府煙煤(SF)和晉城無煙煤(JC)在不同溫度下熱解氣體釋放速率及其釋放量。
1 實驗部分
1.1 實驗原料
實驗選用內蒙褐煤(NM)、神府煙煤(SF)、晉城無煙煤(JC),其工業分析和元素分析見表1。煤粉粒徑為70~125 μm。
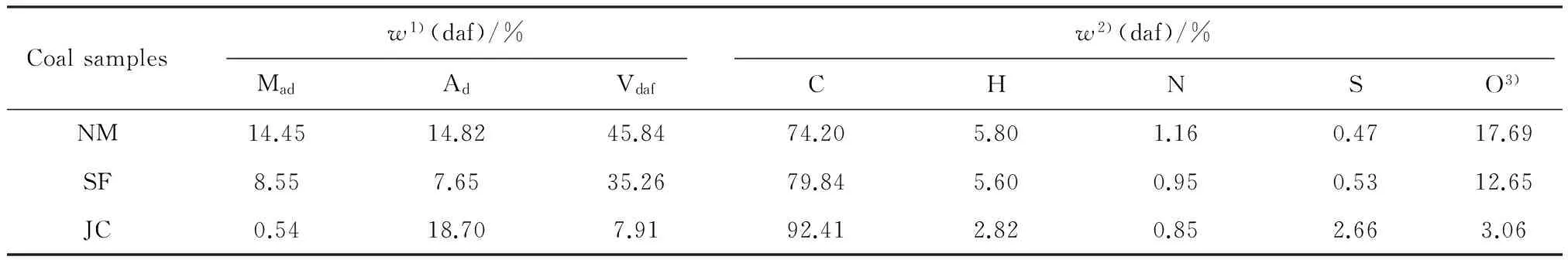
表1 實驗煤樣的工業分析和元素分析Table 1 Proximate and ultimate analysis of coal samples
1) Proximate analysis; 2) Utimate analysis; 3) By difference; Ad—Ash content of dry basis; Mad—Air dried moisture; Vdaf—Volatile matter content and ash-free basis
1.2 常壓熱解實驗
熱解裝置如圖1所示,采用內徑30 mm、長1 000 mm的剛玉管反應器,底部由法蘭保證密封性。反應載體為下部墊有單層高溫耐火棉、外徑29.5 mm的剛玉料斗,通過硅鉬棒加熱,在管式爐中剛玉料斗位置處形成200 mm的高溫恒溫區。實驗前將下部法蘭打開,將剛玉料斗固定于恒溫區位置。采用高純氮氣作為載氣,通過質量流量計確保氮氣流量穩定(1 700 mL/min)。
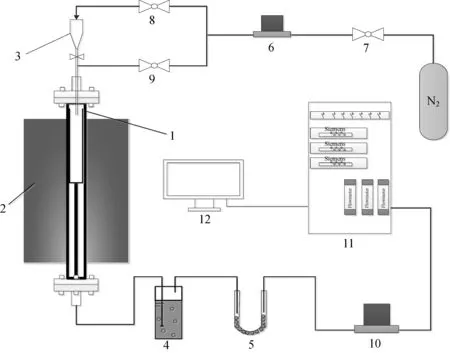
1—Alundum tube; 2—Electric heater; 3—Hopper; 4—Cooler; 5—Dryer; 6—Flow controller; 7,8,9—Valve; 10—Flowmeter; 11—Siemens gas analyzer; 12—Computer 圖1 管式爐熱解裝置流程示意圖Fig.1 Schematic diagram of tubular furnace setup
稱取5 g預先干燥后的煤樣置于加料斗3中,檢查裝置氣密性后,打開閥門9通入氮氣進行吹掃,以置換爐內空氣。打開加熱電源,使管式爐按設定程序升溫。達到預定熱解溫度(本文選取熱解溫度為873~1 273 K,以100 K為間隔)并穩定一段時間后,打開閥門8,同時關閉閥門9,打開加料斗下部止水夾,使氣體攜帶煤粉進入爐內,并留在料斗中直至停止實驗,在此過程中保證爐內恒溫區溫度不變。煤樣受熱分解,熱解后生成的氣體使用飽和碳酸鈉溶液洗滌冷卻后通過變色硅膠,再送入紅外氣體分析儀11,并通過聯用計算機每10 s記錄一次氣體組分數據。由此可以在線分析熱解過程反應器內的氣體組成變化情況。
煤的熱解過程中,二次反應的影響較為重要。本實驗中,使用氮氣流量為1 700 mL/min,而煤樣用量為5 g,且煤樣粒徑很小,充足的氮氣可以快速將熱解氣體帶出反應體系,因此本實驗忽略氣體的二次反應對于熱解氣體產物的影響。煤樣熱解過程中,除CO、CO2、H2外,氣體中亦存在多種氣態烴類,其中以CH4含量最高。由于本實驗對微量的CnHm難以進行定量測定,因此實際操作中不考慮其對實驗結果的影響。
Nelson等[11]研究了褐煤快速熱解特性,結果表明,隨著熱解溫度自873 K升高至1 273 K,焦油產率由20%下降至5%以下。由于本實驗中加入的煤量較少,且該裝置難以對焦油進行準確的定量收集和分析,故而不分析反應條件對焦油的影響。
1.3 數據處理方法
由紅外氣體分析儀實時記錄熱解氣體中各組分含量。實驗前保證進入裝置內部的N2流量穩定不變,在加入煤樣過程中,只有熱解產生的氣體對管式爐內氣體組分產生影響。記N2穩定流量為QN2(mL/min),各組分體積分數分別為yCO、yCH4、yCO2和yH2,則各氣體瞬時流量分別為
(1)
式中i表示組分CO、CH4、CO2及H2。
計算得到各組分瞬時流量,作出各組分瞬時流量與時間的關系曲線,再對各曲線進行積分,得到各組分累積釋放量隨時間的變化關系。
2 結果與討論
2.1 褐煤熱解氣體釋放特性
圖2所示為不同熱解溫度(873、1 073、1 273 K)下褐煤熱解氣體釋放特性曲線。
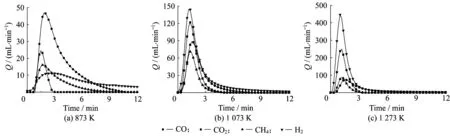
圖2 不同熱解溫度下內蒙褐煤熱解氣體流量Fig.2 Gas flow from pyrolysis of NM lignite at different temperatures
由圖2可以看出隨著熱解溫度升高,反應持續時間越短,即瞬時流量到達零位置所需時間越短。溫度越高,煤樣升溫速率越快,煤樣內部反應更容易達到所需活化能而釋放出氣體產物。高溫條件對于熱解反應有促進作用,這與其他研究者的報道是一致的[12]。
對比不同熱解溫度條件下的內蒙褐煤熱解氣體釋放曲線可知,隨著溫度升高,H2與CO逐漸成為熱解氣體中的主要成分,而CH4與CO2在這4種氣體產物中所占比例逐漸減小。當熱解溫度為1 073 K時,煤中CO2和CH4已基本釋放完畢,繼續提高溫度對氣體產率幾乎沒有影響。提高熱解溫度可以促進一些較難分解的含氧雜環發生裂解生成CO,同時,煤焦中的大分子物質進一步縮聚,產生較多量的H2,即溫度升高促進了CO和H2的生成,從而使得CO2和CH4所占比例下降。
將同一溫度下不同氣體瞬時流量相加,即可得到熱解氣體總流量隨時間變化曲線,見圖3。從圖3可以發現,溫度自873 K上升至1 273 K,氣體釋放量峰值明顯增大,呈倍數增長趨勢。表2列出了不同溫度下氣體釋放量峰值,可以發現,1 073 K時的熱解氣體總流量峰值為873 K時的4倍,而1 273 K時的峰值為1 073 K時的2倍,即隨著溫度升高,內蒙褐煤內部揮發分脫除程度增加顯著。結合圖2可知,氣體釋放總量的增加主要是由于氣體產物中CO與H2組分含量增幅明顯,溫度升高極大促進了煤樣中的裂解及縮聚反應,產生了大量的氣態產物。這與文獻[13]報道一致。
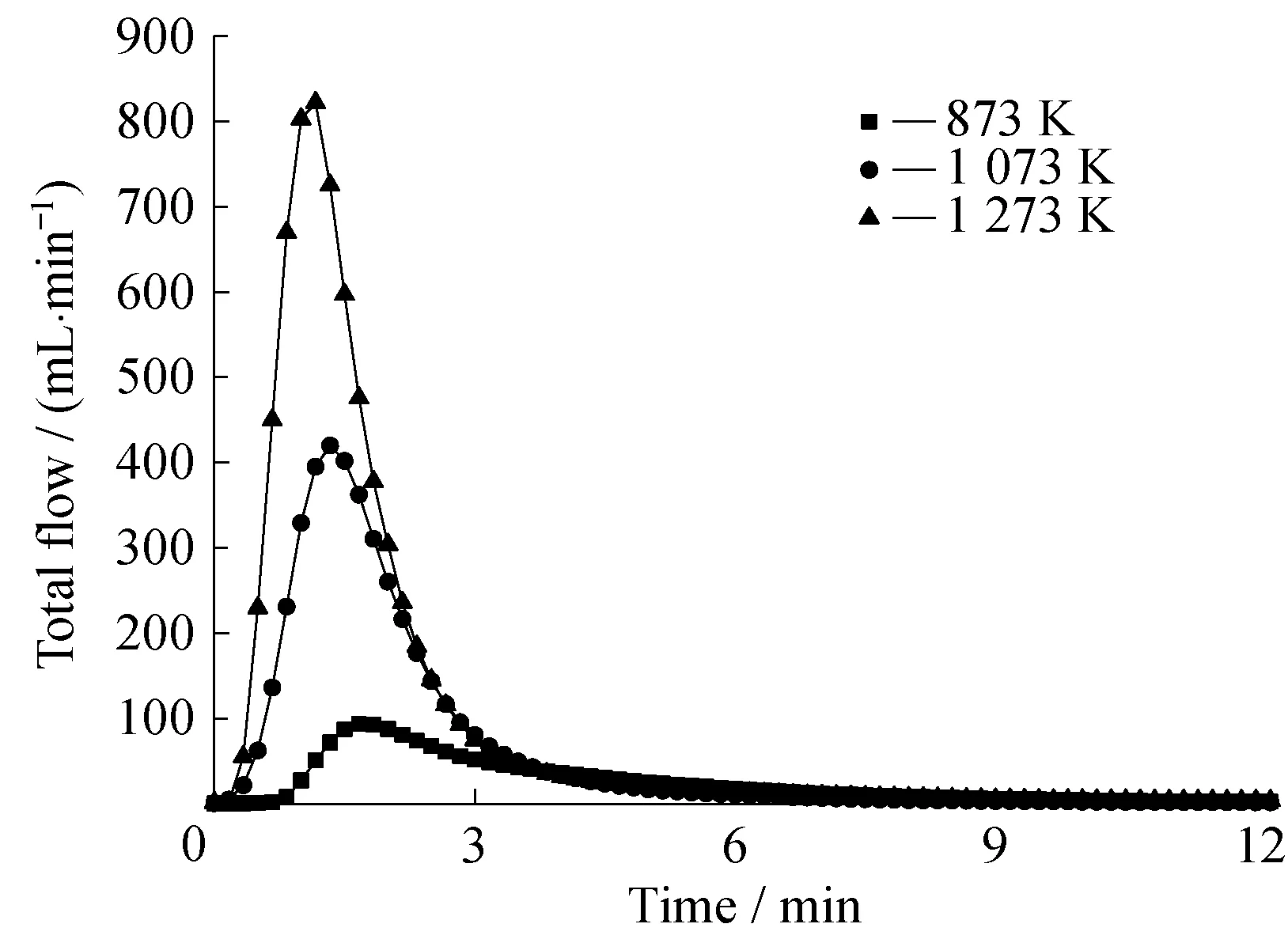
圖3 內蒙褐煤熱解氣體總流量隨時間變化曲線Fig.3 Curves of total flow from NM lignite at different temperatures表2 不同溫度下氣體釋放總量峰值Table 2 Peak value of gas release under different temperatures

Temperature/KPeakvalueofgasrelease/(mL·min-1)87393.301073416.061273819.97
隨著溫度升高,熱解氣體產率逐漸升高,當溫度低于1 273 K時,CO2含量始終高于CH4,隨著溫度升高,CO2與CH4含量差值也逐漸減小,這也與文獻[14]在高頻爐熱解裝置上對煤熱解氣相生成規律所得結論一致。比較圖2(a)、2(b)、2(c)中CH4和CO2曲線可以發現,隨著溫度升高,CO2與CH4瞬時流量的差值不斷減小,在較高溫度(1 273 K)下,CO2的峰值低于CH4,而熱解產生CO2持續時間始終比CH4長,最終導致CO2釋放總量高于CH4。
圖4所示為4種主要氣體產物瞬時流量隨時間的變化曲線。由圖4可知,CO與H2表現出了相似的變化特征:隨著溫度升高,氣體釋放量明顯增加。表明提高熱解溫度對H2和CO的釋放有明顯的促進作用,且在較高溫度下,這種作用更加明顯。CO2和CH4的釋放特性有所不同:溫度高于1 073 K后,溫度的升高對于氣體釋放量的提升并不明顯。溫度從1 073 K上升到1 273 K,CH4增幅并不明顯,而CO2釋放量出現了小幅下降。
研究表明[15],當溫度高于673 K時,CO的釋放與羰基官能團的裂解有關。當溫度高于673 K時,煤中的羰基裂解產生CO;當溫度高于773 K時,含氧雜環也可以產生CO;當溫度升高到973 K以上,CO的釋放與醚鍵的脫除有關。此外,Jüntgen等[16]研究表明,在慢速加熱條件下,即使溫度升高到1 273 K以上,仍會有H2及CO逸出,說明在此溫度下熱解固體殘留物中仍然有H、O存在于鍵能很高的結構中。由圖4(a)可見,CO釋放量在1 173 K到1 273 K時出現了一個突增,表明溫度為1 273 K時,褐煤煤樣中存在較低溫度下難以分解的含氧雜環,受熱后裂解產生大量CO。
CO2釋放特性不同于其他氣體(圖4(b)),其在973 K時達到釋放最大值,這是因為低溫下CO2主要來源于羧基基團分解[19-20],當溫度高于923 K時,CO2主要來源于官能團之間交聯生成和氧醚鍵的斷裂生成。當溫度高于973 K時,煤中羧基基本分解完成,CO2的釋放量幾乎不受溫度影響。
韓峰等[21]利用TG-MS在10 K/min條件下研究了水城褐煤的熱解行為,結果表明,CH4和CO2釋放初始溫度較低,CO2的逸出速率在673 K左右達到峰值,而CH4在500 K左右逸出速率達到峰值,繼續升高溫度,逸出速率減小。
由圖4(c)可見,CH4逸出速率隨溫度變化趨勢與文獻[21]有差異:隨著溫度升高,CH4逸出速率與溫度正相關。不同于慢速熱解,本實驗中熱解速率較高,煤中的低分子化合物和脂肪側鏈在短時間內受熱分解為CH4等氣態烴類,隨著溫度升高,CH4釋放速率增大,釋放量也隨之增加。
圖4(d)所示為H2的釋放特性曲線,與慢速熱解規律類似,H2生成溫度較高,隨著溫度升高,H2逸出速率增大。一般認為,H2是煤二次熱解的產物,是高溫下芳香物質聚合以及氫化芳香環脫氫的結果[16]。
表3所示為內蒙褐煤熱解前后的元素分析及其碳氫質量比(mC/mH)。煤焦中的mC/mH不僅可以反映焦中兩大重要元素的構成比例,還可以反映其結構單元的芳香程度,以判斷煤焦的縮合程度。隨著煤焦mC/mH的升高,煤焦的芳香度逐漸增加。
一般認為,H2主要來源于有機質的縮合和烴類的環化、芳構化及裂解反應。此外,高溫狀態下含碳有機質的水煤氣反應也會生成H2,反應為強吸熱反應[17],溫度的升高會促使H2釋放量增加。溫度每升高100 K,H2瞬時流量峰值幾乎為上一溫度點對應峰值的2倍,可見在熱解氣體產物中,H2含量受溫度影響最大。結合表3可見,隨著溫度升高,煤焦的mC/mH逐漸升高,表明升高溫度,煤焦進一步縮聚,產生了大量的H2。同時,隨著溫度升高,mC/mH增幅逐漸減小,可見繼續升高溫度,H2釋放量的增幅也會減小。
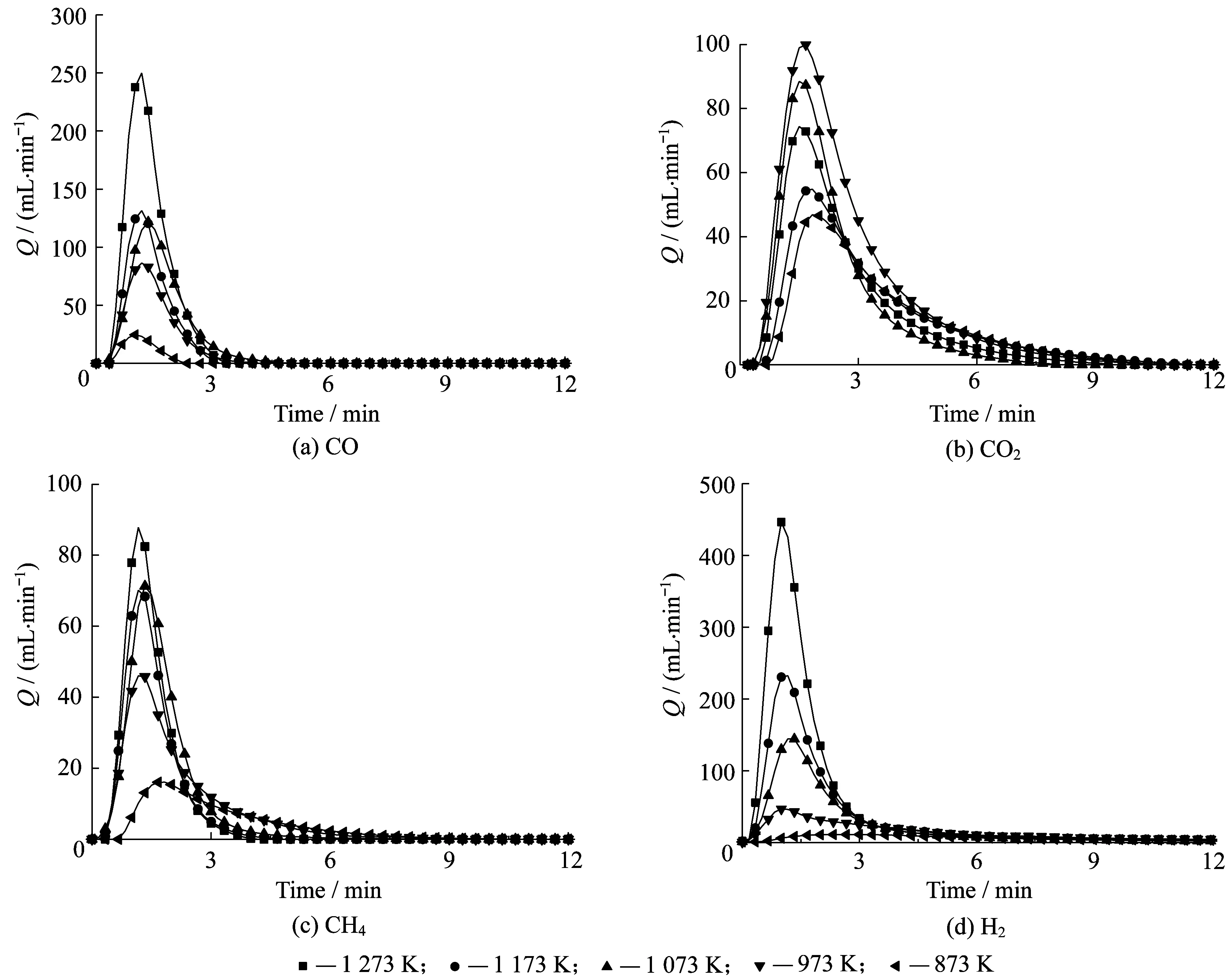
圖4 內蒙褐煤熱解氣體組分釋放曲線Fig.4 Release curves of gases from pyrolysis of NM lignite表3 NM褐煤熱解前后焦性質變化Table 3 Properties of the chars of NM lignite
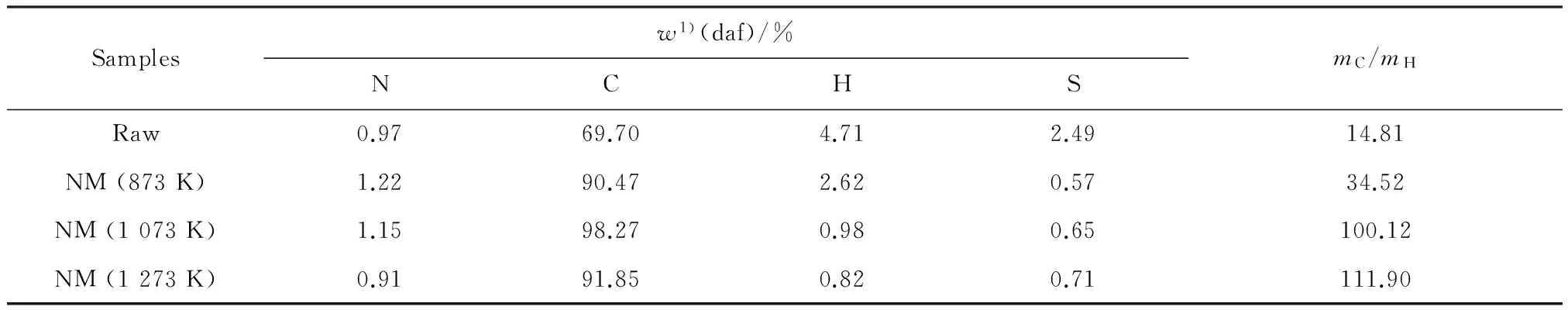
Samplesw1)(daf)/%NCHSmC/mHRaw0.9769.704.712.4914.81NM(873K)1.2290.472.620.5734.52NM(1073K)1.1598.270.980.65100.12NM(1273K)0.9191.850.820.71111.90
1) Ultimate analysis
研究表明CH4是煤熱解氣體中含量最高的碳氫化合物,其來源較多[18],包括煤中的大分子結構降解、烷基基團的分解、半焦的縮聚、焦油的二次反應以及生成的自由基和揮發分的加氫反應生成。溫度從873 K升高到1 073 K,甲烷釋放量增加較為明顯,繼續升高溫度對CH4釋放影響較小,表明1 073 K條件下煤樣中的脂肪側鏈結構基本分解完全,繼續升高溫度對甲烷的生成影響很小。
2.2 熱解氣體總量
煤階是描述煤變質程度的重要因素,變質程度不同最終導致了煤中揮發分和元素組成的不同,最終將產生熱解行為的差異。通過對瞬時流量曲線積分,可得煤樣熱解過程中各氣體釋放總量。圖5所示為實驗所用3種煤樣在不同溫度下熱解所得氣體總量。
由圖5可知,3種煤樣的CO和H2的釋放總量隨著溫度升高而增加。比較不同溫度條件下氣體釋放總量可見,當溫度為1 273 K時,CO、H2釋放總量較973 K條件下有大幅提升,3種煤樣的CO、H2釋放總量均增加了約1.5倍,表明溫度對于不同煤階煤樣熱解產物中CO、H2總量均有較大影響,升高溫度對于促進CO和H2生成效果顯著。CO2及CH4釋放總量受溫度影響較小,當溫度為1 273 K與973 K時兩種氣體釋放總量變化不大,且從圖中可以看出,溫度升高對于甲烷的產生有一定的抑制作用。
CO、H2釋放與煤中含氧、含氫官能團的分解有關,高溫下官能團分解更徹底,產生的CO、H2總量更多。CO2和CH4釋放量隨溫度變化并不明顯,CO2主要來源于—COOH的分解,CH4來源于煤中脂肪側鏈和芳香側鏈裂解,在973 K條件下,這3種結構基本裂解完全,繼續升高溫度并不會促進其生成,因此在實驗溫度條件下CO2和CH4釋放總量隨溫度變化不大。
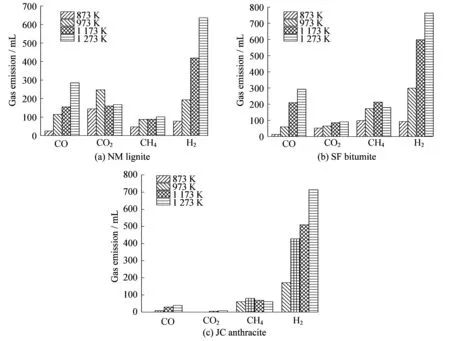
圖5 褐煤、煙煤、無煙煤熱解隨溫度的變化Fig.5 Gas emissions at different temperatures of NM lignite,SF bitumite and JC anthracite
實驗結果表明,3種煤樣熱解氣體組成不盡相同。在內蒙褐煤、神府煙煤熱解實驗中,所考察的4種氣體產物在各溫度下均存在且含量較高,而晉城無煙煤熱解氣體產物則主要以CH4和H2為主,CO2及CO含量極低。褐煤及煙煤中存在著較多的含氧官能團,受熱后分解形成CO及CO2,因此內蒙褐煤和神府煙煤熱解氣體中CO、CO2釋放量較多,晉城無煙煤中H、O體積分數為2.3%、2.0%,表明其中含氧官能團及脂肪烴、烷基側鏈非常少,因此熱解氣體中最主要的成分為H2。隨著煤化程度加深,煤中的氧含量降低,含氧官能團減少,因此CO及CO2釋放總量較褐煤及煙煤顯著減小。
由圖5可見,在較高溫度下,H2是熱解氣體中含量最高的成分,1 273 K條件下,H2的釋放量均遠高于其他3種氣體。高溫段H2的產生主要是由于縮聚反應[21],環數較小的芳環變為環數更大的芳環,釋放出H2。比較3種煤樣的H2釋放總量可見,3種煤樣在1 273 K溫度下H2釋放總量均接近于700 mL,差異較小,表明在該溫度下,這3種煤樣的煤階對于H2的釋放量影響較小,最終H2產率與煤階幾乎無關。
圖6所示為3種煤樣在不同溫度下熱解氣體總量與溫度的對應關系。可見,低溫時熱解氣體總量NM>SF>JC,隨著溫度升高,最終導致氣體總量為SF>NM>JC。熱解氣體中CO與H2含量與煤階無明顯對應關系,然而由圖可見隨著溫度升高,JC熱解氣體中CO與H2總量較NM和SF少,主要是由于JC熱解氣體中CO含量小。NM及SF中含氧量較高,即含氧官能團較多,導致CO釋放量較大,進而增加了熱解氣體中CO與H2含量。
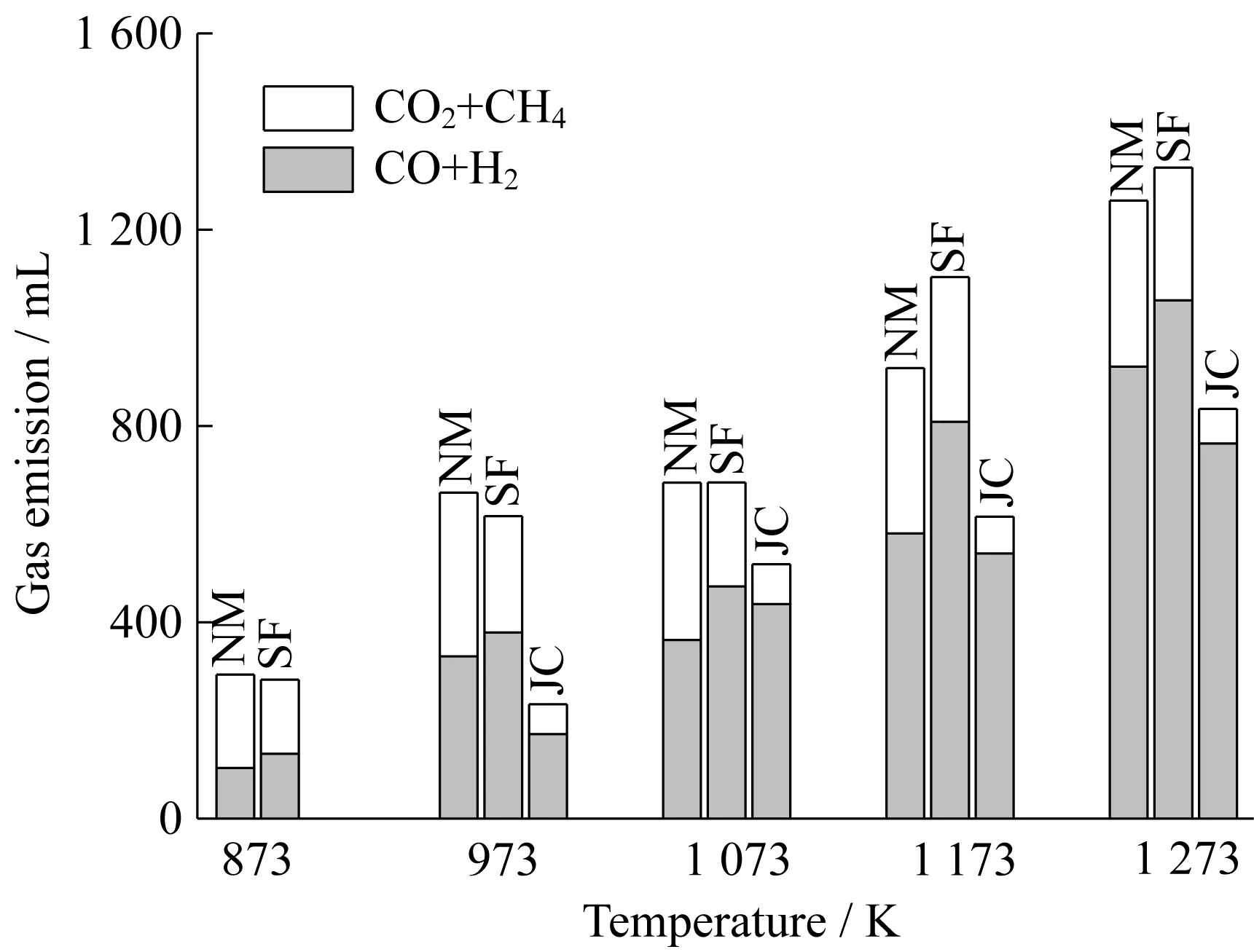
圖6 不同溫度下熱解氣體總量Fig.6 Gas emissions of pyrolysis at different temperatures
3 結 論
(1) 反應條件中,溫度是對反應特性影響最為重要的因素之一。溫度的高低直接且較為明顯地影響有效氣體的釋放量。升高溫度,反應時間隨之縮短,氣體產物中有效氣體含量尤其是H2生成量大幅上升,說明在氣化反應初期,升高溫度有利于煤顆粒盡早完成揮發分的脫除過程。
(2) 高溫下煤熱解產生有效氣體組分所占比例隨著煤階升高而增大,煤階對于氣體產物中CO2和CH4的含量影響較大,而對于H2的影響較小,且隨著溫度升高,H2的釋放量幾乎不受煤階影響。
[1] 于廣鎖,牛苗任,王亦飛,等.氣流床煤氣化的技術現狀和發展趨勢[J].現代化工,2004,24(5):33-34.
[2] 黃瀛華,范麗萍,曹建勤,等.煤及煤焦微觀結構特征與氣化反應性[J].燃料化學學報,1992,20(3):293-299.
[3] WU Y,WU S,GU J,etal.Differences in physical properties and CO2gasification reactivity between coal char and petroleum coke[J].Process Safety & Environmental Protection,2009,87(5):323-330.
[4] SHARMA A,KADOOKA H,KYOTANIi T,etal.Effect of microstructural changes on gasification reactivity of coal chars during low temperature gasification[J].Energy & Fuels,2001,16(1):54-61.
[5] FENG B,BHATIA S K,BARRY J C.Variation of the crystalline structure of coal char during gasification[J].Energy & Fuels,2003,17(3):744-754.
[6] 謝克昌.煤的結構與反應性[M].北京: 科學出版社,2002.
[7] ZHOU C,LIU G,YAN Z,etal.Transformation behavior of mineral composition and trace elements during coal gangue combustion[J].Fuel,2012,97(7):644-650.
[8] 吳詩勇,顧菁,李莉,等.高溫下快速和慢速熱解神府煤焦的理化性質[J].煤炭學報,2006,31(4):492-496.
[9] 劉鐵峰,房倚天,王洋.煤高溫快速熱解規律研究[J].燃料化學學報,2009,37(1):20-25.
[10] HINDMARSH C J,THOMAS K M,WANG W X,etal.A comparison of the pyrolysis of coal in wire-mesh and entrained-flow reactors[J].Fuel,1995,74(8):1185-1190.
[11] NELSON P F,SMITH I W,TYLER R J,etal.Pyrolysis of coal at high temperatures[J].Energy Fuels,1988,2(4):391-400.
[12] 崔童敏,李超,周志杰,等.神府煙煤快速熱解特性研究[J].燃料化學學報,2015,43(11):1287-1294.
[13] 陳路,周志杰,劉鑫,等.煤快速熱解焦的微觀結構對其氣化活性的影響[J].燃料化學學報,2012,40(6):648-654.
[14] 袁帥,陳雪莉,李軍,等.煤快速熱解固相和氣相產物生成規律[J].化工學報,2011,62(5):1382-1388.
[15] 朱學棟,朱子彬,韓崇家,等.煤的熱解研究:Ⅲ.煤中官能團與熱解生成物[J].華東理工大學學報(自然科學版),2000,26(1):14-17.
[16] JüNTGEN H.Review of the kinetics of pyrolysis and hydropyrolysis in relation to the chemical constitution of coal[J].Fuel,1984,63(6):731-737.
[17] 趙融芳,黃偉,常麗萍,等.三種不同煤階煤的模擬熱解實驗研究:Ⅰ.氣態產物組成特性及其演化規律[J].煤炭轉化,2000,23(4):37-41.
[18] HEROD A A,LAZARO M J,DOMIN M,etal.Molecular mass distributions and structural characterisation of coal derived liquids[J].Fuel,2000,79(3):323-337(15).
[19] WANG J.Experimental study of coal topping process in a downer reactor[J].Industrial & Engineering Chemistry Research,2005,44(3):463-470.
[20] 余劍,朱劍虹,郭鳳,等.生物質在微型流化床中熱解動力學與機理[J].燃料化學學報,2010,38(6):666-672.
[21] 韓峰,張衍國,蒙愛紅,等.水城褐煤熱解的氣體產物析出特征及甲烷的生成反應類型研究[J].燃料化學學報,2014,42(1):7-12.
Evolution Characteristics of Gas from Pyrolysis of Typical Coals
LU Zhi-feng, WANG Yi-fei, LI Ji-lin, WANG Fu-chen, YU Guang-suo
(Key Laboratory of Coal Gasification and Energy Chemical Engineering of Ministry of Education,Shanghai Engineering Research Center of Coal Gasification,East China University of Science and Technology,Shanghai 200237,China)
Pyrolysis of three typical coal samples was studied in a tubular furnace reactor under the temperature of 873-1 273 K in order to understand the fast pyrolysis behavior of coal samples and to capture the characteristics of gas release.Infrared gas analysis system was used to record the gas component during the process.The results show that higher temperature promotes the decomposition of hydrogen/oxygen containing functional groups in coal.The release amount of H2and CO increased by 4-5 times when the temperature increased from 873 K to 1 273 K.Coal rank has little influence on effective component of gas product at the experimental temperature range.At the temperature of 1 273 K,the release amount of H2was almost independent on coal rank.
coal pyrolysis; gas release; infrared gas analysis system
1006-3080(2016)06-0764-07
10.14135/j.cnki.1006-3080.2016.06.004
2016-03-08
陸志峰(1991-),男,江蘇泰興人,碩士生,從事煤氣化及煤顆粒反應動力學研究。E-mail:lzfecust@163.com
王亦飛,E-mail:wangyf@ecust.edu.cn
TQ53
A

