稻曲病菌薄壁分生孢子制備的影響因素分析
時婷婷, 王忠文, 蔡 超, 楊 平, 覃 茜, 張君成
(廣西大學農學院, 南寧 530004)
稻曲病菌薄壁分生孢子制備的影響因素分析
時婷婷, 王忠文, 蔡 超, 楊 平, 覃 茜, 張君成*
(廣西大學農學院, 南寧 530004)
本文研究了培養基、溫度、振蕩速度等因素對稻曲病菌Ustilaginoideavirens薄壁分生孢子產孢量的影響。結果表明,稻曲病菌薄壁分生孢子在培養第7天基本達到最大孢子量;該菌最適宜產孢的培養基為馬鈴薯煮汁,在煮汁中添加蔗糖可大幅提高產孢量;適宜的產孢溫度為26~28℃;靜止培養不利于產孢,振蕩培養有利于產孢,并表現為轉速越高產孢量越多;光照條件對產孢量沒有影響。
稻曲病菌; 薄壁分生孢子; 產孢; 培養制備
由稻曲病菌Ustilaginoideavirens(Cooke) Takahashi侵染引起的稻曲病是水稻生產上的重要病害。對該病害的某些方面的研究已相當深入,如在病原菌分子生物學方面,已成功構建了首個BAC文庫,并已獲得了病菌全長基因組信息[1];Zhang等從該病菌中分離獲得一些具病毒性質的dsRNA片段[2]。但該病害的一些基礎研究仍然比較薄弱,如對該病菌的生存繁殖生物學的了解有限,人工誘發該病害的技術還不夠成熟。這直接造成至今對該病害的侵染循環仍不十分清楚,也導致一些與防病控害有關的重大問題,如病菌的致病性與致病機理及寄主抗病性與抗病機理的研究進展緩慢。可見,加強相關基礎研究十分必要,而病菌的繁殖體通常是基礎研究的必需材料。
稻曲病菌繁殖體包括3種形態的孢子:子囊孢子、厚壁分生孢子和薄壁分生孢子[3-4]。目前,實驗室獲取子囊孢子的技術難度大,有關研究多采用無性孢子。而在實驗室培養獲取純凈的厚壁分生孢子也存在一些不易克服的技術障礙,雖然該菌的厚壁分生孢子可以很方便地從發病稻田中大量獲取,但此來源的孢子受到生長季節的限制,也存在容易被污染的嚴重缺陷。因而許多基礎研究使用的材料往往是薄壁分生孢子[5]。獲取薄壁分生孢子,通常采取液體培養基振蕩培養的方法[6]。本文對培養基、溫度和光照等對孢子制備效果的影響進行了初步測定。
1 材料與方法
1.1 菌株
稻曲病菌菌株Uv-105、Uv-110、Uv-2、Uv-6、Uv-24、Uv-54由廣西大學農學院植物病理學實驗室提供。除不同菌株產孢量測定采用全部菌株外,其余測試項均以Uv-105、Uv-110為材料。
1.2 定量移植菌絲塊的準備
用移液管吸取純化的菌株孢子液100 μL 均勻地涂布在PSA(馬鈴薯200 g、蔗糖20 g、瓊脂20 g、水1 000 mL)平板上,置于28 ℃溫箱黑暗下培養4 d,至平板均勻長滿菌絲,用0.5 cm的打孔器打孔,獲得菌絲量一致的瓊脂菌絲塊,在如下各因素測定中定量移植1塊菌絲塊作為振蕩培養初始菌量(另有指明的除外)。
1.3 產孢量與培養時間的關系
將菌絲塊移入裝液量為80 mL(下同)的PS培養液(馬鈴薯200 g、蔗糖20 g、水1 000 mL),置于搖床中在28 ℃、轉速140 r/min下培養,每菌株設置3個重復,每重復培養1瓶。1 d后開始檢測產孢量,以后每2 d取樣用血球計數板檢測產孢量,分析15 d內隨培養時間延長產孢量的變化。
1.4 不同菌株的產孢量
將菌株Uv-2、Uv-6、Uv-24、Uv-54、Uv-105、Uv-110在PSA斜面上活化培養,再移植少許已活化的菌絲體到PSA平板中心培養6周,用0.5 cm打孔器在菌落周緣打孔,移植1菌絲塊至PS培養液中,在28 ℃、140 r/min條件下振蕩暗培養。每菌株設置3個重復,每重復培養1瓶,培養4 d 后用血球計數板測定產孢量。
1.5 培養基對產孢量的影響
用蒸餾水分別將馬鈴薯、甘薯、胡蘿卜、花生芽、干燕麥粒、干大米粒煮汁制成培養基,鮮組織用量為200 g/L,干組織用量為30 g/L。同時設置每種煮汁中添加蔗糖20 g/L的培養基。其他培養基包括:牛肉膏蛋白胨(牛肉膏3g、蛋白胨5 g、水1 000 mL)、酵母膏(酵母膏5 g、水1 000 mL)、理查[硝酸鉀10 g、磷酸二氫鉀5 g、七水硫酸鎂(MgSO4·7H2O)2.5 g、氯化鐵0.02 g、葡萄糖34 g、水1 000 mL]、查彼[硝酸鉀2 g、磷酸二氫鉀1 g、七水硫酸鎂(MgSO4·7H2O)0.5 g、氯化鉀0.5 g、硫酸鐵0.01 g、蔗糖30 g、水1 000 mL]和高氏一號(可溶性淀粉20 g、硝酸鉀1 g、磷酸二氫鉀0.5 g、氯化鈉0.05 g、硫酸鐵0.01 g、水1 000 mL)。培養基中移入菌絲塊后于28℃,140 r/min條件下振蕩培養,每個培養基設置2個重復,每重復培養1瓶,培養5 d后用血球計數板測定產孢量。
1.6 溫度、振蕩速度和光照對產孢量的影響
培養溫度對產孢量的影響:采用PS培養液,設搖床為黑暗狀態,轉速140 r/min,在20、24、25、26、27、28、32℃下振蕩培養。每個培養溫度設置3個重復,每重復培養1瓶,4 d后用血球計數板測定產孢量。
振蕩速度對產孢量的影響:采用PS培養液,在 28℃,黑暗狀態下,分別在0、70、140、175、210 r/min下進行振蕩培養,每個振蕩速度設置3個重復,每重復培養1瓶,4 d后用血球計數板測定產孢量。
光照條件對產孢量的影響:采用PS培養液,在28℃,轉速140 r/min條件下振蕩培養,設置3種光照條件:全黑暗、全光照、及L∥D=12 h∥12 h。每個光照條件設置3個重復,每重復培養1瓶,4 d后用血球計數板測定產孢量。
2 結果與分析
2.1 產孢量與培養時間的關系
稻曲病菌2個菌株Uv-105、Uv-110在初始菌絲量為1塊的條件下,第1~5 天屬于孢子數量快速增長期, 5 d后孢子數量增速下降,曲線逐步變平緩,7 d后產孢數量增幅不大,逐漸趨于飽和(圖1)。依此結果,后續試驗的培養時長選擇為4~5 d。

圖1 培養不同時長后2個菌株的產孢數量Fig.1 Spore yield of 2 strains cultured for different days
2.2 不同菌株的產孢量
菌株Uv-110培養4 d后,其產孢量達22.7×104個/ mL,而菌株Uv-2和Uv-6未檢測到孢子(圖2),表明不同菌株間的產孢能力差異懸殊。

圖2 不同菌株的產孢量Fig.2 Spore yield of different strains
2.3 培養基對產孢量的影響
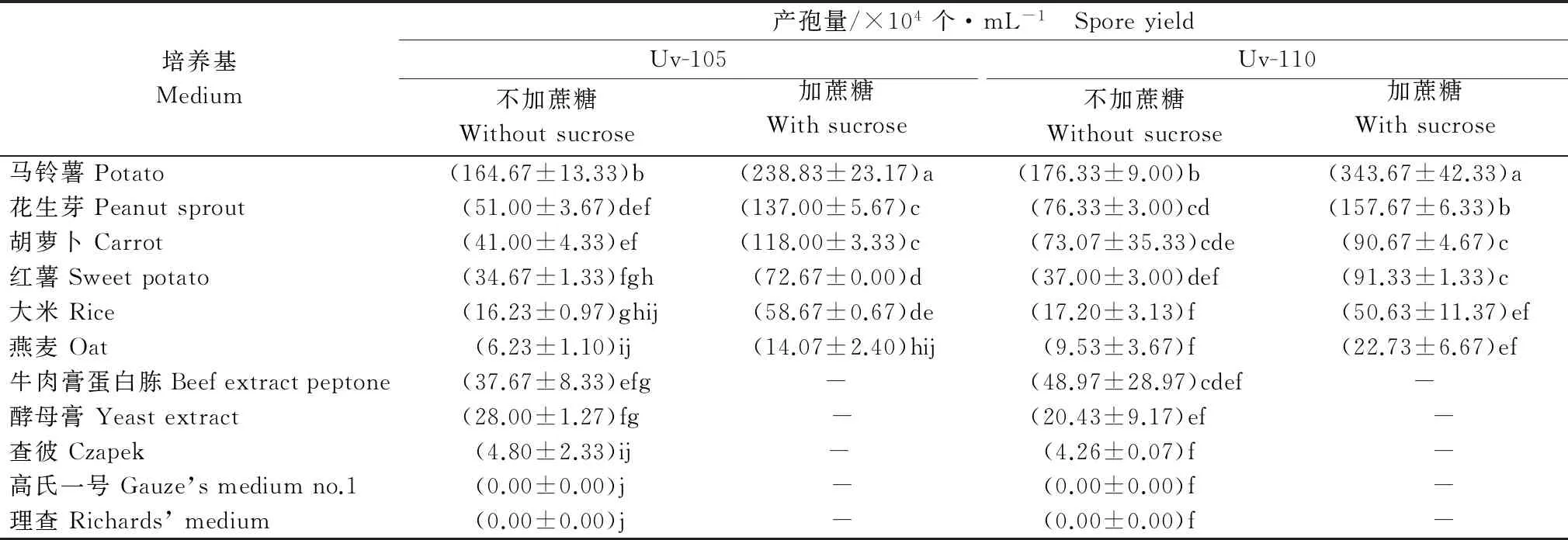
菌株Uv-105、Uv-110在不同的培養基上產孢量差異懸殊,在馬鈴薯煮汁培養基上的產孢量最多;在營養豐富的牛肉膏蛋白胨或酵母膏上的產孢量并不高,在寄主水稻的稻米煮汁培養基上的產孢量也不高;在合成培養基上菌株產孢很少或未檢測到孢子產生(表1),表明該菌在產孢過程中對營養成分有較嚴格的要求,某些培養基含有促進產孢的營養成分,以馬鈴薯的營養成分最適宜稻曲病菌產生薄壁分生孢子。
值得注意的是,在6個含植物煮出汁液中添加蔗糖可大幅提高產孢量(表1),表明稻曲病菌在形成薄壁分生孢子的過程中,要求有充分的碳素營養。
表1 Uv-105和Uv-110在不同培養基上的產孢量1)
Table 1 Spore yield of strain Uv-105 and Uv-110 cultured on different media
培養基Medium產孢量/×104個·mL-1 SporeyieldUv-105不加蔗糖Withoutsucrose加蔗糖WithsucroseUv-110不加蔗糖Withoutsucrose加蔗糖Withsucrose馬鈴薯Potato(164.67±13.33)b(238.83±23.17)a(176.33±9.00)b (343.67±42.33)a花生芽Peanutsprout(51.00±3.67)def(137.00±5.67)c(76.33±3.00)cd(157.67±6.33)b胡蘿卜Carrot(41.00±4.33)ef(118.00±3.33)c(73.07±35.33)cde(90.67±4.67)c紅薯Sweetpotato(34.67±1.33)fgh(72.67±0.00)d(37.00±3.00)def(91.33±1.33)c大米Rice(16.23±0.97)ghij(58.67±0.67)de(17.20±3.13)f(50.63±11.37)ef燕麥Oat(6.23±1.10)ij(14.07±2.40)hij(9.53±3.67)f(22.73±6.67)ef牛肉膏蛋白胨Beefextractpeptone(37.67±8.33)efg-(48.97±28.97)cdef-酵母膏Yeastextract(28.00±1.27)fg-(20.43±9.17)ef -查彼Czapek(4.80±2.33)ij-(4.26±0.07)f -高氏一號Gauze’smediumno.1(0.00±0.00)j-(0.00±0.00)f -理查Richards’medium(0.00±0.00)j-(0.00±0.00)f -
1) 表中數據為平均值±SE,相同菌株數據后標有相同字母表示經鄧肯氏新復極差法檢驗差異不顯著(P>0.05)。下同。 Data in the table are presented as mean ± SE.Data in the same strain followed by same small letters indicates no significant difference by Duncan’s new multiple range test at 0.05 level.The same below.
2.4 培養溫度對產孢量的影響
低溫和高溫條件下產孢量少,26~28℃屬于較適宜的產孢溫度,27℃下產孢量最多(Uv-105為30×104個/ mL, Uv-110為28.80×104個/ mL)(圖3),顯然培養溫度對產孢量有較大的影響。
2.5 振蕩速度對產孢量的影響
靜置(轉速為零)培養的培養基中未檢測到孢子;振蕩培養時,轉速在210 r/min內,產孢量隨轉速的增加而增加,但轉速大于140 r/min時,產孢量的增加幅度不大(表2)。表明靜止培養不利于產孢,振蕩培養有利于產孢,產孢量與振蕩速度有關。
2.6 光照條件對產孢量的影響
3種光照條件下兩個菌株產孢量均無明顯差異(表3),表明光照條件對稻曲病菌薄壁分生孢子的產孢量沒有影響。
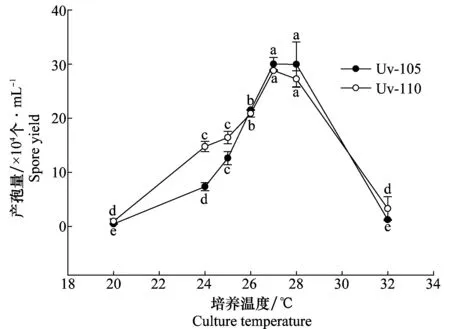
圖3 不同培養溫度下Uv-105和Uv-110菌株的產孢量Fig.3 Spore yield of Uv-105 and Uv-110 cultured at different temperatures

振蕩轉速/r·min-1Shakingspeed產孢量/×104個·mL-1 SporeyieldUv-105Uv-1100(0.00±0.00)e(0.00±0.00)d70(8.18±0.40)d(10.87±0.71)c140(26.53±0.66)c(25.22±3.04)b175(33.71±0.76)b(35.27±1.95)a210(38.24±0.91)a(32.82±0.96)a
表3 不同光照條件下Uv-105和Uv-110的產孢量
Table 3 Spore yield of Uv-105 and Uv-110 cultured at different light conditions

光照條件Lightcondition產孢量/×104個·mL-1 SporeyieldUv-105Uv-110全黑暗Fulldarkness(24.73±6.74)a(24.67±0.53)a全光照Fulllight(25.62±10.86)a(23.96±0.42)aL∥D=12h∥12h(26.38±5.76)a(26.29±0.79)a
3 討論
本試驗結果顯示,培養時間長短是孢子數量增加積累的重要因素,但孢子數量的增加主要集中在培養的前7 d,考慮到長時間培養獲得的薄壁分生孢子的萌發率下降[7],因而實際工作中,培養7 d已足夠。
不同菌株的薄壁分生孢子產孢能力差異懸殊,與有關報道認為不同菌株的厚壁分生孢子產生情況有相似之處[8],但同一菌株產生這兩種孢子是否有相關性還不清楚,不管如何,進行有關的研究,應先對菌株材料的產孢能力有所了解,需要應用大量孢子的,應先篩選產孢量大的菌株。
在不同培養基中稻曲病菌薄壁分生孢子產量差異懸殊,因此要制備大量孢子時,選擇合適的培養基很關鍵。很巧合,實驗室常備的含馬鈴薯汁的培養基為最適宜的產孢培養基。據報道,在大米培養基上稻曲病菌的另一種無性孢子(厚壁分生孢子)的產孢量比在PSA上的多[9-10],而薄壁分生孢子在含大米汁的培養基中產孢量反而比PS培養液中的少,可能是該病菌這兩種無性孢子的形成所需要的關鍵營養成分不一樣。
形成薄壁分生孢子的適宜溫度為26~28℃,與該病菌另一形態無性孢子(厚壁分生孢子)形成適宜溫度一樣[11],表明該病菌兩種形態無性孢子形成的感溫生理有相似性。當溫度升高至32℃時,薄壁分生孢子產生量急劇下降,顯然高溫對產孢極為不利,因此,夏天培養制備孢子最好應具備降溫培養條件。
該病菌在振蕩培養下可產生大量薄壁分生孢子,而同時靜止培養的幾乎未發現孢子產生。由于振蕩培養具有向培養液充氧的作用,可能該孢子的形成需要充分的氧氣供應。不過,在直接與空氣接觸的固體平板上的大菌落,該病菌卻很少產生薄壁分生孢子,因而單從氧氣條件難以解釋稻曲病菌的產孢現象,可能液態水的存在是該孢子形成的另一必要條件。該病菌的液體培養產孢特性與鐮孢菌類的特性一樣[12],不過,鐮孢菌類在固體平板培養基上能正常產生孢子[13],與稻曲病菌的產孢機理有差異。
雖然振蕩速度越高產孢量越大,但高速振蕩容易使液體漂濺瓶塞,導致污染,也容易出現培養瓶碰甩事故。由于140 r/min與210 r/min的產孢量差異并非太大,作者認為采用140~160 r/min較為有利和安全。
光照對稻曲病菌薄壁分生孢子形成沒有影響,說明該孢子的形成對光不敏感,因而在制備孢子時無需增加光照條件。據報道,光照可誘導某些病原菌產生孢子[14],光照也能誘導稻曲病菌形成厚壁分生孢子[15],稻曲病菌兩種無性孢子對光照反應的差異,也說明該病菌這兩種無性孢子的產孢機理不一樣。
[1] Wang Xiaoming, Liu Qingli, Wang Hao, et al.A BAC based physical map and genome survey of the rice false smut fungusVillosiclavavirens[J].BMC Genomics, 2013, 14: 883-897.
[2] Zhang Tingting, Jiang Yinhui, Huang Junbin, et al.Complete genome sequence of a putative novel victorivirus fromUstilaginoideavirens[J].Archives of Virology, 2013, 158(6): 1403-1406.
[3] Ou S H.Rice diseases [M].UK: Commonwealth Agricultural Bureaux, 1985: 307-311.
[4] 張君成, 陳志誼, 張炳欣, 等.稻曲病菌的形態學觀察研究[J].植物病理學報, 2003, 33(6): 517-523.
[5] Ashizawa T, Takahashi M, Moriwaki J, et al.A refined inoculation method to evaluate false smut resistance in rice [J].Journal of General Plant Pathology, 2011, 77(1): 10-16.
[6] 俞咪娜, 陳志誼, 于俊杰, 等.來源于同一穗不同稻曲球的稻曲病菌的致病性及遺傳多樣性[J].植物病理學報, 2013, 43(6): 561-573.
[7] 張君成, 張炳欣, 陳志誼, 等.稻曲病菌分生孢子的生物學研究[J].植物病理學報, 2003, 33(1): 44-47.
[8] 程明淵, 劉洪濤, 閻萬元, 等.人工培養條件下稻曲病菌厚垣孢子產生因素初探[J].吉林農業科學, 1996(2): 62-64.
[9] 周永力, 章琦.稻曲病菌分離技術的初探[J].中國水稻科學, 1999, 13(3): 186-188.
[10]王疏, 杜毅, 褚茗莉, 等.稻曲病菌孢子形成的培養技術及人工接種研究[J].遼寧農業科學, 1992(5): 35-37.
[11]王桂華, 李桂榮.稻曲病菌人工培養方法[J].植物病理學報, 1990, 20(1): 32.
[12]Pasquet J C, Chaouch S, Macadre C, et al.Differential gene expression and metabolomic analyses ofBrachypodiumdistachyoninfected by deoxynivalenol producing and non-producing strains ofFusariumgraminearum[J].BMC Genomics, 2014, 15: 629-645.
[13]Spolti P, Barros N C, Gomes L B, et al.Phenotypic and pathogenic traits of two species of theFusariumgraminearumcomplex possessing either 15-ADON or NIV genotype [J].European Journal of Plant Pathology, 2012, 133(3): 621-629.
[14]冷偉鋒, 李保華, 國立耘, 等.蘋果輪紋病菌誘導產孢方法[J].植物病理學報, 2009, 39(5): 23-25.
[15]王疏, 白元俊, 周永力, 等.稻曲病菌的病原學[J].植物病理學報, 1998, 28(1): 19-24.
(責任編輯:楊明麗)
Study on factors influencing preparation of thin-walled conidia ofUstilaginoideavirens
Shi Tingting, Wang Zhongwen, Cai Chao, Yang Ping, Qin Qian, Zhang Juncheng
(CollegeofAgriculture,GuangxiUniversity,Nanning530004,China)
The effect of medium, temperature, and shaking speed, etc.on the yield of thin-walled conidia of fungusUstilaginoideavirenswas studied in this paper.The results showed that the maximum amount of conidia was got 7 days post start of growth.Potato broth was the best medium for sporulation of the fungus, and spore yield could be increased greatly when sucrose was added to the broths.Suitable temperature for sporulation was 26-28℃.Static culture was unfavorable way for sporulation.Shaking culture was favorable way for sporulation, and spore yield increased with increase of rotate speed.Different light conditions showed no effect on the spore yield.
Ustilaginoideavirens; thin-walled conidia; sporulation; preparation
2015-12-18
2016-01-28
廣西自然科學基金(2011GXNSFA018068)
S 435.111
A
10.3969/j.issn.0529-1542.2017.01.022
* 通信作者 E-mail:jczhang@gxu.edu.cn

