乙肝前S1抗原在乙肝診療中的臨床價值以及與HBV-DNA相關性研究
陳華宏,陳 謀,洪潔華,林玉葉
(揭陽市人民醫院檢驗科,廣東揭陽522000)
乙肝前S1抗原在乙肝診療中的臨床價值以及與HBV-DNA相關性研究
陳華宏,陳 謀,洪潔華,林玉葉
(揭陽市人民醫院檢驗科,廣東揭陽522000)
目的研究慢性乙肝患者血清中乙肝前S1抗原(PreS1-Ag)、HBeAg、HBV-DNA之間相關性,探討其在慢性乙型肝炎病情監測上的臨床價值。方法⑴分析不同載量HBV-DNA慢性乙型肝炎患者中PreS1-Ag、HBeAg陽性率的差異;⑵根據HBeAg的檢測結果,把1219個病例分為陽性組和陰性組,探討兩組中PreS1-Ag、HBV-DNA之間陽性率的差別。結果⑴PreS1-Ag和HBe-Ag陽性率都隨著HBV-DNA載量的增加而增加,且PreS1-Ag陽性率比HBe-Ag陽性率高;⑵在HBe-Ag陽性的病例中,PreS1-Ag和HBV-DNA的陽性率分別為89.42%、87.76%,兩者之間無統計學差異(χ2=1.55,P>0.05),而在HBe-Ag陰性的病例中,PreS1-Ag和HBV-DNA的陽性率分別為60.4%、52.4%,兩者之間有統計學差異(χ2=247.6,P<0.01)。結論HBV-PreS1抗原在對乙肝病毒復制及傳染性的提示作用中與HBV-DNA有較高的相關性,有效補充了目前乙肝診療以HBV-DNA和HBeAg為主要的檢測手段,聯合檢測能更全面判斷體內乙肝病毒的活躍程度及變異狀況,在慢性乙肝診療中有著較高的臨床價值,值得臨床推廣。
慢性乙型肝炎;PreS1-Ag;HBV-DNA;HBe-Ag
慢性乙型肝炎(CHB)是指乙肝病毒檢測為陽性,病程超過半年或發病日期不明確而臨床有慢性肝炎表現者。其病理機制錯綜復雜,易形成慢性狀態,與肝硬化,肝癌關系密切,是一種發病率高,難治愈,易反復的常見病,監測并清除乙肝病毒是慢性乙型肝炎(CHB)治療的關鍵。長期以來臨床主要通過檢測HBV-DNA和HBeAg來監測體內乙肝病毒的復制狀況和抗病毒治療療效。但是從近期的研究中顯示,即使以上兩個指標結果均為陰性,也不能完全排除乙肝病毒在體內已停止復制的可能。另外由于檢測HBV-DNA所依賴的基因擴增技術(PCR),其實驗條件高,設備和試劑昂貴,目前能夠開展的醫療單位非常少[1],且基因擴增技術(PCR)技術受病毒滴度、實驗室污染等因素影響易產生假陰性或假陽性結果,因此迫切需要尋找更加簡單快捷,同時特異性和敏感性好的檢測指標來協助慢性乙肝的診斷和治療。PreS1-Ag作為乙肝dane顆粒的一種衣殼蛋白,含有肝細胞膜受體,具有很強的免疫原性,在乙肝病毒感染肝細胞和機體免疫應答中起著重要的作用[2,3]。研究表明,PreS1-Ag是反映乙肝病毒感染、裝配、復制的重要指標[4],再加上其檢測方法簡單,結果穩定,無需大型儀器等優點,正受到臨床越來越多的關注[5]。
1 材料與方法
1.1 一般資料選擇自2015年6月到2016年9月在廣東省揭陽市人民醫院進行慢性乙肝治療的患者1219例,其中男性患者646例,女性患者573例,年齡在15~68歲之間,平均年齡是39.1歲。乙型肝炎診斷依據為中華醫學會肝病學分會和中華醫學會感染病分會聯合發布的2010版《中國乙型肝炎防治指南》的標準。所有參與研究的患者均屬自愿。
1.2 方法所有標本均在清晨空腹抽血3ml送檢,于37度水浴10min,離心后吸取血清上機檢測PreS1-Ag、HBV-DNA和“乙肝二對半”三個(組)項目。其中,PreS1-Ag和“乙肝二對半”二個項目均采用酶聯免疫法(ELISA)進行檢測,使用上海科華生物技術有限公司試劑,儀器為Tecan前處理及FAME全自動酶聯免疫分析儀,所有實驗均上機操作,實行標準化管理,以確保結果的準確性;HBVDNA采用基因擴增技術(PCR)進行定量檢測,使用中山大學達安基因股份公司DA7600實時熒光定量PCR擴增儀,試劑為中山大學達安基因股份公司生產的HBV-DNA PCR試劑盒,所有實驗嚴格按試劑說明書進行操作。
1.3 統計學分析將HBV-DNA陽性的病例根據拷貝數從低到高分成四組,分別統計出各組中PreS1-Ag和HBe-Ag兩者各自的陽性率;再將所有乙型肝炎研究對象分為HBe-Ag陽性和陰性兩組,統計出兩組中PreS1-Ag和HBV-DNA各自的陽性例數;最后采用SPSS 19.0統計學軟件處理相關的數據,用四格表卡方檢驗計數資料,應用χ2檢驗組間差異,P<0.05表示差異有統計學意義。
2 結果
2.1 不同HBV-DNA載量中PreS1-Ag、HBe-Ag的陽性率比較在819例HBV-DNA陽性患者中,PreS1-Ag的陽性率高達89.0%,而HBe-Ag的陽性率僅為55.2%,可見相對于HBe-Ag,PreS1-Ag和HBV-DNA在陽性率方面有著更高的吻合率;另外在500~<103、104~105、106~107、≥108從低到高的四組HBV-DNA載量中,PreS1-Ag對應的陽性率分別為76.2%、83.8%、91.2%、100%,而HBe-Ag對應的陽性率是27.6%、32.1%、57.2%、98.0%,這顯示隨著HBV-DNA載量的不斷增加,PreS1-Ag和HBe-Ag的陽性比例都逐漸增大[6],表明兩者與HBV-DNA均有明顯的相關性;同時在每個載量組中,PreS1-Ag的陽性率都明顯高于HBe-Ag的陽性率,這也進一步說明HBV-PreS1抗原和HBVDNA的吻合度明顯優于HBe-Ag。見表1,圖1。
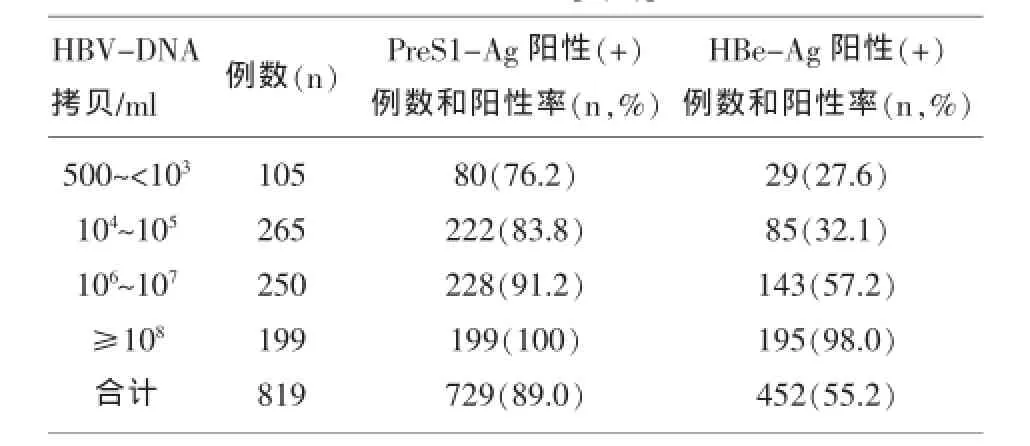
表1 不同HBV-DNA載量中PreS1-Ag、HBe-Ag的陽性率比較[n(%)]
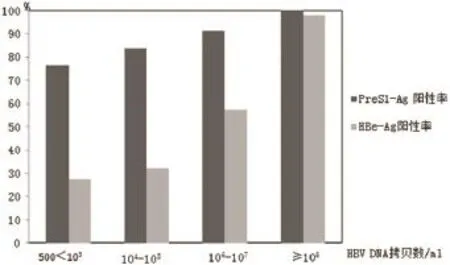
圖1 不同HBV-DNA載量PreS1-Ag和HBe-Ag陽性率對比
2.2 HBe-Ag陰、陽性與PreS1-Ag、HBV-DNA的檢出率比較表2可見在所統計的總共1219例慢性乙肝患者中,PreS1-Ag和HBV-DNA的陽性率分別為72.68%、67.19%,在482例HBe-Ag陽性的病例中,PreS1-Ag和HBV-DNA的陽性率分別為89.42%、87.76%,兩者之間無統計學差異(χ2=1.55,P>0.05),見表3;而在737例HBe-Ag陰性的病例中,PreS1-Ag和HBV-DNA的陽性率分別為60.4%、52.4%,兩者之間有統計學差異(χ2=247.6,P<0.01),見表4。

表2 HBe-Ag陰、陽性與PreS1-Ag、HBV-DNA的檢出率比較

表3 HBe-Ag陽性組PreS1-Ag和HBV-DNA的陽性率關系

表4 HBe-Ag陰性組PreS1-Ag和HBV-DNA的陽性率關系
3 討論
乙型肝炎病毒(HBV)的感染是一個在全球范圍內都得到高度關注的健康話題,它也是導致患者慢性肝臟問題的最常見病因。據統計,在我國大概有10%的HBV攜帶患者,其中約有25%的的患者最終會發展成為慢性乙肝、原發性的肝癌以及肝硬變。目前,臨床上對HBV病毒的主要檢查方法是進行“乙肝二對半”的檢測,同時再通過檢測HBV-DNA來監測患者體內的乙肝病毒復制狀況。但因檢測HBV-DNA所依賴的基因擴增技術(PCR),其實驗條件要求高,同時所使用的儀器設備及實驗試劑都比較昂貴,導致其在基層單位的普及度不廣泛,從而在一定程度上影響了乙肝防治工作的開展進行。近年來我院開展了HBVPreS1抗原的檢測,在協助慢性乙肝的診斷治療中取得了良好的效果。
本文的研究結果顯示,在表1和圖1所統計的從低到高的四組HBV-DNA載量中,PreS1-Ag和HBe-Ag兩者對應的陽性率分別為76.2%、27.6%;83.8%、32.1%;91.2%、57.2%;100%、98.0%,即隨著HBV-DNA拷貝數的不斷增加,PreS1-Ag和HBe-Ag的陽性比例都逐漸增大[6],提示兩者均與HBV-DNA存在正相關[7],這也說明PreS1-Ag、HBe-Ag和HBV-DNA三者在監測乙肝病毒復制方面有一致性;同時我們也觀察到,在全部819例HBV-DNA陽性患者中,PreS1-Ag和HBe-Ag的陽性率分別為89.0%、55.2%,可見無論在總的HBVDNA陽性患者中,還是細分到各個不同HBVDNA載量組中,PreS1-Ag的陽性率都要明顯高于HBe-Ag的陽性率,這也說明PreS1-Ag與HBVDNA的相關性優于HBe-Ag,其在反映病毒復制和傳染性上比HBe-Ag更有價值,可彌補因乙肝病毒C區缺失而致HBe-Ag不表達所造成的診斷和治療困難。
表2和表3結果顯示,在所統計的總1219例慢性乙肝患者中,PreS1-Ag和HBV-DNA的陽性率分別為72.68%、67.19%,兩者的陽性率接近,尤其是在HBe-Ag陽性的標本中,PreS1-Ag和HBVDNA的陽性率分別高達為89.42%、87.76%(χ2= 1.55,P>0.05),兩者之間無統計學差異[8],顯示在HBe-Ag陽性患者中,兩者對于監測乙肝病毒復制方面有高度的一致性,即當患者HBe-Ag和PreS1-Ag同時呈陽性時,直接提示乙肝病毒在該體內復制活躍,可見,PreS1-Ag作為判斷體內乙肝病毒復制的新標志,在監測乙肝病毒感染和復制中有重要價值。
表4結果則顯示在HBe-Ag陰性的病例中,PreS1-Ag和HBV-DNA的陽性率分別為60.4%、52.4%,兩者之間有統計學差異(χ2=247.6,P<0.01),這說明PreS1-Ag雖然對于部分因為乙肝病毒C區基因變異而導致HBe-Ag檢測呈陰性的乙肝患者的診斷治療有重要意義,但在監測病毒復制方面,PreS1-Ag并不能完全代替HBV-DNA[9],因為相對于作為最直接的分子生物學指標的HBV-DNA[10],PreS1-Ag是乙肝病毒血清學標志物,其陰陽性轉化會滯后于HBV-DNA的載量變化,從而出現HBV-DNA已轉陰性而PreS1-Ag暫時呈陽性結果的現象;另外,當乙肝病毒雖存在復制但前S區缺失或變異時,則會導致PreS1-Ag呈陰性而HBV-DNA呈陽性結果[11];而當乙肝病毒在極低拷貝狀態復制時也會因PCR方法學上的極限而導致HBV-DNA未能檢測出,可見PreS1-Ag、HBe-Ag和HBV-DNA雖然都是監測病毒復制的指標,但檢測方法學有所不同,表達的意義也有所區別,單項獨立檢測,容易出現漏診或誤判,而三者聯合檢測,有助于提高HBV檢測的敏感性,能更早期且更全面的對乙肝病毒的活動性進行判斷和療效評估,避免誤判病情,貽誤治療[12,13]。
總之,乙肝PreS1-Ag作為判斷體內乙肝病毒存在的新標志,在監測乙肝病毒感染和復制中與HBe-Ag、HBV-DNA有密切的相關性,再加上其檢測方法簡單方便,結果穩定,無需大型儀器等優點,非常適合在沒有條件進行基因擴增技術(PCR)檢測的基層單位開展[14];而在有條件開展HBVDNA檢測的單位,開展PreS1-Ag檢測是對目前臨床常用的以HBV-DNA及HBeAg為主要的乙肝病毒監測指標進行了有效的補充,能更全面地監測乙肝病毒在體內的復制和變異情況,在慢性乙型肝炎(CHB)的診斷治療、判斷預后及疾病轉歸中有著重要的臨床階值[15],值得臨床推廣。
[1]陳立章,薛靜,劉立亞,李戰戰,等.血清HBV-DNA定量檢測與凝血指標對乙肝患者病情診斷的研究[J].中國現代醫學雜志,2013,23(30):31-36.
[2]Kessler HH,preininger S,Stelzl E,et al.ldentification of different states of hepatitis B virus infection with a quantitative PCR assay [J].Clin Diagn Lab Immunol,2000,26(8):129-131.
[3]Funk ML,Rosenberg DM,Lok AS.World-wide epidemiology of HBeAg-negative chronic hepatitis B and associated precore and core promoter variants[J].J Viral Hepat,2002,23(9):637-638.
[4]周紅波,周美英.乙型肝炎HBeAg陰性患者前S1抗原與HBVDNA定量檢測的相關性探討[J].實驗與檢驗醫學,2012,30(3):312-314.
[5]楊玉潔,張緒署,蘇麗君,等.應用Pre-S1 Ag診斷HBV感染的可能性研究[J].實驗與檢驗醫學,2013,31(1):15-17.
[6]柳枝,黃欣.前S1抗原在診療乙肝病毒復制時的臨床價值[J].實驗與檢驗醫學,2009,27(4):353.
[7]王書華,張立平,陳六生.乙型肝炎病毒前S1抗原陽性在乙型肝炎病情診斷及預后判斷中的應用[J].國際檢驗醫學雜志,2016,37(1):101-102.
[8]李文波,雷毅,高武,等.HBV-DNA Pres1-Ag與乙型肝炎HBeAg聯合檢測的意義及相關性分析[J].國際檢驗醫學雜志,2015,36(22):3311-3313.
[9]李彩東,吳斌,陳錫蓮,等.乙型肝炎病毒前S1抗原與HBV DNATKG HBV-M及肝功能的相關性探討[J].國際檢驗醫學雜志,2015,36(7):936-938.
[10]朱紅英.乙肝S1前蛋白和乙肝DNA的相關性研究[J].實驗與檢驗醫學,2013,31(6):629-630.
[11]陳康.乙肝病毒PreS1抗原和HBV-DNA檢測在病毒感染和復制中的意義[J].淮海醫藥,2008,9(5):430-431.
[12]竇亞玲,李永哲,劉志肖,等.乙型肝炎病毒前S1抗原檢測的臨床階值[J].中華檢驗醫學雜志,2006,11(8):714-716.
[13]Sugauchi F,Ohno T,Orito E,et al.Influence of hepatitis B virus genotypes on the development of pro-S deletions and advanced liver disease[J].J Med Viral,2003,70(4):537-539.
[14]欒琳,苑司生.HBV前S1抗原與血清標志物聯合檢測的臨床意義[J].實用醫藥雜志,2010,27(04):326-327.
[15]徐肖丁,張義文,周錦霞,等.聯合檢測乙肝五項、前S1抗原與乙肝DNA的臨床應用[J].實驗與檢驗醫學,2011,29(4):366-368.
R512.6+3,R446.62
A
1674-1129(2017)01-0102-03
10.3969/j.issn.1674-1129.2017.01.034
2016-10-10;
2016-11-24)

