阿苯達唑致重度肝損傷病例分析及文獻復習
蘇風華,何登明
阿苯達唑致重度肝損傷病例分析及文獻復習
蘇風華,何登明*
藥物性肝損傷;阿苯達唑;病例分析
阿苯達唑(Albendazole),商品名腸蟲清,是高效廣譜驅腸蟲藥物,其不良反應主要累及消化系統、皮膚及其附件、神經系統、血液系統等,常見嚴重不良反應主要包括:腦炎/脫髓鞘腦病、肝損害、貧血、白細胞減少[1]。筆者報道1例青年女性,不到2年的時間內先后發生2次阿苯達唑藥物性重度肝損傷,結合2015版的《藥物性肝損傷診治指南》,報告如下。
1 病例報告
1.1 第一次發病情況女,24歲,因上腹部不適伴惡心9 d,皮膚、鞏膜黃染4 d入院。無病毒性肝炎、脂肪肝等慢性肝病史,無飲酒史,家族中無類似患者。查體:未見肝掌、蜘蛛痣等慢性肝病體征,皮膚、鞏膜重度黃染,肝脾未觸及。肝功能:總膽紅素238 μmol/L、直接膽紅素129.7 μmol/L、白蛋白39 g/ L、球蛋白25 g/L、谷丙轉氨酶1177 U/L、谷草轉氨酶490 U/L、γ-谷氨酰轉肽酶67 U/L、堿性磷酸酶92 U/ L;凝血酶原時間國際標準化比率1.25;乙型五項、甲肝IgM抗體、丙肝抗體,戊肝IgM抗體、弓形蟲IgM抗體、風疹病毒IgM抗體、巨細胞病毒IgM抗體、單純皰疹病毒IgM抗體、EB病毒IgM抗體等病毒標志物均陰性;自身免疫性肝病陰性;甲功五項及銅藍蛋白正常。發病前1月曾自服阿苯達唑400 mg(2片),同時還服用幾日的某種瘦身保健品(具體不詳),無服用其他可疑藥物、食物史。入院診斷:藥物性肝損傷(阿苯達唑或保健品)。鑒于阿苯達唑的肝損傷發生率較低及損傷發生在服用阿苯達唑1個月后,肝損傷的來源更傾向于保健品。給予異甘草酸鎂、還原型谷胱甘肽等常規保肝治療,肝功能逐漸好轉,45 d后恢復正常,隨診6個月無復發。
1.2 第二次發病情況該患者1年后,再次因上腹部不適伴惡心、皮膚、鞏膜黃染7 d入院。發病前1個月再次自服阿苯達唑400 mg,無服用其他藥物史。肝功能:總膽紅素201 μmol/L、直接膽紅素126.8 μmol/L、白蛋白40 g/L、球蛋白34.2 g/L、谷丙轉氨酶941 U/L、谷草轉氨酶490 U/L、γ-谷氨酰轉肽酶81 U/L、堿性磷酸酶98 U/L;凝血酶原時間國際標準化比率1.20;各項肝炎標志物、自身免疫性肝病抗體均陰性;銅藍蛋白及α-1抗胰蛋白酶正常;肝平掃及強化CT檢查提示:肝右葉鈣化灶,脾大,膽囊結石并膽囊炎;電子胃鏡未見異常。給予常規保肝治療后,肝功能逐漸恢復。
該患者兩次發病的起病、發展、轉歸過程完全一致(圖1)。結合既往病史,考慮第二次發病屬于典型的藥物再激發反應。因此,該例患者明確診斷為:藥物性肝損傷,肝細胞損傷型,急性,RUCAM 10分(極可能,阿苯達唑),嚴重程度3級。
2 討論
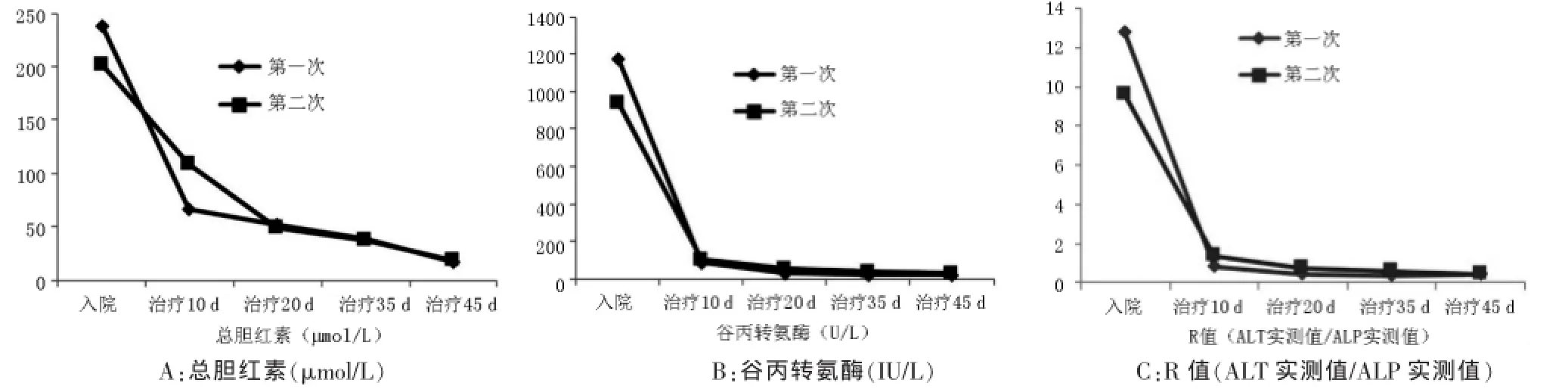
圖1 兩次發病肝功能主要指標變化情況
藥物性肝損傷(drug-induced liver injury,DILI)是指由各類處方或非處方的化學藥物、生物制劑、傳統中藥(TCM)、天然藥(NM)、保健品(HP)、膳食補充劑(DS)及其代謝產物乃至輔料等所誘發的肝損傷[2]。已知全球有1100多種上市藥物具有潛在肝毒性,我國急性DILI約占急性肝損傷住院比例的20%[2]。隨著乙肝疫苗的廣泛接種,HBV感染發生率將逐漸下降,DILI必然受到更多的關注。比如,近年土三七引起的肝小靜脈閉塞病就受到了廣泛關注[3]。
阿苯達唑為高效廣譜驅蟲藥,藥代動力學顯示其口服后95%不吸收,在腸道內直接作用于成蟲和蟲卵,24 h內由糞便排出;其余5%由肝吸收,在肝微粒體酶和NADPH的作用下轉化成丙硫咪唑亞砜和丙硫咪唑砜,前者可殺組織內幼蟲和腸道內成蟲,48 h內由腎排出。阿苯達唑的不良反應以神經系統不良反應[4-8]和過敏性反應的報道較多[9-12],引起嚴重肝損傷的報道較為少見。本例患者第一次發病前除口服阿苯達唑外,還同時服用保健品,近年來,保健品導致藥物性肝損傷的報道越來越多,所以第一次發病不排除保健品因素所致肝損傷。第二次發病時,患者只服用過阿苯達唑,RUCAM因果關系評分達到10分,根據藥物性肝損傷藥物再激發反應的理論,確定為阿苯達唑導致的藥物性肝損傷。
阿苯達唑不良反應的發生有一定的潛伏期,短的如過敏性休克、過敏性藥疹等速發型過敏反應多在用藥后30 min內發生,神經系統不良反應多在用藥后3 d至數月發生,最長的如血液系統損害多在用藥半年內發生[1]。本例阿苯達唑肝損傷的潛伏期較長,兩次發病都是在服藥后1個月左右開始出現自覺癥狀。文獻報道阿苯達唑肝損害潛伏期多在服藥后數小時至幾日,1個月或數月后發病罕見報道[13-16]。不同病例潛伏期的長短可能在發病機制上存在差異。
藥物性肝損傷發生機制有直接肝不良反應和特異質性肝不良反應兩種。直接肝不良反應是指攝入體內的藥物和(或)其代謝產物對肝產生的直接損傷,具可預測性,與藥物劑量密切相關,潛伏期短,個體差異不顯著[2]。特異性肝不良反應作用是由于藥物代謝酶系、跨膜轉運蛋白及溶質轉運蛋白的基因多態性導致酶或轉運蛋白功能異常,增加了宿主對DILI的易感性,具不可預測性,臨床較為常見,個體差異顯著,與藥物劑量常無相關性,動物實驗難以復制,臨床表現多樣,又可分為免疫特異質性DILI和遺傳特異質性DILI[2]。從發病機制上看,本例阿苯達唑肝損害考慮為特異質性肝不良反應,遺傳特異質性DILI可能性較大,藥物代謝相關基因多態性可能是導致其發生嚴重肝損傷的主要原因。劉毅[13]報道1例口服史克腸蟲清后3 d即出現明顯癥狀,首次立即出現畏寒、發熱等過敏反應,第二次服藥后乏力、食欲缺乏、尿黃,皮膚、鞏膜黃染等表現,考慮為免疫變態反應介導的藥物性肝炎。因藥物代謝涉及多種酶類及蛋白質,具體何種基因多態性決定了阿苯達唑對本例患者產生肝不良反應,有待深入研究。
該例肝損傷較重,嚴重程度達到3級,屬于重度肝損傷,雖然凝血機制并未受損,但總膽紅素和谷丙轉氨酶升高幅度均超過10倍正常上限。根據受損靶細胞類型,本例阿苯達唑肝損傷臨床分型為典型的肝細胞損傷型,主要以谷丙轉氨酶及膽紅素升高為主,堿性磷酸酶升高及白蛋白下降不明顯,無明顯瘀膽情況。雖然本例肝損傷較重,但對常規保肝藥物治療比較敏感,40 d內肝功能完全恢復正常,這也符合其肝細胞損傷性的病理特點。王婧等[16]報道,41例接受阿苯達唑治療的廣州管圓線蟲病患者,發生肝功能異常者26例,主要表現為轉氨酶輕中度升高,僅1例出現總膽紅素升高。可見阿苯達唑引起重度肝損傷者并不常見。國外亦有阿苯達唑引起肝損傷的報道,但不如國內報道多[17-21]。
盡管阿苯達唑耐受性良好、價格經濟、療效肯定,且用于“蛔蟲病、蟯蟲病”適應證是作為非處方藥管理的。趙世丹等[1]對58例個案報道進行分析時,未明確診斷或自行服用的達30例,占個案報道總數的51.72%,其中不乏嚴重不良反應的病例。該例患者服用阿苯達唑就是典型的自發行為,未在任何醫師指導下進行,亦未進行大便蟲卵等相關檢查,僅在自覺“食欲不佳”的情況下,憑兒時祖母的“定期打蟲”觀念和“腸蟲清”廣告的影響而自行決定服用阿苯達唑。
總之,阿苯達唑可在特定人群中發生重度肝損傷,應嚴格把握適應證,盡可能在醫師指導下應用,避免在診斷不明確的情況下自行服用等不合理使用現象,以最大限度減少其不良反應的發生。
[1]趙世丹,王慧,劉翠麗.阿苯達唑不良反應的文獻分析[J].中國藥物警戒,2013,10(5):299-302.
[2]中華醫學會肝病學分會藥物性肝病學組.藥物性肝損傷診治指南[J].臨床肝膽病雜志,2015,31(11):1752-1769.
[3]從明,何芳.土三七致肝小靜脈閉塞病3例[J].當代醫學,2014,20(20):132-133.
[4]劉琦,田淑芬,吳珊.腸蟲清所致的變態反應性腦病1例[J].實用醫學雜志,2011,27(14):2618.
[5]王蘋莉,倪渝鯤.阿苯達唑致脫髓鞘腦病1例[J].藥物流行病學雜志,2011,20(7):381.
[6]袁春云,陳瑤,尹煒凡.丙硫咪唑致腦干及高頸段脊髓脫髓鞘病1例報告[J].臨床神經病學雜志,2010,23(5):388.
[7]王夏紅,李蜀渝,穆俊林.咪唑類驅蟲藥致遲發性腦病45例分析[J].中國誤診學雜志,2004,4(3):443-444.
[8]唐干烈.腸蟲清治療囊蟲病致遲發性腦水腫1例[J].蛇志,2000,12(3):79-80.
[9]周永紅.腸蟲清引起結腸過敏性紫癜1例報告[J].浙江臨床醫學,2004,6(10):834.
[10]張金才,隋志芳.腸蟲清致過敏性紫癜1例[J].濰坊醫學院學報,2004,26(2):150.
[11]劉思同.服用史克腸蟲清引起過敏性紫癜1例報道[J].井岡山醫專學報,2001,8(1):88.
[12]劉福文,謝淑榮,楊萬榮.腸蟲清致嚴重蕁麻疹一例[J].小兒急救醫學,2001,8(2):84.
[13]劉毅.史克腸蟲清致急性肝損傷一例[J].臨床肝膽病雜志,2001,17(3):155.
[14]張琪.阿苯達唑致發熱肝臟損害1例[J].藥物流行病學雜志,2009,18(5):385-386.
[15]李國進.腸蟲清致肝臟損害1例[J].人民軍醫,1991(10):59.
[16]王婧,鄭曉燕,陰赪宏,等.阿苯達唑致廣州管圓線蟲病患者肝損害的臨床分析[J].中國病原生物學雜志,2008,3(3):209-211.
[17]Bagheri H,Simiand E,Montastruc JL,et al.Adverse drugs relation to anthelmintics[J].The Annals of Pharmacotherapy,2004,38(3):383-388.
[18]El-Mufti M,Kamag A,Ibrahim H,et al.Albendazole therapy of hydatid disease:2-year follow-up of 40 cases[J].Ann Trop Med Parasitol,1993,87(3):241-246.
[19]Ríos David,Restrepo Juan C.Albendazole-induced liver injury:a case report[J].Colomb Med,2013,44(2):119-120.
[20]Choi GY,Yang HW,Cho SH,et al.Acute drug-induced hepatitis caused by albendazole[J].J Korean Med Sci Korea South,2008,23(5):903-905.
[21]Amoruso C,Fuoti M,Miceli V,et al.Acute hepatitis as a side effect of albendazole:a pediatric case[J].Pediatr Med Chir,2009,31(6):262-264.
[2016-08-20收稿,2016-09-18修回][本文編輯:董冰媛]
R657.3
B
10.14172/j.issn1671-4008.2017.03.014
271000山東泰安,解放軍88醫院全軍肝病診治中心(蘇風華,何登明)
何登明,Email:hedengming@sina.com

