替莫唑胺聯合全腦放療治療肺癌腦轉移的療效評價
趙蕾+孫萍


[摘要] 目的 觀察替莫唑胺聯合全腦放療治療肺癌腦轉移的臨床療效、不良反應及生存時間。 方法 回顧性分析43例肺癌腦轉移患者,全腦放療采用CT模擬定位三維適形放射治療(3D-CRT)技術,1次/d,每周5次,共2周。在給予全顱腦放療的同時給予替莫唑胺同期化療,150 mg/(m2·d),每周期為28 d,根據患者的耐受情況可繼續口服替莫唑胺4~6周期。利用Kaplan-Meier法計算生存率。 結果 43例患者客觀緩解率為79.1%(34/43),其中CR為14.0%(6/43),PR為65.1%(28/43),PD 出現9例。截止至2016年11月30日,43例患者中死亡7例,其中1例因顱內病灶進展死亡,6例因合并轉移其他重要臟器衰竭死亡。全組患者隨訪至截止日期的生存率(OS)和無疾病進展率(PFS)分別為 49.1%和 56.9%。替莫唑胺聯合全腦放療的不良反應較輕,患者均可耐受。 結論 替莫唑胺聯合全腦放療治療肺癌腦轉移有較好的臨床療效,同時患者對治療可耐受。
[關鍵詞] 替莫唑胺;全腦放療;肺癌;腦轉移
[中圖分類號] R734.2 [文獻標識碼] B [文章編號] 1673-9701(2017)07-0075-04
[Abstract] Objective To observe the clinical efficacy, adverse reactions and survival time of temozolomide combined with whole brain radiotherapy in lung cancer. Methods 43 patients with lung cancer combined with brain metastases were retrospectively analyzed. Whole-brain radiotherapy was performed by CT simulated location and three-dimensional conformal radiotherapy(3D-CRT) technique, once a day, 5 times a week for 2 weeks. During the same time of whole brain radiotherapy, temozolomide concurrent chemotherapy was given, 150 mg/(m2·d), each cycle for 28 days. According to the patient's tolerance, the temozolomide could be orally given for 4 to 6 cycles continuously. The survival rate was calculated using the Kaplan-Meier method. Results The objective remission rate was 79.1% (34/43) in 43 patients, among whom CR was14.0%(6/43), PR was 65.1%(28/43), and 9 cases showed PD. As of November 30, 2016, among the 43 patients, 7 cases were died, of whom 1 case died of progressive intracranial lesions, and 6 cases died of other important organ failure due to metastasis. The overall survival(OS) and disease-free progression rate(PFS) were 49.1% and 56.9% respectively follow up to the deadline. The adverse reactions of temozolomide combined with whole brain radiotherapy were less, and the patients were able to tolerate. Conclusion Temozolomide combined with whole brain radiotherapy has a good clinical effect in the treatment of brain metastases from lung cancer, while the patients have a good tolerability.
[Key words] Temozolomide; Whole brain rediotherapy; Lung cancer; Brain metastases
據報道,從20世紀30年代開始,肺癌的發病率急速上升,并且很快成為全世界第一位的癌癥死因[1]。進入20世紀90年代后,盡管部分發達國家男性肺癌發病率緩慢下降,但是更多的發展中國家和發達國家的女性肺癌例數卻每年遞增。因此,肺癌的發病率仍居全世界惡性腫瘤的前列,并且肺癌發病率和死亡率均隨著年齡增長而上升,一般40歲以后肺癌發病率明顯上升,發病率和死亡率到75歲左右達到高峰,然后有所下降。中晚期肺癌容易轉移到全身各處,而顱腦是肺癌較為常見的轉移部位之一。肺癌腦轉移已經嚴重影響患者生活質量及總生存時間,且合并腦轉移的肺癌患者的5年生存率大大下降[2]。由于肺癌患者已有遠處轉移,沒有手術機會切除腫塊,因此對這類患者常常以姑息對癥支持治療為主[3,4]。全腦放療是肺癌腦轉移姑息治療的最重要手段,全腦放療目前已被NCCN指南列入治療惡性腫瘤腦轉移的標準治療方式。替莫唑胺(temozolomide,TMZ)是新型的烷化劑類化療藥物,它容易透過血-腦脊液屏障,藥物有效利用率較高,不良反應較小,而且服用方法簡便,患者也具有良好的依從性,同時與放療聯合應用可增加放療增敏性[5]。本研究選擇2015年2月~2016年2月煙臺毓璜頂醫院口服替莫唑胺聯合全腦放療的43例肺癌腦轉移患者進行回顧性分析,旨在觀察和探討替莫唑胺聯合全腦放療對肺癌腦轉移患者的臨床治療效果、不良反應及生存曲線。
1 資料與方法
1.1 一般資料
收集我院2015年2月~2016年2月的肺癌腦轉移患者共43例,均滿足以下條件:(1)均有肺癌病理診斷并行顱腦增強MRI或者增強CT加以證實;(2)年齡35~72歲;(3)體力狀況ECOG評分0~1分,預計生存期≥3個月;(4)患者血液學檢驗及心臟、肝臟等重要器官功能無明顯異常。一般資料見表1。
1.2 治療方法
放療方法及劑量均相同,全腦放療采用CT模擬定位三維適形放射治療(3D-CRT)技術,1次/d,每周5次,在全腦放療的同時給予口服替莫唑胺化療,150 mg/(m2·d),連續口服5 d,停藥23 d后再次給予替莫唑胺,每周期為28 d(要求繼續替莫唑胺全身化療的患者不再接受其他相關抗腫瘤治療),根據患者是否可耐受的情況繼續給藥4~6周期。除此之外,若患者出現因腦轉移瘤或全腦放療引起頭痛、頭暈、惡心、嘔吐等癥狀應及時給予地塞米松及甘露醇等脫水、降顱內壓治療。聯合治療的同時需監測血象變化,如有白細胞或血小板降低應及時給予重組人粒細胞集落因子及重組人白介素-11皮下注射行升白細胞及血小板治療。若有胃腸道反應,如惡心、嘔吐等不適,則給予止吐等緩解癥狀的支持治療。
1.3 隨訪
后期的隨訪主要是通過門診復查隨訪和電話隨訪。隨訪是從每例患者開始治療的第1天起,直至隨訪截止日期,或患者死亡、失訪。隨訪的截止日期為2016年11月30日。隨訪的間隔日期為1~3個月。失訪者則按最后1次隨訪時間計算生存時間。
1.4 療效評價
基線標準是每位患者治療前1個月內的顱腦增強MRI/CT的影像學檢查結果。患者在治療期間每周均需復查1次血液學檢驗,包括血常規及血肝腎功檢驗。全部治療結束后1個月需復查1次影像學檢查,如顱腦增強MRI或者顱腦增強CT,用以評價近期治療效果。2個月后再次復查影像學檢查進行評價治療效果,此后每3個月需要復查1次顱腦增強MRI/CT評價臨床療效。按照實體瘤的RECIST標準[6,7]評價近期治療效果:完全緩解(Complete Remission,CR)、部分緩解(Partial Remission,PR)、穩定(Stable Diseasse,SD)和疾病進展(Progressive Disease,PD)。口服替莫唑胺期間應詳細記錄服用替莫唑胺出現的相關不良反應,及不良反應出現的時間和程度。不良反應則使用由美國國立衛生研究院(National Institute of Health,NIH)制訂的通用不良事件術語標準4.0(Common Terminology Criteria Adverse Events Version 4.0,CTCAE v4.0)[8]進行評估是否需要調整替莫唑胺劑量。而患者的生存指標主要觀察總生存率(Overall Survival rate,OS)和無進展生存率(Progression Free Survival,PFS)。
1.5 統計學方法
采用SPSS 19.0統計學軟件進行統計學分析,自放療第1日開始計算其生存時間。觀察并記錄所有患者的總生存時間(OS)和疾病的無進展生存時間(PFS)。用Kaplan-Meier法繪制生存曲線以描述患者的存活時間。
2 結果
2.1 隨訪情況
隨訪時間3.1~15.2個月,中位隨訪時間為8.2個月,其中3例失訪(按最后一次隨訪之月計算生存時間),隨訪率93.02%。
2.2 近期療效
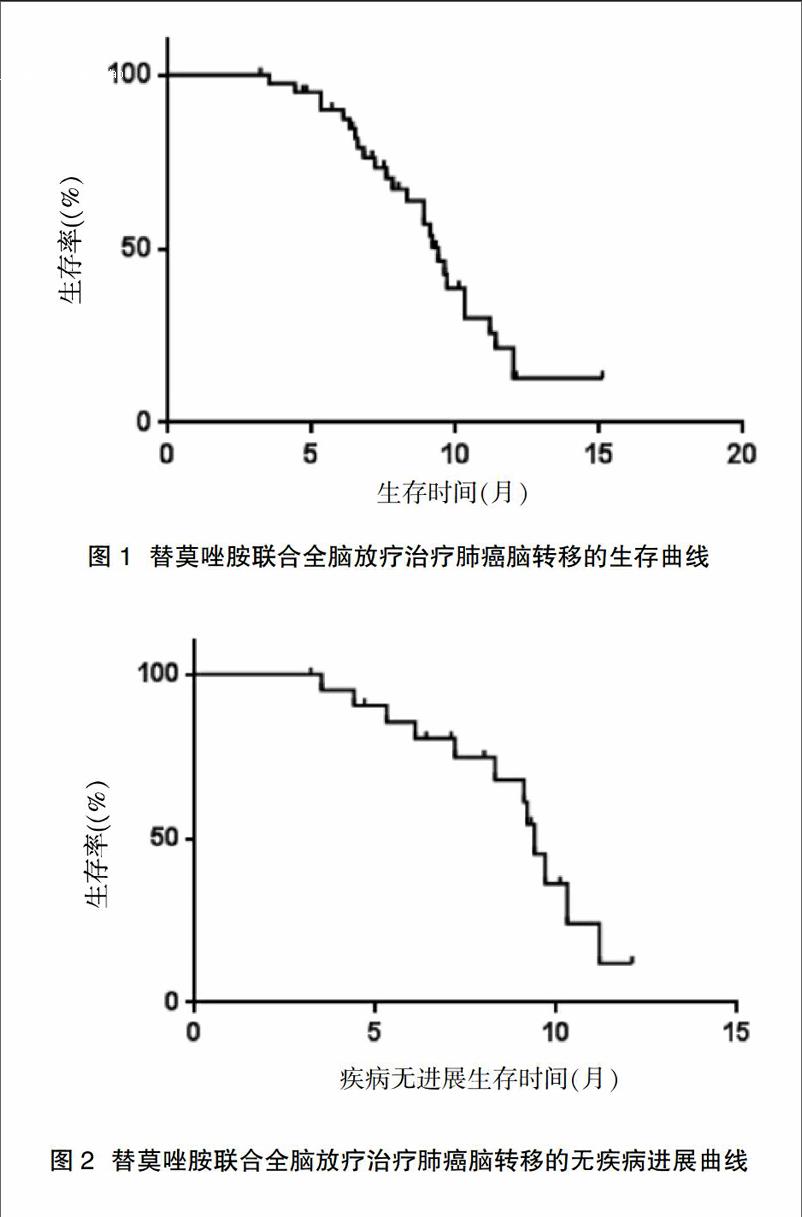
43例患者客觀緩解率(CR+PR)為79.1%(34/43),其中CR為14.0%(6/43),PR為65.1%(28/43),PD為20.9%(9/43)。截止至2016年11月30日,43例患者中死亡7例,其中1例因顱內病灶進展死亡,6例因合并轉移至其他重要臟器衰竭死亡。全組患者隨訪至截止日期的生存率(OS)和無疾病進展率(PFS)分別為 49.1%和 56.9%(圖1、2)。
2.3 不良反應
口服替莫唑胺化療期間,主要不良反應集中在血液學和胃腸道(表2)。在本組患者中,并沒有觀察到有關肝、腎等主要臟器的毒性反應,也沒有患者因不良反應而減少替莫唑胺劑量。只有1例患者在全腦放療期間因3級胃腸道反應中斷口服替莫唑胺1 d,表明患者對替莫唑胺耐受性較好。
3 討論
目前肺癌是威脅人類生命的惡性腫瘤之一,預后較差,較早出現遠處轉移,其中腦轉移較為常見。雖然目前全腦放療已作為肺癌腦轉移的一線治療措施,但是仍有一部分患者因顱內轉移灶進展或者并發癥發生而死亡。而且目前能夠通過血腦屏障的化療藥物有限,替莫唑胺作為第二代烷化劑-咪唑四嗪類衍生物的一種新型口服藥物[9],被大多數人用于治療原發性和復發性的惡性腦膠質瘤。替莫唑胺在酸性環境下不宜分解,但它可以在生理條件下的pH值可通過一些化學反應轉化為有活性的產物5-(3-甲基)-1-三氮烯-1-咪唑基-4-氨甲酰(MTIC)[10,11],它可以在腫瘤細胞分裂的各個時期發揮作用,從而烷基化腫瘤細胞,發揮它的細胞毒作用[12,13]。替莫唑胺可以通過血腦屏障,而它的口服生物利用率約100%,在中樞神經系統的藥物濃度為血漿藥物濃度的40%[14]。長期小劑量的替莫唑胺持續給藥可以降低腫瘤細胞的耐藥性。有文獻報道,只有極少數的患者會在口服替莫唑胺治療過程中出現血液學不良反應,因此在治療過程中基本沒有患者需要減少藥物劑量或調整治療時間[15]。替莫唑胺可以通過聯合放療獲得增敏性,而放療本身具有對細胞的殺傷作用,與替莫唑胺代謝產物所具有的細胞毒性可以協同治療腦多發轉移瘤。提前1~2 h口服替莫唑胺可以更大地發揮替莫唑胺的放療增敏性,與全腦放療協同發揮抗腫瘤作用[15]。Motomura等[16]研究證實,替莫唑胺聯合精確放療具有協同作用以及良好的耐受性。
大多數學者認為在有限的生存時間內盡可能地提高患者的生存質量、延長患者的總生存期是對中晚期惡性腫瘤患者,尤其是合并遠處轉移的患者來說最有益的觀念[17,18]。目前顱腦多發轉移瘤最主要的治療措施之一就是全腦放療,但在采用全腦放療治療腦轉移瘤時,如何照射、用多大劑量照射及照射多長時間是我們臨床上需要解決的主要問題。
綜上所述,替莫唑胺聯合全腦放療,大部分患者耐受性良好,且顱腦相關癥狀得到明顯緩解,替莫唑胺聯合全腦治療有明顯的治療效果。與此同時藥物的不良反應也無明顯增加,可顯著延長患者的生命,提高患者的生存質量,該治療方法值得我們在臨床上廣泛應用,減輕患者及其家屬痛苦。但是本研究的病例數較少,隨訪時間較短,對其遠期療效及不良反應的研究還需要大樣本和長時間的隨訪觀察。
[參考文獻]
[1] 錢桂生.為提高我國呼吸系統疾病的診治水平而努力[J].中華肺部疾病雜志,2012,5(1):1-3.
[2] 錢浩.肺癌綜合治療[M].南京:江蘇科學技術出版社,2008:508-512.
[3] Alberg AJ,Ford JG,Samet JM.Epidemiology of lung cancer:AG-CP evidence-based clinical practice guidelines(2nd edition)[J].Chest,2007,132(Suppl 3):29S-55S.
[4] 張海波.對轉移性肺癌診斷與治療的分析與研究[J].吉林醫學,2011,32(36):7776.
[5] Balana C,Capellades J,Teixidor P,et al.Clinical course of highfrade glioma patients with a “biopsy-only” surgical apporach:A need for individuallysed treatment[J].Clin Transa Oncol,2007,9(12):797-803.
[6] Daviskas E,Anderson SD.Hyperosmolar agents and clearance of mucus in the diseased airway[J].J Aerosol Med,2006,19(1):100-109.
[7] Mandelberg A,Amirav I.Hypertonic Saline or High Volume Normal Saline for Viral Bronchiolitis:Mechanisms and Rationale[J].Pediatric Pulmonology,2010,45(1):36-40.
[8] 卜擎燕,熊寧寧,鄒建東,等.ICH國際醫學用語詞典(MedDRA):藥事管理的標準醫學術語集[J].臨床藥理學,2008,12(5):587-590.
[9] 趙曉輝,賈漪濤,王志敏,等.血管內皮抑素聯合影像引導放療治療非小細胞肺癌腦轉移患者的效果[J].中國腫瘤生物治療雜志,2010,17(6):661-664.
[10] 傅浩,萬林林,楊靈,等.放療聯合口服替莫唑胺治療惡性腦膠質瘤術后患者的臨床療效研究[J].中國全科醫學,2011,13(14):13.
[11] 梁惠,董士麗.國內惡性腦膠質瘤術后放療聯合替莫唑胺化療療效與安全性的Meta分析[J].現代腫瘤醫學,2010,17(12):2345-2348.
[12] Cavahere R,Wen PY,Schiff D.Novel therapies for malignant gliomas[J].Neurol Clin,2007,25(4):1141-1171.
[13] Brandes AA,Basso U,Reni M,et al.First-line chemotherapy with cisplatin plus fractionated temozolomide in recurrent glioblastoma multfforme:A phase 1I study of the Gmppe Italiano Cooperativo di Neuro-Oncologia[J].J Clin Oncol,2004,22(9):1598-1604.
[14] Stupp R ,Gander M ,Leyvraz,et al.Current and future developmengts in the use of temozolomide for thee treatment of brain tumors[J].Lancet Oncol,2001,2(9):552-560.
[15] Wen QL,Meng MB,Yang B,et al.Endostar, a recombined humanized endostatin enhances the radioresponse for human nasopharyngeal carcincma and human lung adenocarcinoma xenogrsfts inmice[J].Cancer Sci,2009,100(8):1510-1519.
[16] Motomura K,Natsume A,Kishida Y,et al.Benefits of interferon-βand temozolomide combination therapy for newly diagnosedprimary glioblastoma with the unmethylated MGMT promoter:A multicenter study[J].Cancer,2011,117(8):1721-1730.
[17] Kawabe T,Phi JH,Yamamoto M,et al.Traetment of brain metastasis from lung cancer[J].Prog Neuro Surg,2012,25:148-155.
[18] Kyritsis AP,Markoula S,Levin VA.A systematic approach to the management of patients with brain metastases of known or unknown primary site[J].Cancer Chemother Pharmacol,2012,69(1):1-13.
(收稿日期:2017-01-07)

