外源糖對鹽脅迫下小黑麥幼苗糖代謝的影響
王麗華,李改玲,李 晶,左師宇,曹鑫波,佟昊陽,魏 湜
(東北農業大學農學院,黑龍江哈爾濱 150030)
外源糖對鹽脅迫下小黑麥幼苗糖代謝的影響
王麗華,李改玲,李 晶,左師宇,曹鑫波,佟昊陽,魏 湜
(東北農業大學農學院,黑龍江哈爾濱 150030)
外源糖可以緩解鹽害,提高植物耐鹽性。為探究外源糖對鹽脅迫下小黑麥幼苗糖代謝的影響及其機理,以小黑麥品種東農8809為材料,通過施加0.5 mmol·L-1葡萄糖和0.5 mmol·L-1蔗糖,探討了100 mmol·L-1NaCl脅迫下外源糖處理的小黑麥幼苗相對電導率、碳水化合物含量和糖代謝關鍵酶活性的變化。結果表明,在鹽脅迫下,與未經外源糖處理(CK)相比,外源葡萄糖、蔗糖預處理的小黑麥幼苗葉片的相對電導率顯著降低,可溶性糖含量及蔗糖合成酶、蔗糖磷酸合成酶、果糖-6-磷酸激酶和己糖激酶活性提高,尤其是己糖激酶活性顯著高于其他處理,丙酮酸激酶活性降低。說明鹽脅迫下,施加外源糖可以促進蔗糖和葡萄糖進入蔗糖合成途徑和糖酵解途徑,促進淀粉向可溶性糖轉化,從而提高可溶性糖含量,降低滲透勢,提高細胞吸水能力,以緩解鹽脅迫對小黑麥的傷害程度。
小黑麥;鹽脅迫;外源糖;糖代謝
土壤鹽漬化的問題在全世界廣泛存在,尤其在干旱和半干旱地區更加嚴重。據不完全統計,全世界鹽堿地面積是9.54億hm2,中國各類鹽堿地面積總計9 913.3萬hm2[1]。土壤鹽漬化問題嚴重制約鹽堿地區植物的生長,是影響作物生長和高產的逆境因子之一[2-3]。小黑麥(TriticosecaleWittmack)是小麥和黑麥遠源雜交并經染色體加倍、人工合成的麥類作物新類型,具有抗逆性強的特點[4],但鹽脅迫對其生長依然會產生影響。
葡萄糖和蔗糖作為可溶性糖,參與植物對生物和非生物脅迫響應中的信號調控[5-6]。鹽脅迫時植物細胞內積累一些可溶性糖等物質,調節細胞內滲透勢,維持水分平衡,因而這些可溶性物質的積累在植物的滲透調節過程中起著重要作用[7-10]。施加一定的外源糖可以緩解鹽害,提高植物幼苗的耐鹽性。外源葡萄糖和蔗糖可顯著提高鹽脅迫下玉米體內可溶性糖的含量,降低細胞滲透勢,減緩鹽脅迫引起的細胞失水[11]。在小麥研究中關于外源糖緩解鹽脅迫傷害的報道較多。蔗糖預處理可以緩解鹽脅迫對小麥根系生長的抑制作用,提高可溶性糖含量[12]。外源海藻糖可明顯緩解鹽脅迫對小麥幼苗生長的抑制作用,提高抗鹽性[13]。一定濃度的外源殼聚糖浸種可促進鹽脅迫下小麥種子萌發和幼苗生長,減緩鹽脅迫傷害[14]。滸苔硫酸多糖(EP)能夠在不同程度上促進小麥的生長和生物量的積累,提高其抗 NaCl 的能力[15]。1 mg·mL-1EP能夠在鹽脅迫條件下提高小麥可溶性蛋白、可溶性糖以及脯氨酸含量,增強其滲透調節能力。而在小黑麥上有關外源糖緩解鹽害的效應目前尚缺乏系統研究。本研究在生理生化水平探索外源糖緩解鹽脅迫下小黑麥糖代謝的作用及其機制,以期為鹽堿地農業生產中作物抗鹽栽培措施提供參考。
1 材料與方法
1.1 試驗材料
供試小黑麥品種為東農8809,由東北農業大學小麥栽培生理研究室提供。
1.2 試驗設計
挑選大小一致、沒有損壞的小黑麥種子,將表面消毒后置于培養箱中,25 ℃黑暗催芽,選取芽長一致的種子于植物生長室內用1/2 Hoagland營養液(pH 5.5)培養至兩葉一心。培養條件:晝夜溫度(25±2) ℃/(20±2) ℃,每天光照12 h,光強為1 000 μmol·m-1·s-1,濕度為60%~80%。取兩葉一心小黑麥幼苗,分別用1/2Hoagland營養液+0.5 mmol·L-1葡萄糖、1/2 Hoagland營養液+0.5 mmol·L-1蔗糖(前期進行濃度篩選試驗,篩選出緩解萌發階段鹽脅迫的最佳糖濃度為0.5 mmol·L-1)、1/2 Hoagland營養液(空白對照)、1/2 Hoagland營養液+0.05 mmol·L-1甘露醇(滲透對照)預處理(浸種)3 d;用100 mmol·L-1NaCl(綜合前人研究[16]并經前期鹽濃度篩選試驗確定)進行鹽脅迫處理6 d,以相應糖處理和空白處理為對照。這樣共形成7個處理:對照(CK)、葡萄糖預處理(G)、蔗糖預處理(T)、鹽處理(S)、葡萄糖預處理后鹽處理(G+S)、蔗糖預處理后鹽處理(T+S)、等濃度的甘露醇預處理后鹽處理(M+S)。每個處理3次重復,每次100粒種子。
1.3 測定項目及方法
1.3.1 相對電導率的測定
相對電導率的測定參照Lutts等[17]的方法并改進。稱取0.3 g葉片,用去離子水洗凈后放入試管中,加10 mL去離子水,25 ℃浸泡12 h,用電導率儀測定各組浸出液電導率A;然后將試管置于沸水中20 min,再冷卻至初始溫度,測電導率B,相對電導率=A/B×100%。
1.3.2 小黑麥葉片中碳水化合物含量的測定
可溶性糖含量參照劉麗杰[18]測定糖含量的方法進行測定,具體內容稍作改進。提取葉片可溶性糖時,葉片不需烘干,直接稱取0.3 g新鮮葉片剪碎進行測定。
淀粉含量參照劉麗杰[18]測定糖含量的方法進行測定,標準曲線繪制見1.3.2.1可溶性糖標準曲線的繪制方法。
1.3.3 糖代謝關鍵酶的測定
糖代謝的5個關鍵酶活性參照李改玲[19]的方法,采用由南京建成生物工程研究所提供配制的試劑盒檢測。
1.4 數據處理
試驗結果用Excel 2007和DPS 7.05統計軟件進行數據處理、分析和繪圖。
2 結果與分析
2.1 外源糖對鹽脅迫下小黑麥幼苗葉片相對電導率的影響
由圖1可以看出,與CK比較,G和T處理的小黑麥葉片相對電導率分別降低了2.34和1.38個百分點。與CK相比,鹽脅迫(S)后,小黑麥葉片相對電導率顯著升高。鹽脅迫下,G+S和T+S處理葉片相對電導率較S處理分別降低了3.83和6.39個百分點,與S處理的差異均達到顯著水平,G+S與T+S處理間也差異顯著;等濃度的甘露醇預處理沒有引起鹽脅迫下小黑麥體內相對電導率明顯下降。說明外源糖預處理能夠維持鹽脅迫下小黑麥葉片細胞膜的穩定性。

G:葡萄糖;T:蔗糖;M:甘露醇。圖柱上的字母不同表示處理間差異顯著。下同。
G:glucose;T:sucrose;M:mannitol.Different letters on the columns indicate the significat differences among the treatments at 0.05 level.The same below.
圖1 葡萄糖和蔗糖預處理對鹽脅迫下小黑麥幼苗葉片相對電導率的影響
Fig.1 Effects of salt stress on relative electrical conductivity in leaves of triticale seedling pretreated with glucose and sucrose
2.2 外源糖對鹽脅迫下小黑麥葉片碳水化合物含量的影響
由表1可知,G、T和S處理的小黑麥葉片可溶性糖含量較CK分別提高了32.87%、33.65%和51.41%,與CK差異均顯著。在鹽脅迫下,G+S和T+S處理較S處理顯著提高了葉片的可溶性糖含量,增幅分別為10.13%和10.87%;而等濃度的甘露醇預處理引起葉片的可溶性糖含量下降。說明在鹽脅迫下,外源葡萄糖和蔗糖預處理能夠促進小黑麥幼苗可溶性糖的積累,有利于降低細胞滲透勢,提高細胞吸水能力。
G和T處理的淀粉含量與CK差異不顯著,但S處理顯著提高了淀粉含量。鹽脅迫下G+S、T+S和M+S處理葉片淀粉含量相比S處理均有所降低,但差異均未達到顯著水平。說明外源糖預處理對鹽脅迫下小黑麥幼苗葉片淀粉含量影響微弱。

表1 外源糖處理后小黑麥幼苗葉片可溶性糖含量和淀粉含量的變化
同列數值后的字母不同表示處理間差異顯著。
Different letters after the values in the same column indicate the significant differences among the treatments at 0.05 level.
2.3 外源糖對鹽脅迫下小黑麥幼苗葉片糖代謝關鍵酶活性的影響
2.3.1 對蔗糖合成酶(SS)活性的影響
與CK相比,G、T和S處理均顯著提高小黑麥葉片的SS活性,其中G、T處理增幅分別為21.74%、43.20%(圖2)。鹽脅迫下,G+S和T+S處理SS活性較S處理分別提高了10.08%和14.07%,其中T+S處理與S處理差異顯著;M+S處理顯著降低了SS活性。
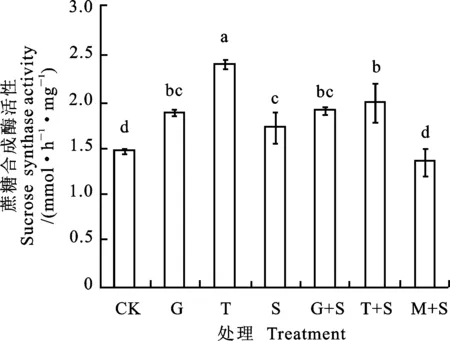
圖2 葡萄糖和蔗糖預處理對鹽脅迫下小黑麥幼苗葉片蔗糖合成酶活性的影響
2.3.2 對蔗糖磷酸合成酶(SPS)活性的影響
與CK相比較,G和T處理均提高了小黑麥葉片SPS活性,S處理顯著降低了SPS活性。鹽脅迫下,G+S和T+S處理均顯著提高了SPS活性,增幅分別為24.09%和20.02%;M+S處理顯著降低SPS活性(圖3)。

圖3 葡萄糖和蔗糖預處理對鹽脅迫下小黑麥幼苗葉片蔗糖磷酸合成酶活性的影響
2.3.3 對丙酮酸激酶(PK)活性的影響
G和T處理的小黑麥葉片PK活性與CK相比沒有顯著差異,S處理顯著升高(圖4)。鹽脅迫下,G+S、T+S和M+S處理的PK活性較S處理均顯著降低,其中S處理的PK活性分別是G+S和T+S處理的1.50倍和1.82倍。
2.3.4 對己糖激酶(HK)活性的影響
與CK相比,G、T和S處理均顯著提高了小黑麥葉片HK活性,其中G和T處理的HK活性分別是CK的2.73倍和3.50倍(圖5)。鹽脅迫下,G+T和T+S處理HK活性較S處理顯著提高,分別是S處理的3.23倍和3.52倍;M+S處理相對于S處理無明顯變化。
2.3.5 對果糖-6-磷酸激酶(PFK)活性的影響
與CK相比,G、T和S處理的小黑麥葉片PFK活性均顯著提高,其中G和T處理分別是CK的1.525倍和1.65倍(圖6)。鹽脅迫下,G+S和T+S處理較S處理均顯著提高PFK活性,但M+S處理顯著降低了PFK活性。
3 討 論
鹽分脅迫對植物的傷害中,最先接觸的是細胞膜。鹽脅迫導致細胞質膜透性增大,且鹽濃度越高,細胞質膜透性越大,相對電導率增大。丁順華研究發現,鹽溶液中加入海藻糖可以使鹽脅迫下小麥幼苗細胞質膜透性顯著降低,表明外源海藻糖可在一定程度上保護細胞質膜的完整性。在本研究中,鹽脅迫下,小黑麥細胞內浸出液相對電導率均顯著升高,而0.5 mmol·L-1葡萄糖和蔗糖浸種均不同程度地降低了鹽脅迫下葉片相對電導率,這與前人研究結果相一致。說明外源糖預處理能夠降低相對電導率,維持鹽脅迫下小黑麥葉片細胞膜的穩定性。

圖4 葡萄糖和蔗糖預處理對鹽脅迫下小黑麥幼苗葉片丙酮酸激酶活性的影響

圖5 葡萄糖和蔗糖預處理對鹽脅迫下小黑麥幼苗葉片己糖激酶活性的影響
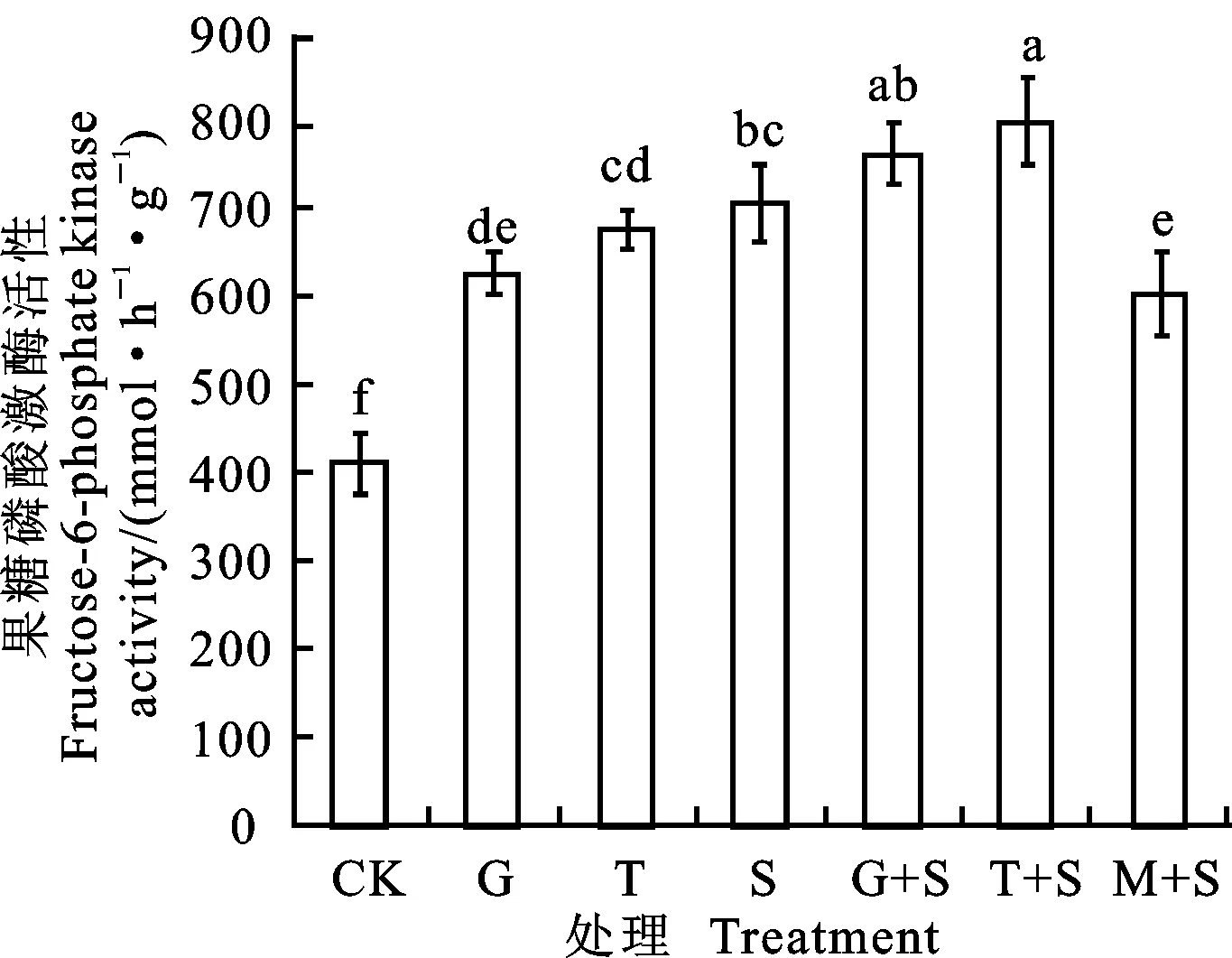
圖6 葡萄糖和蔗糖預處理對鹽脅迫下小黑麥幼苗葉片果糖-6-磷酸激酶活性的影響
糖是光合作用的主要產物之一,其不僅作為代謝物質為植物生長發育提供能量,還是主要的細胞滲透調節劑之一,并作為植物體內的一種信號分子參與調控植物生長發育進程。已有大量報道表明,外源糖類物質及其他一些碳水化合物可以緩解鹽脅迫對植物代謝活動的影響。氨基乙酸甜菜堿可以增加鹽脅迫下水稻幼苗可溶性蛋白的含量,緩解鹽脅迫對光合系統的傷害作用[20];外源海藻糖能夠增強小麥幼苗的耐鹽性,外源葡萄糖和果糖可以提高鹽脅迫下水稻種子發芽率和發芽指數[21]。王康君等研究發現,鹽脅迫下小麥種子萌發期α-淀粉酶活性和可溶性糖含量下降,導致萌發率降低。鹽脅迫可以對枸杞產生水分脅迫和離子傷害,為緩解水分脅迫,枸杞葉片可溶性糖含量有所增加,淀粉含量減少[22]。前人的研究都表明,鹽脅迫下可溶性糖含量上升有利于提高植物的抗鹽性。本研究中不論非鹽脅迫還是鹽脅迫下,與CK相比,外源糖處理的小黑麥葉片可溶性糖含量均升高。說明在鹽脅迫下,外源糖預處理能夠促進小黑麥幼苗可溶性調節物質的積累,降低細胞滲透勢,提高細胞吸水能力,從而緩解滲透脅迫所造成的傷害。本研究也表明,外源糖預處理能夠降低鹽脅迫下小黑麥幼苗葉片中淀粉含量,促進葉片中淀粉向可溶性糖轉化。
鹽脅迫下小麥和大麥生長受抑制,原因在于葉片提前衰老,從而減少了生長部位同化產物的供應。葉片提前衰老則是生理代謝活性降低的結果。Krishnaraj[23]指出,在鹽脅迫下,耐鹽小麥品種比鹽敏感小麥品種的葡萄糖代謝活性高。楊涓對枸杞的研究表明,鹽脅迫會提高SS活性,說明了鹽脅迫影響了糖類物質的運輸[22]。魯少尉等對番茄的研究表明,鹽脅迫下番茄葉片中的蔗糖合成酶和蔗糖磷酸合成酶活性從番茄開花后即開始不斷降低[24]。本研究結果與前人研究相同。丙酮酸激酶、已糖激酶和黑糖-6-磷酸激酶是糖酵解中的三個關鍵酶,它們催化的反應都是不可逆的。己糖激酶催化葡萄糖轉化為6-磷酸葡萄糖,在己糖異構酶的作用下生成6-磷酸果糖,在果糖-6磷酸激酶的作用下磷酸化生成1,6-二磷酸果糖。最后在丙酮酸激酶的作用下磷酸烯醇式丙酮酸生成丙酮酸和1分子ATP。本研究中,在鹽脅迫下,用外源葡萄糖、蔗糖預處理的小黑麥蔗糖合成酶、蔗糖磷酸合成酶活性比較高,促進蔗糖進入各種途徑,催化蔗糖的合成,從而提高可溶性糖含量。果糖-6-磷酸激酶和己糖激酶活性比較高,尤其是己糖激酶活性顯著高于其他處理,丙酮酸激酶活性較低,通過糖酵解途徑,促進葡萄糖的分解,降低滲透勢,提高細胞的吸水能力。綜上所述,施加外源葡萄糖和蔗糖均可以明顯緩解鹽脅迫對小黑麥的傷害程度。
[1] ROLLAND F,BAENA-GONZALEZ E,SHEEN J.Sugar sensing and signaling in plants:conserved and novel mechanisms [J].AnnualReviewofPlantBiology,2006,57:675.
[2] 劉良全,張水利,景小元,等.幾種化學調控物質對鹽脅迫下小麥幼苗生長及生理指標的調控作用[J].麥類作物學報,2010,30(1):73.
LIU L Q,ZHANG S L,JING X Y,etal.Effect of seed soaking with four chemical regulators on root and seedling growth of different wheat genotypes under nacl stresses [J].JournalofTriticeaeCrops,2010,30(1):73.
[3] 丁順華.外源海藻糖對小麥耐鹽性的效應[D].濟南:山東師范大學,2001:3-6.
DING S H.Effect of exogenous trehalose on salt tolerance of wheat [D].Jinan:Shandong Normal University,2001:3-6.
[4]劉 慧,王立群,黃占權.對小黑麥啤酒制麥工藝的探討[J].黑龍江糧油科技,2000,21(1):28.
LIU H,WANG L Q,HUANG Z Q.Discussion of technology of triticale beer [J].HeilongjiangOilTechnology,2000,21(1):28.
[5]KEUNEN E,PESHEV D,VANGRONSVELD J,etal.Plant sugars are crucial players in the oxidative challenge during abiotic stress:extending the traditional concept [J].PlantCellEnvironment,2013,36:1242.
[6]BAENA-GONZALEZ E,SHEEN J.Convergent energy and stress signaling [J].Cell,2008,12(9):1360.
[7]LIU F,JENSEN C R,ANDERSEN M N.A review of drought adaptation in crop plants:changes in vegetative and reproductive physiology induced by ABA-based chemical signals [J].AustralianJournalofAgriculturalResearch,2005,56:1245.
[8]PRAXEDES S C,DA MATTA F M,LOUREIRO M E.Effects of long-term soil drought on photosynthesis and carbonhyd rate in mature robusta coffee(CoffeacanephoraPierrevar.kouillou) leaves [J].EnvironmentalandExperimentalBotany,2006,56:263.
[9] 王玉鳳,王慶祥,商麗威.NaCl和Na2SO4脅迫對玉米幼苗滲透調節物質含量的影響[J].玉米科學,2007,15(5):69.
WANG Y F,WANG Q X,SHANG L W .Effects of NaCl and Na2SO4stress on osmotic adjustment substances in maize seedlings [J].JournalofMaizeSciences,2007,15(5):69.
[10] 阮成江,謝慶良.鹽脅迫下沙棘的滲透調節效應[J].植物資源與環境學報,2002,11(2):45.
RUAN CH J,XIE Q L.Osmotic adjustment effect ofHippophaerhamnoidesL.under salt stress [J].JournalofPlantResourcesandEnvironment,2002,11(2):45.
[11] 趙 瑩.外源糖緩解玉米鹽脅迫生理生化機制研究[D].大慶:黑龍江八一農墾大學,2014:4-5.
ZHAO Y.Effects of exogenous sugar on the attenuation of salt stress and its physiological basis in maize seedling [D].Daqing:Heilongjiang Bayi Agricultural University,2014:4-5.
[12] 閆素芳,于 洋,葛 青,等.外源蔗糖對小麥幼苗耐鹽性的影響[J].中國生態農業學報,2012,20(2):225.
YAN S F,YU Y,GE Q,etal.Effect of exogenous sucrose application on wheat seeding salt tolerance [J].ChineseJournalofEco-Agriculture,2012,20(2):225.
[13] 丁順華,李艷艷,王寶山.外源海藻糖對小麥幼苗耐鹽性的影響[J].西北植物學報,2005,25(3):513.
DING S H,LI Y Y,WANG B S.Effect of exogenous trehalose on salt tolerance of wheat seedling [J].ActaBotanyBoreal-OccidentSinica,2005,25(3):513.
[14] 王玉萍,于丹,李成,等.殼聚糖對鹽脅迫下小麥種子萌發及幼苗生理特性的影響[J].干旱地區農業研究,2016,34(1):180.
WANG Y P,YU D,LI C,etal.Effect of chitosan on seed germination and seedling physiological characters of wheat under salt stress [J].AgriculturalResearchintheAridAreas,2016,34(1):180.
[15] 李 冰.滸苔硫酸多糖對NaCl脅迫下植物的影響[D].北京:中國科學院大學,2013:2-3.
LI B.Effect of sulfated polysaccharides fromEnteromorphaproliferaon plants under NaCl stress [D].Beijing:Chinese Academy of Sciences,2013:2-3.
[16] 郭 偉,于立河.腐殖酸浸種對鹽脅迫下小麥萌發種子及幼苗生理特性的影響[J].麥類作物學報,2012,32(1):90.
GUO W,YU L H.Effect of seed soaking with humic acid on soluble sugar accumulation and allocation in germinated wheat seed under salt stress [J].JournalofTriticeaeCrops,2012,32(1):90.
[17]LUTTS S,KINET J M,BOUHARMONT J.NaCl-induced senescence in leaves of rice (OryzasativaL.)cultivars differing in salinity resistance [J].AnnalsofBotany,1996,78:389.
[18] 劉麗杰.低溫下ABA調控冬小麥糖代謝及抗寒基因表達的研究[D].哈爾濱:東北農業大學博士學位論文,2013:11-14.
LIU L J.Effects of ABA on sugar metabolism and expression of antifreeze genes of winter wheat [D].Harbin:Northeast Agricultural University,2013:11-14.
[19] 李改玲.外源糖調控鹽脅迫下小黑麥糖代謝及光合特性的研究[D].哈爾濱:東北農業大學,2016.
LI G L.Exogenous sugar alleviate effects of salt stress on the triticale’s sugar metabolism and photosynthetic characteristics [D].Harbin:Northeast Agricultural University,2016.
[20]DEMIRAL T,TRKAN I.Exogenous glycinebetaine affects growth and proline accumulation and retards senescence in two rice cultivars under NaCl stress [J].JournalEnvironmentalandExperimentalBotany,2006,56(1):72.
[21] 凌騰芳,宣 偉,樊穎瑞,等.外源葡萄糖、果糖和NO供體(SNP)對鹽脅迫下水稻種子萌發的影響[J].植物生理與分子生物學學報,2005,31(2):205.
LING T F,XUAN W,FAN Y R,etal.Effect of exogenous glucose and fructose and snp on rice seed germination under salt stress [J].JournalofPlantPhysioloryandMolecularBiology,2005,31(2):205.
[22] 楊 涓.鹽脅迫下枸杞糖蛋白及糖代謝變化的研究[D].銀川:寧夏大學,2005:7-11.
YANG J.Researches on cell wall glycoprotiein and sucrose-metabolizing ofLyciumBarbarumL.under salt stress [D].Ningxia:Ningxia University,2005:7-11.
[23]KRISHNARA S,THORPE T A.Salinity stress effects on [14C-1]-and [14C-6]-glucose metabolism of a salt-tolerant and salt-susceptiblevariety of wheat [J].InternationalJournalofPlantScience,1996,157(1):110.
[24] 魯少尉,齊 飛,李天來.NaCl及等滲PEG脅迫對番茄葉片光合特性及蔗糖代謝的影響[J].華北農學報,2012,27(3):136.
LU S W,QI F,LI T L.Effect of NaCl and PEG iso-osmotic stresses on photosynthetic characteristics and sucrose metabolizing in tomato leaf [J].ActaAgriculturaeBoreali-Simica,2012,27(3):136.
Effect of Exogenous Sugar on the Sugar Metabolism in Triticale Seedling under Salt Stress
WANG Lihua,LI Gailing,LI Jing,ZUO Shiyu,CAO Xinbo,TONG Haoyang,WEI Shi
(Agricultural College,Northeast Agricultural University,Harbin,Helongjiang 150030,China)
Salt stress destroys the integrity of cells and inhibits the growth of plants. Exogenous sugar can alleviate salt stress and improve salt tolerance in plants. In order to know the effects and antimicrobial properties of exogenous sugar on sugar metabolism in triticale seedling under 100 mmol·L-1NaCl,Dongnong 8809 was used as experimental material and treated with 0.5 mmol·L-1glucose and 0.5 mmol·L-1sucrose. The relative electrical conductivity,carbohydrate content and activities of key enzymes in glycometabolism were studied,and the impact of exogenous sugar on triticale under salt stress was analyzed. The results showed that under salt stress,exogenous glucose and sucrose pretreatment can significantly reduce relative electrical conductivity,improve the content of soluble sugar and the activities of key enzymes,including sucrose synthase,sucrose phosphate synthase,fructose-6-diphosphate kinase and hexokinase,in glycometabolism especially the activity of hexokinase exceeds others significantly. So that exogenous sugar can promote glucose and sucrose to go into the sugar metabolic pathways,promote the transformation of starch to soluble sugar,improve the content of soluble sugar,reduce osmotic potential,and improve the water absorbing capacity. Thus,exogenous sugar can acleviate the injury of salt stress to triticale.
Triticale; Salt stress; Exogenous sugar; Glycometabolism
時間:2017-04-07
2016-10-01
2016-11-28 基金項目:國家科技支撐計劃項目(2012BAD14B06) 第一作者E-mail:wanglihua81494@163.com 通訊作者:魏 湜(E-mail:weishi5608@163.com)
S512.4;S311
A
1009-1041(2017)04-0548-06
網絡出版地址:http://kns.cnki.net/kcms/detail/61.1359.S.20170407.1021.034.html

