胰島素抵抗與尿毒癥患者心血管疾病的相關性分析
繆旭+莫冬梅+劉付敬樟
[摘要]目的 研究胰島素抵抗與尿毒癥患者心血管疾病的關系。方法 選取我院2014年8月~2016年8月接收的60例尿毒癥患者作為尿毒癥組,選取同期的45例健康體檢者作為對照組。比較兩組的胰島素抵抗指數(HOMA-IR)以及腎功能指標、心臟功能指標、炎癥因子及氧化應激指標水平,分析HOMA-IR與各指標的相關性。結果 尿毒癥組的HOMA-IR低于對照組,差異有統計學意義(P<0.05)。HOMA-IR與LVEF、S成正相關(r=0.507、0.618,P<0.05),與LVESD、TC、TG、LDL-C成負相關(r=-0.386、-0.458、-0.797、-0.683,P<0.05)。尿毒癥組的炎癥因子及氧化應激指標水平高于對照組,差異有統計學意義(P<0.05)。HOMA-IR與MDA、T-AOC、SOD、AOPP、hs-CRP、IL-6、IL-8、TNF-α水平成負相關(r=-0.783、-0.317、-0.896、-0.453、-0.367、-0.474、-0.526、-0.602,P<0.05)。結論 尿毒癥患者心血管疾病的發生與胰島素抵抗存在密切關系,對評估患者病情及預后有一定的臨床價值。
[關鍵詞]胰島素抵抗;尿毒癥;心血管疾病;相關性
[中圖分類號] R722.1 [文獻標識碼] A [文章編號] 1674-4721(2017)03(a)-0079-03
[Abstract]Objective To study the relationship between insulin resistance (IR) and cardiovascular disease in patients with uremia.Methods 60 uremic patients in our hospital from August 2014 to August 2016 were selected as the uremia group,and the same period of the same period,45 healthy persons were selected as the control group.The level of HOMA-IR,renal function,cardiac function,inflammatory factors and oxidative stress were compared,and the correlation between HOMA-IR and each index was analyzed.Results The level of HOMA-IR in the uremia group was lower than that in the control group,with significant difference (P<0.05).HOMA-IR was positively correlated with LVEF and S (r=0.507,0.618,P<0.05),and was negatively correlated with LVESD,TC,TG,LDL-C (r=-0.386,-0.458,-0.797,-0.683,P<0.05).Inflammatory factors and oxidative stress in the uremia group was higher than that in the control group,with significant difference (P<0.05).HOMA-IR was negatively correlated with the levels of MDA,T-AOC,SOD,AOPP,hs-CRP,IL-6,IL-8,TNF-α(r=-0.783,-0.317,-0.896,-0.453,-0.367,-0.474,-0.526,-0.602,P<0.05).Conclusion There is a close correlation between the occurrence of cardiovascular disease and IR in patients with uremia,and it has a certain clinical value to assess the patient′s condition and prognosis.
[Key words]Insulin resistance;Uremia;Cardiovascular disease;Correlation
尿毒癥(慢性腎功能衰竭終末期)是腎內科常見疾病之一,流行病學調查顯示,在我國每年進行血液透析治療的患者中,尿毒癥約占278人次/100萬,而有44.0%~51.0%的尿毒癥患者合并心血管疾病[1-2],這是其死亡的主要原因。有研究顯示,心血管疾病與胰島素抵抗引起的糖脂代謝紊亂、血管內皮細胞損傷有關[3],但是關于尿毒癥患心血管并發癥的發生是否有關鮮有報道。本研究選取我院接收的慢性腎功能衰竭(尿毒癥期)患者及45例健康體檢者作為研究對象,對此進行初步探討,現報道如下。
1資料與方法
1.1一般資料
選取我院2014年8月~2016年8月接收的60例慢性腎功能衰竭(尿毒癥期)患者為尿毒癥組,其中男性44例,女性16例;年齡37~66歲,平均(45.38±5.96)歲;吸煙史26例,飲酒史11例。均符合《腎臟病學》制訂的診斷標準,年齡≥18歲,知情同意,均同意配合此次研究,排除繼發性腎病、藥物相關性腎病患者,排除合并腎結石、輸尿管結石、腎動脈狹窄、腎囊腫患者。
選取同期的45例健康體檢者作為對照組,其中男性33例,女性12例;年齡35~69歲,平均(45.82±5.96)歲;吸煙史21例,飲酒史8例。所有入選者均知情同意,經心電圖、腎常規等檢查排除心肺疾病及腎臟疾病。兩組的一般資料比較,差異無統計學意義(P>0.05),具有可比性。
1.2方法
所有研究對象入組后,于清晨采取空腹肘靜脈血5 ml,分置于A、B兩管。A管加入乙二胺四乙酸鈉(EDTA-Na)抗凝,離心(3000 r/min,10 min),取血漿。采用日本日立醫療器械有限公司生產的7600-110分析儀,應用葡萄糖氧化酶法測定空腹血糖(FBG)、空腹胰島素(FINS),胰島素抵抗指數(HOMA-IR)=FINS×FBG/22.5。B管凝血60 min(20~25℃)后,離心(3000 r/min,10 min),取血清,采用普朗醫療器械公司的PUZS-300全自動生化分析儀檢測血肌酐(SCr)、尿素氮(BUN)及總膽固醇(TC)、三酰甘油(TG)、低密度脂蛋白(LDL-C);血清丙二醛(MDA)、總抗氧化能力(T-AOC)、超氧化物歧化酶(SOD)及晚期蛋白氧化產物(AOPP)、白細胞介素6(IL-6)、白細胞介素8(IL-8)、腫瘤壞死因子-α(TNF-α)、C反應蛋白(CRP),MDA測定采用硫代巴比妥酸比色法,T-AOC測定采用比色法,SOD測定采用羥胺測定法,AOPP、hs-CRP、IL-6、IL-8、TNF-α采用酶聯免疫吸附法。采用Philips Ie33型超聲診斷儀及配套探頭,觀察左室射血分數(LVEF)、左室收縮末期內徑(LVESD)及二尖瓣環收縮期速度(S)。
1.3統計學處理
采用SPSS 20.0統計學軟件對數據進行分析,計量資料以均數±標準差(x±s)表示,采用t檢驗,計數資料以百分數表示,采用χ2檢驗,胰島素抵抗與心功能指標的相關性采用Spearman相關系數分析,以P<0.05為差異有統計學意義。
2結果
2.1兩組HOMA-IR與心功能指標、腎功能指標的相關性分析
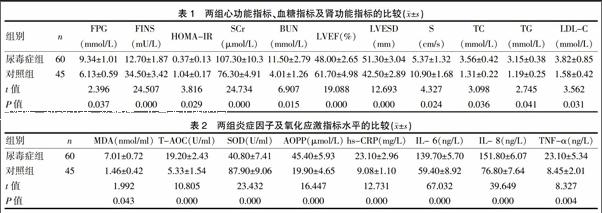
尿毒癥組的FINS 、HOMA-IR、LVEF、S水平低于對照組,FPG、SCr、BUN、LVESD、TC、TG、LDL-C水平高于對照組,差異有統計學意義(P<0.05)(表1)。HOMA-IR與LVEF、S成正相關(r=0.507、0.618,P<0.05),與LVESD、TC、TG、LDL-C成負相關(r=-0.386、-0.458、-0.797、-0.683,P<0.05)。
2.2兩組HOMA-IR與炎癥因子及氧化應激指標水平的相關性分析
尿毒癥組的MDA、T-AOC、SOD、AOPP、hs-CRP、IL-6、IL-8、TNF-α水平高于對照組,差異有統計學意義(P<0.05)(表2)。HOMA-IR與MDA、T-AOC、SOD、AOPP、hs-CRP、IL-6、IL-8、TNF-α成負相關(r=-0.783、-0.317、-0.896、-0.453、-0.367、-0.474、-0.526、-0.602,P<0.05)。
3討論
連續性血液凈化治療是尿毒癥患者常用的治療手段之一,且取得了較好的治療效果,但是文獻報道,部分尿毒癥患者會出現心血管系統、血管徑路等并發癥[4],影響治療效果,給患者的身體、心理、經濟等造成重大損失,同時,高達60%的尿毒癥患者因心血管疾病出現死亡。目前,臨床上對尿毒癥出現心血管疾病的相關因素進行了研究,針對存在高危因素的人群加強其監測,對于出現心血管疾病的尿毒癥患者,根據誘發因素給予干預措施,這對改善患者預后具有積極作用。
胰島素抵抗,即胰島素反應性降低,研究表顯示,胰島素抵抗存在是心血管疾病發生的危險因素之一[5]。對尿毒癥患者心血管疾病發病機制的研究顯示,糖脂代謝紊亂在其發生中發揮重要作用,但是胰島素抵抗與其關系鮮有報道。本研究中,尿毒癥合并心血管疾病組的HOMA-IR顯著低于單純尿毒癥組及健康體檢者(P<0.05),提示尿毒癥合并心血管疾病患者存在胰島素抵抗。此外,HOMA-IR與LVEF、S成正相關(r=0.507、0.618,P<0.05),與LVESD成負相關(P<0.05),提示胰島素抵抗與尿毒癥患者心血管疾病發生密切相關。進一步分析其原因,血液黏稠度增加是心血管疾病發病的高危因素,血液黏稠度增加可導致血流動力學減慢,心肌缺血缺氧,進而引起心肌細胞死亡,同時,血脂水平升高可導致動脈粥樣硬化,而動脈粥樣硬化是導致心血管疾病發生的病理基礎[6-8],HOMA-IR與TC、TG、LDL-C成負相關(P<0.05),提示胰島素抵抗存在會導致血糖水平升高以及TC、TG、LDL-C水平升高,使得體內糖脂代謝紊亂,進而誘發心血管疾病發生。
慢性腎功能衰竭患者在高尿酸狀態下,產生了過多的維持氧化與抗氧化系統平衡的氧自由基(超氧陰離子自由基、羥基自由基等),使得腎臟組織正常的氧化/還原反應的動態平衡被破壞,進而誘發腎臟組織產生大量的細胞因子及生長因子,促進了尿毒癥的發生與發展,因此,氧化應激反應被臨床工作者認為是尿毒癥的重要發病機制之一[9-10]。目前,臨床上常用的氧化應激指標有MDA、SOD、AOPP、T-AOC,其中MDA是膜脂過氧化的終產物之一,其水平能夠反映機體細胞的損傷程度,SOD的活力反映了機體清除氧自由基的能力,各種蛋白質氧化的終末產物總稱為AOPP,其最主要的作用是介導炎癥因子釋放,導致蛋白質氧化損傷,而T-AOC代表機體對氧自由基的酶性及非酶性清除能力總和。本研究結果顯示,HOMA-IR與氧化應激指標水平成負相關(P<0.05),且尿毒癥合并心血管疾病組患者的炎癥因子及氧化應激指標水平顯著高于單純尿毒癥組(P<0.05),提示胰島素抵抗存在,其導致的氧化應激反應可能是誘發心血管疾病發生的另一個重要原因。
動脈粥樣硬化在一定程度上也是慢性免疫炎癥過程,研究顯示,胰島素抵抗存在會誘發炎癥反應,釋放炎癥因子,如IL-6、IL-8、TNF-α、hs-CRP等[11-15]。炎癥因子在機體細胞免疫中發揮重要作用,其中hs-CRP多由機體中白細胞介素與TNF-α等炎癥因子刺激肝臟細胞而合成,是至今研究最為廣泛的急性期反應物,可在應激或炎癥反應下短期上升,促進白細胞釋放超氧化物歧化酶和蛋白水解酶引起組織損傷;TNF-α和IL-6、IL-8在許多系統中具有協同作用,能夠激活血管內皮細胞、增加內皮細胞黏附分子表達以及刺激中性粒細胞產生炎性介質使中性粒細胞在細胞內集聚,是反應過敏性相關疾病發生及評估炎癥疾病進展狀況的重要指標。本研究中,HOMA-IR與炎癥因子水平成負相關(P<0.05),提示胰島素抵抗狀態的存在會導致尿毒癥患者體內炎癥因子的釋放,而炎癥因子大量釋放會造成心肌損傷,心血管形成血栓,導致心血管疾病發生。
綜上所述,尿毒癥患者心血管疾病的發生與胰島素抵抗存在密切關系,這對評估患者病情及預后有一定的臨床價值。
[參考文獻]
[1]譚永順,王敏,倪曉娜,等.血液透析聯合灌流對尿毒癥患者同型半胱氨酸和頸動脈內膜的影響[J].中國臨床保健雜志,2016,19(1):66-69.
[2]趙璐杰,李超林,邱君,等.左卡尼汀聯合血液透析治療尿毒癥性周圍神經病變的臨床療效觀察[J].中國血液凈化,2013,12(7):371-374.
[3]楊偉.老年2型糖尿病患者體質量指數與胰島素抵抗及脂質代謝異常的相關性研究[J].中華實用診斷與治療雜志,2010,24(4):414-415.
[4]湯利華,袁忠明.老年糖尿病胰島素抵抗與心血管內分泌激素的相關性[J].中國老年學雜志,2014,34(13):3561-3562.
[5]張明華,葉平,駱雷鳴,等.口服葡萄糖耐量試驗正常北京社區人群血糖、胰島素水平及胰島素抵抗指數與心血管危險因素的相關性研究[J].現代預防醫學,2015,42(9):1624-1627,1635.
[6]鄭亮,吳宏,錢定廣,等.上海市高行老年社區人群動脈硬化性心血管疾病患病率的現況調查與危險因素分析[J].中國循證心血管醫學雜志,2016,8(6):680-682,690.
[7]李蕓.腹膜透析患者胰島素抵抗、代謝紊亂的預后及干預的前瞻性研究[D].上海:復旦大學,2010.
[8]翟玫,翟穎,孟紅,等.非糖尿病冠心病患者糖化血紅蛋白與血脂相關性分析[J].中國分子心臟病學雜志,2016,16(3):1692-1694.
[9]楊沿浪.蕪湖市健康體檢人群慢性腎臟病流行病學調查及其相關危險因素分析[D].廣州:南方醫科大學,2014.
[10]曾薇,齊偉,羅志鋒,等.內質網應激在尿毒癥血清致內皮細胞功能異常中的作用[J].解放軍醫學雜志,2011,36(2):133-136.
[11]曾海鷗,陳圳煒,羅敏虹,等.透析方式對非糖尿病終末期腎臟病患者臨床指標及胰島素抵抗影響的比較[J].中國血液凈化,2016,15(4):219-225.
[12]蘇凱杰,唐子勇.慢性腎病患者的胰島素抵抗與心血管并發癥[J].醫學研究生學報,2016,28(6):653-657.
[13]陳丹燕.尿毒癥血液透析患者Treg/Th17細胞功能平衡失調對心血管并發癥的影響[D].重慶:重慶醫科大學,2012.
[14]李新,姜黎,楊杪,等.CTRP3下調炎癥因子表達改善胰島素抵抗的3T3-L1脂肪細胞胰島素敏感性[J].中國病理生理雜志,2014,30(10):1833-1838.
[15]蒲素,余葉蓉,陸志明.炎癥因子對胰島素抵抗動物模型血管內皮細胞功能影響的研究[J].四川大學學報(醫學版),2010,41(3):398-402.
(收稿日期:2017-01-06 本文編輯:祁海文)

