由醫療器械國際標準化特點試論中醫醫療器械國際標準化發展
徐曉婷 張海明
(1 上海市中醫藥研究院中醫藥國際標準化研究所,上海,201203; 2 天津市醫療器械質量監督檢驗中心,天津,300384)
規范與標準
由醫療器械國際標準化特點試論中醫醫療器械國際標準化發展
徐曉婷1張海明2
(1 上海市中醫藥研究院中醫藥國際標準化研究所,上海,201203; 2 天津市醫療器械質量監督檢驗中心,天津,300384)
從ISO/IEC中與醫療器械相關技術委員會內各成員國參與度、交叉領域發展現狀、標準體系完善情況以及國際標準與各國法律法規相適配等方面入手,總結分析和比較當前中醫醫療器械國際標準化現狀并對其發展提出建議:注重人才培養,鼓勵企業積極參與;關注市場需求,考慮與各國法律法規相適配;加強與有關組織之間的溝通與協調,協同發展;完善中醫醫療器械標準化體系。
醫療器械;中醫醫療器械;標準化
醫療器械的國際標準化工作長期以來一直依托于國際電工組織(International Electrotechnical Commission,IEC)和國際標準化組織(International Organization for Standardization,ISO)這兩大國際標準化權威組織中的技術委員會(TC)及其分技術委員會(SC)開展。醫療器械[1],是指直接或者間接用于人體的儀器、設備、器具、體外診斷試劑及校準物、材料以及其他類似或者相關的物品,包括所需要的計算機軟件;其效用主要通過物理等方式獲得,不是通過藥理學、免疫學或者代謝的方式獲得,或者雖然有這些方式參與但是只起輔助作用;其目的是:1)疾病的診斷、預防、監護、治療或者緩解;2)損傷的診斷、監護、治療、緩解或者功能補償;3)生理結構或者生理過程的檢驗、替代、調節或者支持;4)生命的支持或者維持;5)妊娠控制;6)通過對來自人體的樣本進行檢查,為醫療或者診斷目的提供信息。
中醫醫療器械則是指在診療活動中,在中醫理論指導下應用的醫療器械。2009年國際標準化組織/中醫藥技術委員會(ISO/TC249)成立后,中醫醫療器械的國際標準化工作就主要依托ISO/TC249開展[2]。
ISO/TC249秘書處設在中國[3-4],其工作范疇為所有起源于古代中醫并能共享同一套標準的傳統醫學體系標準化領域的工作,涵蓋傳統與現代繼承發展的兩大領域,具體負責中藥原材料質量與安全、中藥制成品質量與安全、醫療設備質量與安全及信息等領域的標準化工作,也包括服務類標準,但僅限于設備和藥品的安全使用及傳遞,不涉及臨床或者產品的操作。該委員會現有個7工作組,其中涉及中醫醫療器械的工作組有3個,分別為第三工作組(WG3針灸針的質量與針灸安全使用)、第四工作組(WG4除針灸針以外的醫療器械的質量與安全)及與IEC/SC62D聯合的工作組(JWG6有源醫療設備)。截止至2017年3月,ISO/TC249已發布中醫藥國際標準14項,正在制作中的項目44項,其中與中醫醫療器械相關的項目占42%。然而隨著中醫醫療器械國際標準化工作向縱深進行,也逐漸面臨著一些問題。本文從現代醫學體系的醫療器械國際標準化發展的一些特點入手,分析和比較當前中醫醫療器械國際標準化現狀并對其發展提出相關建議。
1 醫療器械標準化特點及中醫醫療器械標準化對應情況
1.1 資源優勢國家占主導地位 由于近代以來我國醫療器械發展長期落后于歐美國家[5-6]且標準化工作起步較晚[7],因此醫療器械的國際標準化工作長期由歐美發達國家主導,這從承擔ISO/IEC中各醫療器械相關TC的秘書處情況可見一二。由表1可見,在ISO中除中醫藥外其他與醫療器械相關的17個TC中,德國和美國各承擔6個TC的秘書處,瑞典承擔2個TC的秘書處,丹麥、加拿大和馬來西亞各承擔1個TC的秘書處。在IEC中與醫療器械相關的4個TC中,英國承擔2個TC的秘書處,德國和美國各承擔1個TC的秘書處[8]。因ISO/TC249是國際標準化組織的中醫藥技術委員會,其業務范圍涵蓋中醫醫療器械,所以由中國承擔ISO/IEC的秘書處中目前只有ISO/TC249與醫療器械相關。
在具體參與國際標準化方面,由于我國醫療器械產業技術實力較發達國家仍存在較大差距,企業規模大多有限,缺乏參與或主導國際標準制修訂的動力和經費。因此在大多數TC中我國專家占全體專家的比例很小,以IEC/TC62為例[9]有1 280名專家,中國專家共48名,占比僅為3.8%。在國際標準提案國家方面,大部分國際標準提案均由歐美發達國家主導,除ISO/TC249外各醫療器械相關TC中由中國專家提案的醫療器械國際標準可謂鳳毛麟角。中國專家參與國際標準化的形式大多只體現在參與標準討論,獲取標準信息等方面。
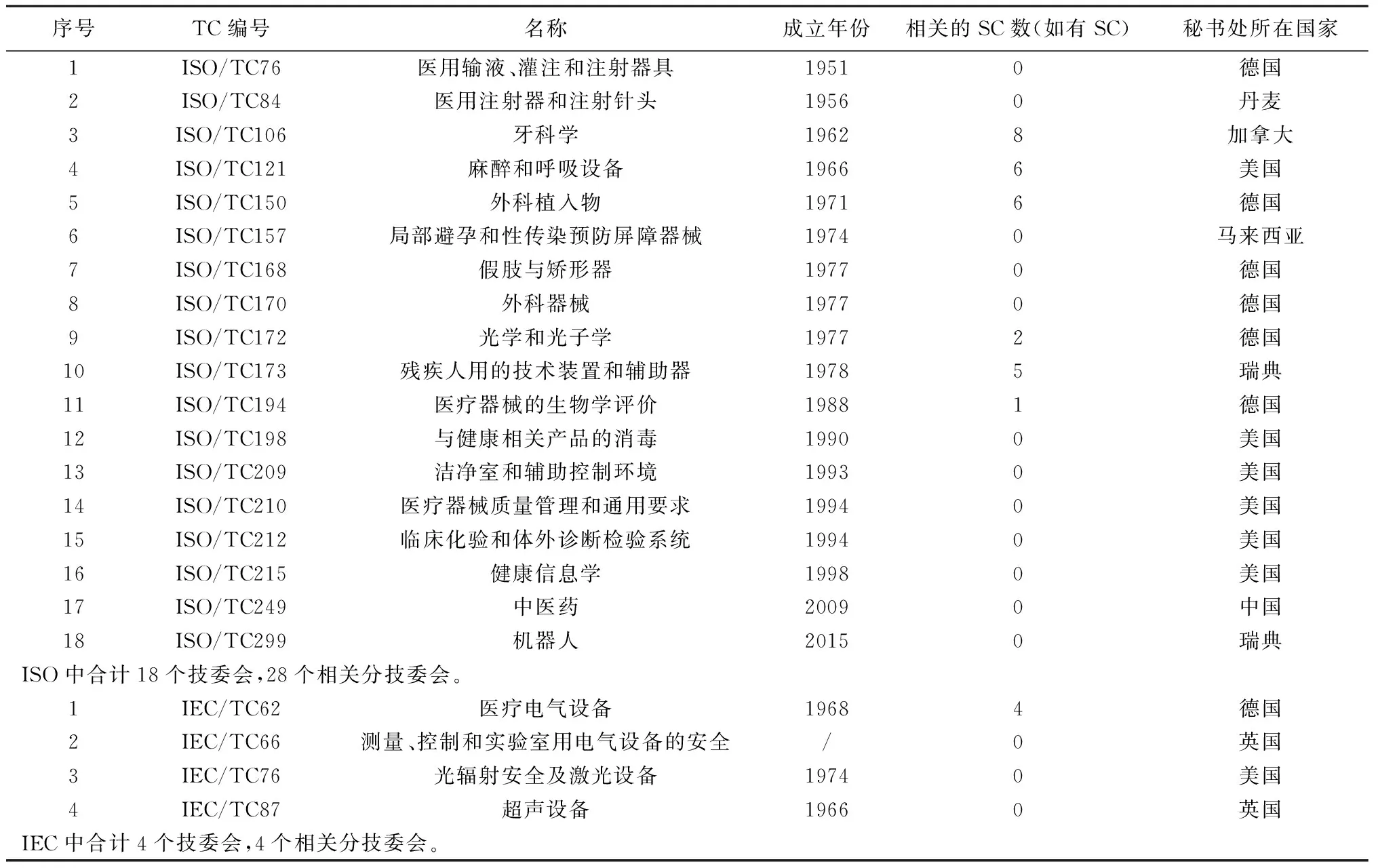
表1 ISO/IEC中醫療器械相關TC情況
由于中醫藥是我國為數不多具有原創優勢的科技領域,ISO/TC249工作范圍內的醫療器械為中醫醫療器械,而中醫醫療器械的主要設計、生產、銷售及應用國家為中國,因此ISO/TC249里的醫療器械工作組里中國專家占主導地位,中國提案占比也達到50%以上。美國、德國等歐美發達國家雖然也參與到ISO/TC249的工作中,但并未如在其他TC中一樣表現出搶占主導權的積極性,主要是在中醫醫療器械領域西方發達國家無論在產品研發、制造和市場占有方面都不具有優勢。
1.2 各領域交叉發展,協同合作已成趨勢 隨著醫療器械在各個領域的迅速發展,尤其是在交叉領域取得了突飛猛進的發展[10],眾多跨專業跨學科的技術不斷涌現,因此各個醫療器械TC之間往往存在一些工作范圍的交叉。由于IEC/TC62醫療電氣設備的工作范圍包含所有有源醫療器械,而其他醫療器械TC也有很多有源產品,因此在產品特性上存在著交叉;而ISO/TC210醫療器械質量管理和通用要求和ISO/TC215健康信息學的工作范圍包含術語、質量管理等基礎性要求,也與一些醫療器械相關TC間存在交叉。根據ISO/IEC導則,存在領域交叉的TC可以選擇5種不同的工作模式建立聯系,而5種模式中聯系最為緊密的形式即為雙方成立聯合工作組(JWG)。由表2可見IEC/TC62與其他醫療器械TC或SC共成立了27個聯合工作組。而ISO/TC210及ISO/TC215與其他TC及SC的聯系也是通過與IEC/TC62建立聯系而間接達成的。因此從發展規律上看,醫療器械的TC或SC幾乎都會與IEC/TC62、ISO/TC210及ISO/TC215這3個TC建立某種程度的聯系。而這種聯系可能是以成立聯合工作組或者聯絡組織的形式存在,且隨著工作的推進和市場需求的轉變而不斷產生變化。
目前ISO/TC249已與IEC/SC62D及ISO/TC215建立了聯系,并分別成立了聯合工作組。由于當前ISO/TC249中的標準多為產品標準,較少系統的考慮質量體系管理及風險控制等要求,隨著以后ISO/TC249中醫醫療器械標準的豐富,未來也有可能與ISO/TC210的工作范圍產生交叉。
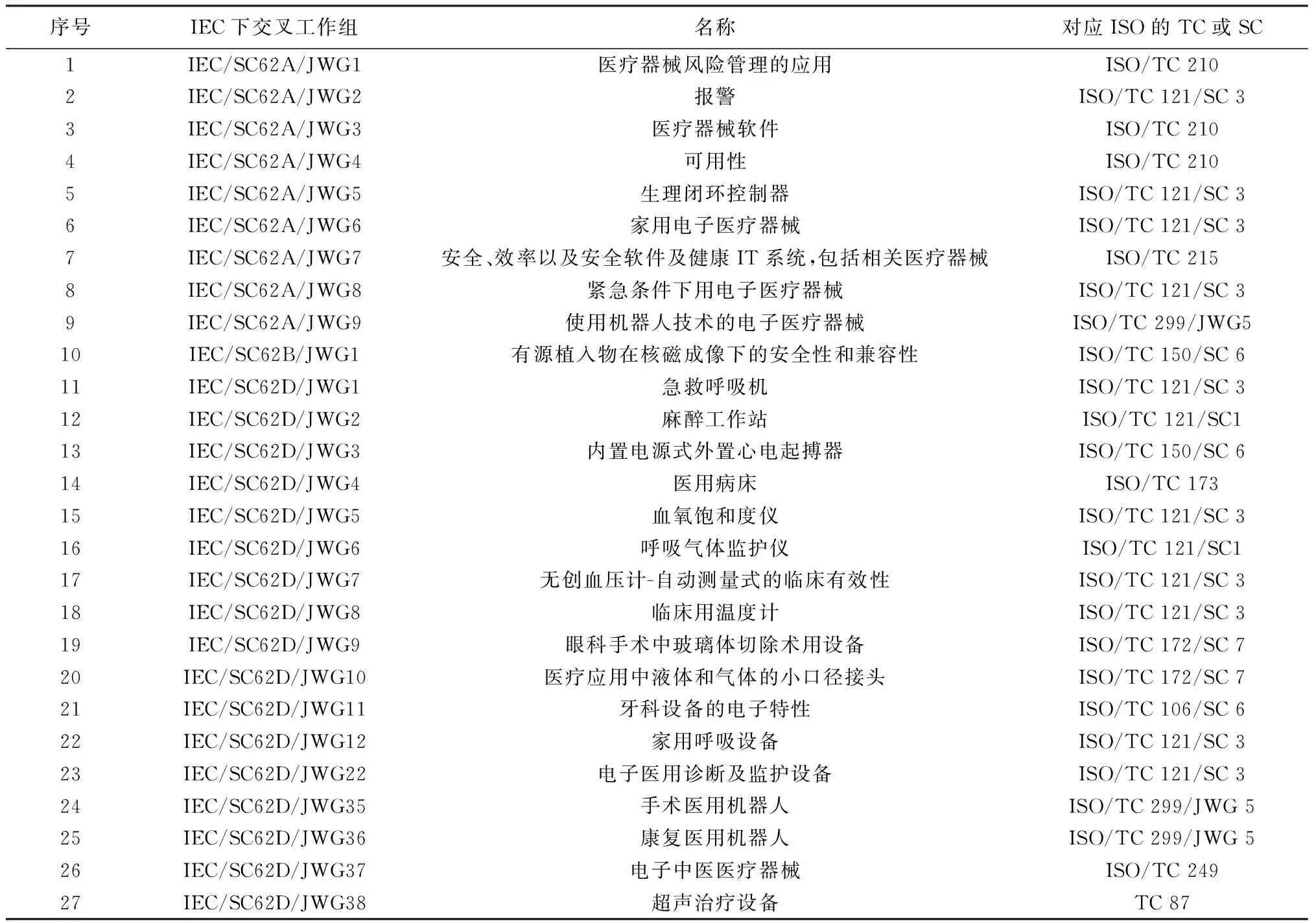
表2 IEC/TC62中的聯合工作組

表3 基礎標準、類標準、流程標準及產品標準
1.3 標準體系豐富 ISO和IEC的醫療器械標準體系構架全面完整,邏輯框架清晰嚴謹。在整體框架內,以安全和基本性能標準覆蓋醫療器械全領域,保障上市的醫療器械產品符合監管法規的要求。ISO 16142-1:2016中對這些重要標準和指南進行了分類,包括:基礎標準、類標準、過程標準及產品標準[12]。見表3。在醫療器械各TC內,根據自身技術特點及產品的性能要求,制定覆蓋產品生命周期各階段的標準,整個生命周期貫穿了風險控制的理念。而在ISO/TC249內的醫療器械標準,目前主要為產品標準,通過引用IEC 60601-1[13]等標準構成完整的標準體系。
1.4 專家構成多元化 ISO和IEC中各TC的專家是由成員國中相應領域的專家自愿報名產生的。醫療器械TC中的專家多來自于醫療器械制造及貿易商、臨床使用機構、教學和科研機構以及監管認證機構等。由于醫療器械更多地涉及到制造和貿易,因此各醫療器械相關TC中來自于制造和貿易領域的專家最多[14]。以ISO/TC150為例[15],來自制造和貿易領域的專家占總數的百分比達到70%(見圖1、圖2)。
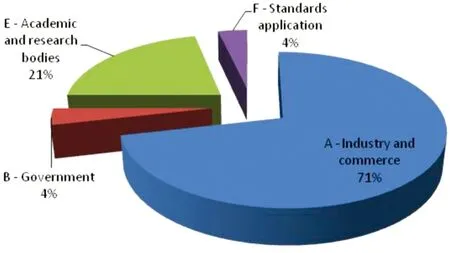
圖1 ISO/TC150/SC2/WG3中各領域專家占比情況
而ISO/TC249中大部分專家卻來自于科研機構,以ISO/TC249/JWG6為例,76名專家中有44名來自于科研機構,比例高達57.9%。這既說明中醫醫療器械的制造企業對國際標準化意識不強,同時也顯示出市場的占有率有限,特別是國際市場。
1.5 標準與各國法律法規相適配 在WTO/TBT協定中明確將“標準”定義為“非強制執行的文件”,世界上主要發達國家的標準也都是非強制執行的文件。也就是說,就國際標準本身而言,一般都不具備“強制執行”的屬性;當然,若有關法律法規規定應執行標準,這時標準因被引用而間接地“強制執行”了。
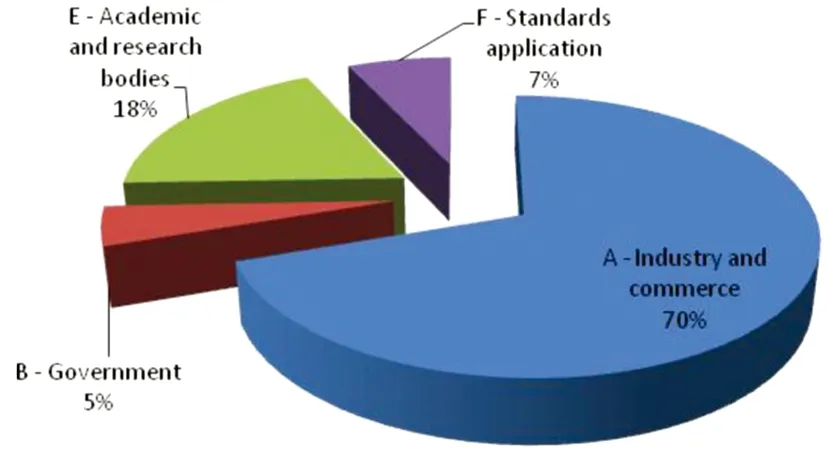
圖2 ISO/TC150/SC4/WG1中各領域專家占比情況
由于醫療器械產品與人體健康息息相關,因此在大部分國家均對醫療器械產品制訂了相應的法律法規進行重點管理。如歐美統一市場針對有源植入醫療器械的指令90/385/EEC、針對動物源醫療器械指令2003/32/EC;美國21 CFR part8xx系列法規條例;中國的醫療器械監督管理條例等。這些法律法規在相應范圍內具有強制性。而這些法律法規中的一些技術內容往往與國際標準內容有所交叉,這就必然存在國際標準與相應法律法規相適配的情況。因為即使制訂了醫療器械國際標準,但該國的法律法規不予采納,實際上國際標準仍然未能產生對相關領域應有的影響。因為如果醫療器械產品不符合國際標準但符合本國的法律法規仍是可以在該國進行生產經營活動的,只是由于產品與國際標準不符,可能影響其銷量。
從1992年以來,醫療器械標準與各國監管機構法律法規的適配問題借助GHTF(The Global Harmonization Task Force全球協調工作組)平臺開展,在2011年后GHTF又進一步演變為IMDRF(International Medical Device Regulators Forum,國際醫療器械監管者論壇)。各國針對醫療器械國際標準在各國與法律法規的適配情況進行了統計和協調,然而目前在對詳細醫療器械國際標準的轉化統計中未見中醫醫療器械標準的統計情況[16]。
2 對中醫醫療器械國際標準化工作的建議
2.1 注重人才培養,鼓勵企業積極參與 標準化有助于規范市場行為,引領經濟社會發展,促進相關產品在技術上的相互協調和配合。“一流的企業做標準”,誰掌握標準制定的主導權,誰就對市場占有了一定的話語權,只有企業代表參與標準制作才能更好地體現產業以及企業的利益,促進產業和經濟發展。而標準化工作有利于穩定和提高產品和服務的質量,促進企業走質量效益型發展道路,提高企業競爭力。以首項發布的中醫醫療器械國際標準《ISO 17218:2014一次性使用無菌針灸針》為例,主導該標準的企業自國際標準發布后出口貿易同比增加30%。
歐美發達國家在ISO/IEC相關醫療器械TC中占據主導地位,其對市場就有著極大的影響力。以ISO/TC150/SC2/WG3的注冊專家為例,在人造血管領域美國戈爾(Gore)、德國蛇牌(Aesculap)以及德國百多力(Biotronik)市場份額達60%以上,而在WG3的專家中,有20人來自于產業,其中有6人來自于這3家公司,占產業專家參與數的30%。與此相反的是,中醫醫療器械國際標準化的參與專家多以科研機構專家居多,產業代表屈指可數。因此,中醫醫療器械產業如要快速發展,必須鼓勵企業積極參與國際標準化工作,并注重國際標準化人才的培養,以標準帶動企業發展。
2.2 關注市場需求,考慮與各國法律法規相適配 按照功能劃分,中醫醫療器械大致可分為治療性設備和診斷性設備。在ISO/TC 249制作的國際標準中,大部分為治療性設備,如針灸針、拔罐器具、艾灸器具、中藥煎煮設備等都具有廣泛的海外市場應用基礎。而診斷性設備,如現代科技指導下研發的四診儀等設備,因海外市場需求有限,多用于科研教學。然而隨著中醫藥在海外的廣泛傳播及使用,為了確保中醫醫療器械的安全使用以及便于當地政府對有關器械的質量把控和合理監管,中醫醫療器械國際標準制作的需求也越來越迫切。因此,中醫醫療器械的發展也應該與時俱進,根據實際市場需求制定各級各類標準,把控風險,提高醫療質量。
同時,因醫療器械與人身健康息息相關,為了切實發揮標準作用促進國際貿易,在制定國際標準時也應注意盡量避免與各國法律法規之間產生沖突,影響標準采標及使用。隨著ISO/TC249發布中醫醫療器械國際標準數逐漸增多,為了保證標準在各個國家的有效實施,建議進一步關注IMDRF并借助有關平臺進一步解決所發布的中醫醫療器械國際標準與各國法律法規相適配的問題。
2.3 加強與有關組織之間的溝通與協調,協同發展 為了合理利用專家資源,提高效率,中醫醫療器械國際標準的制作應借鑒歐美發達國家制作標準的豐富經驗,建議ISO/TC249與ISO/IEC有關TC以及其他相關組織進行溝通與協調,定期交流信息分享經驗,協同發展中醫醫療器械國際標準。
2.4 完善中醫醫療器械標準化體系 ISO/TC249目前正在制作的中醫醫療器械標準以產品標準為主,聚焦產品質量與安全,特別是電子器械的安全與基本性能,服務標準作為新興領域也正在積極拓展中。但隨著對中醫醫療器械產品認識的進一步深入,建議制定基礎標準或類標準以進一步完善標準化體系,體現中醫醫療器械特點。
中醫醫療器械的國際標準化是整個中醫藥國際標準化的重要組成部分,加強中醫醫療器械的國際標準化工作將為推進中醫藥國際標準化和中醫藥國際化戰略起到十分重要的作用。
[1]中華人民共和國國務院.醫療器械監督管理條例(國務院令第650號)[Z].北京,2015.
[2]中國標準化(英文版)編輯部.制定中醫藥國際標準捍衛人類健康專訪ISO/TC 249秘書長:沈遠東(英文)[J].中國標準化(英文版),2015,73(4):35-39.
[3]包文虎,王璐,李靜,等.我國參與ISO中醫藥國際標準化水平評價初探[J].世界中醫藥,2015,10(5):788-792.
[4]上海中醫藥大學附屬曙光醫院.中醫藥國際標準化的探索者與組織者——ISO/TC249工作介紹[J].上海中醫藥雜志,2015,49(6):封二.
[5]李燕靜.淺析我國醫療器械行業發展狀況及其建議[J].中國外資(上半月),2013,9(4):44.
[6]張志軍.影響我國醫療器械行業競爭力制約因素及相應對策探討[J].中國醫療器械雜志,2012,36(4):293-295.
[7]薛松,姚麗平,王國華,等.醫療器械行業現狀分析[J].中國處方藥,2013,11(6):25-26.
[8]肖憶梅,歐陽昭連,李軍.醫療器械國際標準體系現狀與借鑒[J].中國醫藥導刊,2016,18(3):316-317.
[9]國際電工委員會(IEC).IEC/TC62情況[EB/OL].http://www.iec.ch/dyn/www/f?p=103:173:3563108721689::::FSP_ORG_ID,FSP_LANG_ID:1245,25.2017-03-29.
[10]林立明.淺析我國醫療器械行業發展現狀及發展趨勢[J].科技創新導報,2016,13(21):107-108.
[11]魏學敏.醫療器械風險管理及法規要求[J].大家健康(下旬版),2016,6(2):279-279.
[12]國際標準化組織(ISO).ISO 16142-1:2016 Medical devices——Recognized essential principles of safety and performance of medical devices——Part 1:General essential principles and additional specific essential principles for all non-IVD medical devices and guidance on the selection of standards.2016-03.
[13]國際電工委員會(IEC).IEC 60601-1-2012 Medical electrical equipment-Part 1:General requirements for basic safety and essential performance.2012-08.
[14]劉毅,李悅菱,廖曉曼,等.ISO與國內醫療器械標準化機構設置比較研究[J].首都醫藥,2013,20(16):8-10,11.
[15]國際標準化組織.ISO/TC150介紹.https://www.iso.org/committee/53058.html.2017-03-29.
[16]國際醫療器械監管者論壇.醫療器械國際標準在各成員國的轉化統計情況[EB/OL].http://www.imdrf.org/docs/imdrf/final/procedural/imdrf-proc-151002-medical-electrical-n36.pdf.2015-10-02.
(2017-03-25收稿 責任編輯:王明)
Analysis the development on international standardization of TCM medical devices from the characteristics of international standardization of medical devices
Xu Xiaoting1,Zhang Haiming2
(1InstituteofTCMInternationalStandardization,ShanghaiUniversityofTCM,Shanghai201203,China; 2TianjinMedicalDeviceQualitySupervisionandTestingCenter,Tianjin300384,China)
From the participation of member bodies in different technical committees of ISO/IEC, development on overlapping areas of medical devices, standardization system and adaption between international standards and national regulations, this article is to analyze and conclude the development situation on international standardization of TCM medical devices and put forward the following suggestions: strengthening on talents education and training, encouraging participation from TCM medical devices enterprises, focusing on market demands, taking the adaption between the international standards and national regulations into consideration and strengthening the communication and cooperation between different organizations to improve the standard system of TCM medical devices.
Medical device; TCM medical device; Standardization
上海市中醫藥事業發展三年行動計劃(編號:ZY3-GJHZ-1-1001)——中醫藥國際標準化建設
徐曉婷(1981.11—),女,碩士,中級經濟師,標準化工程師,研究方向:中醫藥國際標準化,Email:xuxiaoting@hotmail.com
R194.2;R2
A
10.3969/j.issn.1673-7202.2017.05.056

