自體外周血造血干細胞移植治療多發性骨髓瘤的效果分析
曾艷+王勁
[摘要]目的 探討自體外周血造血干細胞移植(APBSCT)治療多發性骨髓瘤(MM)患者的效果。方法 回顧性分析2008年2月~2016年12月在我院治療并行APBSCT的MM患者20例,通過化療聯合重組人粒細胞集落刺激因子(G-CSF)動員外周血造血干細胞,以口服馬法蘭等預處理后行APBSCT治療并評估其療效。結果 20例患者移植成功,無移植相關死亡;隨訪移植后3個月患者療效明顯優于移植前,差異有統計學意義(P<0.05)。結論 MM患者行APBSCT安全有效,移植后可明顯提高療效,對于改善MM患者預后具有重要意義。
[關鍵詞]多發性骨髓瘤;自體外周血造血干細胞移植;療效
[中圖分類號] R733 [文獻標識碼] A [文章編號] 1674-4721(2017)04(b)-090-04
Therapeutic effect of autologous hematopotietic stem cell transplantation for multiple myeloma
ZENG Yan WANG Jing▲
Department of Hematology,Institute of Field Surgery,Daping Hospital,the Third Military Medical Unversity,Chongqing 400042,China
[Abstract]Objective To investigate the clinical effect of autologous hematopotietic stem cell transplantation (APBSCT) for patients with multiple myeloma (MM).Methods 20 cases of MM in our hospital from February 2008 to December 2016 were given the chemotherapy combined with granulocyte colony stimulating factor (G-CSF) for mobilizing autologous hematopotietic stem cells.APBSCT was performed after pretreatment of oral melphalan,and the effect were evaluated.Results 20 cases were succeeded in transplantation and there was no transplantation-related death.Therapeutic effect of patients after APBSCT was obviously better than that before transplantation (P<0.05).Conclusion APBSCT is a safe and efficient therapy for patients with MM,and has the important significance to improving therapeutic effects and prognosis of patients with MM.
[Key words]Multiple myeloma;Autologous hematopotietic stem cell transplantation;Efficiency
多發性骨髓瘤(multiple myeloma,MM)是一種血液系統惡性腫瘤,骨髓中漿細胞異常增生導致血或尿中出現單克隆免疫球蛋白,其典型臨床表現有骨痛、貧血、腎功損害及感染等,目前病因不明,尚屬于不可治愈性疾病。其治療方案為化療,但傳統化療完全緩解率低,生存時間短,大劑量化療會導致骨髓抑制嚴重,治療相關死亡率高。有研究表明[1],大劑量化療后聯合自體造血干細胞移植可提高患者完全緩解率和生存時間。現對近年來我院血液科接受自體外周血造血干細胞移植(auto peripheral blood stem cell transplantation,APBSCT)的20例MM患者臨床資料、療效等進行分析,旨在探討APBSCT對改善MM患者預后的意義,為臨床診治提供幫助。
1資料與方法
1.1一般資料
選擇2008年2月~2016年12月在我院治療并行APBSCT的MM患者共20例(其中6例患者行2次APBSCT),所有患者均符合《血液病診斷及治療標準》[2]中的MM診斷標準,排除其同期行聯合化療但未行APBSCT的MM患者。在APBSCT前均告知患者及其家屬移植過程中可能存在的相關風險并符合醫學倫理要求,經患者及家屬同意并簽署移植知情同意書后行APBSCT。20例患者中男性13例(65%),女性7例(35%),男∶女為1.86∶1;發病中位年齡49歲,發病高峰年齡為48~52歲(共7例);臨床免疫分型:IgG型12例,IgA型5例,λ輕鏈型2例,不分泌型1例;Durie-Salmon臨床分期:Ⅰ期3例,Ⅱ期10例,Ⅲ期7例;ISS臨床分期:Ⅰ期4例,Ⅱ期8例,Ⅲ期8例。
1.2方法
1.2.1移植前化療方案 20例患者中有1例為原發耐藥患者,1例為復發后行APBSCT治療,其余患者均為誘導治療緩解后行APBSCT。移植前所有患者接受中位數4(3~13)個療程化療,4例患者接受硼替佐米為主方案化療,包括,①VD方案:硼替佐米(規格:1 mg國藥準字J20140065;規格:3.5 mg,國藥準字J20120055;廠家:西安楊森制藥有限公司;用法:1.3 mg/m2第1、4、8、11天)、地塞米松(40 mg/d靜脈滴注4 d);②PAD方案:硼替佐米、吡柔吡星[廠家:深圳萬樂藥業有限公司,規格:20 mg,國藥準字H10930106,10 mg/(m2·d)靜脈滴注4 d]、地塞米松;③VTD方案:硼替佐米、沙利度胺(每晚1次,50~200 mg/次)、地塞米松。16例患者接受非硼替佐米為主方案化療,包括,①VAD方案:長春新堿(規格:1 mg,國藥準字H44021772;廠家:深圳萬樂藥業有限公司;用法:0.4 mg/d或長春瑞濱1 ml∶10 mg,國藥準字H19990278;廠家:江蘇豪森藥業股份有限公司;用法10 mg/d靜脈滴注4 d)、吡柔比星[10 mg/(m2·d)靜脈滴注4 d]、地塞米松(40 mg/d靜脈滴注4 d);②VADC方案:長春新堿或長春瑞濱、吡柔比星、地塞米松、環磷酰胺(規格:0.2 g,國藥準字H32020857,廠家:江蘇恒瑞醫藥股份有限公司,用法:200 mg/d靜脈滴注4 d);③VADE方案:長春新堿或長春瑞濱、吡柔比星、地塞米松、依托泊苷(規格:0.1 g,國藥準字:H11021801,廠家:江蘇恒瑞醫藥股份有限公司;用法:100 mg/d靜脈滴注4 d)。所有患者同時間斷服用沙利度胺治療。
1.2.2自體外周血干細胞動員方案 20例患者均采用化療聯合重組人粒細胞集落刺激因子(G-CSF)動員自體造血干細胞,具體方案:長春新堿0.4 mg/d,第1~4天;環磷酰胺2~4 g/(m2·d)×2 d;依托泊苷100 mg/d×3 d;米托蒽醌6 mg/(m2·d)×3 d;化療后白細胞降至最低時開始皮下注射G-CSF,5 μg/(m2·d),持續5 d左右,若外周血白細胞>4×109/L、血小板>50×109/L,開始用血細胞分離機采集APBSC,持續2~3 d,每天采集1次。
1.2.3移植預處理方案 18例患者采用單用馬法蘭(200 mg/m2)進行預處理,2例患者采用馬法蘭聯合硼替佐米(馬法蘭200 mg/m2;硼替佐米1.3 mg/m2,移植前6 d(-6 d)、-3 d。其中6例行兩次自體干細胞移植患者,1例患者第1次采用馬法蘭200 mg/m2,第2次采用馬法蘭180 mg/m2聯合硼替佐米1.3 mg/m2(-6、-3 d),其余5例患者2次均采用馬法蘭預處理,200 mg/m2。
1.2.4移植后治療 患者移植后18例患者每2~3個月來院繼續鞏固化療,其中2例患者采用硼替佐米+馬法蘭+地塞米松方案,6例患者采用沙利度胺維持治療,其余10例患者采用非硼替佐米為主方案維持治療(具體方案同于移植前化療方案)。
1.3療效評價
本組MM患者在APBSCT前后療效評價均采用2012年NCCN指南[3],分為完全緩解(CR)、接近完全緩解(nCR)、良好部分緩解(VGPR)、部分緩解(PR)、無變化(NC)、進展(PD)、平臺期和CR后復發。
1.4生存分析
所有患者均通過電話隨訪至2016年12月。總生存時間(OS)定義為患者確診為MM至患者死亡或隨訪終止的時間。無進展生存時間(PFS)定義為患者自接受治療至疾病進展、復發或死亡的時間。
1.5統計學方法
采用SPSS17.0統計學軟件進行數據分析,非正態分布計量資料以中位數(范圍)表示;組間療效比較采用Fisher確切概率法檢驗;生存曲線采用壽命表法繪制;以P<0.05為差異有統計學意義。
2結果
2.1回輸外周血干細胞數
患者動員后均采集足夠的造血干細胞,采集的CD34+細胞中位數為2.56(1.38~9.27)×106/kg;采集的單個核細胞(MNC)中位數為4.12(2.3~18.6)×108/kg。
2.2造血重建時間
患者行APBSCT后中性粒細胞恢復至大于0.5×109/L的中位時間為11(6~18)d;血小板恢復至大于20×109/L的中位時間為14(9~22)d。
2.3療效評價
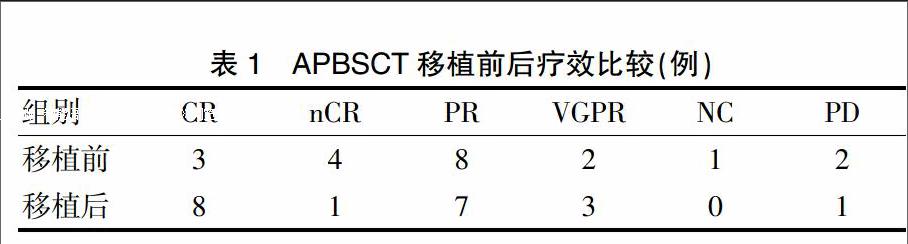
所有患者移植后造血功能均順利重建,無移植相關死亡。移植前患者總反應率(CR+nCR+PR+VGPR)為85%,其中CR率為15%,CR+nCR率為35%、VGPR+PR率為50%;移植后3個月患者總反應率為95%,其中CR率為40%,CR+nCR率為45%、VGPR+PR率為50%,移植后3個月患者的療效較移植前差異有統計學意義(P<0.05),見表1。
表1 APBSCT移植前后療效比較(例)
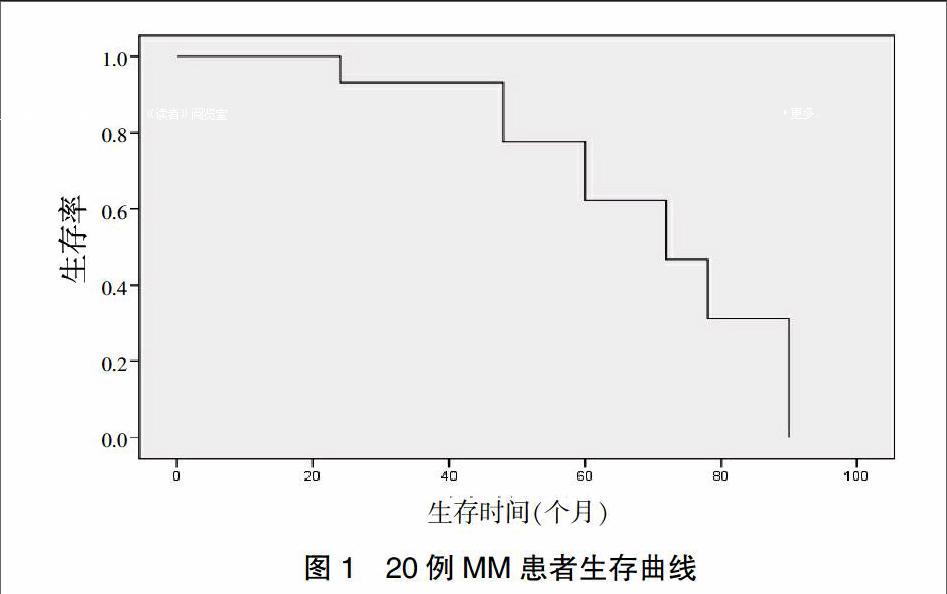
2.4生存分析
隨訪至2016年12月,20例患者中死亡6例,20例患者生存時間11~84個月,3年總生存率為93.0%,5年生存率為62.1%,中位無進展生存(PFS)時間27個月,3年PFS率為51.5%。生存曲線見圖1。
3討論
MM約占血液系統惡性疾病的10%,屬于血液系統第二大腫瘤[4-5]。目前仍屬于不可治愈性疾病,絕大部分患者面臨疾病復發、進展,難以長期生存,異基因造血干細胞移植雖具有治愈的潛能,但其移植相關并發癥、死亡率高,其治療方案仍以化療為主,但傳統化療患者生存時間短,預后差。近年來隨著大劑量化療聯合自體造血干細胞移植以及新型靶向藥物(如硼替佐米、沙利度胺及來那度胺等)的臨床應用,使其治療方面取得了顯著進展,大大改善了患者緩解深度并延長生存時間,甚至部分年輕患者可獲得“臨床治愈”[6-8]。為了獲得更好的治療反應,自體造血干細胞移植支持下的大劑量化療以及與新型靶向藥物的聯合使用成為了目前臨床研究熱點[9-10]。
在蛋白酶體抑制劑以及免疫調節劑用于治療MM患者之前,傳統誘導化療CR率在10%左右,大劑量化療后以自體造血干細胞為支持大大提高了患者的CR率和改善其生活質量[11-13]。美國國立綜合癌癥網絡(NNCN)指南推薦65歲以下的MM患者化療后聯合APBSCT為標準一線治療方案[3]。本次研究顯示,絕大部分MM患者對誘導化療比較敏感,移植后總有效率為95%,CR率為40%,說明APBSCT可以進一步提高患者的緩解率,但是本研究中移植后MM患者總CR率較某些文獻報道低[14],這可能與本研究樣本量較少以及誘導化療期間較少患者使用硼替佐米為主方案有關。
硼替佐米為一種新型蛋白酶體抑制劑,國內外研究表明其對于初治或復發難治MM患者均可取得較為滿意的臨床療效,故NNCN指南推薦以硼替佐米為主的化療方案可作為初治MM患者及復發難治患者的一線選擇。本研究有4例患者誘導化療接受硼替佐米為主方案,其中2例移植前達到CR,移植后3例達到CR,4例均長期無病生存。Zhang等[15]研究5例行APBSCT的MM患者,在移植前、移植后、預處理以及移植后維持治療均使用硼替佐米,所有患者造血重建順利,無移植相關死亡,隨訪至報道時仍處于無病生存狀態。說明硼替佐米為主方案聯合自體造血干細胞移植治療MM有效,且移植后繼續硼替佐米維持鞏固治療可顯著延長患者無病生存期,提高生活質量[16]。
即使大劑量化療后行APBSCT也很難將絕大部分患者PFS延長至3年以上,因此移植后維持治療具有重要意義,它可以延長患者生存時間,改善生活質量[17]。一項Meta分析顯示[18],APBSCT后應用沙利度胺可改善患者PFS,降低疾病進展率和死亡率。本研究中,18例患者在移植后1個月來院維持治療,8例患者單用沙利度胺維持治療,10例患者采用聯合化療,只有1例患者半年內復發,其余患者移植后1年內病情穩定。有學者報道[19],移植后持續使用硼替佐米、沙利度胺、來那度胺等藥物鞏固治療,對于MM患者是一個很好的治療手段,尤其對于復發難治性患者,可以提高治療反應率。
對于二次自體造血干細胞移植是否用于鞏固治療,尤其是對于初次移植后獲得高質量緩解的患者是否能從二次移植中獲益,目前仍存在爭議。多項研究顯示[20-21],MM患者行2次APBSCT較單次行APBSCT可獲得更好的預后,提示二次移植療效優于單次移植,尤其是對于初次移植未達到CR的患者可能會獲益于二次移植。本研究中6例患者行二次自體移植,移植前為PR狀態,一次移植后仍為PR,二次移植后均達到CR或VGPR,說明二次移植比一次移植可取得更好的療效,但因病例數較少,還需進一步觀察遠期療效。
綜上所述,APBSCT可在誘導化療基礎上進一步提高患者CR率,風險小,移植相關死亡率低,可進一步改善MM患者療效及生活質量,是治療MM患者安全有效的方法[22]。
[參考文獻]
[1]Blade J,Rosifiol L,Cibeira MT,et al.Hematopoietic stem cell transplantation for multiple myeloma beyond 2010[J].Blood,2010,115(18):3655-3663.
[2]張之南,沈悌.血液病診斷及療效標準[M].3版.北京:科學出版社,2007:232-235.
[3]Anderson KC,Alsina M,Bensinger W,et al.Multiple myeloma Clinical practice guidelines in oncology[J].J Natl compr Canc Netw,2011,9(10):1146-1183.
[4]Kyle RA,Rajkumar SV.Multiple myeloma[J].N Engl J Med,2004,351(18):1860-1873.
[5]Siegel RL,Miller KD,Jemal A.Cancer statistics[J].CA Cancer J Clin,2015,65(1):5-29.
[6]Martinez-Lopez J,Blade J,Mateos MV,et al.Long-term prognostic significance of response in multiple myeloma after stem cell transplantion[J].Blood,2011,118(3):529-534.
[7]Brenner H,Gondos A,Pulte D.Recent major improvement in long-term survival of younger patients with multiple myeloma[J].Blood,2008,111(5):2521-2526.
[8]Pulte D,Redaniel MT,Brenner H,et al.Recent improvement in survival of patients with multiple myeloma: variation by ethnicity[J].Leuk Lymph,2014,55(5):1083-1089.
[9]邱錄貴,安剛.多發性骨髓瘤的現狀與展望[J].中華血液學雜志,2011,32(10):649-651.
[10]Barlogie B,Mitchell A,van Rhee F,et al.Curing myeloma at last:defining criteria and providing the evidence[J].Blood,2014,124(20):3043-3051.
[11]Hahn T,Wingard JR,Anderson KC,et al.The role of cytotoxic therapy with hematopoietic stem cell transplantation in the therapy of multiple myeloma:an evidence-based review[J].Biol Blood Marrow Transplant,2003,9(1):4-37.
[12]Artinez-Lopez J,Blade J,Mateos MV,et al.Long-term prognostic significance of response in multiple myeloma after stem cell transplantation[J].Blood,2011,118(3):529-534.
[13]Cook G,Ashcroft AJ,Cairns DA,et al.The efect of salvage autologous stem-cell transplantation on overall survival in patients with relapsed multiple myeloma (final results from BSBMT/UKMF Myeloma X Relapse [Intensive]): a randomised,open-label,phase 3 trial[J].Lancet Haematol,2016,3(7):e340-e351.
[14]汪娟,傅琤琤,吳德沛,等.自體造血干細胞移植治療多發性骨髓瘤的回顧性療效分析[J].中華醫學雜志,2013, 93(2):114-118.
[15]Zhang Q,Bat H,Wang CB,et al.Bortezomib combined withautologousperipheral blood hematopoietic stem celltransplantation for therapy of patients with multiple myeloma[J].Zhongguo Shi Yan Xue Ye Xue Za Zhi,2011,19(5):1234-1236.
[16]Sonneveld P,Goldschmidt H,Rosinol L,et al.Bortezomib-based versus nonbortezomib-based induction treatment before autologous stem-cell transplantation in patients with previously untreated multiple myeloma:a meta-analysis of phase Ⅲ randomized,controlled trials[J].J Clin Oncol,2013,31(26):3279-3287.
[17]Cornell RF,D'Souza A,Kassim AA,et al.Maintenance versus induction therapy choice on outcomes after autologous transplantation for multiple myeloma[J].Biol Blood Marrow Transplant,2017,23(2): 269-277.
[18]Hahnast C,Von Lilienfeldtoal M,Van HP,et al.Improved progression-free survival and overall survival with thalidomide maintenance therapy in multiple myeloma:a meta-analyis of randomized trials in 2274 patients[J].Haematol Hematology J,2010,95(3):391.
[19]Blade J,Cibeira MT,Fernandez DC,et al.Multiple myeloma[J].Ann Oncol,2010,21 Suppl 7:S313-S319.
[20]Schmidt-Hieber M,Blau IW,Trenschel R,et al.Reduced-toxicity conditioning with fludarabine and treosulfan prior to allogeneic stem cell transplantation in multiple myeloma[J].Bone Marrow Transplant,2007,39(7):389-396.
[21]Barlogie B,Attal M,Crowley J,et al.Long-term follow-up of autotransplantation trials for multiple myeloma:update of protocols conducted by the Intergroupe Francophone du Myelome,Southwest Oncology Group and the University of Arkansas for Medical Sciences[J].J Clin Oncol,2010,28(7):1209-1214.
[22]Cohen YC,Zuckerman T,Yeshurun M,et al.Efficacy and safety of autologous hematopoietic cell transplantation in elderly patients with multiple myeloma:a retrospective national multi-site cohort study[J].Ann Hematol 2017,96(2):271-278.
(收稿日期:2017-02-10 本文編輯:任 念)

