創傷后應激障礙生物學基礎及治療研究進展
李碩碩,劉謙東,袁增強
(1.中國科學院大學生物物理研究所腦與認知國家重點實驗室,北京 100101;2.山東省日照市人民醫院急診科,山東日照 276800;3.軍事醫學研究院軍事認知與腦科學研究所,北京 100850)
創傷后應激障礙(post-traumatic stress disorder,PTSD)是指在經歷重大創傷事件如戰爭、重大災害(地震、交通事故等)或性侵害之后所表現出的慢性精神疾病。PTSD的癥狀包括噩夢、失眠、閃回,以及對創傷事件相關人物、場所和情景的逃避,過度警覺及負向認知情緒變化。2014年,世界精神衛生調查顯示,12個月內全球PTSD患病率平均為1.1%,但實際終身患病率遠高于此。PTSD可發生于任何年齡段,癥狀出現一般在經歷事件后3個月內,但也有延遲數年出現〔精神疾病診斷與統計手冊第5版(Diagnostic and Statistical Manual of Mental Disorders Fifth Edition,DSM5)中將延遲發生(delay onset)改為延遲出現(delay expression)〕,癥狀典型符合診斷標準。PTSD的主要癥狀可能會隨時間發生變化,生活壓力或新的外傷刺激都會對PTSD癥狀的重現及強度產生影響。老年個體健康水平、認知功能的下降和社會孤立會加重PTSD癥狀[1]。
在諸多PTSD風險因素中,性別、環境和基因因素對PTSD的發生發展影響較大。根據2004年世界衛生組織調查報告,PTSD女性終身患病率(9.7%)明顯高于男性(3.6%),這可能與女性受到性侵害和暴力的概率顯著高于男性相關。2016年,美國一項對于患有PTSD士兵的研究表明,PTSD癥狀表現具有性別差異[2]。環境因素中,戰爭和自然災害是導致PTSD患病率顯著升高的2種誘因。1988年,對美國越戰退伍軍人的調查表明,在1200例退伍老兵中,預計PTSD終身患病率為30.9%,正在經受PTSD折磨的有15.2%。2006年,美國的另一項研究對此數據重新分析指出,PTSD終身患病率為18.7%,在戰后11~12年中有9.1%老兵患有PTSD[3]。2008年汶川地震的發生導致該地區PTSD高發,震后1年,青少年PTSD發病率為19.2%,18個月依然高達7.5%[4],遠高于正常人群。基因突變會使PTSD患病風險增加,目前已報道C反應蛋白(C-reactive protein,CRP)和編碼FK506結合蛋白5(FK506 binding protein 5,FKBP5)的單核苷酸多態性與PTSD癥狀顯著相關[5-6]。另外,研究表明藥物濫用和酗酒常與PTSD共發[7]。從生理層面到精神層面,從分子到大腦,多種因素與PTSD的發病密切相關,多種發病因素為進一步認識PTSD提供了更多線索,也為PTSD的治療帶來巨大挑戰。本文對PTSD患者中的內分泌紊亂、免疫失調和神經環路基礎改變進行詳細闡述,同時對臨床治療及在研新藥作簡要概述,為進一步揭示PTSD的病理機制及治療提供理論依據。
1 創傷后應激障礙的病理基礎
1.1 下丘腦-垂體-腎上腺(hypothalamic-pituitaryadrenal,HPA)軸紊亂
HPA軸是人體主要的內分泌調節系統,在壓力應激、能量代謝、免疫反應中都發揮重要作用。在正常應激反應中,下丘腦感受到外界刺激活動增強,分泌促腎上腺皮質激素釋放因子(corticotrophin releasing factor,CRF)刺激腺垂體分泌更多的促腎上腺皮質激素(adrenocorticotropic hormone,ACTH)調控腎上腺等靶器官,從而使腎上腺分泌的皮質醇和腎上腺激素等壓力激素水平增加。壓力激素可負反饋調控HPA軸活動。ACTH和皮質醇都能通過負反饋調節抑制下丘腦和腺垂體活動,避免產生過多的壓力激素。PTSD患者HPA軸紊亂,表現為過多的CRF和低水平的皮質醇(圖1)。皮質醇是調節應激反應的重要物質,在應激條件下對多個組織或器官發揮調節作用,從而增強機體對外界刺激的抵抗力和適應能力。臨床研究發現,PTSD患者體內CRF水平增高,但皮質醇水平下降,表明PTSD患者HPA軸調控的神經內分泌網絡紊亂。皮質醇水平的降低會引起中樞神經系統的應激失調,導致CRF及腎上腺素通路持續激活,從而產生PTSD關鍵癥狀,如易激惹、過度的恐懼反應、對恐怖事件相關情景事物過度敏感和閃回等。低水平皮質醇能使交感神經活動增加,促進學習,使得PTSD患者對創傷事件的記憶增強[8]。
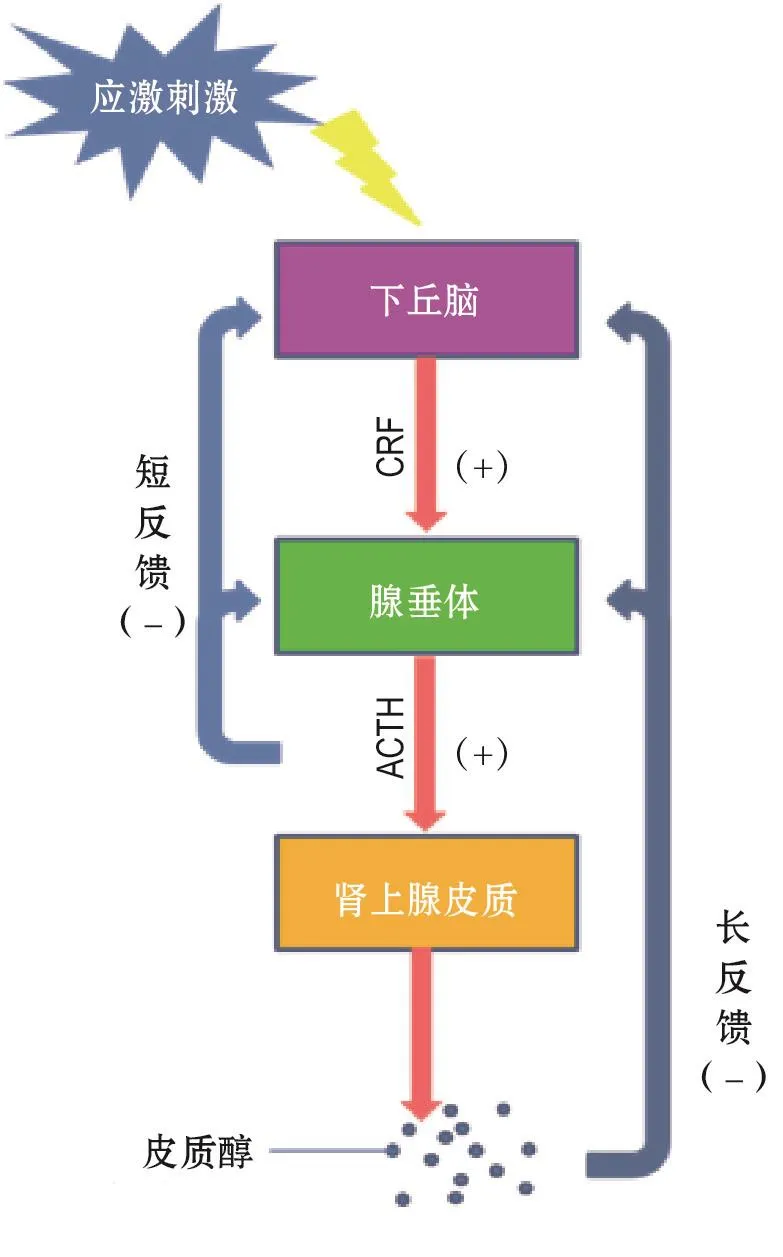
圖1 應激條件下皮質醇的調節示意圖.CRF:促腎上腺皮質激素釋放因子;ACTH:促腎上腺皮質激素.
皮質醇可透過細胞膜,通過與糖皮質激素受體(glucocorticoid receptor,GR)結合發揮作用。GR在腦中分布廣泛,其中海馬表達量較高,而海馬是受HPA軸負反饋調控的主要腦區。地塞米松實驗認為,皮質醇激素的下調是由于HPA軸負反饋增強導致[9]。有文獻報道,PTSD患者不僅在杏仁核、海馬和前額葉GR表達異常,GR對皮質醇的親和力也有增強[10]。PTSD患者腦中GR表達的變化引起HPA軸功能調節紊亂,可能是PTSD發病的因素之一[11-12]。FKBP5基因多樣性與PTSD及其他壓力應激障礙發病風險增加相關。FKBP5是一個重要的GR復合體功能調控蛋白,同時還是細胞內超短負反饋環的一部分,能夠調控GR的活性。通過對1585名美國退伍軍人的研究發現,常見的4種FKBP5單核苷酸(rs9296158,rs3800373,rs1360780和rs947008)突變與FKBP5蛋白水平升高相關,從而導致了GR對皮質醇的耐受和HPA軸負反饋通路異常。同時作者還指出FKBP5的單核苷酸多態性(single nucleotide polymorphism,SNP)可能與壓力引起的皮質醇水平升高且不能快速恢復有關,持續高水平的皮質醇將潛在增加PTSD的發病風險[13]。FKBP5的單核苷酸多態性與童年遭受虐待的成年PTSD患者癥狀的嚴重程度密切相關[14]。
1.2 神經炎癥與免疫系統失調
PTSD患者往往主述自身健康水平下降,如罹患心血管、呼吸和消化系統疾病,以及炎癥和自身免疫病等[15-16]。研究表明,PTSD患者免疫系統功能發生明顯改變,炎癥反應增強。Bam等[17]從PTSD患者外周血中提取總RNA進行轉錄組測序,并對變化基因進行功能分析顯示,PTSD患者炎癥相關基因表達異常,免疫網絡失調。2015年,美國一項針對666 269名伊拉克戰爭參戰士兵的研究發現,與健康對照者相比,PTSD患者免疫性疾病發病風險大幅度增加,且不存在性別差異[18]。
眾多研究認為,應激條件下神經解剖和神經內分泌的改變會使免疫系統失調,增加了對自身免疫或炎癥疾病的易感性,并加速其病程發展,從而加重患者的疾病負擔。在正常壓力條件下,HPA軸可和免疫系統相互調控維持穩態,腫瘤壞死因子α(tumor necrosis factor α,TNF-α)和白介細胞素-6(interleukin-6,IL-6)刺激HPA軸產生更多的皮質醇,皮質醇可負反饋地調節HPA軸避免過多的炎癥反應。在長期或過強的壓力條件下及PTSD患者中,皮質醇對HPA軸負反饋調控途徑不足以抑制炎癥,使其保持在正常水平。免疫細胞不僅可通過釋放炎癥因子調控神經可塑性變化,從而加強記憶形成和鞏固;還可通過炎癥因子調控神經內分泌系統,從而影響神經疾病的發生發展進程。小膠質細胞是腦內維持穩態的一類重要細胞,對于中樞神經系統出現的微小病理改變非常敏感,能有效地清除斑塊、損傷,甚至不必要的神經元和突觸。有報道提出,小膠質細胞在個體接受外界壓力刺激或危險信號時被激活且數量增多,而后在長期壓力過程中,小膠質細胞數量下降至低于正常水平[19]。對于多個研究的元分析發現,在PTSD患者血清中,炎癥因子TNF-α,IL-1β,IL-6和干擾素γ(interferon γ,IFN-γ)均高于健康對照組。作者認為慢性低水平炎癥可能是PTSD治療的一個分子標志[20]。另有文章認為,血漿中CRP的濃度可能與PTSD的發展相關[21],在再次創傷引起更多的細胞因子產生,這與再次創傷時PTSD癥狀加劇相關。這些現象說明炎癥反應的發生不僅使得個體更易于發展成PTSD,也可能是個體對壓力敏感的生物學基礎[22]。長期暴露于慢性炎癥條件下,小鼠會呈現出抑郁樣表現[23]。在慢性壓力條件下,小膠質細胞的激活增加了對突觸的修剪和重塑,神經元樹突棘數量下降,導致小鼠焦慮、抑郁樣表現[24]。在對于PTSD患者免疫細胞及免疫因子的研究中發現,Th1細胞與血漿中IFNγ水平均上調,且具有相關性[25],Treg的表型發生改變[26]。總之,免疫系統穩態失衡可能參與PTSD的發病進程,對于PTSD患者免疫系統的研究可為臨床診治提供新的策略。
1.3 神經結構和環路改變
神經影像學研究發現,PTSD患者腦結構發生改變,海馬、前額葉皮質(prefrontal cortex,PFC)和前扣帶回體積縮小,大腦白質發生非特異性損害。功能性磁共振研究表明,在接受負向刺激時,PTSD患者杏仁核和前扣帶回皮質過度活躍[27]。杏仁核一直以來被認為在恐懼記憶的習得和表現中發揮至關重要的作用[28-29],且杏仁核區的活動受到皮質的調控。在條件恐懼的情況下,杏仁核中的中央杏仁核(central amygdala,CeA)區發生神經可塑性的改變,使得恐怖記憶得以儲存[30]。在PTSD患者中,杏仁核反應過度,造成加重的恐懼反應和持續的創傷記憶。在恐懼反應中,前額葉皮質和海馬與杏仁核有著緊密聯系。海馬是參與學習記憶的主要腦區,在恐懼的消除和調控壓力狀態下神經內分泌的過程中發揮重要作用,海馬功能失調導致患者記憶缺失和信息處理受損。PFC是情緒調控的主要腦區,光遺傳學結合神經成像手段表明,PFC中的緣前皮質(prelimbic cortex,PL)區能整合來自基底外側杏仁核(basolateral amygdala,BLA)區和腹側海馬(ventral hippocampus,vHPC)區的信息,調控恐懼反應[31]。PFC參與PTSD患者的情緒調控,且在PTSD患者中呈現活度下降,灰質密度降低。在危險信號或壓力刺激下,杏仁核腦區過度興奮,視覺皮質興奮,同時PFC活度下降,語言中樞布洛卡區出現空白。前額葉對杏仁核的抑制作用下調。腹側PFC和前扣帶回受到抑制,不僅使恐懼記憶增強,同時也損壞情緒調控環路,臨床表現為恐懼記憶再現、憤怒和愧疚等應激反應。情緒環路調控障礙除上述失調的表現以外,在一些人群中表現為過強的調節。在接收到外界信號刺激時,腹側PFC活動增強,從而能增加對杏仁核的抑制,使杏仁核活度下降,產生情緒調節過強,如麻木、痛覺缺失和現實感喪失等行為表現(圖2)。近來,科學家發現外側韁核(lateral habenula,LHb)區和腹側被蓋區(ventral tegmental area,VTA)也參與壓力應激反應調控。PTSD模型小鼠LHb腦區神經元LTP增強,同時記憶相關的分子水平增加[32]。PTSD患者杏仁核神經活度增強,而VTA區活度下降[33]。PTSD模型大鼠VTA區神經元發生長期的生理性變化,從而加重了PTSD的癥狀[34]。不同的癥狀表現及環路投射更能說明PTSD的病癥是動態變化的系統紊亂疾病,其調控機制尚不清楚,這也是進一步揭示其病理機制和治療的主要障礙。
2 PTSD的治療方式及效果
對PTSD患者的治療有多種方法,目前臨床多采用心理治療與藥物治療相結合,以藥物治療為主,同時輔以心理治療[36]。近年來物理治療在PTSD患者上也有獲益,但還處于試驗階段,到臨床應用還需要進一步的探索。
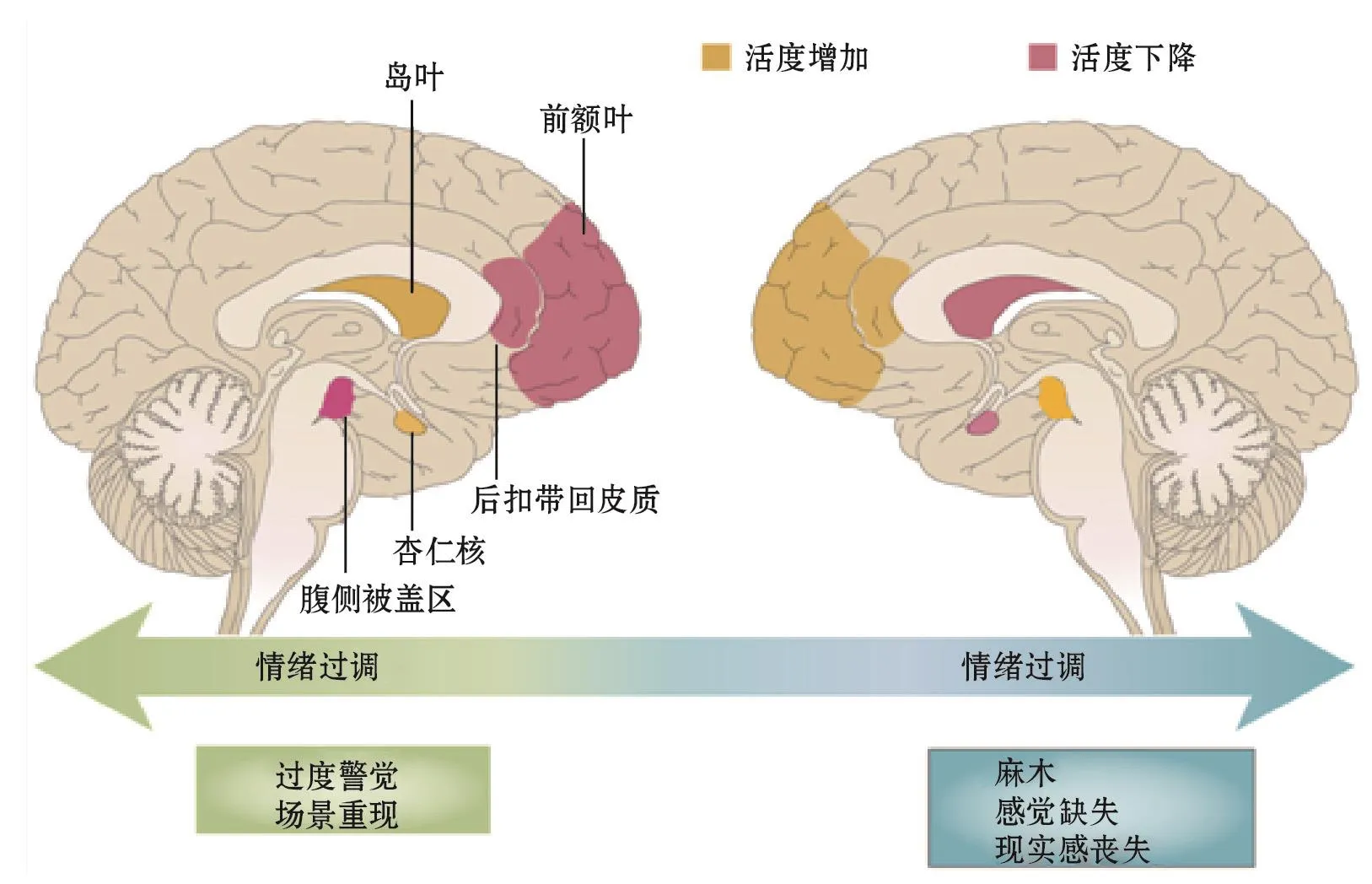
圖2 PTSD患者腦中情緒調控障礙示意圖[35].
2.1 藥物治療
2.1.1 抗抑郁藥
目前獲美國FDA批準用于臨床PTSD患者治療的藥物只有舍曲林(sertraline)和帕羅西汀(paroxetine),它們都是選擇性5-羥色胺重攝取抑制劑(selective serotonin reuptake inhibitor,SSRI),可顯著改善患者的焦慮、抑郁樣行為,是治療PTSD的首選藥物。在2014年進行的一項隨機雙盲測試中,從70名伊朗退伍軍人PTSD患者中隨機選取35名接受舍曲林治療10周,劑量為每日50~200 mg,另35名給予安慰劑,通過臨床總體印象嚴重度量表(Clinical Global Impression Scale-severity,CGI-S)和事件影響修正量表(Impact of Event Scale-Revised,IES-R)分析表明,服用舍曲林可顯著改善PTSD患者的癥狀,作者認為舍曲林是一種安全有效的治療藥物[37]。此外多個研究報道,帕羅西汀無論是對PTSD患者還是模型動物都有較好的治療效果[38-39]。基于PTSD患者伴隨焦慮、抑郁樣行為表現,很多抗焦慮、抑郁的三環類藥物也被嘗試在臨床應用,但由于其副作用較大,患者更易于中途停止治療[40]。
2.1.2 抗驚厥藥
文獻報道,使用拉莫三嗪(lamotrigine)可減輕治療抵抗性PTSD患者的攻擊性或攻擊性相關行為[41]。在2014年的另一項研究中,將拉莫三嗪和加巴噴丁(gabapentin)聯用治療PTSD,發現抗驚厥藥物可明顯改善PTSD患者的閃回和噩夢癥狀[42]。但這些研究患者例數較少,還需要進一步臨床試驗。
2.1.3 其他藥物
基于HPA軸紊亂,研究者設計的藥物〔如米非司酮(mifepristone)和氫化可的松〕也取得了明顯的改善效果,但它們還需要大量的臨床試驗[43]。給予PTSD患者去甲腎上腺素受體拮抗劑進行治療,能減輕杏仁核過度活動引起的創傷記憶增強,但并不能增強PFC對杏仁核的抑制效應[44]。谷氨酸是中樞神經系統重要的興奮性神經遞質,研究表明,PTSD患者腦內谷氨酸水平的升高對于創傷記憶的鞏固與增強具有重要作用[45]。以谷氨酸受體為靶點的在研藥物在治療PTSD中顯示有效,但還需要更多的研究證明[46]。目前臨床也在嘗試將≥2種藥物聯合用于PTSD治療。
目前技術手段尚不能充分揭示人腦的結構和功能,PTSD的藥物治療也僅限于針對其發生的生物學變化,而不能有效地根治病因,治療PTSD的藥物發展面臨很多挑戰。
2.2 物理療法
2.2.1 經顱磁刺激(transcranial magnetic stimulation,TMS)
TMS作為一種非侵入性的大腦刺激過程,通過給予特定順序和頻率的脈沖可改變神經元的電活動。因其非侵入性和對目標腦區的精確刺激而被認為是一種可替代的治療方法[47]。根據對多個試驗預后效果評價和比較,TMS被認為是一種新的科學的治療方法[48]。但目前該方法還存在很多問題,如設備的參數在眾多研究中不盡一致、治療機制尚不清楚等。現認為有效的目標腦區主要集中在PFC,但也有研究人員認為,該法的有益效果是由于影響了其他情緒調控腦區產生的。這種治療方法還不夠成熟完善,還需進一步探索和臨床驗證[49-50]。
2.2.2 深部腦刺激(deep brain stimulation,DBS)
文獻報道,靶向PTSD模型大鼠杏仁核區的DBS能減輕焦慮樣行為和電擊引起的過度警覺,且效果比帕羅西汀的療效更為顯著[51],目前認為DBS的作用機制是減輕條件恐懼引起的神經可塑性改變[52],從而減輕恐懼記憶形成。DBS有較好發展前景,未來可使PTSD患者受益[53-54]。
2.3 心理療法
心理療法在PTSD的治療中早于藥物治療,目前很多形式的心理療法在PTSD的治療中被認為是有效的。心理治療主要有針對行為療法(聚焦創傷療法,trauma-focused treatments)和非針對行為療法(非聚焦創傷療法,non-trauma-focused treatments),且根據多個研究結果的分析認為,針對行為療法比非針對行為療法更為有效[55]。
2.3.1 針對行為療法
針對行為療法主要有認知行為治療(cognitive behavioral therapies,CBT)和眼動脫敏再加工(eye movement desensitization and reprocessing,EMDR)。CBT是通過行為矯正技術來改變患者不合理的認知觀念,包括延長暴露治療和焦慮管理訓練。延長暴露治療通過長時間將患者暴露在引起恐懼的線索或記憶中以達到脫敏,從而減少恐懼等負面情緒。CBT主要包括資料收集、呼吸訓練、心理教育、在體暴露(in vivo exposure)和想象暴露[56]5個步驟,其對難民和尋求庇護者有較好的效果[57]。焦慮管理訓練主要是通過教給患者處理不良情緒的技巧來改善患者對焦慮的應時能力,增加患者自信心和積極的生活態度。在EMDR治療中,治療師用雙邊刺激形式鼓勵患者在回想起創傷事件時有相反的意念[58]。它主要是通過促進信息加工的過程,改變患者對創傷事件的認知和處理,幫助患者迅速降低焦慮,誘導積極情感,使患者能改善行為和人際關系。EMDR有暴露和認知的成分,比CBT療效更佳[59]。
2.3.2 非針對行為療法
非針對行為療法包括支持治療、人際關系治療及非直接咨詢,因其更易于堅持,對患者也有很大的幫助[60]。對PTSD患者的治療,來自社會(尤其是家庭)的積極支持和配合也起到很關鍵的作用。
3 結語
對于PTSD的研究雖已取得了巨大進步,但其發生發展的病理生理學機制尚不清楚。目前研究認為,PTSD是一種由多系統紊亂而影響到中樞和外周對壓力應激響應的疾病進程,臨床治療多為藥物和心理療法相結合,預后效果個體差異較大。腦解剖結構和神經環路的變化、免疫系統的改變、神經內分泌系統紊亂以及基因多態性都是PTSD發病的重要因素,但對于這些影響因素之間的內在聯系還缺少深入的研究,如細菌脂多糖誘發的神經炎癥存在明顯的腦區特異性[61],在PTSD中神經炎癥的發生是否具有腦區特異性?是否與恐懼反應的環路相關聯?神經內分泌受神經環路的調控,同時也負反饋地影響神經可塑性,這些跨系統的信息交流也為藥物發展提供了可能的靶點。全面具體的認識PTSD的生物學病理基礎是研究的重要前提,個體化的治療法案是其治療的關鍵,其研究方向從單因素的分析向多系統之間交互調控的發展是必然趨勢。
[1]Lohr JB,Palmer BW,Eidt CA,Aailaboyina S,Mausbach BT,Wolkowitz OM,et al.Is post-traumatic stress disorder associated with premature senescence? a review of the literature[J].Am J Geriatr Psychiatry,2015,23(7):709-725.
[2]Koo KH,Hebenstreit CL,Madden E,Maguen S.PTSD detection and symptom presentation:racial/ethnic Differences by gender among veterans with PTSD returning from Iraq and Afghanistan[J].J Affect Disord,2016,189:10-16.
[3]Dohrenwend BP,Turner JB,Turse NA,Adams BG,Koenen KC,Marshall R.The psychological risks of Vietnam for U.S.veterans:a revisit with new data and methods[J].Science,2006,313(5789):979-982.
[4]Geng FL,Fan F,Zhang L.Poor sleep quality associated with PTSD,anxiety,and depression among adolescents exposed to 2008 Wenchuan earthquake,China[J].Chin J Clin Psychol(中國臨床心理學雜志),2012,20(2):172-175.
[5]Michopoulos V,Rothbaum AO,Jovanovic T,Almli LM,Bradley B,Rothbaum BO,et al.Association of CRP genetic variation and CRP level with elevated PTSD symptoms and physiological responses in a civilian population with high levels of trauma[J].Am J Psychiatry,2015,172(4):353-362.
[6]Watkins LE,Han S,Harpaz-Rotem I,Mota NP,Southwick SM,Krystal JH,et al.FKBP5 polymorphisms,childhood abuse,and PTSD symptoms:results from the national health and resilience in veteransstudy[J].Psychoneuroendocrinology,2016,69:98-105.
[7]Miller MW, Reardon AF,Wolf EJ,Prince LB,Hein CL.Alcohol and drug abuse among U.S.veterans:comparing associations with intimate partner substance abuse and veteran psychopathology[J].J Trauma Stress,2013,26(1):71-76.
[8]Yehuda R.Clinical relevance of biologic findings in PTSD[J].Psychiatr Q,2002,73(2):123-133.
[9]Bremner D,Vermetten E,Kelley ME.Cortisol,dehydroepiandrosterone,and estradiol measured over 24 hours in women with childhood sexual abuse-related posttraumatic stress disorder[J].J Nerv Ment Dis,2007,195(11):919-927.
[10]Liberzon I,López JF,Flagel SB,Vázquez DM,Young EA.Differential regulation of hippocampal glucocorticoid receptors mRNA and fast feedback:relevance to post-traumatic stress disorder[J].J Neuroendocrinol,1999,11(1):11-17.
[11]Zhang JH,Li M ,Shi YX,Han F.Expression of glucocorticoid receptors in medial prefrontal cortex is increased in posttraumatic stress disorder rats[J].Acta Anat Sin(解剖學報),2011,42(2):151-154.
[12]Liu NY,Han F,Du Z,Shi YX.Expression changes of glucocorticoid receptors in the central amygdaloid nucleus of PTSD-like rats[J].J China Med Univ(中國醫科大學學報),2008,37(2):148-151.
[13]Binder EB.The role of FKBP5,a co-chaperone of the glucocorticoid receptor in the pathogenesis and therapy of affective and anxiety disorders[J].Psychoneuroendocrinology,2009,34(Suppl 1):S186-S195.
[14]Binder EB,Bradley RG,Liu W,Epstein MP,Deveau TC,Mercer KB,et al.Association of FKBP5 polymorphisms and childhood abuse with risk of posttraumatic stress disorder symptoms in adults[J].JAMA,2008,299(11):1291-1305.
[15]Boscarino JA.Posttraumatic stress disorder and physical illness:results from clinical and epidemiologic studies[J].Ann N Y Acad Sci,2004,1032:141-153.
[16]KubzanskyLD, KoenenKC.Isposttraumatic stress disorder related to development of heart disease?An update[J].Cleve Clin J Med,2009,76 (Suppl 2):S60-S65.
[17]Bam M,Yang X,Zumbrun EE,Zhong Y,Zhou J,Ginsberg JP,et al.Dysregulated immune system networks in war veterans with PTSD is an outcome of altered miRNA expression and DNA methylation[J].Sci Rep,2016,6:31209.
[18]O′Donovan A,Cohen BE,Seal KH,Bertenthal D,Margaretten M,Nishimi K,et al.Elevated risk for autoimmune disorders in Iraq and Afghanistan veterans with posttraumatic stress disorder[J].Biol Psychiatry,2015,77(4):365-374.
[19]Kreisel T,Frank MG,Licht T,Reshef R,Ben-Menachem-Zidon O, Baratta MV, et al.Dynamic microglial alterations underlie stress-induced depressive-like behavior and suppressed neurogenesis[J].Mol Psychiatry,2014,19(6):699-709.
[20]Passos IC,Vasconcelos-Moreno MP,Costa LG,Kunz M,Brietzke E,Quevedo J,et al.Inflammatory markers in post-traumatic stress disorder:a systematic review,meta-analysis,and meta-regression[J].Lancet Psychiatry,2015,2(11):1002-1012.
[21]Eraly SA,Nievergelt CM,Maihofer AX,Barkauskas DA,Biswas N,Agorastos A,et al.Assessment of plasma C-reactive protein as a biomarker of posttraumatic stress disorder risk[J].JAMA Psychiatry,2014,71(4):423-431.
[22]Neigh GN,Ali FF.Co-morbidity of PTSD and immune system dysfunction:opportunities for treatment[J].Curr Opin Pharmacol,2016,29:104-110.
[23]Mello BS,Monte AS,McIntyre RS,Soczynska JK,Custódio CS,Cordeiro RC,et al.Effects of doxycycline on depressive-like behavior in mice after lipopolysaccharide(LPS)administration[J].J Psychiatr Res,2013,47(10):1521-1529.
[24]Wohleb ES,Terwilliger R,Duman CH,Duman RS.Stress-induced neuronal colony stimulating factor 1 provokes microglia-mediated neuronal remodeling and depressive-like behavior[J].Biol Psychiatry,2018,83(1):38-49.
[25]Zhou J,Nagarkatti P,Zhong Y,Ginsberg JP,Singh NP,Zhang J,et al.Dysregulation in microRNA expression is associated with alterations in immune functions in combat veterans with post-traumatic stress disorder[J].PLoS One,2014,9(4):e94075.
[26]Jergovic′M,Bendelja K,Vidovi c′A,Savi c′A,Vojvoda V,Aberle N,et al.Patients with posttraumatic stress disorder exhibit an altered phenotype of regulatory T cells[J].Allergy Asthma Clin Immunol,2014,10(1):43.
[27]Hayes JP,Vanelzakker MB,Shin LM.Emotion and cognition interactions in PTSD:a review of neurocognitive and neuroimaging studies[J].Front Integr Neurosci,2012,6:89.
[28]LeDoux JE.Emotion circuits in the brain[J].Annu Rev Neurosci,2000,23:155-184.
[29]Ehrlich I,Humeau Y,Grenier F,Ciocchi S,Herry C,Lüthi A.Amygdala inhibitory circuits and the control of fear memory[J].Neuron,2009,62(6):757-771.
[30]Li H,Penzo MA,Taniguchi H,Kopec CD,Huang ZJ,Li B.Experience-dependent modification of a central amygdala fear circuit[J].Nat Neurosci,2013,16(3):332-339.
[31]Sotres-Bayon F,Sierra-Mercado D,Pardilla-Delgado E,Quirk GJ.Gating of fear in prelimbic cortex by hippocampal and amygdala inputs[J].Neuron,2012,76(4):804-812.
[32]Park H,Rhee J,Park K,Han JS,Malinow R,Chung C.Exposure to stressors facilitates longterm synaptic potentiation in the lateral habenula[J].J Neurosci,2017,37(25):6021-6030.
[33]Hughes KC,Shin LM.Functional neuroimaging studies of post-traumatic stress disorder[J].Expert Rev Neurother,2011,11(2):275-285.
[34]Corral-Frias NS,Lahood RP,Edelman-Vogelsang KE,French ED,Fellous JM.Involvement of the ventral tegmental area in a rodent model of post-traumatic stressdisorder[J].Neuropsychopharmacology,2013,38(2):350-363.
[35]Yehuda R,Hoge CW,McFarlane AC,Vermetten E,Lanius RA,Nievergelt CM,et al.Post-traumatic stress disorder[J].Nat Rev Dis Primers,2015,1:15057.
[36]Zhang DW,Gan JL.Progressing in PTSD pharmcological tharepy[J].J Clin Psychiatry(臨床精神醫學雜志),2010,20(1):66-67.
[37]Panahi Y,Moghaddam BR,Sahebkar A,Nazari MA,Beiraghdar F,Karami G,et al.A randomized,double-blind,placebo-controlled trial on the efficacy and tolerability of sertraline in Iranian veterans with post-traumatic stress disorder[J].Psychol Med,2011,41(10):2159-2166.
[38]Kucukalic′A,Bravo-Mehmedbasic′A,Dzubur-Kulenovic′A.Paroxetine in the treatment of post traumatic stress disorder:our experiences[J].Bosn J Basic Med Sci,2008,8(1):76-79.
[39]Bentefour Y,Bennis M,Garcia R,M'hamed SB.Effects of paroxetine on PTSD-like symptoms in mice[J].Psychopharmacology(Berl),2015,232(13):2303-2312.
[40]Albucher RC,Liberzon I.Psychopharmacological treatment in PTSD:a critical review[J].J Psychiatr Res,2002,36(6):355-367.
[41]Kozaric′-Kovacˇic′D,Eterovic′M.Lamotrigine abolished aggression in a patient with treatment-resistant posttraumatic stress disorder[J].Clin Neuropharmacol,2013,36(3):94-95.
[42]Kishimoto A,Goto Y,Hashimoto K.Post-traumatic stress disorder symptoms in a female patient following repeated teasing:treatment with gabapentin and lamotrigine and the possible role of sensitization[J].Clin Psychopharmacol Neurosci,2014,12(3):240-242.
[43]Golier JA,Caramanica K,Demaria R,Yehuda R.A pilot sudy of mifepristone in combat-related PTSD[J].Depress Res Treat,2012,2012:393251.
[44]McGhee LL,Maani CV,Garza TH,Desocio PA,Gaylord KM,Black IH.The effect of propranolol on posttraumatic stress disorder in burned service members[J].J Burn Care Res,2009,30(1):92-97.
[45]Reul JM,Nutt DJ.Glutamate and cortisol-a critical confluence in PTSD?[J].J Psychopharmacol,2008,22(5):469-472.
[46]Burgdorf J,Kroes RA,Zhang XL,Gross AL,Schmidt M,Weiss C,et al.Rapastinel(GLYX-13)has therapeuticpotentialforthe treatmentof post-traumatic stress disorder:characterization of a NMDA receptor-mediated metaplasticity process in the medial prefrontal cortex of rats[J].Behav Brain Res,2015,294:177-185.
[47]Wahbeh H,Senders A,Neuendorf R,Cayton J.Complementary and alternative medicine for posttraumatic stress disorder symptoms:a systematic review[J].J Evid Based Complementary Altern Med,2014,19(3):161-175.
[48]Clark C,Cole J,Winter C,Williams K,Grammer G.A review of transcranial magnetic stimulation as a treatment for post-traumatic stress disorder[J].Curr Psychiatry Rep,2015,17(10):83.
[49]Horvath JC, Perez JM,Forrow L,Fregni F,Pascual-Leone A.Transcranial magnetic stimulation:a historical evaluation and future prognosis of therapeutically relevant ethical concerns[J].J Med Ethics,2011,37(3):137-143.
[50]Karsen EF,Watts BV,Holtzheimer PE.Review of the effectiveness of transcranial magnetic stimulation for post-traumatic stress disorder[J].Brain Stimul,2014,7(2):151-157.
[51]Stidd DA,Vogelsang K,Krahl SE,Langevin JP,Fellous JM.Amygdala deep brain stimulation is superior to paroxetine treatment in a rat model of posttraumatic stress disorder[J].Brain Stimul,2013,6(6):837-844.
[52]Sui L,Huang S,Peng B,Ren J,Tian F,Wang Y.Deep brain stimulation of the amygdala alleviates fear conditioning-induced alterations in synaptic plasticity in the cortical-amygdala pathway and fear memory[J].J Neural Transm(Vienna),2014,121(7):773-782.
[53]Langevin JP,Koek RJ,Schwartz HN,Chen JWY,Sultzer DL,Mandelkern MA,et al.Deep brain stimulation of the basolateral amygdala for treatment-refractory posttraumatic stress disorder[J].Biol Psychiatry,2016,79(10):e82-e84.
[54]Koek RJ,Langevin JP,Krahl SE,Kosoyan HJ,Schwartz HN,Chen JW,et al.Deep brain stimulation of the basolateral amygdala for treatment-refractory combat post-traumatic stress disorder(PTSD):study protocol for a pilot randomized controlled trial with blinded,staggered onset of stimulation[J].Trials,2014,15:356.
[55]Bisson JI,Roberts NP,Andrew M,Cooper R,Lewis C.Psychological therapies for chronic posttraumatic stress disorder(PTSD) in adults[J].Cochrane Database Syst Rev,2013,(12):CD003388.
[56]Chen SL,Li LJ.Psychotherapy strategies of PTSD[J].J Clin Psychol Med(臨床精神醫學雜志),2005,15(3):180-181.
[57]M?rkved N,Hartmann K,Aarsheim LM,Holen D,Milde AM,Bomyea J,et al.A comparison of narrative exposure therapy and prolonged exposure therapy for PTSD[J].Clin Psychol Rev,2014,34(6):453-467.
[58]Leer A,Engelhard IM,Altink A,van den Hout MA.Eye movements during recall of aversive memory decreases conditioned fear[J].Behav Res Ther,2013,51(10):633-640.
[59]Seidler GH,Wagner FE.Comparing the efficacy of EMDR and trauma-focused cognitive-behavioral therapy in the treatment of PTSD:a meta-analytic study[J].Psychol Med,2006,36(11):1515-1522.
[60]Schottenbauer MA,Glass CR,Arnkoff DB,Gray SH.Contributions of psychodynamic approaches to treatment of PTSD and trauma:a review of the empirical treatment and psychopathology literature[J].Psychiatry,2008,71(1):13-34.
[61]Noh H,Jeon J,Seo H.Systemic injection of LPS induces region-specific neuroinflammation and mitochondrial dysfunction in normal mouse brain[J].Neurochem Int,2014,69:35-40.

