德國衛生技術評估決策轉化路徑及方法探析
呂蘭婷
中國人民大學公共管理學院 中國人民大學醫改研究中心 北京 100872
·衛生技術評估·
德國衛生技術評估決策轉化路徑及方法探析
呂蘭婷*
中國人民大學公共管理學院 中國人民大學醫改研究中心 北京 100872
德國與我國有著相似醫療保障體系背景,并且已經形成以國家層面三大衛生技術評估(Health Technology Assessment, HTA)機構為主的嚴謹的HTA管理流程和高效的決策轉化路徑,是全球基于HTA進行衛生領域循證決策的典型代表。本文通過文獻研究和實地調研,分析梳理了德國HTA應用及其決策轉化的路徑和方法,最終結合我國現階段HTA決策轉化面臨的問題和挑戰,有針對性地提出了幾條促進我國HTA決策轉化的啟示性建議。
衛生技術評估; 決策轉化; 循證決策; 德國
衛生技術評估(Health Technology Assessment, HTA)最早誕生于20世紀70年代的美國,是衛生政策和衛生管理決策系統的重要輔助工具和方法。[1]根據世界衛生組織[2]在2015年發布的關于全球處于不同地區、不同經濟發展水平國家(有125個成員國參加)的HTA現狀的全面評估報告,超過半數的國家已將HTA及其結果引入到對衛生技術的準入、管理、監測等一系列決策過程中。HTA通過決策轉化應用于衛生政策制定,已經在優化全球衛生配置上發揮了巨大的作用。[3-5]
而在我國,HTA領域發展相對滯后,尤其是在進一步利用HTA結果以實現更好的決策轉化方面。面對當前我國衛生體系醫療費用的不合理快速增長以及有限醫療資源分配、利用不合理的問題,國家對循證決策提出了更高的要求,未來在醫療技術準入、醫保報銷、藥品定價等諸多方面,HTA結果將越來越多的作為決策依據完成其決策轉化,從而輔助循證決策。同是社會醫療保險為主的國家,德國在HTA應用和決策轉化方面保持持續創新地探索,尤其在實現HTA服務于決策轉化過程中,德國有效地發揮了政府層面宏觀監督指導和社會層面的具體細則實施的作用,通過利用HTA這一科學決策工具選擇高效的、必要的、富有成本收益的醫療服務進入社會醫療保險報銷系統,在有力控制了醫療費用增長的同時為患者提供了更加優質的健康服務。
1 德國HTA情況概述
1.1 德國HTA組織機構的發展及特點
1.1.1 HTA的發展
20世紀90年代以來,伴隨著循證醫學運動(Evidence-based Medicine Movement)在德國的發起,HTA和衛生經濟學等也引起了廣泛的討論。同時,受驅于緊張的衛生醫療費用預算,外加聯邦衛生部對將HTA運用于醫保報銷決策的濃厚興趣,越來越來多的利益相關者達成廣泛共識,即通過對現有衛生技術進行評估后進行準入決策以控制費用增長,并同時確保提供更加質優高效服務。隨后,來自疾病基金協會、醫師協會、醫學科研高校、學術研究組織等的學術工作小組作為中堅力量,開始致力于開展各種HTA項目研究,或是為各協會的相關疾病報銷、內部決策等提供決策支持,或是從科研學術的角度致力于HTA方法、應用、培訓等方面的研究和工作。1997—2002年,成立于漢諾威醫學院(Hannover Medical School)下的衛生保健技術評估科學工作組,在聯邦政府的資助下進行了一系列多達50項的HTA項目,為德國HTA數據庫的建立以及HTA相關方法的后續改進奠定了良好的基礎。[6]
在2000年德國衛生體系改革浪潮的推進下,德國衛生技術評估局(DAHTA,隸屬于德國醫學文獻與情報學會,DIMDI)正式成立,被要求對聯邦資助的HTA項目進行系統管理,并通過組建一個信息化數據庫囊括相關HTA項目成果用于支持國家衛生決策。2004年,伴隨著法定醫療保險現代化法(the Statutory Health Insurance Modernization Act)出臺,由眾多利益相關方組成的衛生自我管理體系中的最高決策機構——聯邦聯合委員會(G-BA)正式誕生;該委員會由德國自我管理衛生系統中的四大主導組織構成:聯邦醫保基金協會(GKV-Spitzenverband)、德國醫院聯盟(DKG)、國家法定健康保險醫師協會(KBV)和國家法定健康保險牙醫協會(KZBV)。[7]G-BA被賦予組織或委托開展HTA項目的職責:在聯邦衛生部的監督下G-BA可通過基于HTA的循證決策過程發布具有法律約束力的標準、指令等,對藥品、診斷、治療過程、醫療器械和非醫學治療的提供和報銷做出相關規定。隨后,G-BA依據一項新法案(GKV)建立了一個獨立的HTA機構——衛生保健質量與療效研究院(IQWiG)。而IQWiG的主要職責就是進行HTA評估為G-BA決策提供參考,開展的HTA評估包括藥品的收益和成本效益評估、非藥品醫療技術的干預項目評估(比如醫療設備、診斷治療方法、疾病預防篩查等)。至此,德國基于三大HTA組織機構的國家層面HTA決策轉化體系正式組成。
1.1.2 HTA組織機構的特點
德國衛生體系強調各方自我管理,在政府對相關的機構職能、財政預算等宏觀層面的體系框架進行規劃設計后,具體運行方案由醫療服務體系中的各方代表談判確定,主要依靠行業力量進行自我管理以及服務購買者、使用者之間的制約。[8]審視德國HTA以及HTA決策轉化機制的成長發展過程,政府支持和監督、從法律層面確保HTA決策轉化成果落實到位以及基于國家層面HTA機構的各行業協會、相關院所、組織、患者群體等利益相關方都可參與決策的嚴謹決策轉化流程缺一不可。從最開始的循證醫學運動統一認識,到之后的各種背景下的學術科研工作小組不斷探索HTA方法、管理流程和決策轉化機制,再到最后形成以德國自我管理體系中的最高決策機構為中心的三大HTA管理機構,并通過立法確定其基于HTA的決策轉化成果的嚴格落實;形成了能適用于不同層級、不同組織,并針對各種不同技術類型的HTA評估方法及決策轉化機制。
1.2 德國HTA決策轉化管理流程
1.2.1 HTA決策轉化管理相關法規指令
德國在立法以及國家政策高度上確定了HTA決策轉化的順暢運行。首先G-BA由2004年法定醫療保險現代化法出臺成立,其基于HTA進行循證決策的權力由德國社會法第五冊(SGB Ⅴ)賦予(聯邦衛生部負責監督)。[9]而主要實施HTA評估的機構IQWiG同樣是由G-BA在2004年依據新法案(GKV)建立,并且其開展HTA評估輔助G-BA決策的職責在SGB Ⅴ中進行了明文規定。在建立國家層面的HTA機構之上,德國持續探索完善HTA決策轉化機制,2010年11月11日,德國議會通過了市場對醫藥產品的改革法案(AMNOG),這項法案新賦予了G-BA和IQWiG一項重要的職責:對新獲批準上市的藥品進行額外效益評估,以輔助社會醫療保險機構對新藥的定價和報銷方面的政策制定。DAHTA也是德國醫改的產物,雖然在實際決策制定中的直接作用弱于其他兩大機構,但其建立的HTA數據庫對決策轉化證據支持也起到了積極作用。
1.2.2 HTA決策轉化的相關方
目前,在德國的HTA管理體系中,主要形成了G-BA、IQWiG、DIMDI這三個國家層面的HTA組織機構,分別實現決策轉化整體性管理、評估科學化管理以及HTA的信息平臺化管理等;各機構各有功能定位,又通過信息共享來共同實現全國HTA的完善系統管理。G-BA是德國HTA決策轉化體系中的主導管理者,負責基于包括HTA評估結果等證據做出衛生決策。最終決策轉化的HTA項目可在G-BA內部開展,大部分委托IQWiG、高等院校研究機構等獨立第三方評估機構進行,同時也參考DIMDI的HTA信息庫信息。
德國參與HTA決策轉化管理的相關方除了組成G-BA四大支柱組織:聯邦醫保基金協會、德國醫院聯盟、國家法定健康保險醫師協會和國家法定健康保險牙醫協會之外,根據社會法和患者參與法案(the Patient Involvement Act)的相關規定,特殊的患者代表或是維護患者權益的組織代表也有權參與G-BA決策流程(但無表決權)。其他利益相關方,如患者家屬、醫藥企業、醫藥企業協會等也有途徑參與決策過程。還有具體決策的關鍵方:德國衛生體系最終決策主體是G-BA決策委員會(Plenum)以及其下的九個子委員會(subcommittees)。
1.2.3 HTA決策轉化具體管理流程
在進行具體的HTA決策轉化管理時,主要包括五個階段:評估申請——開題咨詢——外部科學評估——聽證會——決議及指令發布(圖1)。首先,由G-BA決策委員會內部成員,或患者代表、社會醫療保險醫療服務提供者和基金資助者,以及一些特殊醫藥技術供應商等都可以提出HTA評估申請。之后,G-BA從提交的申請中選定正式開展評估的項目,并進一步確定具體評估問題,然后根據受眾的不同、判定標準的差異,任命子委員會負責相關證據收集以及管理獨立的HTA評估工作。然后,根據具體評估需求,決策委員會一般委托IQWiG等HTA評估機構進行外部評估。之后由G-BA根據HTA初步結果確定是否需要舉行聽證會,尤其是涉及到第三方利益時,一般書面和口頭兩種方式的聽證會都要舉行。最后,根據HTA評估結果以及聽證會結果,由子委員會匯總所有商議結果并做出初步決策意見呈交決策委員會,決策委員會再據此做出最終決策并撰寫詳細國家指令上交給衛生部并公布在G-BA官網供公眾審閱。最終,如果衛生部在兩個月內沒有提出異議,該指令將被發布到聯邦公報上,并且一般在發布后第二天,相應指令規定即在全國生效實施。
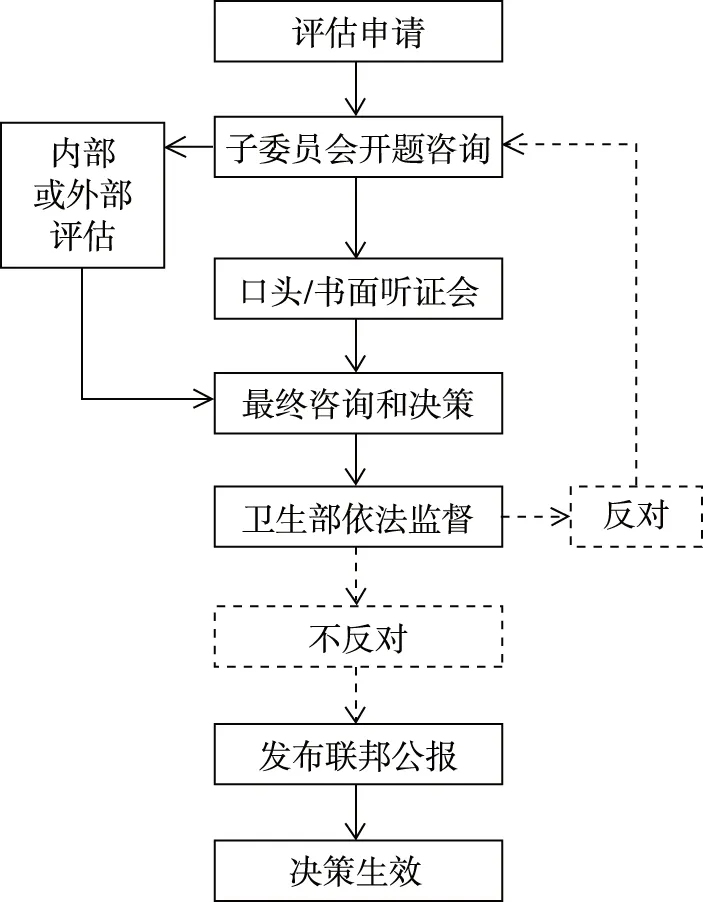
圖1 G-BA主導的HTA決策轉化過程
2 從藥品準入管理看德國HTA決策轉化情況
2.1 藥品準入HTA決策轉化過程
2.1.1 相關法規指令
德國從法律層面確保HTA決策轉化,最新關于藥品準入的法規是2010年11月德國議會通過的市場對醫藥產品的改革法案(AMNOG),G-BA和IQWiG開始致力于對新藥的額外效益評估(以下簡稱AMNOG評估),即對新獲批準上市的藥品進行額外效益評估,用于新藥定價和醫保報銷等方面的藥品醫保準入政策制定。
2.1.2 藥品準入HTA決策轉化具體過程
2010年之后,G-BA和IQWiG開展的AMNOG評估就已經成為醫保對具有新的活性成分體系藥品的醫保內定價參考基礎。AMNOG評估將新藥的額外效益結果劃分為六類:重大(持續重大的改善,如可治愈,存活時間大量延長,長時間免于嚴重的病癥,嚴重副作用影響極大減緩)、可觀(有顯著的改善,如明顯病情減緩,存活時間適當延長,嚴重病癥的緩解,嚴重副作用影響減緩或其他副作用明顯減緩)、少量(適當的高于邊際收益的改善,如嚴重病癥的減緩,副作用減少)、邊際(無額外效益)和低于已準入參照藥品。
具體決策流程及HTA在相應環節的作用如圖2。在新藥獲批上市三個月內,醫藥公司上交醫保準入申請和藥品相關信息,G-BA委托IQWiG等第三方HTA機構完成AMNOG評估。評估初步結果將在網上公示,醫藥公司、協會和專家等利益相關方都可據此提交書面或口頭意見。接下來的三個月內,G-BA將基于HTA評估結果、各利益相關方意見以及其他證據做出該藥品醫保準入的最終決策。決策詳細內容包括額外效益的程度、適宜接受新藥治療的患者群、質量保證的行政要求以及治療成本說明等,如果新藥品具有額外效益,這些都將作為新藥醫保定價談判的基礎證據。接下來醫藥公司與聯邦醫保支付基金協會將據此談判確定新藥報銷支付價格的協商以及零售折扣價格。在這個談判階段G-BA提供平臺并且管理全過程,雙方將按照G-BA安排好的議程進行談判,如果在特定時間段內談判沒有達成共識,定價最終決策權將被轉交給仲裁委員會。仲裁委員會將依據歐洲價格水平確定最終價格,或者,由于定價進行到這一步與新藥的成本效益性關系極大,仲裁委員會可以繼續要求HTA機構開展更深入的經濟學評價,并且基于進一步的HTA結果來確定新藥適宜的價格。然而,如果G-BA評估認為新藥相比于參照藥品并不具備額外效益,新藥將需在上市六個月內被納入到已有參考定價系統中,意味著該新藥的年治療成本不得高于參照藥品所在參考定價藥品組已設的基準線。
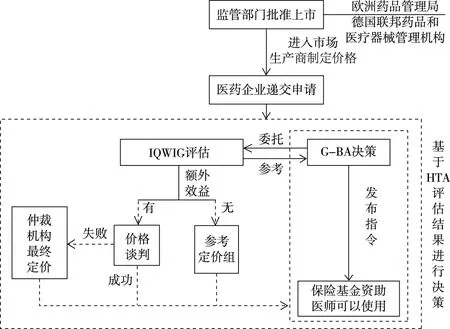
圖2 德國新藥醫保準入方面HTA決策轉化過程
總之,受市場改革作用影響,在新藥上市后的快速定價報銷決策中,HTA被作為一種科學有效地方法嵌入到了決策過程,HTA決策轉化也從原有醫保準入決策擴展到藥品定價談判與決策中。
2.2 藥品準入HTA決策轉化成果
根據實地調研所得材料,截至2015年8月10日,IQWiG已經審核進行了114份AMNOG評估(表1),高效應對了歐洲新藥上市后醫保準入決策速度較慢的問題,并且保證了決策的科學性。表1展示了2011年以來在德國許可上市的新藥對比已有藥品沒有額外效益的占比為56%,意味著在AMNOG評估機制下一半以上的新上市藥品失去了以前實際存在的不合理優勢(即在相比已有藥品沒有額外效益的情況下還具有定相對較高價格的可能性),從而在很大程度上控制了新藥價格上漲。從這個例子可見,德國在HTA決策轉化上的持續探索不僅快速響應了衛生體系決策、管理需求,還為德國衛生醫保系統的持久健康運營奠定了科學合理的決策基石。
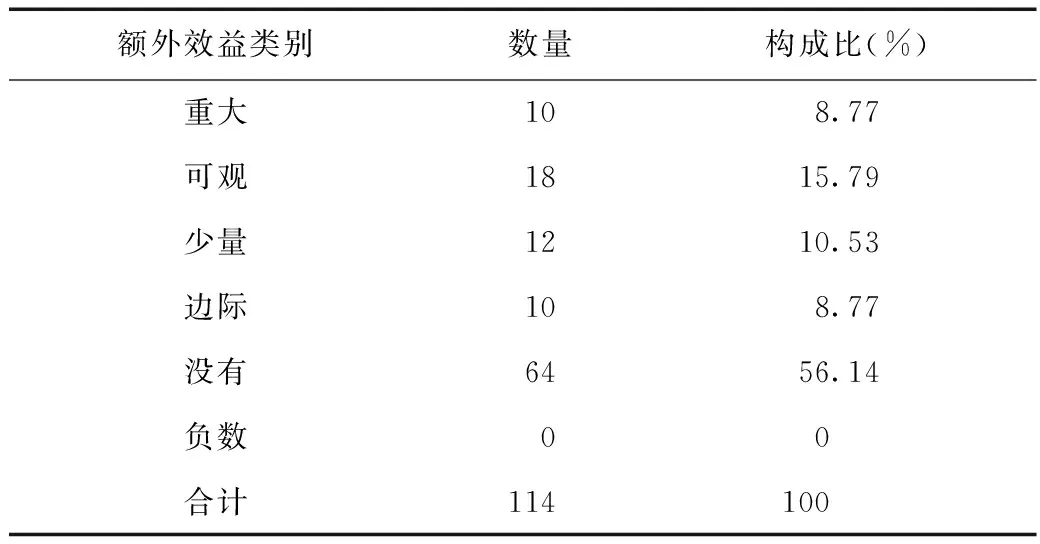
表1 基于AMNOG的藥物評估情況匯總表
數據來源于調研資料;數據統計截至2015年8月10日。
3 德國HTA決策轉化經驗及對我國的啟示
3.1 加強HTA決策轉化的意義認知,推動相關制度和機構能力建設
審視德國的HTA發展進程,德國HTA發展起步于一些研究機構、學術團體等自下而上的探索;多方利益相關者也慢慢對HTA的應用優勢有了認知;在衛生醫療費用不斷增長壓力下,國家層面如聯邦衛生部與多方利益相關者達成通過基于HTA的循證決策控制費用增長并同時確保提供質優高效服務的廣泛共識;最終發展出寫入社會法案的國家層面的G-BA、IQWiG以及DIMDI三大HTA組織機構。并且,根據改革發展需求,德國也在國家層面快速回應并積極出臺相應法案來進一步促進HTA在更廣范圍的決策轉化。此外,為維持這些HTA組織機構的良性發展,聯邦政府提供了較為穩定的資金支持,并且培養了多學科背景的專業人才,以切實做到采用科學的評估方法以產出較高質量的HTA報告。
我國HTA決策轉化的現實發展滯后,相關研究者、決策者、執行者等甚至未完全形成HTA決策轉化意義的認知,部分決策者仍采用經驗主義決策的做法來進行相關決策;而現有的研究者也專注于特定領域的評估活動而且學術成果無法形成有效的決策影響。德國與我國都是以社會醫療保險為主的國家,德國順暢的HTA決策轉化機制已經為其醫保、衛生體系健康發展起到了關鍵作用。醫改已經進入到深水區的我國也應認清HTA決策發展需求,加強HTA決策轉化的意義認知,在持續發展現有HTA研究之上,嘗試借助國家層面的政策、法定約束力量研究構建促進HTA決策轉化的相關制度機制、方法路徑等,真正實現HTA的循證決策價值。尤其是在衛生法的修訂出臺呼聲漸漲的背景下,嘗試將HTA這種科學的決策方法或機制納入相關法律,并明確相關組織機構權責,盡早探索建立起我國的HTA決策轉化相關制度機制有著很大的意義和必要性。此外,要真正實現我國HTA的決策轉化的最大化效用,必須要保證產出的HTA具有較高的質量、較強的時效、較好的操作性等,而這些都是基于完備的HTA組織機構能力建設基礎之上的,同時完備的人才梯隊建設、穩健的評估研究經費支援等也很重要。
3.2 探索建立透明、多方參與的HTA決策轉化方式,促進循證決策
德國HTA決策轉化過程中,一方面,聯邦衛生部會及時根據G-BA關于HTA的最新方法、研究前沿等成果向聯邦議院和聯邦參議院提出相關的立法倡議;而另一方面,G-BA也會基于自身和IQWiG、DIMDI的評估報告來向醫療服務提供者、社會醫療保險基金以及患者發布相關報銷指令等。這兩種面向不同的決策需求而實施的分層式決策轉化模式,使HTA應用決策的形式更加具有針對性和科學性,分別靈活地實現了決策制定的過程導向和效果導向。并且不論是在評估過程中還是在具體的決策轉化中都有各利益相關方的廣泛參與,這種廣泛參與的形式也促進了有效地決策轉化。此外,在這個過程中,HTA組織機構之間的互助也有利于促進決策參考報告的產出,進而加快了決策過程。尤其是G-BA和IQWiG之間,G-BA的很多決策都基于IQWiG提供的評估結果;雖然,基于法案IQWiG由G-BA建立,但是近些年來IQWiG不斷發展,形成了科學的自我評估方法體系以及較為透明的評估流程等,已成長為與全球HTA金標準的英國NICE接近的獨立專業機構。
我國決策轉化機制并未有效建立,目前所開展的評估活動更多地停留在學術階段,缺乏向決策轉化的實現方法和路徑的宣傳、培訓以及激勵;此外,國內現有的HTA機構呈現零散分布,相互之間聯系甚微,無法形成評估合力來實現有效決策輔助。參考借鑒德國的經驗,在大環境中,借助政府力量,切實建立起透明的、多方參與的、具有決策影響力的HTA決策轉化路徑,并保證完善相關的宣傳和激勵等保障機制配套建設,通過完善路徑引導、鼓勵和促進政府真正進行循證決策。
3.3 建立國家層面的獨立HTA機構并構建我國HTA決策成果共享網絡平臺,推進我國HTA決策轉化體系建設
德國基于國家層面三大HTA機構的各自HTA決策轉化運行順暢,并且HTA機構之間也形成了有效的共享機制:HTA方法指南以及HTA報告成果等不僅在G-BA、IQWiG等的官方網站中被及時公示以供各方參考學習,而且在應用早期就形成了國家層面的HTA信息庫;此外,聯邦公報也公布相關成果以便進行更廣范圍的成果傳播。信息共享和廣泛的成果傳播不僅有利于決策轉化過程,更有利于決策轉化后的政策落地。
在我國,尚沒有形成有影響的HTA成果共享,導致很多相類似的評估在低水平的重復進行,很大程度上浪費了研究資源,也無助于我國HTA的整體質量提升和HTA有效決策轉化。查看我國目前已有的HTA組織機構官方網站信息,發現僅有國家衛計委內部評估機構網站等提供了項目介紹以及決策轉化成果傳播信息。國際經驗證明實現HTA的整體式發展、高質量建設,不同評估機構間的成果共享網絡平臺建設非常必要。[10]建議首先建立國家層面的獨立HTA機構,發展成熟后可嘗試在省市級支援組建HTA機構,根據各地實際差異致力于地方決策轉化實施,基于現實需求,進行及時、獨立、客觀地循證決策活動,更好地滿足多元化的決策需要。同時將各HTA機構納入同一網絡實現資源共享和決策轉化成果傳播,積極穩妥推進我國HTA決策轉化體系建設。
[1] Drummond M F,Schwartz J S,J?nsson B,et al. Key principles for the improved conduct of health technology assessments for resource allocation decisions[J]. International journal of technology assessment in health care, 2008, 24(3): 244-258.
[2] World Health Organization. 2015 Global Survey on Health Technology Assessment by National Authorities[R]. Geneva:WHO Document Production Services, 2015.
[3] 陳英耀, 劉文彬, 耿勁松, 等. 發展我國衛生技術評估的政策建議[J]. 中國衛生質量管理, 2015, 22(1): 61- 64.
[4] 王海銀, 何達, 王賢吉, 等. 國內外衛生技術評估應用進展及建議[J]. 中國衛生政策研究, 2014, 7(8): 19-23.
[5] 陳潔, 于德志, 耿慶山. 衛生技術評估[M].1版. 北京: 人民衛生出版社, 2013.
[6] Fricke F U, Dauben H P, 宗欣, 等. 衛生技術評估: 德國視角[J]. 中國藥物經濟學, 2010(1): 12.
[7] 李珍, 趙青. 德國社會醫療保險治理體制機制的經驗與啟示[J]. 德國研究, 2015(2): 9.
[8] 張倩, 陳英耀, 應曉華. 法國、德國、荷蘭衛生技術評估發展歷程及思考[J]. 中國衛生質量管理, 2011, 18(1): 4-7.
[9] Perleth M, Gibis B, Gohlen B. A short history of health technology assessment in Germany [J]. Int J Technol Assess Health Care, 2009, 25(Suppl 1): 112-119.
[10] 呂蘭婷, 王虎峰. 我國藥品支付價格形成及談判定價中引入衛生技術評估的路徑探討[J]. 中國藥房, 2015, 26(15): 2020-2023.
(編輯 薛云)
Paths and methods of decision-making transformation for health technology assessment in Germany
LVLan-ting,FURong-hua
HealthReformandDevelopmentCenter,SchoolofPublicAdministrationandManagement,RenminUniversityofChina,Beijing100872,China
Germany has a similar health insurance system as China, and has already formed standardized management processes as well as efficient decision-making transformation paths for health technology assessment (HTA) that perform well mainly based on three major HTA institutions at the national level. The HTA decision-making transformation system in Germany has proven to be a typical representative in evidence-based decision-making for health policies worldwide. Based on the outcomes of literature analysis and field research, this paper summarizes the paths and methods of Germany’s HTA decision-making transformation, and finally proposes several targeted policy recommendations to promote the HTA decision-making transformation in China
Health technology assessment; Decision-making transformation; Evidence-based decision-making; Germany
中國人民大學科學研究基金(中央高校基本科研業務費專項資金資助)項目(15XNQ005) 作者簡介: 呂蘭婷,女(1983年—),博士,副教授,主要研究方向為衛生政策、衛生經濟、決策分析模型與衛生資源管理。 E-mail:lanting.lu@ruc.edu.cn 付榮華
R197
A
10.3969/j.issn.1674-2982.2017.04.009
2016-05-29
2016-12-08

