MnOx/ZSM-5催化劑催化NO氧化性能的研究
孫保民, 楊曉初, 肖海平, 萬震天, 汪 濤
(華北電力大學 電站設備狀態監測與控制教育部重點實驗室,北京 102206)
?
MnOx/ZSM-5催化劑催化NO氧化性能的研究
孫保民, 楊曉初, 肖海平, 萬震天, 汪 濤
(華北電力大學 電站設備狀態監測與控制教育部重點實驗室,北京 102206)
為實現快速選擇性催化還原(SCR)反應條件,開發低成本NO氧化催化劑,采用浸漬法制備了不同Mn負載量的MnOx/ZSM-5催化劑,采用電感耦合等離子體(ICP)、X射線衍射(XRD)、掃描電子顯微鏡(SEM)和N2吸附/脫附等技術對催化劑特征進行了表征,并考察了其催化NO氧化活性.結果表明:Mn負載量對MnOx/ZSM-5催化劑催化NO氧化的活性有顯著影響,較高的負載量可以提供更多的反應中心,但過高的負載量會導致活性組分在催化劑表面積聚,減小催化劑比表面積和降低表面分散度.Mn負載量為5.2%的樣品表現出最佳的NO催化氧化效率,400 ℃下NO轉化率達到50.6%,但低溫下催化NO氧化活性較差,還需進一步優化制備條件,以提高MnOx/ZSM-5催化劑的反應性能.
催化氧化; 錳基催化劑; NO; 快速SCR
NOx是主要的大氣污染物,其危害廣泛.根據NOx的形成特點,NOx的控制技術大致可分為燃燒前、燃燒中和燃燒后處理3大類.其中,用于尾部煙氣的選擇性催化還原(SCR)方法應用最為廣泛[1-2].
典型的SCR反應使用NH3作為還原劑,在氧氣存在的條件下,通過催化劑將NO還原為N2,并生成H2O,如式(1)所示.
4NH3+4NO+O2←→4N2+6H2O
(1)
隨著NOx中NO2比例的提高,系統中還會發生快速SCR反應(式(2))和NO2-SCR反應(式(3)和式(4)).在諸多研究中證實,快速SCR反應比常規SCR反應和NO2-SCR反應具有更快的反應速率,快速SCR反應可以顯著降低還原NOx所需的反應溫度[3-5].
4NH3+2NO+2NO2←→4N2+6H2O
(2)
8NH3+6NO2←→7N2+12H2O
(3)
2NH3+2NO2←→N2+N2O+3H2O
(4)
為實現快速SCR反應所需的反應工況,需要提高煙氣中NO2比例,將部分NO氧化為NO2,使得NO2在總NOx中所占體積分數提高至50%左右.
Pt基催化劑展現出優異的催化NO氧化性能[6-7],但其造價昂貴,難以實現大規模應用.MnOx為活性組分的催化劑,由于其優秀的氧化還原特性,已被廣泛用于脫硝反應的研究中,并展現出良好的催化NO氧化活性[8-10].但Mn基催化劑存在抗硫性差的問題,研究者們通過引入助劑以提高Mn基催化劑的抗硫性能.于國峰等[11]在其研究中引入鈰(Ce)作為助劑,顯著提高了Mn/TiO2催化劑的抗硫性能,Ce的加入會使SO2在催化劑表面的吸附及催化劑Lewis酸性位的消失得到有效抑制,同時還能降低硫酸鹽在催化劑表面的穩定性,從而提高催化劑的抗硫性能.Chang等[12]使用錫(Sn)作為助劑,有效改善了MnOx-CeO2催化劑的抗硫性能,Sn的加入顯著提高了氧空位濃度和表面酸性,有利于催化反應的進行.
分子篩催化劑在NOx選擇性還原過程中熱穩定性較好,N2選擇性高,且催化劑失活后易于再生和回收處理[13].其中,ZSM-5分子篩具有豐富的三維孔道和酸性位,可以提供優越的反應空間和電子環境,有利于活性金屬氧化物的分散[14].任曉光等[15]以ZSM-5為載體制備了CuO/ZSM-5催化劑,使用CH4作為還原劑,獲得了良好的脫硫脫硝效果.王坤鵬等[16]使用離子交換法制備了一系列Cu/ZSM-5催化劑,5種催化劑樣品在170~190 ℃范圍內先后達到接近100%的最高凈化效率.
筆者通過浸漬法制備了一系列MnOx/ZSM-5催化劑,并對其催化NO氧化性能進行考察,探索MnOx/ZSM-5催化劑作為快速SCR反應預氧化催化劑的可能性.
1 實驗
1.1 材料和試劑
實驗中所使用H-ZSM-5分子篩購自南開大學催化劑廠,硅鋁物質的量比為25.使用50%Mn(NO3)2溶液(分析純,國藥試劑)作為MnOx前驅體.實驗用水均為去離子水.
1.2 催化劑制備
使用等體積浸漬法制備了不同Mn負載量(即Mn元素質量分數,下同)的MnOx/ZSM-5催化劑.為了獲得預定Mn負載量的催化劑,使用去離子水將50%Mn(NO3)2溶液稀釋至所需濃度,取10 g H-ZSM-5加入特定濃度的Mn(NO3)2溶液中,使用超聲波強化分子篩與溶液混合3 h.浸漬后樣品在105 ℃下干燥12 h,空氣氛圍550 ℃煅燒2 h.催化劑成品經粉碎、篩分后,選取粒徑250~425 μm樣品備用.所得催化劑依次記為Mn(y)/ZSM-5,y為催化劑樣品中Mn負載量.
1.3 催化劑表征
電感耦合等離子體(ICP)測試用于對MnOx/ZSM-5樣品中Mn元素質量分數進行定量分析.測試通過IRIS Intrepid II XSP等離子體發射光譜儀進行,等離子體功率為1 150 W.
X射線衍射(XRD)分析測試通過Bruker D8 Advance射線衍射儀進行,Cu靶、Kα射線,掃描角度10°~80°,掃描速率0.2 (°)/s.
樣品的比表面積通過Micromeritics Tristar 3020 II型N2吸附儀測定.采用BET法測定比表面積及平均孔徑.
催化劑表面形貌通過FEI QUNTA 650掃描電子顯微鏡(SEM)進行測定,工作電壓為1 kV.
1.4 實驗裝置
實驗室自行搭建的固定床反應裝置如圖1所示.石英反應器高800 mm、內徑12 mm,外用電爐加熱,程序升溫控制,使用K型熱電偶對反應器內溫度進行測定.實驗氣體來自鋼瓶氣,使用質量流量計(北京匯博隆儀器)對各氣體體積流量進行控制.使用Testo350煙氣分析儀對反應器出、入口NO和NO2體積分數進行測量.
1.5 NO吸附-脫附性能測試
NO吸附-脫附性能測試在自建反應裝置上進行,每次實驗裝入1 g催化劑樣品.NO吸附過程在室溫下進行,吸附時通入體積流量為1 L/min的混合氣體(NO體積分數為0.1%,其余為N2),待樣品吸附飽和后,停止通入NO,使用N2(體積流量為1 L/min)吹掃30 min后開始脫附實驗.脫附實驗中,樣品在室溫下以20 K/min的速率升溫到500 ℃,載氣為N2,體積流量為1 L/min.使用Testo350煙氣分析儀記錄反應器出口NO和NO2體積分數的變化.
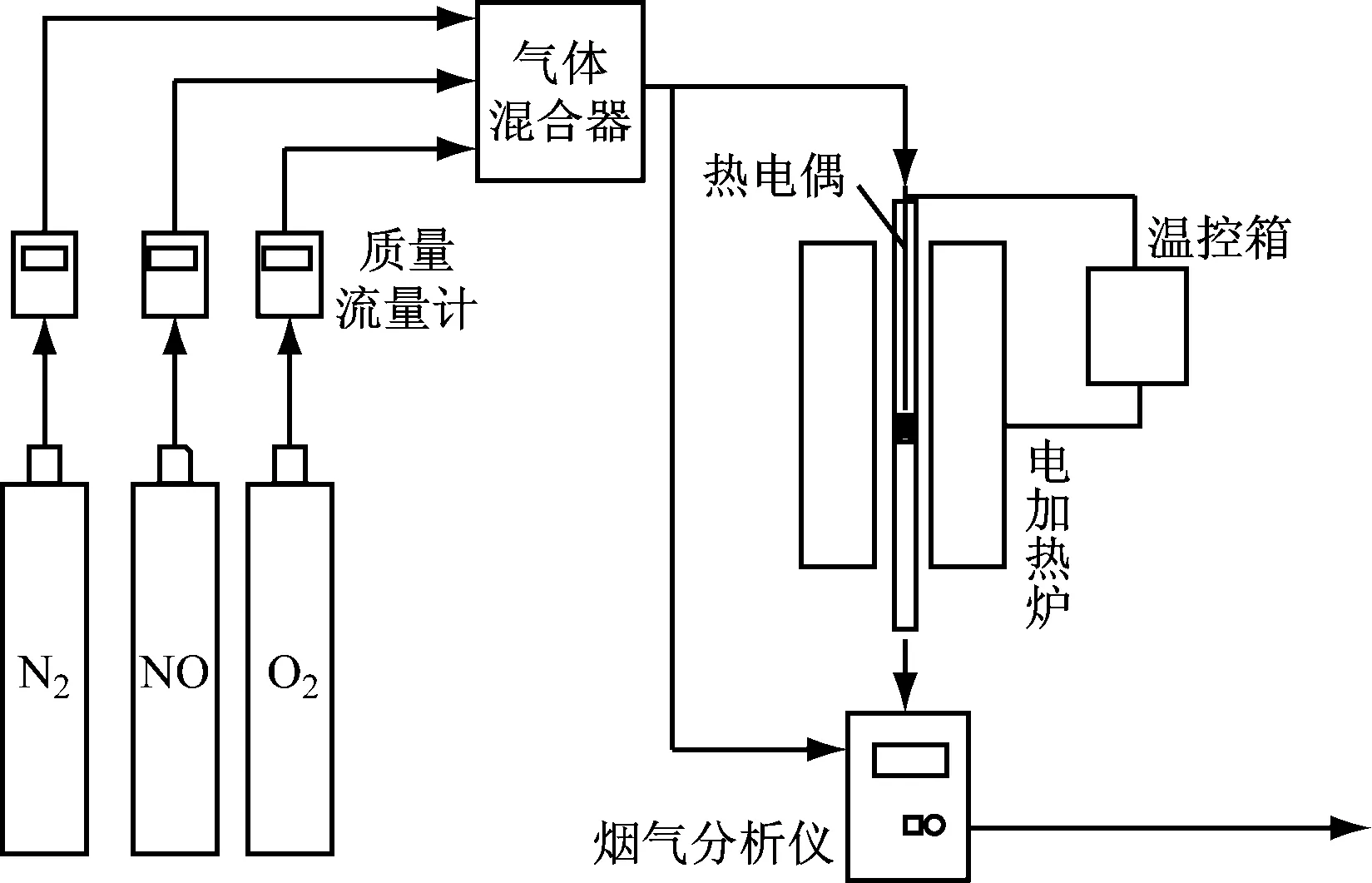
圖1 實驗裝置簡圖
1.6 催化NO氧化性能實驗
催化NO氧化性能實驗同樣在自建固定床反應器上進行.實驗溫度范圍為50~500 ℃.反應器入口氣體總體積流量為1 L/min,其中NO體積分數為0.1%,O2體積分數為5%,其余為N2.每次實驗裝入1 g催化劑樣品,體積空速約為30 000 h-1.使用Testo350煙氣分析儀對反應器入口及出口NO和NO2體積分數進行檢測.通過如下公式得到NO轉化率X(NO)、NO2生成率X(NO2)和NO2選擇性S(NO2):
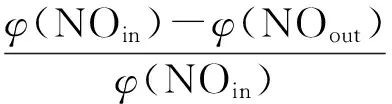
(5)
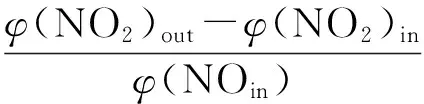
(6)
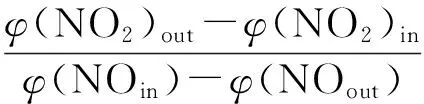
(7)
在考察O2體積分數對催化NO氧化性能的影響時,反應器入口O2體積分數在1%~8%變化,其他反應條件不變.通過記錄反應器出、入口NO體積分數,得到該反應條件下NO轉化率.
2 結果與討論
2.1 MnOx/ZSM-5催化劑的表面物理特性
使用ICP對催化劑樣品中Mn負載量進行測定,得到4種催化劑樣品Mn負載量分別為2.5%、5.2%、10.1%和19.8%.
表1為MnOx/ZSM-5催化劑的比表面積和平均孔徑,H-ZSM-5分子篩具有較大的比表面積,其比表面積為365.28 m2/g,有利于活性組分在催化劑表面的分散.將MnOx負載于H-ZSM-5載體后,樣品比表面積有所減小,且樣品的比表面積隨Mn負載量的增加而減小.其中,Mn負載量為2.5%和5.2%的樣品比表面積略有減小,分別為310.98 m2/g和307.42 m2/g,仍可為催化反應提供充足的反應環境;負載量最大的樣品比表面積減小最為明顯,Mn(19.8)/ZSM-5樣品的比表面積僅為253.46 m2/g,說明負載量過高,活性組分MnOx填充到ZSM-5的孔道,不利于催化反應的進行.MnOx負載后的催化劑,平均孔徑分布也略有變化,但各樣品的平均孔徑均遠大于NO、O2和NO2等氣體的分子直徑.較大的比表面積有利于反應氣體在催化劑表面的吸附和快速脫附,有利于促進化學反應的進行,從而提高催化劑的催化性能.
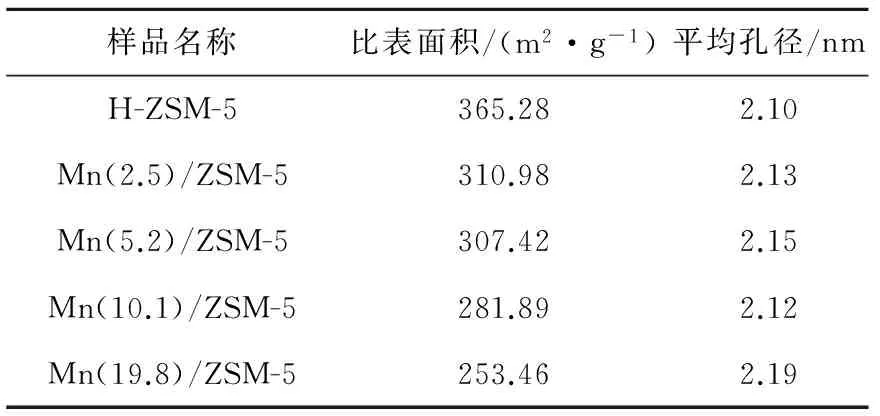
表1 催化劑樣品比表面積和平均孔徑
圖2為不同Mn負載量的MnOx/ZSM-5催化劑的XRD譜圖,催化劑樣品在2θ= 23.3°、29.3°和45.5°處均出現了ZSM-5的衍射峰,說明Mn元素加入未對ZSM-5的晶體結構產生影響.4種樣品中,Mn負載量高于10.1%樣品的XRD譜圖中,在2θ=32.9°和38.2°處出現了明顯的Mn2O3衍射峰,表明采用上述方法制備的MnOx/ZSM-5催化劑中活性組分MnOx主要以Mn2O3的形式存在.這也與其他學者研究得到的結論一致[17-18].在Mn負載量較小的樣品中未出現MnOx晶相的衍射峰,表明在Mn負載量<10.1%的樣品中,MnOx在催化劑表面以無定形的形式存在,具有更好的分散度,更有利于催化反應的進行.
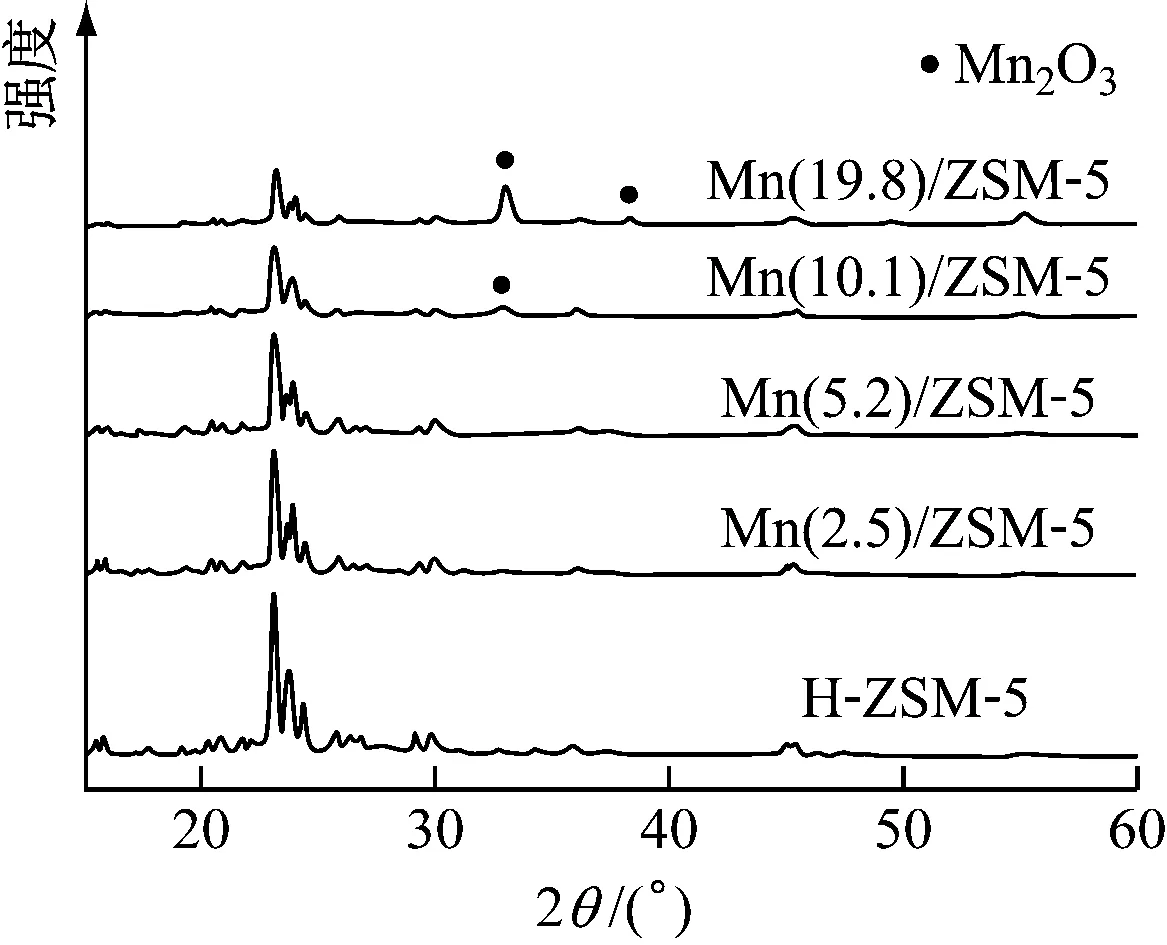
圖2 MnOx/ZSM-5催化劑的XRD譜圖
圖3為MnOx/ZSM-5催化劑的SEM照片.從圖3可以看到,Mn(5.2)/ZSM-5樣品催化劑活性組分分散度較好,部分ZSM-5晶粒邊緣可見亮白色MnOx物質;Mn(19.8)/ZSM-5樣品表面活性組分負載量過高,導致活性組分分散度降低并阻塞ZSM-5孔道,比表面積減小,不利于催化反應的進行.這也與N2吸附/脫附及XRD表征結果相一致.

(a) Mn(5.2)/ZSM-5樣品
2.2 NO程序升溫脫附
圖4所示為MnOx/ZSM-5催化劑NO程序升溫脫附測試曲線.其中,圖4(a)為NO脫附特性曲線,4種催化劑樣品分別在低溫段(110 ℃附近)和高溫段(370 ℃附近)出現2個NO脫附峰.Guo等[17]在其研究中指出,NO會被MnOx表面活性氧氧化為NO2,NO2進一步被氧化為硝酸鹽.因而,110 ℃附近的脫附峰主要來自弱吸附的NO解吸附,而370 ℃附近的脫附峰來源于催化劑表面硝酸鹽的分解.Mn(2.5)/ZSM-5樣品具有最大的比表面積,有利于NO氣體的弱吸附,因此低溫段NO脫附量最大.但由于其Mn負載量低,不能為NO的進一步反應提供足夠的反應中心,高溫段NO脫附量最低.其余3個樣品最大NO脫附峰均出現在高溫段,其中Mn(5.2)/ZSM-5樣品NO脫附量最大.圖4(b)為NO2脫附特性曲線,與NO脫附曲線類似,催化劑表面NO2脫附峰分別出現在130 ℃附近和350 ℃附近.根據之前所述NO在MnOx表面吸附和氧化機理,低溫下NO2脫附峰主要來源于NO被表面氧氧化后生成的NO2,高溫脫附峰來源于硝酸鹽的分解.在低溫段,Mn(2.5)/ZSM-5和Mn(5.2)/ZSM-5樣品表面可觀察到較為明顯的NO2脫附峰,說明較大的比表面積及較好的表面分散度有利于NO2從催化劑表面釋放,較高的負載量會導致NO2的進一步氧化,但4種樣品低溫段NO2脫附量均遠小于高溫段NO2脫附量.在350 ℃附近,4種樣品均出現明顯的NO2脫附峰,說明表面硝酸鹽為NO在MnOx/ZSM-5表面吸附的主要產物.4種樣品中,Mn(5.2)/ZSM-5高溫下NO和NO2脫附量最大,表明其具有較多的MnOx反應中心和更好的表面分散度,有利于NO吸附和反應的進行,因而Mn(5.2)/ZSM-5樣品表面有更多的硝酸鹽產物生成.
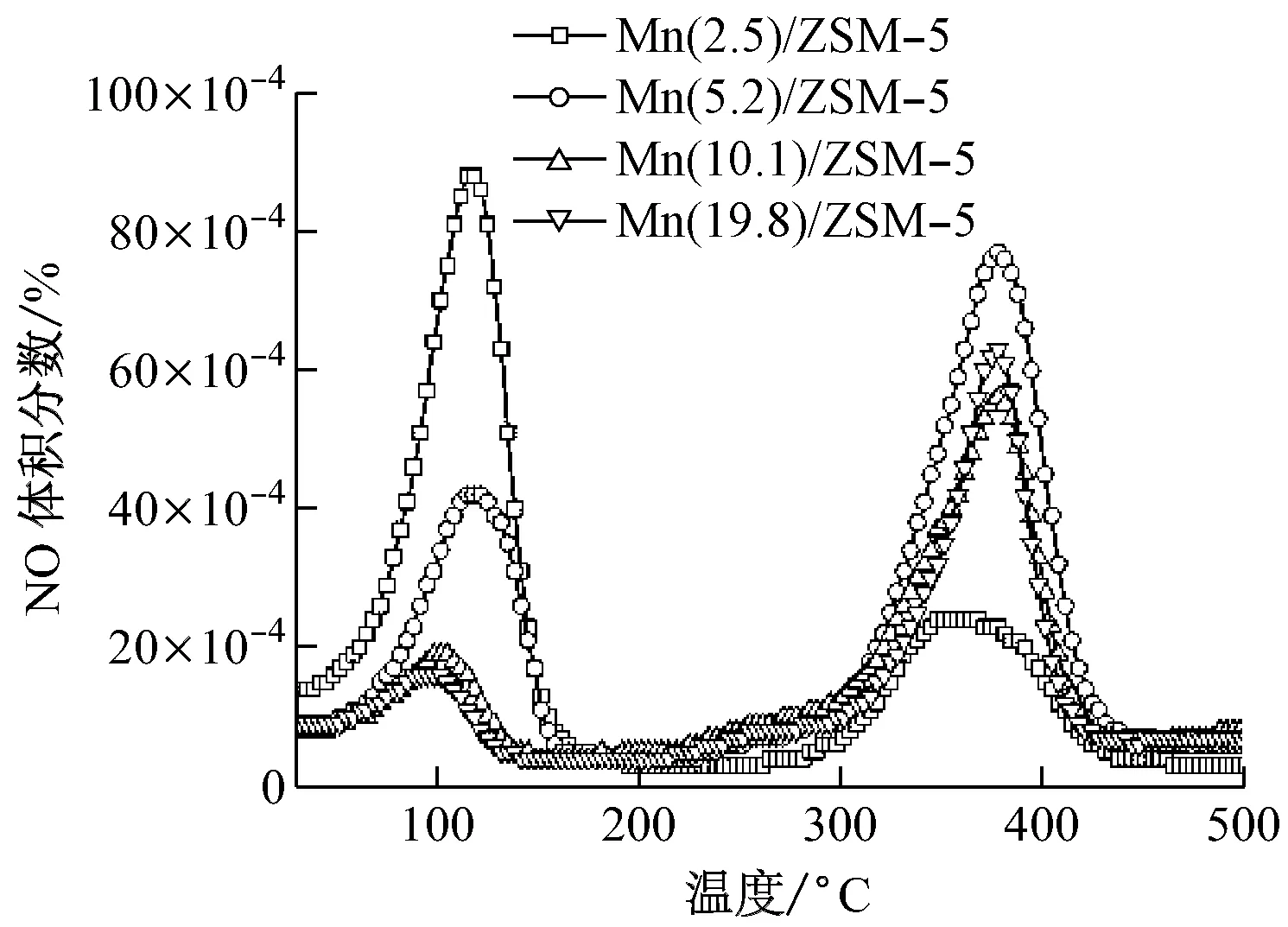
(a) NO體積分數
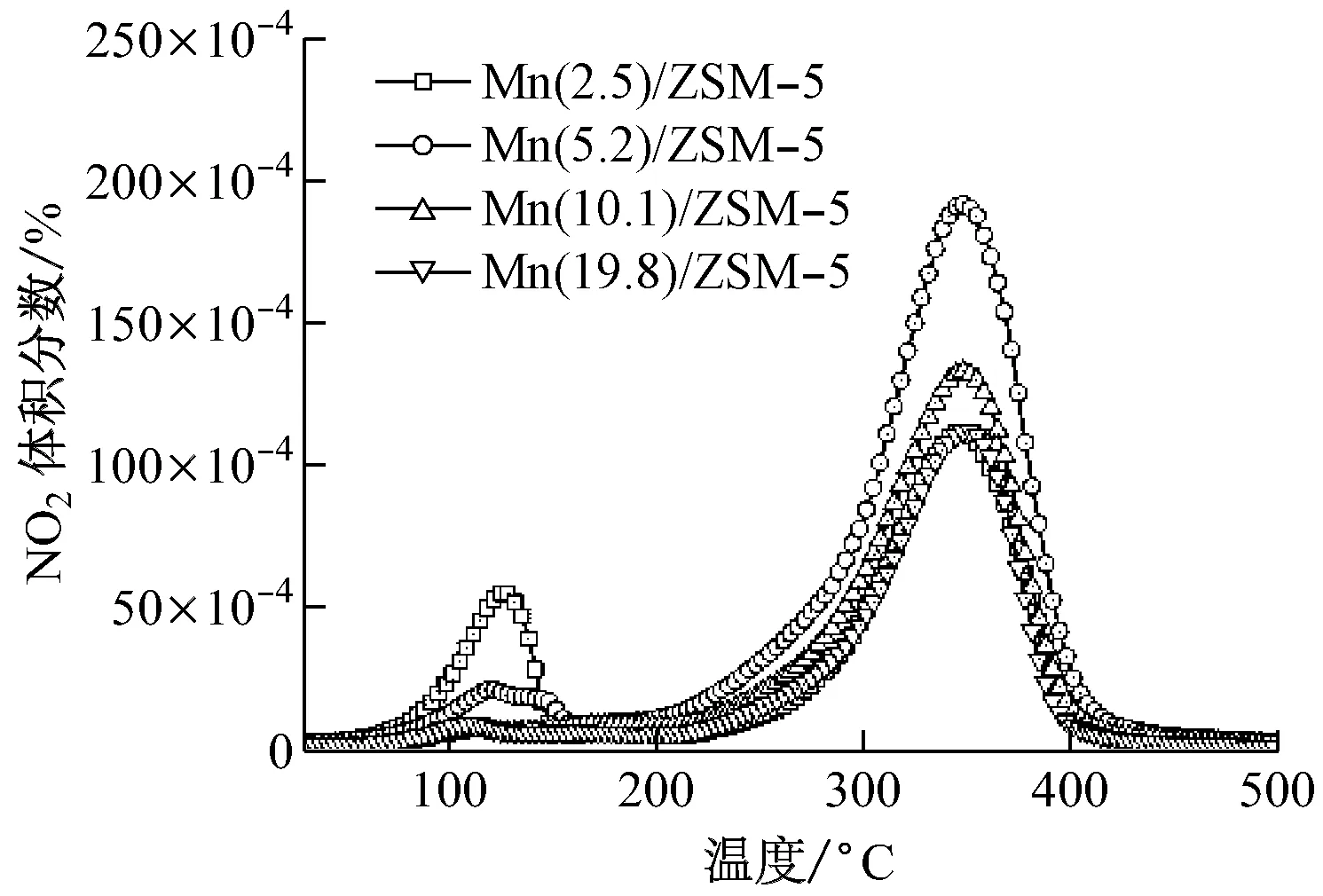
(b) NO2 體積分數
2.3 MnOx/ZSM-5催化氧化NO性能實驗
圖5(a)為4種Mn負載量樣品催化NO氧化性能.從圖5(a)可以看到,低溫下反應主要受動力學限制,NO的轉化率隨著反應溫度的升高而升高.在反應溫度低于250 ℃時,4種樣品均未表現出很好的催化NO氧化效果.當反應溫度高于250 ℃后,NO轉化率明顯上升,并在400 ℃達到最大.4種樣品中,Mn(5.2)/ZSM-5樣品表現出了最為優異的催化效果,400 ℃下實現50.6%的最大催化NO轉化率.在反應溫度高于400 ℃后,反應受熱力學限制,NO轉化率降低.圖5(b)為Mn(5.2)/ZSM-5樣品催化NO氧化反應的NO2生成率及選擇性分析.從圖5(b)可見,NO2的生成特性與NO轉化特性一致,NO2的生成率先隨反應溫度的升高而升高,在溫度高于400 ℃后,受熱力學限制,生成率降低.NO2的選擇性同樣受反應溫度的影響,在低于250 ℃的溫度下,由于未達到表面硝酸鹽的分解溫度,NO2的選擇性較差,吸附在MnOx/ZSM-5表面的NO主要轉化為硝酸鹽.在反應溫度高于250 ℃后,表面硝酸鹽分解,NO2選擇性明顯提升,且在溫度高于400 ℃后,并未隨NO2生成率的下降發生明顯變化,在250~500 ℃的實驗范圍內,NO2的選擇性均保持在90%左右,NO2是MnOx/ZSM-5催化NO氧化的主要產物,且NO2主要來源于表面硝酸鹽的分解.
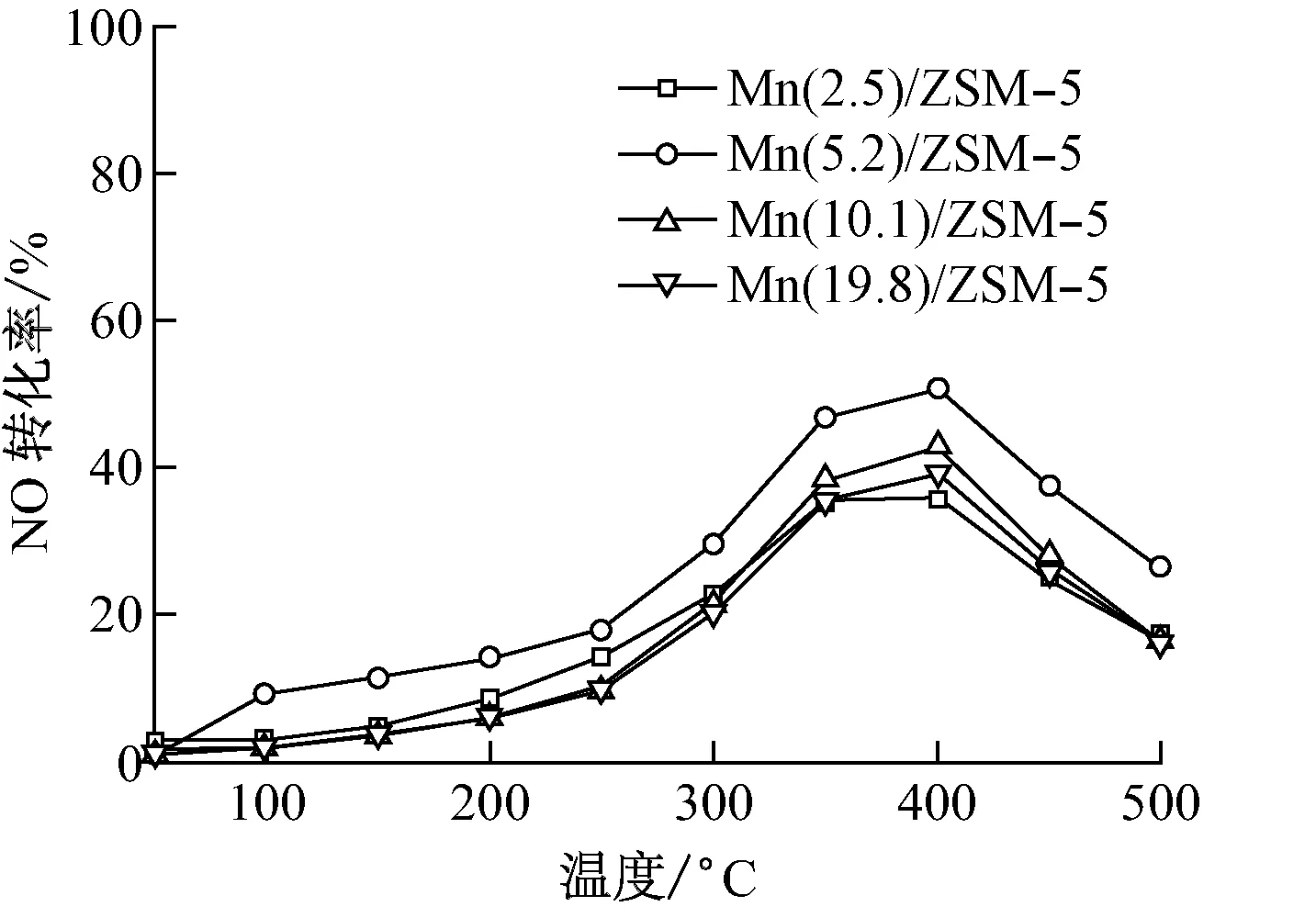
(a) NO轉化率
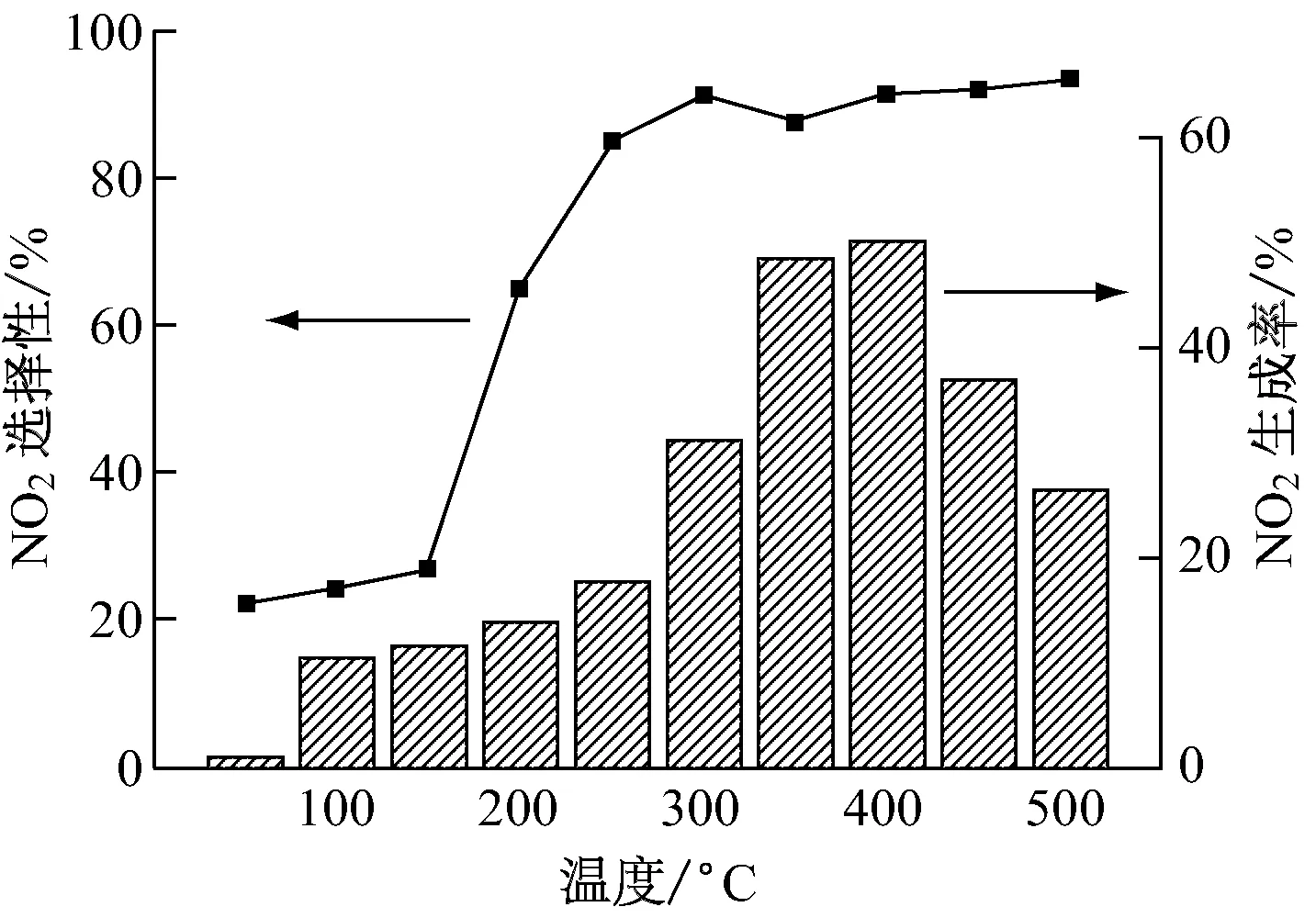
(b) Mn(5.2)/ZSM-5樣品的NO2生成率及選擇性
Tang等[19]在其研究中指出,硝酸鹽是NO氧化為NO2過程中的重要中間產物,NO首先在Mn活性位上吸附生成亞硝酰基,之后被活性氧氧化為硝酸鹽,硝酸鹽分解生成NO2.Zhao等[20]在對MnOx/TiO2催化劑的研究中得到了相似的結論,NO和O2吸附在MnOx表面后生成亞硝酸鹽和硝酸鹽,亞硝酸鹽和硝酸鹽分解釋放出NO2,并且在MnOx存在的情況下,亞硝酸鹽可以迅速地被氧化為硝酸鹽.
還有研究者對沸石分子篩催化NO氧化的性能進行了研究.Loiland等[21]在其研究中指出,H型沸石分子篩對NO氧化有一定的催化作用,配位在分子篩骨架位上的NO+是反應的重要中間產物.Akter等[22]對幾種H型分子篩催化NO和NH3氧化的活性進行了考察,實驗結果證明H型分子篩對催化NO氧化具有一定的活性,且較小的孔徑有利于反應的進行,但在實驗范圍內(100~450 ℃),H型分子篩NO催化氧化效率未高于4%.
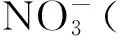
*+NO←→*-NO+
(8)
(9)
(10)
*+1/2O2←→O*
(11)
NO+1/2O2←→NO2
(12)
與其他研究者制備的Mn基催化劑相比,實驗中MnOx/ZSM-5并未展現出足夠高的低溫催化NO氧化活性.程俊楠等[8]以二氧化鋯為載體,制備了Mn/ZrO2催化劑,在300 ℃下獲得了84%的最高NO轉化率.同時,他們還對Mn/ZrO2催化劑催化NO氧化的機理進行了總結,認為在低溫下NO的反應速率>NO的吸附速率>NO2的脫附速率,NO2的脫附速率為速率控制步,高溫下則完全相反,NO2的脫附速率>NO的吸附速率>NO的反應速率,反應速率主要受NO反應速率的限制.Zhao等[20]在其研究中指出,氧化鋯同時具有酸堿性和氧化還原性,作為載體時易與活性組分發生相互作用,因而可提高催化劑的反應活性.
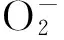
Chen等[24]在其研究中指出,載體種類對于過渡金屬的催化活性具有很大影響,并且煅燒溫度、煅燒次數、MnOx負載量和稻殼灰的制備溫度4項制備條件中,煅燒溫度對MnOx/稻殼灰催化劑的NO氧化活性影響最大.
通過以上分析可以得知,載體的性能對于Mn基催化劑催化NO氧化性能具有顯著的影響,TiO2和ZrO2由于具有很好的儲氧能力、優秀的氧化還原性能、并可以與活性組分相互作用,從而可提高催化劑的反應活性.同時,煅燒溫度等制備條件也對催化劑的反應活性有很大的影響.文中所制備的MnOx/ZSM-5催化劑在低溫下NO2脫附量低、NO2選擇性差,吸附后的NO絕大部分轉化為硝酸鹽停留在催化劑表面,NO2主要來源于高溫下表面硝酸鹽的分解,因而低溫下催化NO氧化活性較差.同時,ZSM-5作為載體對于NO氧化反應沒有體現出明顯的促進作用,MnOx/ZSM-5催化劑催化NO氧化性能的表現與其他學者研究中單一組分MnOx催化NO氧化的性能十分接近[23].在后續的研究中,還需要進一步完善制備方法,通過引入助劑、控制反應條件等方式提高MnOx/ZSM-5低溫催化NO氧化活性.
2.4 O2體積分數對催化氧化NO效果的影響
圖6給出了O2體積分數對NO催化氧化效率的影響,選用的催化劑樣品為Mn(5.2)/ZSM-5.在各O2體積分數下,NO催化氧化效率均呈現出隨反應溫度的升高先提高后下降的趨勢,在400 ℃達到最大.在O2體積分數<5%時,各反應溫度下催化劑均未表現出優異的NO催化氧化性能;相同溫度下催化NO氧化效率隨O2體積分數的升高而提高,O2體積分數對NO轉化效果作用明顯,是反應的控制因素.隨著O2體積分數的升高,O2體積分數對催化效果的影響減弱,O2體積分數高于5%后,各溫度下NO催化氧化效率的變化規律趨于一致,NO催化氧化效率并未隨O2體積分數改變發生明顯變化,NO轉化率主要受反應溫度的影響.O2體積分數低于5%時,O2體積分數對反應影響顯著,提高O2體積分數可以顯著提高NO催化氧化效率,但在O2體積分數高于5%后,O2體積分數的影響可以忽略,反應溫度等條件對催化NO氧化的效率具有更大影響.
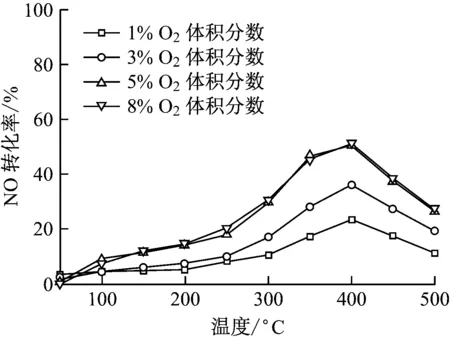
圖6 O2體積分數對NO催化氧化效率的影響
3 結 論
(1) 采用浸漬法制備了一系列MnOx/ZSM-5催化劑,活性組分負載量對催化劑活性具有很大影響.較高的負載量可以為催化劑提供更多的活性中心,但過高的負載量會導致催化劑表面活性組分的積聚,阻塞分子篩孔道,降低催化劑比表面積及表面分散度,不利于催化反應的進行.
(2) 經550 ℃煅燒后,Mn在催化劑表面主要以Mn2O3的形式存在.O2體積分數較低時,NO轉化率隨O2體積分數的升高而提高,O2體積分數高于5%后,O2體積分數不再對NO催化氧化效率產生明顯影響.
(3) Mn負載量為5.2%的樣品具有較大的比表面積、較好的表面分散度和較為豐富的反應中心,吸附NO后表面硝酸鹽生成量最大,表現出最佳的催化NO氧化活性,400 ℃下NO轉化率達到50.6%.
(4) 所制備的MnOx/ZSM-5催化劑低溫下催化NO催化氧化效率較差,NO2的生成主要來源于高溫下表面硝酸鹽的分解.在后續的研究中,還需要進一步優化制備條件,引入助劑,以提高MnOx/ZSM-5催化劑的反應活性及抗硫性能.
[1] 張楚瑩, 王書肖, 邢佳, 等. 中國能源相關的氮氧化物排放現狀與發展趨勢分析[J]. 環境科學學報, 2008, 28(12): 2470-2479.
ZHANG Chuying, WANG Shuxiao, XING Jia, et al. Current status and future projections of NOxemissions from energy related industries in China[J]. Acta Scientiae Circumstantiae, 2008, 28(12): 2470-2479.
[2] 李德波, 廖永進, 徐齊勝. 我國電站鍋爐SCR脫硝系統服役過程中的運行規律[J]. 動力工程學報, 2014, 34(6): 477-481.
LI Debo, LIAO Yongjin, XU Qisheng. Operation status of SCR denitrification system for domestic power boilers[J]. Journal of Chinese Society of Power Engineering, 2014, 34(6): 477-481.
[3] KOEBEL M, ELSENER M, MADIA G. Reaction pathways in the selective catalytic reduction process with NO and NO2at low temperatures[J]. Industrial & Engineering Chemistry Research, 2001, 40(1): 52-59.
[4] GROSSALE A, NOVA I, TRONCONI E, et al. NH3-NO/NO2SCR for diesel exhausts after treatment: reactivity, mechanism and kinetic modelling of commercial Fe-and Cu-promoted zeolite catalysts[J]. Topics in Catalysis, 2009, 52(13): 1837-1841.
[5] IWASAKI M, SHINJOH H. A comparative study of “standard”, “fast” and “NO2” SCR reactions over Fe/zeolite catalyst[J]. Applied Catalysis A: General, 2010, 390(1/2): 71-77.
[6] AUVRAY X, OLSSON L. Stability and activity of Pd-, Pt-and Pd-Pt catalysts supported on alumina for NO oxidation[J]. Applied Catalysis B: Environmental, 2015, 168-169: 342-352.
[7] AUVRAY X, PINGEL T, OLSSON E, et al. The effect gas composition during thermal aging on the dispersion and NO oxidation activity over Pt/Al2O3catalysts[J]. Applied Catalysis B: Environmental, 2013, 129: 517-527.
[8] 程俊楠,張先龍,楊保俊,等.催化氧化NO催化劑Mn/ZrO2的制備與性能研究[J]. 環境科學學報, 2014, 34(3): 620-629.
CHENG Junnan, ZHANG Xianlong, YANG Baojun, et al. Preparation and NO catalytic oxidation activity of Mn/ZrO2catalyst[J]. Acta Scientiae Circumstantiae, 2014, 34(3): 620-629.
[9] 安忠義, 禚玉群, 陳昌和. 煅燒溫度對Mn/TiO2催化劑催化NO氧化活性的影響[J]. 燃料化學學報, 2014, 42(3): 370-376.
AN Zhongyi, ZHUO Yuqun, CHEN Changhe. Influence of calcination temperature on the catalytic activity of Mn/TiO2for NO oxidation[J]. Journal of Fuel Chemistry and Technology, 2014, 42(3): 370-376.
[10] QI G, LI Wei. NO oxidation to NO2over manganese-cerium mixed oxides[J]. Catalysis Today, 2015, 258: 205-213.
[11] 于國峰, 顧月平, 金瑞奔. Mn/TiO2和Mn-Ce/TiO2低溫脫硝催化劑的抗硫性研究[J]. 環境科學學報, 2013, 33(8): 2149-2157.
YU Guofeng, GU Yueping, JIN Ruiben. Effects of SO2on the low-temperature SCR Mn/TiO2and Mn-Ce/TiO2catalysts[J]. Acta Scientiae Circumstantiae, 2013, 33(8): 2149-2157.
[12] CHANG Huazhen, CHEN Xiaoyin, LI Junhua, et al. Improvement of activity and SO2tolerance of Sn-modified MnOx-CeO2catalysts for NH3-SCR at low temperatures[J]. Environmental Science & Technology, 2013, 47(10): 5294-5301.
[13] 許俊強, 張丹, 郭芳, 等. 新型高效高穩定NOx催化還原用分子篩催化劑的研究進展[J]. 硅酸鹽學報, 2015, 43(2): 241-250.
XU Junqiang, ZHANG Dan, GUO Fang, et al. Development on novel highly efficient and stable molecular sieve catalysts for catalytic reduction of nitrogen oxide[J]. Journal of the Chinese Ceramic Society, 2015, 43(2): 241-250.
[14] ZHU Lin, ZHANG Lei, QU Hongxia, et al. A study on chemisorbed oxygen and reaction process of Fe-CuOx/ZSM-5 via ultrasonic impregnation method for low-temperature NH3-SCR[J]. Journal of Molecular Catalysis A: Chemical, 2015, 409: 207-215.
[15] 任曉光, 李富霞, 李鵬. CuO/ZSM-5系列催化劑的脫硫脫硝性能研究[J]. 環境科學學報, 2013, 33(6): 1728-1733.
REN Xiaoguang, LI Fuxia, LI Peng. Desulfurization and denitrifition properties of the CuO/ZSM-5 catalysts[J]. Acta Scientiae Circumstantiae, 2013, 33(6): 1728-1733.
[16] 王坤鵬, 宋崇林, 賓峰, 等. Cu/ZSM-5分子篩催化劑SCR催化性能[J]. 燃燒科學與技術, 2012, 18(1): 73-78.
WANG Kunpeng, SONG Chonglin, BIN Feng, et al. Performance of selective catalytic reduction over Cu/ZSM-5 zeolite catalysts[J]. Journal of Combustion Science and Technology, 2012, 18(1): 73-78.
[17] GUO Li, XIAN Hui, LI Qifeng, et al. NO adsorption behaviors of the MnOxcatalysts in lean-burn atmospheres[J]. Journal of Hazardous Materials, 2013, 260: 543-551.
[18] LOU Xiaorong, LIU Pengfei, LI Jun, et al. Effects of calcination temperature on Mn species and catalytic activities of Mn/ZSM-5 catalyst for selective catalytic reduction of NO with ammonia[J]. Applied Surface Science, 2014, 307: 382-387.
[19] TANG Nian, LIU Yue, WANG Haiqiang, et al. Mechanism study of no catalytic oxidation over MnOx/TiO2catalysts[J]. The Journal of Physical Chemistry C, 2011, 115(16): 8214-8220.
[20] ZHAO Baohuai, RAN Rui, WU Xiaodong, et al. Comparative study of Mn/TiO2and Mn/ZrO2catalysts for NO oxidation[J]. Catalysis Communications, 2014, 56: 36-40.
[21] LOILAND J A, LOBO R F. Oxidation of zeolite acid sites in NO/O2mixtures and the catalytic properties of the new site in NO oxidation[J]. Journal of Catalysis, 2015, 325: 68-78.
[22] AKTER N, HAN Lixin, HUAMAN D, et al. NO and NH3oxidation over zeolite materials[J]. Materials Today: Proceedings, 2016, 3(2): 550-555.
[23] AN Zhongyi, ZHUO Yuqun, XU Chao, et al. Influence of the TiO2crystalline phase of MnOx/TiO2catalysts for NO oxidation[J]. Chinese Journal of Catalysis, 2014, 35(1): 120-126.
[24] CHEN Guoqing, GAO Jihui, XU Lili, et al. Optimizing conditions for preparation of MnOx/RHA catalyst particle for the catalytic oxidation of NO[J]. Advanced Powder Technology, 2012, 23(2): 256-263.
Study on Catalytic Activity of MnOx/ZSM-5 for NO Oxidation
SUN Baomin, YANG Xiaochu, XIAO Haiping, WAN Zhentian, WANG Tao
(MOE's Key Laboratory of Condition Monitoring and Control for Power Plant Equipment, North China Electric Power University, Beijing 102206, China)
To achieve fast SCR reaction conditions, low-cost MnOx/ZSM-5 catalysts with different Mn loadings were prepared for NO oxidation using incipient impregnation method, which were subsequently characterized by ICP, XRD, SEM and N2adsorption/desorption technology, so as to study their activities on NO oxidation. Results show that the catalytic activity is significantly affected by the Mn loading. High Mn loading provides more reaction sites, but excessively high Mn loading would cause aggregation of active components, thus reducing the specific surface area and lowering the surface dispersion of catalysts. The sample with 5.2% Mn loading has the best catalytic activity, in which case, the NO conversion rate can reach the maximum value of 50.6% at 400 ℃. However, the catalytic activity for NO oxidation is unsatisfactory at lower temperatures, therefore, to further improve the reaction performance of MnOx/ZSM-5 catalysts, the preparation conditions need to be optimized.
catalytic oxidation; Mn-based catalyst; NO; fast SCR
2016-06-03
2016-07-22
中央高校基本科研業務費專項資金資助項目(JB2015RCY06)
孫保民(1959-),男,山東聊城人,教授,博士,研究方向為高效清潔燃燒及低污染控制. 楊曉初(通信作者),男,博士研究生,電話(Tel.):15911126011;E-mail:yxcncepu@163.com.
1674-7607(2017)06-0475-08
X701.3
A
610.30

