干擾素聯合恩替卡韋治療HBeAg陽性慢性乙型肝炎的療效及安全性分析
楊旭,鄒園濤,曾妮
(1 南昌大學第四臨床醫學院,南昌 330031;2 南昌大學公共衛生學院)
干擾素聯合恩替卡韋治療HBeAg陽性慢性乙型肝炎的療效及安全性分析
楊旭1,鄒園濤1,曾妮2
(1 南昌大學第四臨床醫學院,南昌 330031;2 南昌大學公共衛生學院)
目的 比較干擾素(IFN)聯合恩替卡韋(ETV)與IFN、ETV單用對HBeAg陽性慢性乙型肝炎患者的療效和安全性。方法 計算機檢索PubMed、EMbase、Cochrane Library、知網、萬方、維普等數據庫,收集以IFN聯合ETV、IFN或ETV單獨使用為主要干預措施,對HBeAg陽性的慢性乙型肝炎患者進行治療的隨機對照試驗,數據資料用Review Manager5.0進行分析。結果 ①共納入12篇隨機對照試驗研究,1 313例HBeAg陽性慢性乙型肝炎患者。②與單用ETV相比,IFN聯合ETV治療患者HBV DNA低于下限率在治療后48周(RR=1.21,95%CI:1.03~1.41)增加,HBeAg轉陰率在治療后12周(RR=1.72,95%CI:1.06~2.81)、24周(RR=1.84,95%CI:1.34~2.68)和48周(RR=1.76,95%CI:1.42~2.17)增加,HBeAg轉換率在治療后24周(RR=1.62,95%CI:1.16~2.28)和48周(RR=1.82,95%CI:1.46~2.27)增加。③與單用IFN相比,IFN聯合ETV治療患者ALT復常率在治療后12周(RR=1.47,95%CI:1.14~1.89)、24周(RR=1.74,95%CI:1.47~2.06)和48周(RR=1.37,95%CI:1.22~1.54)增加,HBV DNA低于下限率在治療后12周(RR=2.02,95%CI:1.52~2.68)、24周(RR=1.90,95%CI:1.57~2.30)和48周(RR=1.42,95%CI:1.26~1.61)增加,HBeAg轉陰率在治療后24周(RR=1.80,95%CI:1.34~2.43)和48周(RR=1.38,95%CI:1.16~1.65)增加,HBeAg轉換率在治療后24周(RR=1.75,95%CI:1.17~2.60)和48周(RR=1.38,95%CI:1.09~1.73)增加。④IFN聯合ETV治療與單用ETV或IFN相比不良反應無統計學差異。結論 HBeAg陽性的慢性乙型肝炎患者聯合使用IFN與ETV的療效優于單用ETV或IFN,并且安全。
慢性乙型肝炎;聯合治療;干擾素;恩替卡韋;HBeAg陽性;Meta分析
慢性乙型肝炎是由乙型肝炎病毒(HBV)持續感染引起的肝臟慢性炎癥性疾病,是全球性的重大公共衛生問題[1,2],且肝炎病毒引起的死亡在全球死因排名上升到第7位[3]。全球HBsAg陽性的慢性乙型肝炎攜帶者約有2.48億,其中20%~30%患者會出現肝硬化、肝癌等嚴重的并發癥,且每年超過68.6萬人死于此類并發癥[4,5]。目前治療慢性乙型肝炎的主要藥物有干擾素(IFN)和核苷(酸)類似物(NAs),但兩類藥物在臨床實踐中對HBeAg陽性的慢性乙型肝炎患者治療效果仍不理想[6]。我國2015年慢性乙型肝炎防治指南顯示,同步聚乙二醇干擾素(PEG-IFN)α與NAs的聯合治療方案能否提高療效仍不明確[7]。恩替卡韋(ETV)作為一種高耐藥屏障的NAs類藥物,聯用IFN對HBeAg陽性的慢性乙型肝炎患者療效尚存在爭議。因此本研究采用Meta分析方法綜合評價IFN聯合ETV對HBeAg陽性慢性乙型肝炎的療效和安全性,以期為臨床決策提供依據。
1 資料與方法
1.1 檢索策略 計算機檢索PubMed、EMbase、Cochrane Library、中國知網(CNKI)、萬方數據知識服務平臺(WanFang Data)、維普中文科技期刊數據庫(VIP),檢索時限均為建庫起至2016年7月26日。中文檢索詞包括干擾素、恩替卡韋、慢性乙型肝炎、乙型肝炎、HBeAg、隨機對照實驗、隨機;英文檢索詞包括interferon、entecavir、chronic hepatitis B、HBeAg positive、randomized controlled trial;并通過引文追蹤法查找可能遺漏的相關文獻。
1.2 納入與排除標準 納入標準:①隨機對照試驗,無論是否采用盲法;②HBeAg陽性需要治療的慢性乙型肝炎患者;③聯合組的干預措施為IFN-α注射聯合ETV口服治療,對照組為單用IFN-α或ETV治療,聯合治療時間至少6個月;④聯合組和對照組在年齡、性別、生化等方面具有均衡的可比性,治療各組具有單一變量;⑤中英文文獻。排除標準:①合并感染丙型肝炎、人類免疫缺陷病毒;②合并有失代償期肝硬化、其他非病毒性慢性肝臟疾病、肝功能失代償、肝移植者等;③有IFN治療禁忌證(如總膽紅素≥10×正常值上限,中性粒細胞計數<1.0×109/L,血小板計數<50×109/L,精神病史等);④伴有嚴重的肝腎功能障礙者、妊娠及哺乳期女性、未控制的甲狀腺疾病患者、惡性腫瘤患者等;⑤6個月內接受過抗病毒、免疫調節劑治療。
1.3 有效性、安全性評價方法 比較聯合組與對照組的HBeAg轉陰率和轉換率、HBV DNA低于下限率、ALT復常率等進行有效性評價:比較聯合組與對照組的不良反應發生率進行安全性評價。
1.4 文獻篩選、資料提取及納入研究的偏倚風險評價 兩位評價員獨立篩選文獻、提取資料并交叉核對。文獻篩選時首先閱讀文題和摘要進行初篩,在排除明顯不相關的文獻后,進一步閱讀全文進行復篩,以確定最終是否納入。資料提取內容主要包括:①納入研究的基本信息,包括第一作者、發表時間等;②研究對象的基線特征(各組的樣本數、患者的年齡、性別等);③干預措施的治療類型、治療時間、隨訪時間等;④結局指標。本文對納入文獻的質量評價依照Cochrane Handbook for Systematic Reviews 5.1.0中推薦的隨機對照試驗偏倚風險方法進行[8]。
1.5 統計學方法 采用RevMan 5.0統計軟件。計數資料采用相對危險度(RR)為效應指標,各效應量均給出其點估計值和95%CI,納入研究結果間的異質性運用χ2檢驗(檢驗水準為α=0.100),同時結合I2定量判斷異質性的大小。當P≥0.1時,各研究結果間無統計學異質性,則采用固定效應模型進行Meta分析;當P<0.1、I2>50%時,各研究結果間存在統計學異質性,則進一步分析異質性來源,對可能導致異質性的因素進行亞組分析,若未找到明顯的臨床異質性來源,則采用隨機效應模型。Meta分析的檢驗水準為α=0.05。納入研究數量較多時采用“倒漏斗圖”評價發表偏倚。
2 結果
2.1 文獻檢索結果 初檢共獲得相關文獻953篇,排除了220篇重復性文章,根據論文題目及摘要篩選得到82篇文獻,通過引文追蹤法新納入1篇文獻,再排除與納入及排除標準本研究不符的文獻71篇,共納入12篇文獻[9~20],其中中文9篇、英文3篇。
2.2 納入文獻的基本特征 納入12篇文獻中共有1 313例HBeAg陽性慢性乙型肝炎患者,其中接受IFN聯合ETV治療587例、ETV單藥治療475例、IFN單藥治療251例;治療方案中采用從頭聯合治療方案8篇[9,10,12~16,19]、序貫聯合治療2篇[11,17]、追加聯合治療2篇[18,20]。所有的文獻顯示基線特征具有可比性。
2.3 納入研究的偏倚風險評價結果 納入研究隨機序列產生的偏倚多為不清楚,分配隱藏多為高風險,研究者和受試者施盲均不清楚,研究結局盲法評定為低風險,結局數據的完整性、報告偏倚及其他偏倚多為低風險。納入文獻的各類偏倚風險結果提示偏倚風險較低。
2.4 各組治療有效性比較
2.4.1 ALT復常率 與單用ETV相比,ALT復常率在IFN聯合ETV治療患者治療后12、24、48周比較差異無統計學意義,見表1。與單用IFN相比,ALT復常率在IFN聯合ETV治療患者治療后12周(RR=1.47,95%CI:1.14~1.89)、24周(RR=1.74,95%CI:1.47~2.06)和48周(RR=1.37,95%CI:1.22~1.54)均增加,見表2。
2.4.2 HBV DNA低于下限率 與單用ETV相比,HBV DNA低于下限率在IFN聯合ETV治療患者治療后12、24周比較差異無統計學意義,在48周(RR=1.21,95%CI:1.03~1.41)增加,見表1。與單用IFN相比,HBV DNA低于下限率在IFN聯合ETV治療患者治療后12周(RR=2.02,95%CI:1.52~2.68)、24周(RR=1.90,95%CI:1.57~2.30)和48周(RR=1.42,95%CI:1.26~1.61)均增加,見表2。
2.4.3 HBeAg轉陰率 與單用ETV相比,HBeAg轉換率在IFN聯合ETV治療患者治療后12周(RR=1.72,95%CI:1.06~2.81)、24周(RR=1.84,95%CI:1.34~2.68)和48周(RR=1.76,95%CI:1.42~2.17)增加,見表1。與單用IFN相比,HBeAg轉換率在IFN聯合ETV治療患者治療后12周比較差異無統計學意義,在24周(RR=1.80,95%CI:1.34~2.43)和48周(RR=1.38,95%CI:1.16~1.65)增加,見表2。
2.4.4 HBeAg轉換率 與單用ETV相比,HBeAg轉換率在IFN聯合ETV治療患者治療后12周比較差異無統計學意義,在24周(RR=1.62,95%CI:1.16~2.28)和48周(RR=1.82,95%CI:1.46~2.27)增加,見表1。與單用IFN相比,HBeAg轉換率在IFN聯合ETV治療患者治療后12周比較差異無統計學意義,在24周(RR=1.75,95%CI:1.17~2.60)和48周(RR=1.38,95%CI:1.09~1.73)增加,見表2。
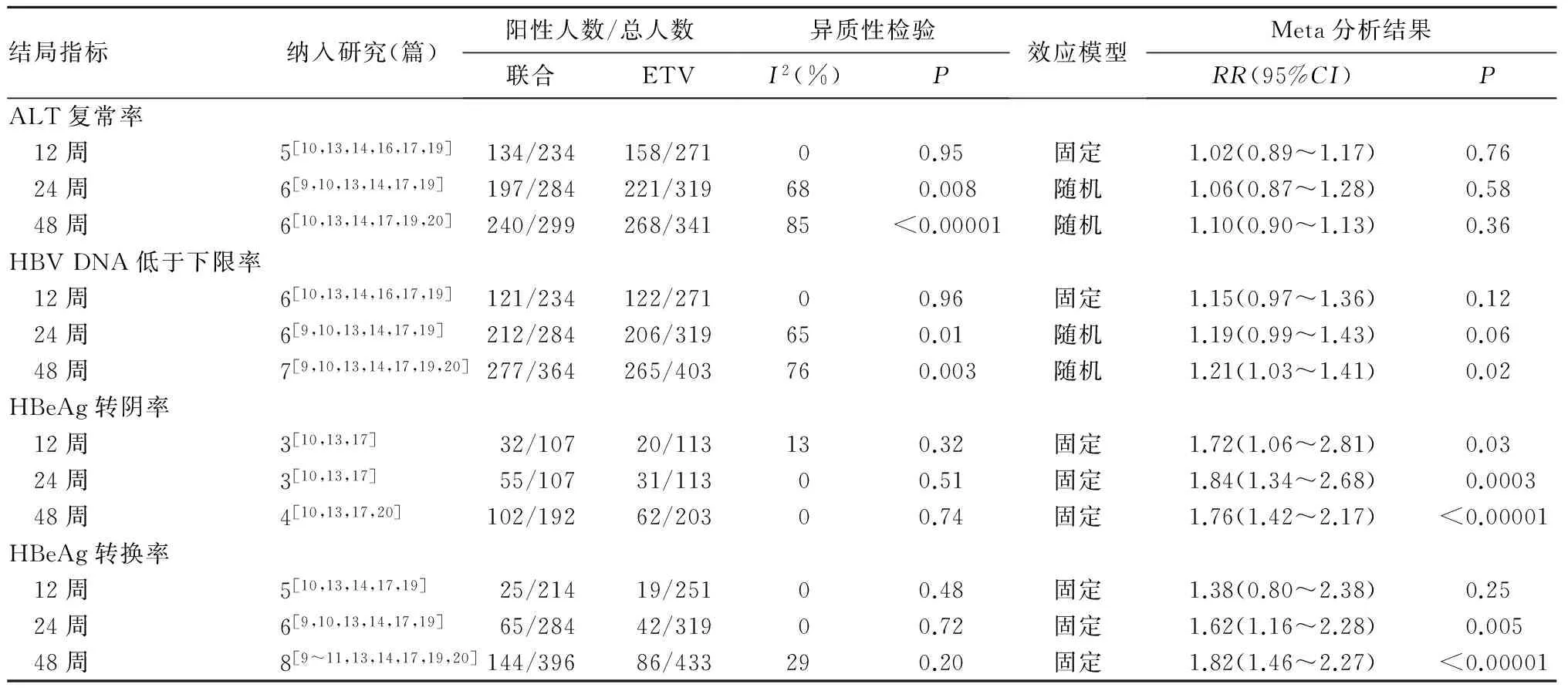
表1 ETV聯合IFN與單用ETV治療HBeAg陽性慢性乙型肝炎的療效比較

表2 ETV聯合IFN與單用IFN治療HBeAg陽性慢性乙型肝炎的療效比較
2.5 各組不良反應比較 共9篇文獻[9,10,13~16,18~20]報告了不良反應,包括發熱、全身疼痛、皮膚瘙癢、白細胞減少、血小板降低等,此類癥狀經對癥治療后大多消失,未對慢性乙型肝炎的治療產生影響。其中,7篇文獻[9,13~16,18,19]表明組間不良反應比較無統計學差異,有2篇文獻[10,20]表明組間不良反應比較差異有統計學意義,但嚴重不良反應比較無統計學差異或都經對癥治療后好轉。
2.6 發表偏倚 用以ETV為對照組的8篇文獻[9~11,13,14,17,19,20]聯合治療48周的HBeAg轉換率來評價聯合治療的文獻的發表偏倚,圖示研究位點呈左右對稱排列,多分布在虛線兩側,且多向上方和中部集中,僅有1篇文獻[11]落在中下部,提示文獻發表性偏倚風險較小。用以IFN為對照組的5篇文獻[10,15,17~19]聯合治療48周的HBeAg轉換率來評價發表偏倚,結果顯示發表性偏倚風險亦較小。
3 討論
HBeAg陽性的慢性乙型肝炎患者有著高的HBV DNA載量和HBeAg陽性狀態,這兩種狀態均能增加肝癌的發生的風險[21,22]。一般認為乙肝“病毒治愈”的概率較小,而“臨床治愈”成為治療的最終目標。HBsAg轉換就被認為乙肝被“臨床治愈”,HBsAg清除被認為是接近乙肝“臨床治愈”的標志,而HBeAg轉換是HBsAg清除的重要必備條件,故降低HBV DNA載量、HBeAg狀態的轉換對HBeAg陽性的慢性乙型肝炎患者具有重要的意義[23]。
在HBeAg陽性慢性乙型肝炎患者治療中,單用PEG-IFNα-2a治療48周后實現31%的HBeAg轉換率[24];而單用ETV 48周后,67%的患者實現了HBV DNA低于下限率,21%實現HBeAg轉換[25]。在本次Meta分析中,聯合治療48周HBeAg轉換率和HBV DNA低于下限率39.2%和61.3%,較單用ETV組和IFN組均有提高。
近期的隨機對照試驗研究發現,PEG-IFNα-2a聯合NAs在HBeAg陰性且持續HBV DNA低于下限的慢性乙型肝炎患者與單用NAs對比并不能顯著提高HBsAg清除率[26];而PEG-IFNα-2a聯合替諾福韋(TDF)治療慢性乙型肝炎患者,與PEG-IFN或TDF單藥治療相比均有更好的HBsAg轉陰率,尤其是在基因型是A型或HBeAg陽性的患者中[27]。一項回顧性研究發現ETV序貫聯合PEG-IFN治療在滿足HBeAg<200 S/CO、HBsAg<1 000 IU/mL和12周HBsAg水平下降>0.5 log10IU/mL的這類HBeAg陽性慢性乙型肝炎患者能取得良好的應答[28]。提示聯合IFN和NAs類藥物在某些經過選擇的HBeAg陽性的慢性乙型肝炎患者效果可能最佳。
針對本次Meta分析結果,與單用ETV相比,聯合IFN用藥能顯著增加HBeAg應答、HBV DNA應答,但對ALT應答無顯著差異,隨著時間的延長,效益值(即RR值)有遞增的趨勢。這提示在以ETV為基礎的聯合IFN治療的療程越長,獲益可能越多。IFN通過免疫調節和抗病毒作用等機制來治療慢性乙型肝炎[2]。慢性乙型肝炎患者通常顯示低效或無效的病毒特異性T細胞應答活性[29],而基于PEG-IFN的聯合治療能誘導HBV特異性T細胞的恢復[30],還能影響記憶T細胞的數量和質量[31]。本研究分析得出,聯合治療效益值隨時間變化趨勢,可能與IFN隨著聯合治療的時間增加效益亦隨之增加有關[32],也有可能與聯合治療的方式不同有關。
與單用IFN相比,聯合ETV用藥能顯著提高HBeAg應答、HBV DNA應答、ALT應答,隨著時間的延長,聯合治療的RR值有先增加后降低的趨勢,在24周時效益值普遍最大。這提示以IFN為基礎的聯合ETV的治療在療程前期獲益明顯,后期獲益有下降的趨勢。ETV能通過顯著抑制逆轉錄中前基因組RNA(pgRNA)逆轉錄到HBV DNA從而降低HBV DNA載量,抑制病毒的復制[2],故能顯著提高HBeAg應答、HBV DNA應答、ALT應答。除了直接抑制逆轉錄,深入研究還發現ETV亦能通過調節Tregs細胞和細胞因子等來調節自身免疫系統,改善機體對HBV的免疫應答[33]。本研究分析得出聯合治療在療程前期獲益明顯,后期獲益有下降的趨勢,這可能與ETV等NAs藥物HBeAg的應答率較低相關[34],也可能與聯合治療后期和治療后療效維持不佳有關[18],也有可能與聯合治療的方式不同有關。
本研究也存在一些不足之處:①納入研究的結局指標不一,如對HBsAg結果的觀察多未出現,HBV DNA低于下限的指標標準不同;②治療時間不一,且多數研究未進行隨訪;③聯合用藥方案、時間和劑量也存在差別,如IFN的劑量和類型不完全統一;④HBV基因型、cccDNA、肝組織學多未測;⑤納入文獻亦存在一定的偏倚風險,尤其是在分配隱藏和盲法上;⑥因納入的研究仍較少,亦無法按照IFN種類、聯合治療方案、高病毒載量與否等進行亞組分析。
綜上所述,HBeAg陽性的慢性乙型肝炎患者聯合使用IFN與ETV的療效優于單用ETV或IFN,并且是安全的。受納入研究的質量和數量所限,本研究結論(尤其是長期療效)尚需開展更多高質量、大規模、長時間、多中心隨機對照試驗研究予以驗證。
[1] WHO Guidelines Approved by the Guidelines Review Committee. Guidelines for the prevention, care and treatment of persons with chronic hepatitis B infection[M]. Geneva: World Health Organization, 2015:45-61.
[2] Trépo C, Chan HL, Lok A. Hepatitis B virus infection[J]. Lancet, 2014,384(9959):2053-2063.
[3] Stanaway JD, Shepard DS, Undurraga EA, et al. The global burden of dengue: an analysis from the Global Burden of Disease Study 2013[J]. Lancet Infect Dis, 2016,16(6):712-723.
[4] Schweitzer A, Horn J, Mikolajczyk RT, et al. Estimations of worldwide prevalence of chronic hepatitis B virus infection: a systematic review of data published between 1965 and 2013[J]. Lancet, 2015,386(10003):1546-1555.
[5] Van Damme P. Long-term Protection After Hepatitis B Vaccine[J]. J Infect Dis, 2016,214(1):1-3.
[6] Lampertico P, Maini M, Papatheodoridis G. Optimal management of hepatitis B virus infection-EASL Special Conference[J]. J Hepatol, 2015,63(5):1238-1253.
[7] 中華醫學會肝病學分會,中華醫學會感染病學分會.慢性乙型肝炎防治指南(2015更新版)[J].中華肝臟病雜志,2015,23(12):888-905.
[8] Higgins JP, Altman DG, Gotzsche PC, et al. The Cochrane Collaboration′s tool for assessing risk of bias in randomised trials[J]. BMJ, 2011,343:d5928.
[9] Liu CJ, Wang CC, Yang SS, et al. 758 entecavir plus peginterferon alfa-2a vs. entecavir alone in thetreatment of hepatttis B e antigen-positive chronic hepatttis B: an interim report[J]. J Hepatol, 2013,58:S308.
[10] 李晶.α-干擾素聯合恩替卡韋治療慢性乙型肝炎早期療效[J].肝臟,2012,17(10):714-716.
[11] 徐敏.臨床觀察恩替卡韋序貫聚乙二醇干擾素α-2a治療HBeAg陽性慢性乙型肝炎的療效[J].山西職工醫學院學報,2016,26(1):36-38.
[12] 趙春紅,程開.恩替卡韋聯合干擾素治療乙型肝炎患者的臨床療效觀察[J].齊齊哈爾醫學院學報,2015,32(15):2214-2215.
[13] 陳炎生,費新應,劉文濤,等.干擾素α-1b聯合恩替卡韋治療HBeAg陽性慢性乙型肝炎33例48周療效觀察[J].臨床內科雜志,2013,30(1):42-43.
[14] 任成儉,熊燕飛.聚乙二醇干擾素α-2a聯合恩替卡韋治療HBeAg陽性慢性乙型肝炎的臨床研究[J].醫學理論與實踐,2016,29(2):154-155.
[15] 丁艾昆,郭利偉,歐陽瑞春,等.聚乙二醇干擾素α-2a聯合核苷(酸)類似物治療HBeAg陽性慢性乙型肝炎的療效觀察[J].中國病原生物學雜志,2015,10(3):272-276.
[16] 曾文,袁靜,劉映霞,等.聚乙二醇干擾素alpha-2a聯合恩替卡韋治療高病毒載量HBeAg陽性慢性乙型肝炎的臨床研究[J].中華實驗和臨床病毒學雜志,2013,27(2):115-118.
[17] 張志敏,季寶玉,李琳.恩替卡韋聯合α-2b干擾素治療慢性乙型肝炎的療效觀察[J].蚌埠醫學院學報,2014,39(5):621-623.
[18] Xie Q, Zhou H, Bai X, et al. A randomized, open-label clinical study of combined pegylated Interferon Alfa-2a (40KD) and Entecavir treatment for Hepatitis B "e" Antigen-Positive Chronic Hepatitis B[J]. Clin Infect Dis, 2014,59(12):1714-1723.
[19] 李健.聚乙二醇干擾素聯合恩替卡韋治療HBeAg陽性慢性乙型肝炎患者的臨床觀察[D].石家莊:河北醫科大學,2015.
[20] Brouwer WP, Xie Q, Sonneveld MJ, et al. Adding peginterferon to entecavir for HBeAg-positive chronic hepatitis B: A multicentre randomized trial (ARES study)[J]. Hepatology, 2014,61(5):1512-1522.
[21] Yang HI, Lu SN, Liaw YF, et al. Hepatitis B e antigen and the risk of hepatocellular carcinoma[J]. N Engl J Med, 2002,347(3):168-174.
[22] Chen CJ, Yang HI, Su J, et al. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level[J]. JAMA, 2006,295(1):65-73.
[23] Liaw YF, Lau GK, Kao JH, et al. Hepatitis B e antigen seroconversion: a critical event in chronic hepatitis B virus infection[J]. Dig Dis Sci, 2010,55(10):2727-2734.
[24] Piratvisuth T, Lau G, Chao YC, et al. Sustained response to peginterferon alfa-2a (40 kD) with or without lamivudine in Asian patients with HBeAg-positive and HBeAg-negative chronic hepatitis B[J]. Hepatol Int, 2008,2(1):102-110.
[25] Chang TT, Gish RG, de Man R, et al. A comparison of entecavir and lamivudine for HBeAg-positive chronic hepatitis B[J]. N Engl J Med, 2006,354(10):1001-1010.
[26] Bourlière M, Rabiega P, Ganne-Carrie N, et al. Effect on HBs antigen clearance of addition of pegylated interferon alfa-2a to nucleos(t)ide analogue therapy versus nucleos(t)ide analogue therapy alone in patients with HBe antigen-negative chronic hepatitis B and sustained undetectable plasma hepatitis B virus DNA: a randomised, controlled, open-label trial[J]. Lancet Gastroenterol Hepatol, 2017,2(3):177-188.
[27] Marcellin P, Ahn SH, Ma X, et al. Combination of tenofovir disoproxil fumarate and peginterferon α-2a increases loss of hepatitis B surface antigen in patients with chronic hepatitis B[J]. Gastroenterology, 2016,150(1):134-144. e10.
[28] Li GJ, Yu YQ, Chen SL, et al. Sequential combination therapy with pegylated interferon leads to loss of hepatitis B surface antigen and hepatitis B e antigen (HBeAg) seroconversion in HBeAg-positive chronic hepatitis B patients receiving long-term entecavir treatment[J]. Antimicrob Agents Chemother, 2015,59(7):4121-4128.
[29] Ye B, Liu X, Li X, et al. T-cell exhaustion in chronic hepatitis B infection: current knowledge and clinical significance[J]. Cell Death Dis, 2015,6:e1694.
[30] de Niet A, Stelma F, Jansen L, et al. Restoration of T cell function in chronic hepatitis B patients upon treatment with interferon based combination therapy[J]. J Hepatol, 2016,64(3):539-546.
[31] Sun B, Wang Y, Meng Q, et al. Dynamics of memory T cells during treatment with interferon-alpha in patients with chronic hepatitis B[J]. Hepatol Res, 2010,40(8):806-812.
[32] Liaw YF, Jia JD, Chan HL, et al. Shorter durations and lower doses of peginterferon alfa-2a are associated with inferior hepatitis B e antigen seroconversion rates in hepatitis B virus genotypes B or C[J]. Hepatology, 2011,54(5):1591-1599.
[33] Jiang Y, Li W, Yu L, et al. Enhancing the antihepatitis B virus immune response by adefovir dipivoxil and entecavir therapies[J]. Cell Mol Immunol, 2011,8(1):75-82.
[34] Buti M. HBeAg-positive chronic hepatitis B: Why do I treat my patients with Nucleos (t) ide Analogs[J]. Liver Int, 2014,34(Suppl 1):108-111.
本刊2017年57卷18期第109頁發表的“哈蟆油抗衰老機制的研究進展”,作者單位為“1廣州軍區廣州總醫院,廣州510010;2廣東藥科大學中藥學院;3廣東省第二人民醫院”。
本刊編輯部
曾妮(E-mail: miracle_625@163.com)
10.3969/j.issn.1002-266X.2017.22.026
R512.6
B
1002-266X(2017)22-0068-05
2016-12-29)

