燈盞花素聯合補氣祛瘀中藥治療AECOPD療效及對免疫球蛋白、氧化應激指標的影響
施偉林陳 茜
(1.浙江省臺州市路橋區第二人民醫院,浙江 臺州 318058;2.恩澤醫療集團路橋院區,浙江臺州 308050)
燈盞花素聯合補氣祛瘀中藥治療AECOPD療效及對免疫球蛋白、氧化應激指標的影響
施偉林1陳 茜2
(1.浙江省臺州市路橋區第二人民醫院,浙江 臺州 318058;2.恩澤醫療集團路橋院區,浙江臺州 308050)
目的 觀察燈盞花素聯合補氣祛瘀中藥治療慢性阻塞性肺疾病急性加重期(AECOPD)療效及對免疫球蛋白、氧化應激指標的影響。方法 將患者130例以隨機數字表法分為對照組和中醫組,各65例,對照組給予西醫治療,中醫組在此基礎上加用燈盞花素聯合補氣祛瘀中藥治療,比較兩組患者臨床療效,治療前后中醫證候積分、肺功能指標、PFSDQ-M量表評分、免疫球蛋白G(IgG)、免疫球蛋白M(IgM)、免疫球蛋白A(IgA)、超氧化物歧化酶(SOD)及丙二醛(MDA)水平等。結果 中醫組患者治療總有效率顯著高于對照組(P<0.05);中醫組患者治療后中醫證候積分顯著低于對照組、治療前(P<0.05);中醫組患者治療后FEV1預計值和FEV1/FVC水平均顯著高于對照組、治療前(P<0.05);中醫組患者治療后PFSDQ-M量表評分顯著低于對照組、治療前(P<0.05);中醫組患者治療后免疫球蛋白水平顯著高于對照組、治療前(P<0.05);同時中醫組患兒治療后SOD和MDA水平顯著優于對照組、治療前(P<0.05)。結論 燈盞花素聯合補氣祛瘀中藥治療AECOPD可有效緩解臨床癥狀,改善肺部功能和生活質量,提高機體免疫力,并有助于調節SOD和MDA水平。
中西醫結合 AECOPD 免疫球蛋白 氧化應激
慢性阻塞性肺疾病(COPD)是一類以不完全可逆氣流受限為主要臨床特征的呼吸系統常見疾病,患者病情常呈進行性發展,而以感染為主多種因素誘發下可出現急性加重[1]。COPD急性加重期(AECOPD)患者可出現肺功能顯著下降,呼吸道癥狀加劇及生活質量惡化,且與住院患者死亡率上升增加關系密切[2]。目前西醫治療AECOP多采用對癥干預,但總體治療效果欠佳,無法延緩病情進展[3]。近年來中醫藥被廣泛用于AECOPD臨床治療,并在減輕呼吸道癥狀、提高生活質量及改善遠期預后方面取得確切效果[4]。本次研究以我院今年來收治的AECOPD患者共130例作為研究對象,分別給予西醫單用治療和在此基礎上加用燈盞花素聯合補氣祛瘀中藥治療,觀察中西醫結合治療AECOPD療效及對免疫球蛋白、氧化應激指標的影響。現報告如下。
1 資料與方法
1.1 病例選擇 納入標準 符合 《慢性阻塞性肺疾病診治指南(2013年修訂版)》西醫診斷標準[5];符合《慢性阻塞性肺疾病中醫證候診斷標準(2011版)》中醫辨證診斷標準[6];年齡45~75歲;患者家屬簽署知情同意書。排除標準:入組前4周服用相關中藥方劑者;急性發病時間>72 h;肺功能分級Ⅳ級者;合并重度呼吸衰竭者;肝腎功能不全者;精神系統疾病者;藥物過敏者;臨床資料不全者。
1.2 臨床資料 選取本院2014年8月至2016年8月收治AECOPD患者共130例。研究方案經醫院倫理委員會批準。患者按隨機數字表法隨機分為對照組和中醫組,各65例。其中對照組患者中男性40例,女性25例;年齡46~71歲,平均(64.29±5.52)歲;COPD病程2~14年,平均(7.27±1.70)年;急性發作病程10~27 h,平均(19.47±8.10)h。中醫組男性38例,女性27例;年齡45~73歲,平均(64.43±5.56)歲;COPD病程2~15年,平均(7.33±1.74)年;急性發作病程10~26 h,平均(19.40±8.06)h。兩組患者臨床資料比較差異無統計學意義(P>0.05)。
1.3 治療方法 對照組患者采用西醫治療,包括1)阿莫西林鈉舒巴坦鈉(山西仟源制藥有限公司生產,國藥準字H20020159,規格1.5 g)靜脈滴注,每日4~6 g;2)特布他林(北京首兒藥廠生產,國藥準字H19983193,規格2.5 mg)口服,每次2.5 mg,每日2次;3)乙酰半胱氨酸 (廣東人人康藥業有限公司生產,國藥準字H20000519,規格0.2 g),每次0.2 g,每日3次。中醫組患者則在此基礎上給予燈盞花素聯合補氣祛瘀中藥輔助治療,包括1)燈盞花素(朗致集團萬榮藥業有限公司生產,國藥準字Z14020180,規格2 mL∶5 mg),每次40 mg,每日1次;2)祛瘀中藥組方:魚腥草20 g,金銀花20 g,桔梗15 g,蘆根15 g,桑白皮15 g,瓜蔞15 g,黃芩15 g,葶藶子15 g,地龍15 g,浙貝母15 g,川牛膝15 g,川芎10 g,桃仁10 g,大黃8 g。加水300 mL煎至100 mL,分2次口服;而兩組患者治療時間均為14 d。
1.4 觀察指標 1)參照《中醫病證診斷療效標準》進行中醫證候積分計算[7]。主要證候包括咳喘、呼吸困難、痰多質稠、胸悶胸痛、食少脘痞便秘及唇甲紫紺,根據嚴重程度分為0,2,4,6分,分值越高提示癥狀越嚴重。2)肺功能指標。包括FEV1預計值和FEV1/FVC水平,檢測儀器采用上海歐啟電子科技有限公司生產MSA-99型肺功能檢測儀。3)生活質量評價采用PFSDQ-M量表評分[5]。主要內容包括日常活動變化、活動氣短、活動疲勞、呼吸困難及疲勞。4)實驗室指標包括免疫球蛋白 (IgG、IGA及IgM)和氧化應激指標(SOD和MDA);其中免疫球蛋白檢測采用免疫比濁法,超氧化物歧化酶(SOD)檢測采用超氧化物歧化酶法,丙二醛(MDA)檢測采用TBA反應比色法,試劑盒由北京中杉金橋生物技術有限公司提供。
1.5 療效標準 顯效:呼吸道癥狀體征明顯改善,中醫證候積分減分率>70%。有效:呼吸道癥狀體征有所改善,中醫證候積分減分率為>30%,且≤70%。無效:未達上述標準。治療總有效率=[(顯效例數+有效例數)/總例數]×100.00%[7]。
1.6 統計學處理 應用SPSS20.0統計軟件分析。計量資料以(±s)表示,采用t檢驗和χ2檢驗。P<0.05為差異有統計學意義。
2 結 果
2.1 兩組患者近期療效比較 見表1。中醫組患者治療總有效率顯著高于對照組(P<0.05)。

表1 兩組患者近期療效比較(n)
2.2 兩組患者治療前后中醫證候積分比較 見表2。中醫組治療后中醫證候積分顯著低于對照組、治療前(P<0.05)。
表2 兩組患者治療前后中醫證候評分比較(分,±s)

表2 兩組患者治療前后中醫證候評分比較(分,±s)
與本組治療前比較,*P<0.05;與對照組治療后比較,△P<0.05。下同。
組 別 時間 咳喘 呼吸困難 痰多質稠 胸悶胸痛 食少脘痞便秘 唇甲紫紺中醫組 治療前(n=65) 治療后對照組 治療前4.32±1.05 4.21±0.97 4.17±0.94 0.76±0.19*△0.90±0.20*△0.70±0.18*△4.39±1.08 4.17±0.95 4.12±0.90 3.88±0.81 0.81±0.19*△3.94±0.84 3.63±0.90 3.91±0.83 0.73±0.22*△0.75±0.16*△3.56±0.87 3.86±0.87(n=65) 治療后1.45±0.42*1.68±0.38*1.26±0.36*1.37±0.37*1.41±0.36*1.35±0.40*
2.3 兩組患者治療前后肺功能指標水平比較 見表3。中醫組患者治療后FEV1預計值和FEV1/FVC水平均顯著高于對照組、治療前(P<0.05)。
2.4 兩組患者治療前后PFSDQ-M量表評分比較 見表4。中醫組患者治療后PFSDQ-M量表評分顯著低于對照組、治療前(P<0.05)。
表3 兩組患者治療前后肺功能指標水平比較(%,±s)
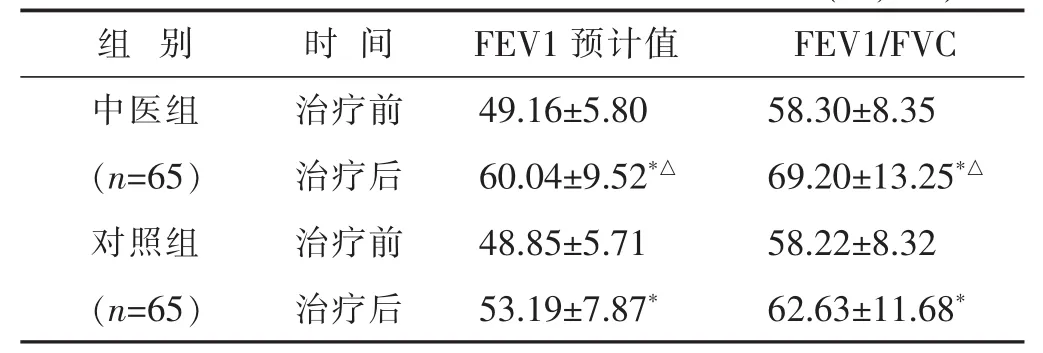
表3 兩組患者治療前后肺功能指標水平比較(%,±s)
與本組治療前比較,*P<0.05;與對照組治療后比較,△P<0.05。下同。
組別 時間 FEV1預計值 FEV1/FVC中醫組 治療前 49.16±5.80 58.30±8.35(n=65) 治療后 60.04±9.52*△69.20±13.25*△對照組 治療前 48.85±5.71 58.22±8.32(n=65) 治療后 53.19±7.87*62.63±11.68*
表4 兩組患者治療前后PFSDQ-M量表評分比較(分,±s)

表4 兩組患者治療前后PFSDQ-M量表評分比較(分,±s)
組別 n 治療前 治療后2周中醫組 65 124.07±21.64 65.88±10.23*△對照組 65 123.86±21.57 80.61±14.87*
2.5 兩組患者治療前后免疫球蛋白水平比較 見表5。中醫組患者治療后免疫球蛋白水平顯著高于對照組、治療前(P<0.05)。
表5 兩組患者治療前后免疫球蛋白水平比較(g/L,±s)

表5 兩組患者治療前后免疫球蛋白水平比較(g/L,±s)
組別時間 IgA IgG IgM中醫組 治療前 0.96±0.22(n=65) 治療后 1.82±0.48*△對照組 治療前 0.92±0.20 5.32±0.77 0.83±0.20 8.70±1.39*△1.54±0.40*△5.39±0.80 0.87±0.22(n=65) 治療后 1.36±0.33*7.55±1.02*1.18±0.31*
2.6 兩組患者治療前后SOD和MDA水平比較 見表6。中醫組患兒治療后SOD和MDA水平顯著優于對照組、治療前(P<0.05)。
表6 兩組患者治療前后SOD和MDA水平比較(±s)
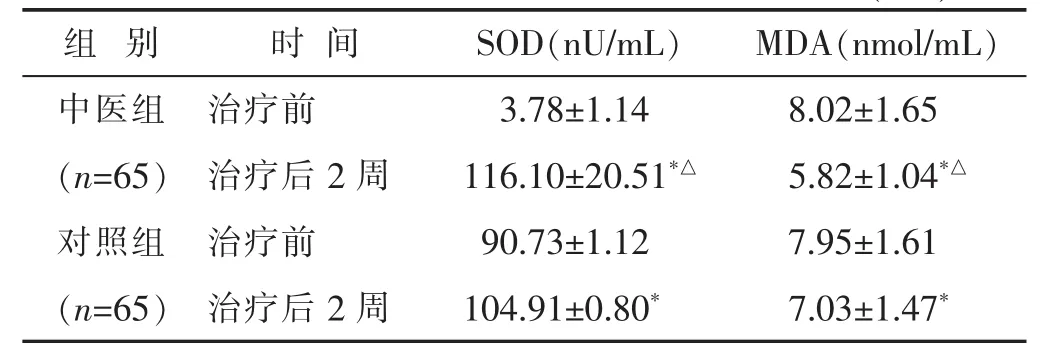
表6 兩組患者治療前后SOD和MDA水平比較(±s)
組 別 時間 SOD(nU/mL) MDA(nmol/mL)中醫組 治療前 3.78±1.14 8.02±1.65(n=65) 治療后2周 116.10±20.51*△5.82±1.04*△對照組 治療前 90.73±1.12 7.95±1.61(n=65) 治療后2周 104.91±0.80*7.03±1.47*
3 討 論
COPD具有發病率高,病情遷延及遠期預后差等特點,給家庭和社會帶來沉重負擔,已成為嚴重社會公共問題;流行病學報道顯示,全球范圍內COPD罹患人數已達6億人,且每年因此死亡人數更接近280萬[8]。而AECOPD已成為導致患者醫療費用增加、肺功能及生活質量下降主要原因之一;而COPD急性發作則是導致患者肺部通氣功能下降和死亡主要原因[9]。AECOPD患者西醫治療主要采用抗感染、祛痰、氣道舒張及激素類藥物等方式,可在一定程度上祛除誘因、緩解氣道急性發作癥狀,但難以抑制進行性進展氣道阻塞和繼發炎癥反應,其長時間使用毒副作用明顯,治療依從性和耐受性較差[10]。如何有效減輕AECOPD患者呼吸道癥狀,改善日常生活質量及遠期預后已越來越受到醫學界的關注。
中醫學將AECOPD歸于“肺脹”“咳嗽”及“喘證”范疇,認為該病主要病機為痰熱壅肺、瘀血阻絡;其中痰壅肺系,肺之氣機損及,易致血瘀氣虛[11]。而帥血無力亦可致瘀血內阻,津液運行不暢,久之則痰飲內生,痰瘀互阻;《血證論》云“須知痰水之壅,由瘀血使然,但去瘀血則痰水自消”[12]。故中醫治療該病當以益氣清肺、化痰散瘀為主。本次研究所用補氣祛瘀中藥組方中,魚腥草清熱解毒,金銀花宣肺泄熱,桔梗祛痰清肺,蘆根清熱瀉火,桑白皮解熱祛痰,瓜蔞清熱化痰,黃芩燥濕解毒,葶藶子消痰平喘,地龍破血逐瘀,浙貝母散結消癰,川牛膝逐瘀通經,川芎活血祛瘀,桃仁止咳平喘,而大黃則通腑泄熱,諸藥合用和共奏清熱化痰之效。現代藥理學研究顯示,丹參提取物具有擴張動脈或微動脈,提高血液灌注速度及改善微循環等作用[13];瓜蔞則能夠有效降低痰液黏稠度,刺激氣道纖毛擺動,繼而加快痰液排出進程[14];而燈盞花素在提高AECOPD患者血樣飽和度,降低炎癥反應水平及改善肺部通氣功能方面作用已被廣泛證實[15]。
本觀察表明,中醫組患者治療總有效率,治療后中醫證候積分顯、FEV1預計值、FEV1/FVC水平及PFSDQ-M量表評分均顯著優于對照組、治療前,證實中西醫結合治療AECOPD有助于緩解臨床癥狀體征,促進肺部功能恢復及改善生活質量;而中醫組患者治療后免疫球蛋白、SOD及MDA水平顯著優于對照組、治療前,證實中藥輔助用于AECOPD治療在提高機體免疫功能水平,改善氧化應激反應方面優勢明顯,筆者認為這可能是該方案具有更佳臨床療效方面重要機制之一。已有研究顯示[16],AECOPD患者因機體長期免疫反應、免疫細胞營養嚴重消耗及病情急性進展,故普遍存在機體細胞免疫功能低下;其中免疫球蛋白水平與患者預后具有明確相關性機體。而氧化/抗氧化系統紊亂被認為在AECOPD發生發展過程中發揮著關鍵作用;患者機體感染所致炎癥反應可誘發過量氧自由基和脂質過氧化物合成釋放,加重機體氧化應激損傷,從而引起病情快速進展[17];其中MDA水平與體內自由基氧化損傷反應強度呈正相關;而SOD活性高低則能夠反映機體抗氧化保護功能強弱[18]。
綜上所述,燈盞花素聯合補氣祛瘀中藥治療AECOPD可有效緩解臨床癥狀,改善肺部功能和生活質量,提高機體免疫力,并有助于調節SOD和MDA水平。
[1] Matera MG,Calzetta L,Cazzola M.β-adrenoceptor modulation in chronic obstructive pulmonary disease:present and future perspectives[J].Drugs,2013,73(15):1653-1663.
[2] Rothberg MB,Pekow PS,Lahti M,et al.Antibiotic therapy and treatment failure in patients hospitalized for acute exacerbations of chronic obstructive pulmonary disease[J].JAMA,2010,303(20):2035-2042.
[3] 董國蕊,王玉霞.沙丁胺醇異丙托溴銨和多索茶堿聯合治療慢性阻塞性肺疾病急性加重期的療效分析[J].中國藥物與臨床,2014,14(5):691.
[4] 龔國良,李欣.痰熱清治療慢性阻塞性肺疾病急性加重期的臨床療效及細胞因子水平的研究[J].中國中藥雜志,2009,34(1):104-106
[5] 中華醫學會呼吸病學分會慢性阻塞性肺疾病學組.慢性阻塞性肺疾病診治指南(2013年修訂版)[J].中華結核和呼吸雜志,2013,36(4):67-69.
[6] 中華中醫藥學會內科分會肺系病專業委員會.慢性阻塞性肺疾病中醫證候診斷標準(2011版)[J].中醫雜志,2012,53(2):177-180.
[7] 國家中醫藥管理局.中醫病證診斷療效標準[M].南京:南京大學出版社,1994:48-49.
[8] Baines KJ,Simpson JL,Gibson PG.Innate immune responses are increased in chronic obstructive pulmonary disease[J]. PLoS One,2011,6(3):e18426.
[9] Kovelis D,Segretti NO,Probst VS,et al.Validation of the modified pulmonary functional status and dyspnea questionnaire and the medical research council scale for use in brazilian patients with chronic obstructive pulmonary disease[J].J Brasil Pneumolo,2008,34(12):1008-1011.
[10]劉經耀,黃洪.特布他林聯合異丙托溴銨氧驅霧化吸入治療慢性阻塞性肺病急性加重期療效觀察[J].中國醫學創新,2013,10(11):58-59.
[11]王至婉,李建生,王明航,等.基于文獻的慢性阻塞性肺疾病急性加重期證候要素分布規律的研究[J].中華中醫藥雜志,2008,23(4):325-326.
[12]蔣世偉,龐立健,朱凌云,等.慢性阻塞性肺疾病中醫“肺虛絡瘀”病機理論探析[J].遼寧中醫藥大學學報,2013,15(8):49-51.
[13]高楓,孫桂波,馬博.丹參活性成分作用機制研究的新進展[J].中藥藥理與臨床,2009,25(4):90-92.
[14]巢志茂,劉靜明,王伏華,等.五種瓜蔞皮揮發性有機酸的分析[J].中國中藥雜志,1992,17(11):673-674,703.
[15]王麗娟,王勇.燈盞花素藥理作用與臨床應用研究進展[J].齊齊哈爾醫學院學報,2005,26(11):1323-1325.
[16]孫寶君,鄒琳,俞森洋.慢性阻塞性肺疾病長期機械通氣患者T細胞亞群、補體及免疫球蛋白的變化[J].中華老年多器官疾病雜志,2005,4(2):115-117.
[17]楊月,李永春.COPD患者氧化劑損傷與抗氧化治療的研究進展[J].中國全科醫學,2005,8(23):1980-1982.
[18]朱偉東,金普放,酈岳.金水六君煎對慢性阻塞性肺疾病患者血清超氧化物歧化酶、丙二醛的影響[J].中國中醫急癥,2011,20(1):30-32.
R563.9
A
1004-745X(2017)05-0929-03
10.3969/j.issn.1004-745X.2017.05.058
2017-01-17)

