替吉奧治療卡培他濱耐藥轉移性乳腺癌的療效分析
王少敏,葉 孟,倪曙民
·論著·
替吉奧治療卡培他濱耐藥轉移性乳腺癌的療效分析
王少敏*,葉 孟,倪曙民
目的 分析卡培他濱單藥治療耐藥后的轉移性乳腺癌患者接受替吉奧單藥治療的療效及安全性。方法 回顧性分析2011年11月—2015年5月寧波大學醫學院附屬醫院腫瘤內科治療的22例轉移性乳腺癌患者的臨床資料。22例患者接受卡培他濱單藥治療,在卡培他濱耐藥后接受替吉奧單藥治療,直至疾病進展、不可耐受的毒副作用或患者拒絕治療。按照實體瘤療效評價標準(RECIST)進行替吉奧臨床療效評價,觀察進展時間(TTP)及總生存期(OS),記錄疼痛評分及CA153水平,根據美國國家癌癥研究所發布的常見不良反應事件評價標準(CTCAE v4.02)進行毒副作用評價。結果 22例卡培他濱耐藥的轉移性乳腺癌患者接受替吉奧治療后5例部分緩解,12例疾病穩定,5例疾病進展,客觀有效率(ORR)為22.7%(5/22),臨床獲益率(CBR)為77.3%(17/22);中位TTP為113 d(22~218 d),中位OS為20.2個月(3.8~38.2個月)。替吉奧治療前有15例患者有疼痛表現,未經提高止痛藥物劑量,治療后10例患者疼痛減輕。開始替吉奧治療時CA153水平與治療過程中最低CA153水平比較,差異有統計學意義〔(174.8±67.4)U/ml與(102.8±69.7)U/ml,t=4.174,P=0.001〕。替吉奧治療的毒副作用均可耐受,主要毒副作用有厭食〔59.1%(13/22)〕、惡心〔50.0%(11/22)〕、乏力〔45.5%(10/22)〕、中性粒細胞計數減少〔45.5%(10/22)〕、貧血〔40.9%(9/22)〕、腹瀉〔36.4%(8/22)〕、手足綜合征〔27.3%(6/22)〕、轉氨酶升高〔22.7%(5/22)〕及嘔吐〔18.2%(4/22)〕等。毒副作用多為Ⅰ~Ⅱ級,僅3例發生Ⅲ級毒副作用。結論 替吉奧單藥對于卡培他濱單藥耐藥的轉移性乳腺癌有一定的療效,而且耐受性良好。因此,對于使用卡培他濱單藥治療后耐藥的轉移性乳腺癌可考慮選用替吉奧單藥治療。
乳腺腫瘤;替吉奧;卡培他濱;抗腫瘤聯合化療方案
王少敏,葉孟,倪曙民.替吉奧治療卡培他濱耐藥轉移性乳腺癌的療效分析[J].中國全科醫學,2017,20(20):2469-2473.[www.chinagp.net]
WANG S M,YE M,NI S M.Therapeutic efficiency of tegafur,gimeracil and oteracil potassium for metastatic breast cancer resistant to capecitabine[J].Chinese General Practice,2017,20(20):2469-2473.
乳腺癌是女性最常見的腫瘤,隨著生活方式的改變及人口老齡化,發病率逐年升高[1]。而相當一部分乳腺癌患者會出現遠處轉移,最常見的轉移部位有骨、肺、肝及腦等。乳腺癌內科治療手段包括化療、內分泌治療、靶向治療等。由于乳腺癌對內科治療手段比較敏感,使得轉移性乳腺癌患者仍有較長的生存期,因此轉移性乳腺癌的治療是臨床中一個值得探討的問題。
卡培他濱為口服氟尿嘧啶類化療藥物,是轉移性乳腺癌治療中有效的化療藥物之一。卡培他濱單藥治療乳腺癌的客觀有效率(ORR)約為20%[2]。卡培他濱聯合其他細胞毒性藥物或靶向藥物在轉移性乳腺癌的治療中也取得了較好的療效[3-8]。卡培他濱的主要毒副作用為手足綜合征,但大多數患者癥狀較輕,其次消化道反應及骨髓毒性也較輕,因此對于晚期乳腺癌治療應用卡培他濱是較好的選擇[9]。替吉奧作為另一種口服的氟尿嘧啶類藥物,同樣具有毒副作用輕及耐受良好的優點,在多種實體腫瘤中獲得較好的療效,在乳腺癌中也有一定的療效[10-14]。盡管兩者均為口服氟尿嘧啶類化療藥物,但在藥物成分及作用機制上有一定的區別。對于卡培他濱治療耐藥的轉移性乳腺癌患者選擇替吉奧治療的療效如何,經PubMed檢索可見兩篇文獻報道[15-16],國內未檢索到相關文獻報道。基于此,本研究對22例轉移性乳腺癌患者在卡培他濱單藥治療耐藥后采用替吉奧單藥治療,取得了一定療效,現報道如下,以期為轉移性乳腺癌患者卡培他濱單藥治療耐藥后的治療提供借鑒。
1 對象與方法
1.1 研究對象 選取2011年11月—2015年5月寧波大學醫學院附屬醫院腫瘤內科治療的22例轉移性乳腺癌患者。患者的臨床分期均為Ⅳ期;均為女性;年齡47~76歲,中位年齡59歲;轉移灶經骨ECT、MRI及CT檢查進行確診;轉移病灶1~6個,中位轉移病灶為2個;20例患者有骨轉移,16例患者有內臟轉移;一般狀況根據美國東部腫瘤協作組(ECOG)評分,0分2例,1分16例,2分4例;激素受體陽性16例,陰性6例;絕經前2例,絕經后20例;既往使用蒽環類化療藥物16例,紫杉類化療藥物15例,吉西他濱11例;既往使用過曲妥珠單抗2例,未使用20例。納入標準:(1)年齡≥18歲;(2)患者無認知功能障礙;(3)所有患者的乳腺癌原發灶手術切除,經病理證實為浸潤性小葉癌或浸潤性導管癌;(4)既往未接受口服氟尿嘧啶類藥物治療;(5)ECOG評分0~2分;(6)中性粒細胞計數≥1.5×109/L,血小板計數≥75×109/L,丙氨酸氨基轉移酶及天冬氨酸氨基轉移酶<2.5×參考范圍上限(肝轉移時<5.0×參考范圍上限),膽紅素<1.25×參考范圍上限;(7)心、肺及腎功能良好,預期生存>3個月;(8)患者對治療方案及潛在風險知情同意。排除標準:(1)ECOG評分≥3分;(2)腦轉移。
1.2 治療方法 所有患者接受卡培他濱片(上海羅氏制藥有限公司生產)單藥口服治療,卡培他濱的初始治療劑量為2 500 mg·(m2)-1·d-1,服藥2周停用1周,可根據毒副作用調整治療劑量,卡培他濱單藥治療后出現疾病進展(PD)定義為卡培他濱耐藥。卡培他濱耐藥后接受替吉奧膠囊(山東新時代藥業有限公司生產)單藥口服治療,替吉奧的治療劑量根據體表面積:<1.25 m2,40 mg,2次/d;1.25~1.50 m2,50 mg,2次/d;>1.50 m2,60 mg,2次/d。替吉奧的常規用法為服藥4周停用2周,對于耐受能力差的患者服藥2周停用1周,治療過程中可根據毒副作用調整治療劑量,120 mg/d調整為100 mg/d,100 mg/d調整為80 mg/d,80 mg/d調整為60 mg/d。替吉奧單藥治療終點至PD、不可耐受的毒副作用或患者拒絕治療。
1.3 觀察指標 (1)療效評價:常規自服用替吉奧42 d后開始評估臨床療效。此后每3周復查腫瘤標志物并觀察癥狀變化,若無明顯進展每2~3個月行系統的影像學檢查評估臨床療效,若有明顯進展及時進行系統的影像學檢查。臨床療效按照實體瘤療效評價標準(RECIST)進行評價。完全緩解(CR):指所有病灶消失,持續4周以上;部分緩解(PR):所有可測量病灶最大直徑總和縮小30%,持續4周以上;PD:所有可測量病灶最大直徑總和增大20%,或出現新病灶;疾病穩定(SD):除CR、PR及PD之外。ORR為CR+PR的患者例數占總例數的百分比。臨床獲益率(CBR)為CR+PR+SD的患者例數占總例數的百分比。(2)進展時間(TTP)及總生存期(OS):TTP為自服用替吉奧日至首次證實為PD日或替吉奧停藥日;OS為自服用替吉奧日至患者死亡日或隨訪截止。(3)疼痛評分:采用數字評分法,記錄患者開始接受替吉奧治療時的疼痛評分,并記錄替吉奧治療42 d后的疼痛評分。(4)CA153水平:CA153水平采用化學發光法檢測,記錄患者開始接受替吉奧治療時的CA153水平,并記錄替吉奧治療過程中最低的CA153水平。(5)毒副作用:毒副作用評價根據美國國家癌癥研究所發布的常見不良反應事件評價標準(CTCAE v4.02)進行評價。
1.4 隨訪 治療結束后通過查閱患者定期復查記錄及電話方式進行隨訪,隨訪至2015-11-20,22例患者資料均完整,20例死亡,2例存活,0例失訪。
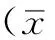
2 結果
2.1 療效及生存分析 22例卡培他濱耐藥的轉移性乳腺癌患者接受替吉奧治療后5例PR,12例SD,5例PD,ORR為22.7%(5/22),CBR為77.3%(17/22)。開始替吉奧治療后,22例患者的中位TTP為113d(22~218d)(見圖1),中位OS為20.2個月(3.8~38.2個月)(見圖2)。
2.1.1 依據激素受體狀態的療效評價 16例激素受體陽性患者,4例PR,10例SD,2例PD,ORR為4/16,CBR為14/16;6例激素受體陰性患者,1例PR,2例SD,3例PD,ORR為1/6,CBR為3/6。
2.1.2 依據既往對卡培他濱治療反應的療效評價 22例患者在接受卡培他濱治療時,7例PR,10例SD,5例PD。7例對卡培他濱PR的患者,耐藥后接受替吉奧治療后,4例PR,3例SD,ORR為4/7,CBR為7/7。10例對卡培他濱SD的患者,耐藥后接受替吉奧治療后,1例PR,6例SD,3例PD,ORR為1/10,CBR為7/10。5例對卡培他濱PD的患者,耐藥后接受替吉奧治療后,3例SD,2例PD,CBR為3/5。

圖1 替吉奧治療卡培他濱耐藥的轉移性乳腺癌患者的TTP曲線
Figure1Kaplan-meiercurveofTTPfortegafur,gimeracilandoteracilpotassiummonotherapyinmetastaticbreastcancerpatientsresistingtocapecitabine
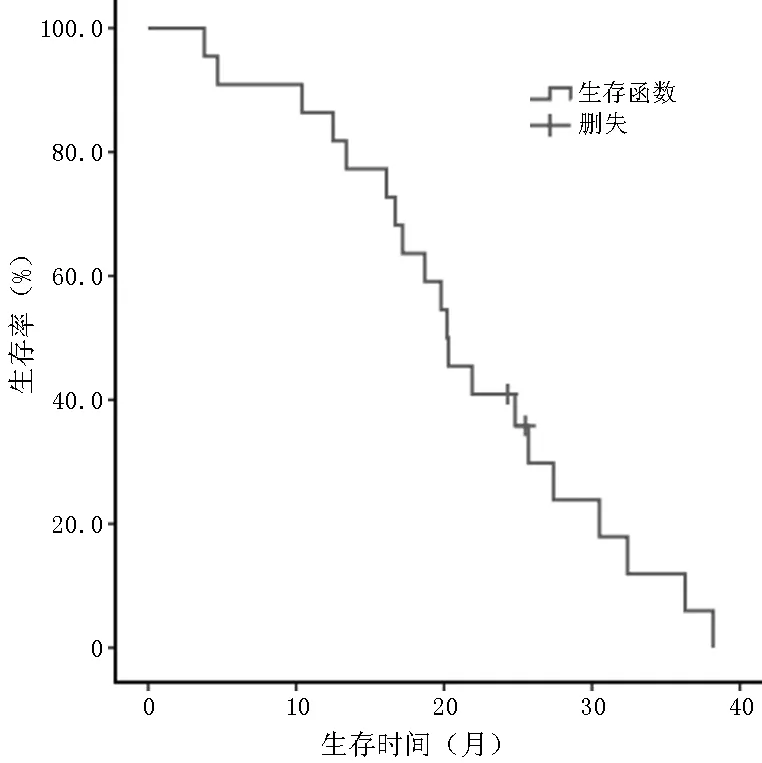
圖2 替吉奧治療卡培他濱耐藥的轉移性乳腺癌患者的OS曲線
Figure 2 Kaplan-meier curve of OS for tegafur,gimeracil and oteracil potassium monotherapy in metastatic breast cancer patients resisting to capecitabine
2.2 治療前后疼痛評分及CA153水平比較 替吉奧治療前15例患者有疼痛表現,未提高止痛藥物劑量,治療后10例患者疼痛減輕。開始替吉奧治療時17例患者CA153水平升高,CA153水平為(174.8±67.4)U/ml,替吉奧治療過程中最低CA153水平為(102.8±69.7)U/ml。治療前后CA153水平比較,差異有統計學意義(t=4.174,P=0.001)。
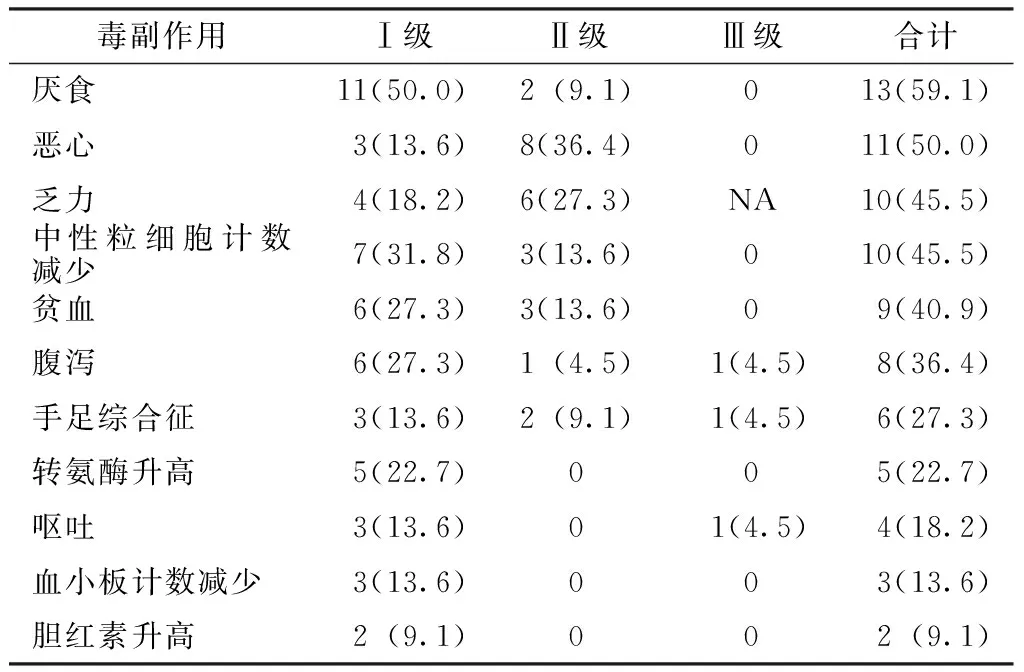
2.3 毒副作用 替吉奧治療的毒副作用均可耐受,無治療相關性死亡。主要毒副作用有厭食(59.1%)、惡心(50.0%)、乏力(45.5%)、中性粒細胞計數減少(45.5%)、貧血(40.9%)、腹瀉(36.4%)、手足綜合征(27.3%)、轉氨酶升高(22.7%)及嘔吐(18.2%)。多數毒副作用均為Ⅰ~Ⅱ級,1例發生Ⅲ級手足綜合征,經調整劑量及對癥治療后好轉;1例發生Ⅲ級嘔吐,1例發生Ⅲ級腹瀉,經停藥后好轉(見表1)。
表1 替吉奧治療的毒副作用發生率〔n(%)〕
Table 1 Incidence rates of side effects of tegafur,gimeracil and oteracil potassium
毒副作用Ⅰ級Ⅱ級Ⅲ級合計厭食11(50.0)2(9.1)013(59.1)惡心3(13.6)8(36.4)011(50.0)乏力4(18.2)6(27.3)NA10(45.5)中性粒細胞計數減少7(31.8)3(13.6)010(45.5)貧血6(27.3)3(13.6)09(40.9)腹瀉6(27.3)1(4.5)1(4.5)8(36.4)手足綜合征3(13.6)2(9.1)1(4.5)6(27.3)轉氨酶升高5(22.7)005(22.7)嘔吐3(13.6)01(4.5)4(18.2)血小板計數減少3(13.6)003(13.6)膽紅素升高2(9.1)002(9.1)
注:NA=不適用
3 討論
5-氟尿嘧啶(5-fluorouracil,5-Fu)自1957年問世以來,已被廣泛應用于頭頸、乳腺及胃腸等多個部位實體惡性腫瘤的治療,并獲得了較好的療效[17]。此后又開發了多種口服氟尿嘧啶制劑,如替加氟、卡培他濱及替吉奧膠囊[18]。5-Fu在體內最終轉變為5-氟-2-脫氧尿嘧啶核苷酸,進而影響細胞DNA的合成。卡培他濱為5-Fu的前體藥物,易從胃腸道吸收,最終經胸苷磷酸化酶(dThdPase)水解為5-Fu。人體有許多組織表達dThdPase,一些人類腫瘤中dThdPase的表達高于周圍正常組織,說明服用卡培他濱可獲得更高的5-Fu組織濃度及更低的5-Fu血藥濃度,因此卡培他濱相對于5-Fu高效低毒。而二氫嘧啶脫氫酶(dihydropyrimidine dehydrogenase,DPD)可將5-Fu分解為無活性的代謝產物,DPD在高表達或較高活性的情況下,可加速5-Fu的清除而導致5-Fu及氟尿嘧啶類口服制劑的耐藥[19]。
替吉奧為口服氟尿嘧啶復方制劑,主要有3種成分:替加氟、吉美嘧啶及奧拉西坦。口服后替加氟在體內逐漸轉化成5-Fu[20]。吉美嘧啶選擇性可逆抑制存在于肝臟的DPD,減少5-Fu的分解代謝而維持體內5-Fu較高的血藥濃度,克服了5-Fu t1/2短、代謝快的不足,從而增強抗腫瘤活性。奧拉西坦口服后主要分布于胃腸道,可選擇性拮抗乳清酸磷酸核糖轉移酶而阻止5-Fu磷酸化轉變為5-Fu脫氧核苷酸,從而在不影響5-Fu抗腫瘤活性的同時減輕胃腸道的毒副作用。替吉奧中的DPD抑制劑吉美嘧啶可減少5-Fu的清除而提高其抗腫瘤作用,因此對于卡培他濱耐藥的轉移性乳腺癌患者,替吉奧應該能繼續取得一定的療效。國外可見兩篇關于這方面的報道[15-16],但治療效果報道不一,一篇報道認為可獲得一定的療效但很有限[15],另一篇報道則認為獲得較好的治療效果[16],兩篇報道均認為耐受性良好。
本研究中22例患者經替吉奧治療后盡管ORR僅為22.7%,但CBR可達77.3%,因此替吉奧單藥治療卡培他濱耐藥的轉移性乳腺癌可獲得較高的SD。口服替吉奧膠囊后毒副作用有厭食、惡心、乏力、中性粒細胞計數減少、貧血、腹瀉、手足綜合征、轉氨酶升高、嘔吐、血小板計數減少及膽紅素升高,多數為Ⅰ~Ⅱ級毒副作用,對患者生活質量幾乎沒有影響。且有10例患者治療后疼痛減輕,使得生活質量得以改善。由于替吉奧CBR較高且耐受性良好,因此對卡培他濱耐藥的轉移性乳腺癌患者不失為一個較好的選擇。進一步分析顯示,激素受體陽性患者的CBR可達14/16,而激素受體陰性患者的CBR僅為3/6,這表明替吉奧可能對激素受體陰性患者的療效較差。另外根據患者既往對卡培他濱的治療反應分析了替吉奧的療效,既往對卡培他濱療效為PR、SD及PD的患者耐藥后轉為替吉奧治療后CBR分別為7/7、7/10及3/5,可見既往能從卡培他濱獲益的患者更容易從替吉奧的治療中獲益,但由于病例數較少,需要更多病例加以證實。22例患者接受替吉奧治療后中位TTP為113 d,即在替吉奧治療后獲得了近4個月的無進展生存,替吉奧治療后患者中位OS達20.2個月,可能延長轉移性乳腺癌患者的生存期。本研究中替吉奧的療效與YAMAMOTO等[16]的結果相近,且療效優于ITO等[15]的研究結果,可能與ITO等[15]的研究中多數患者已接受多線既往化療有關。本研究與以上兩個研究的不同之處在于,前兩個研究中的所有患者雖接受卡培他濱治療,但不考慮既往是否采用卡培他濱單藥或聯合其他藥物治療,而本研究中所有患者為卡培他濱單藥治療后出現耐藥的患者,因此更能說明卡培他濱耐藥的轉移性乳腺癌患者能否從替吉奧治療中獲益。本研究中12例患者療效為SD且5例患者療效為PD,說明替吉奧并非轉移性乳腺癌患者在卡培他濱耐藥后的最佳選擇,但對于老年或一般狀況不佳而不適合靜脈化療或無法選擇其他治療藥物時是一個可供選擇的較佳治療方案。
綜上所述,替吉奧對于卡培他濱耐藥的轉移性乳腺癌患者是一個可選的治療方案,并且可獲得一定的治療效果。但由于本研究病例數相對較少,需要更多的病例對療效進行進一步的驗證,必要時需要多中心合作以了解其治療效果。在多中心合作的支持下,可根據患者的分子生物學特征進一步分析以了解哪些轉移性乳腺癌患者在卡培他濱耐藥后仍能從替吉奧治療中獲得一定的療效,以達到個體化治療,避免不必要的治療。
作者貢獻:王少敏參與文章的構思設計、數據收集及整理、統計學分析、論文撰寫和修改及結果分析;葉孟參與研究的實施及可行性分析;倪曙民參與數據收集及整理。
本文無利益沖突。
[1] FERLAY J,SOERJOMATARAM I,DIKSHIT R,et al.Cancer incidence and mortality worldwide:sources,methods and major patterns in GLOBOCAN 2012[J].Int J Cancer,2015,136(5):E359-386.DOI:10.1002/ijc.29210.
[2] BLUM J L,JONES S E,BUZDAR A U,et al.Multicenter phase Ⅱ study of capecitabine in paclitaxel-refractory metastatic breast cancer[J].J Clin Oncol,1999,17(2):485-493.DOI:10.1200/JCO.1999.17.2.485.
[3] O′SHAUGHNESSY J,MILES D,VUKELJA S,et al.Superior survival with capecitabine plus docetaxel combination therapy in anthracycline-pretreated patients with advanced breast cancer:phase Ⅲ trial results[J].J Clin Oncol,2002,20(12):2812-2823.DOI:10.1200/JCO.2002.09.002.
[4] CHAN S,ROMIEU G,HUOBER J,et al.Phase Ⅲ study of gemcitabine plus docetaxel compared with capecitabine plus docetaxel for anthracycline-pretreated patients with metastatic breast cancer[J].J Clin Oncol,2009,27(11):1753-1760.DOI:10.1200/JCO.2007.15.8485.
[5] WARDLEY A M,PIVOT X,MORALES-VASQUEZ F,et al.Randomized phase Ⅱ trial of first-line trastuzumab plus docetaxel and capecitabine compared with trastuzumab plus docetaxel in HER2-positive metastatic breast cancer[J].J Clin Oncol,2010,28(6):976-983.DOI:10.1200/JCO.2008.21.6531.
[6] MAVROUDIS D,PAPAKOTOULAS P,ARDAVANIS A,et al.Randomized phase Ⅲ trial comparing docetaxel plus epirubicin versus docetaxel plus capecitabine as first-line treatment in women with advanced breast cancer[J].Ann Oncol,2010,21(1):48-54.DOI:10.1093/annonc/mdp498.
[7] STEMMLER H J,DIGIOIA D,FREIER W,et al.Randomised phase Ⅱ trial of gemcitabine plus vinorelbine vs gemcitabine plus cisplatin vs gemcitabine plus capecitabine in patients with pretreated metastatic breast cancer[J].Br J Cancer,2011,104(7):1071-1078.DOI:10.1038/bjc.2011.86.
[8] BACHELOT T,BAJARD A,RAY-COQUARD I,et al.Final results of ERASME-4:a randomized trial of first-line docetaxel plus either capecitabine or epirubicin for metastatic breast cancer[J].Oncology,2011,80(3/4):262-268.DOI:10.1159/000329066.
[9]張明帥,張國慶,歐江華,等.唑來磷酸聯合卡培他濱治療乳腺癌多發骨轉移臨床療效研究[J].中國全科醫學,2011,14(35):4103-4105.DOI:10.3969/j.issn.1007-9572.2011.35.035. ZHANG M S,ZHANG G Q,OU J H,et al.Clinical efficacy research on zoledronic acid combined with capecitabine in treating breast cancer with multiple bone metastases[J].Chinese General Practice,2011,14(35):4103-4105.DOI:10.3969/j.issn.1007-9572.2011.35.035.
[10] SATOH T,SAKATA Y.S-1 for the treatment of gastrointestinal cancer[J].Expert Opin Pharmacother,2012,13(13):1943-1959.DOI: 10.1517/14656566.2012.709234.
[11] MIYAMOTO Y,SAKAMOTO Y,YOSHIDA N,et al.Efficacy of S-1 in colorectal cancer[J].Expert Opin Pharmacother,2014,15(12):1761-1770.DOI:10.1517/14656566.2014.937706.
[12] KAWAHARA M.Efficacy of S-1 in non-small cell lung cancer[J].Expert Opin Pharmacother,2014,15(13):1927-1942.DOI:10.1517/14656566.2014.945424.
[13] SUDO K,NAKAMURA K,YAMAGUCHI T.S-1 in the treatment of pancreatic cancer[J].World J Gastroenterol,2014,20(41):15110-15118.DOI:10.3748/wjg.v20.i41.15110.
[14] TAKASHIMA T,MUKAI H,HARA F,et al.Taxanes versus S-1 as the first-line chemotherapy for metastatic breast cancer(SELECT BC):an open-label,non-inferiority,randomised phase 3 trial[J].Lancet Oncol,2016,17(1):90-98.DOI:10.1016/S1470-2045(15)00411-8.
[15] ITO Y,OSAKI Y,TOKUDOME N,et al.Efficacy of S-1 in heavily pretreated patients with metastatic breast cancer:cross-resistance to capecitabine[J].Breast Cancer,2009,16(2):126-131.DOI: 10.1007/s12282-008-0073-9.
[16] YAMAMOTO D,IWASE S,YOSHIDA H,et al.Efficacy of S-1 in patients with capecitabine-resistant breast cancer-Japan Breast Cancer Research Network(JBCRN)04-1 trial[J].Anticancer Res,2010,30(9):3827-3831.
[17] HEIDELBERGER C,CHAUDHURI N K,DANNEBERG P,et al.Fluorinated pyrimidines,a new class of tumour-inhibitory compounds[J].Nature,1957,179(4561):663-666.
[18] MALET-MARTINO M,MARTINO R.Clinical studies of three oral prodrugs of 5-fluorouracil(capecitabine,UFT,S-1):a review[J].Oncologist,2002,7(4):288-323.
[19] 韓勇,壽成超.影響5-Fu療效的研究進展[J].中國腫瘤臨床,2010,37(21):1255-1259.DOI:10.3969/j.issn.1000-8179.2010.21.014. HAN Y,SHOU C C.The mechanisms involved in 5-Fu efficacy[J].Chinese Journal of Clinical Oncology,2010,37(21):1255-1259.DOI:10.3969/j.issn.1000-8179.2010.21.014.
[20] MIURA K,SHIRASAKA T,YAMAUE H,et al.S-1 as a core anticancer fluoropyrimidine agent[J].Expert Opin Drug Deliv,2012,9(3):273-286.DOI:10.1517/17425247.2012.652945.
(本文編輯:張小龍)
Therapeutic Efficiency of Tegafur,Gimeracil and Oteracil Potassium for Metastatic Breast Cancer Resistant to Capecitabine
WANGShao-min*,YEMeng,NIShu-min
DepartmentofMedicalOncology,theAffiliatedHospitalofSchoolofMedicineofNingboUniversity,Ningbo315020,China
*Correspondingauthor:WANGShao-min,Associatechiefphysician;E-mail:wangshaomin2000@163.com
Objective The purpose of this study is to analyze retrospectively the therapeutic efficiency and safety of tegafur,gimeracil and oteracil potassium monotherapy in patients with metastatic breast cancer resistant to capecitabine monotherapy.Methods We retrospectively ananlyzed the clinical data of 22 cases of patients with metastatic breast cancer in the Department of Medical Oncology,the Affiliated Hospital of School of Medicine Ningbo University between November 2011 and May 2015.All patients accepted capecitabine monotherapy,then they all accepted tegafur,gimeracil and oteracil potassium monotherapy after resistant to capecitabine until tumor progression,intolerable side effects and toxicity or refusal of treatment.The therapeutic efficiency of tegafur,gimeracil and oteracil potassium was evaluated according to the Response Evaluation Criteria in Solid Tumors(RECIST),and then the time to progression and overall survival were observed.The pain score and CA153 value were also recorded.Side effects and toxicities were assessed according to the common terminology criteria for adverse events(CTCAE v4.02) issued by the National Cancer Institute.Results Five patients had partial remission,12 had stable disease,and 5 had disease progress in 22 patients with capecitabine-resistant metastatic breast cancer after tegafur,gimeracil and oteracil potassium treatment.Objective response rate was 22.7%(5/22),clinical benefit response was 77.3%(17/22).Median time to progression was 113 days(22-218 days),median overall survival was 20.2 months(3.8-38.2 momths).A total of 15 patients complained of pain before tegafur,gimeracil and oteracil potassium therapy.Pain relief happened in 10 cases without the increase of analgesic drugs dosage after therapy.Compared with the CA153 value on the beginning of tegafur,gimeracil and oteracil potassium therapy,the lowest CA153 value in the course of therapy decreased signifcantly〔(174.8±67.4)U/ml vs.(102.8±69.7)U/ml,t=4.174,P=0.001〕.The toxic side effects of tegafur,gimeracil and oteracil potassium were well tolerated,and major adverse reactions included anorexia〔59.1%(13/22)〕,nauseas〔50.0%(11/22)〕,fatigue〔45.5%(10/22)〕,neutropenia〔45.5%(10/22)〕,anemia〔40.9%(9/22)〕,diarrhea〔36.4%(8/22)〕,hand-foot syndrome〔27.3%(6/22)〕,transaminase elevation〔22.7%(5/22)〕 and vomiting〔18.2%(4/22)〕et al.Most adverse reactions were Grade Ⅰ-Ⅱ adverse events,Grade Ⅲ adverse events only occurred in 3 cases.Conclusion Tegafur,gimeracil and oteracil potassium monotherapy is effective and well-tolerated in patients with metastatic breast cancer resistant to capecitabine monotherapy.So tegafur,gimeracil and oteracil potassium monotherapy is a selective regime treatment for patients with metastatic breast cancer after they were resistant to capecitabine monotherapy.
Breast neoplasms;Tegafur,gimeracil and oteracil potassium;Capecitabine;Antineoplastic combined chemotherapy protocols
寧波大學校級科研項目(XYY15007)
R 737.9
A
10.3969/j.issn.1007-9572.2017.20.009
2016-10-15;
2017-04-28)
315020浙江省寧波市,寧波大學醫學院附屬醫院腫瘤內科
*通信作者:王少敏,副主任醫師;E-mail:wangshaomin2000@163.com

