兩種新型席夫堿-Mn(Ⅱ)配合物-殼聚糖復合材料的合成表征及其SOD活性
瞿雋申,周 紅,潘志權
(武漢工程大學化學與環境工程學院,湖北 武漢 430073)
?
兩種新型席夫堿-Mn(Ⅱ)配合物-殼聚糖復合材料的合成表征及其SOD活性
瞿雋申,周 紅*,潘志權
(武漢工程大學化學與環境工程學院,湖北 武漢 430073)
以二乙烯三胺、三乙烯四胺分別與間苯二醛反應合成二乙烯三胺-間苯二醛席夫堿(L1)、三乙烯四胺-間苯二醛席夫堿(L2),然后與醋酸錳反應合成了兩種席夫堿-Mn(Ⅱ)配合物,進而與殼聚糖凝膠反應合成了兩種席夫堿-Mn(Ⅱ)配合物-殼聚糖復合材料L1-Mn(Ⅱ)-殼聚糖和L2-Mn(Ⅱ)-殼聚糖,對其結構進行了傅立葉變換紅外光譜(FTIR)、掃描電子顯微鏡(SEM)及X-射線光電能譜(XPS)表征,采用氯化硝基四氮唑藍(NBT)法測定兩種復合材料的SOD活性,并對它們的重復利用性進行了測試。FTIR、SEM及XPS表征結果表明,配合物與殼聚糖成功交聯;L1-Mn(Ⅱ)-殼聚糖、L2-Mn(Ⅱ)-殼聚糖的IC50分別為3.40 μg·mL-1、6.15 μg·mL-1,都具有較好的SOD活性;兩種材料穩定且具有較好的重復利用性。
席夫堿配合物;殼聚糖;SOD活性
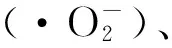
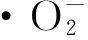
而人體細胞由于某些原因如老化等,可能無法分泌足夠多的SOD與CAT。而外源性攝入SOD與CAT非常困難。因酶類屬于蛋白質,它們難以通過細胞膜且對儲存環境要求極高,這使得研究酶模擬物顯得愈發重要[8-9]。
根據中心金屬離子不同,天然的SOD可以分為銅鋅SOD[10]、鐵SOD[11]、鎳SOD[12-13]與錳SOD。其中錳SOD因具有高活性與低毒性而受到廣泛關注,含錳配合物可能具有很高的SOD潛力以及相對的低毒性。殼聚糖具有天然的低毒性、高生物相容性,被廣泛應用于生物標記[14]、傷口愈合[15]以及作為藥物載體[16],干粉狀的殼聚糖也被應用于藥物領域[17]。而許多金屬配合物在水溶液環境中并不穩定,基于以上考慮,作者結合錳配合物的高SOD活性和殼聚糖的高生物相容性與低毒性,設計并合成了兩種不同的席夫堿配合物,將它們與醋酸錳配合并與殼聚糖結合合成復合材料,并考察了它們的SOD活性和重復利用性。復合材料的合成路線如圖1所示。
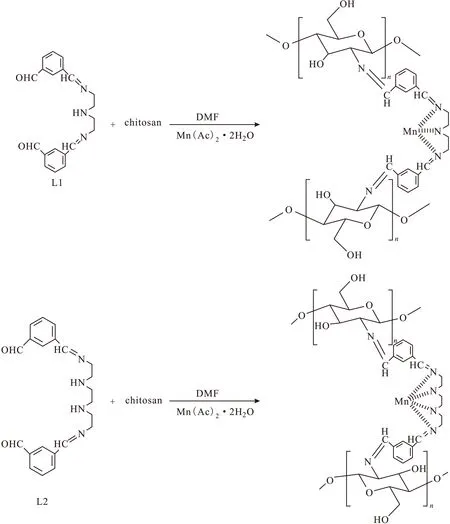
圖1 兩種復合材料的合成路線
1 實驗
1.1 試劑與儀器
二乙烯三胺、三乙烯四胺、間苯二醛、乙醇、甲醇、N,N-二甲基甲酰胺(DMF)、磷酸二氫鈉、磷酸氫二鈉、核黃素(維生素B2)、乙二胺四乙酸二鈉(EDTA)、蛋氨酸(Met),均為分析純,國藥集團化學試劑有限公司,其中二乙烯三胺與三乙烯四胺減壓重蒸后使用,其它試劑均直接使用;三聚磷酸鈉(TPP),分析純,麥克林;殼聚糖(脫乙酰度95%),武漢格奧化學試劑有限公司;氯化硝基四氮唑藍(NBT),阿法埃莎;來源于牛肝的SOD,Sigma公司,保存于-20 ℃冰箱中。
EL204型分析天平,梅特勒-托利多(上海)儀器有限公司;DF-101S型恒溫磁力油浴鍋,鞏義予華儀器廠;DZF-6050型真空干燥箱,上海精宏實驗設備有限公司。
1.2 二乙烯三胺-間苯二醛席夫堿(L1)/三乙烯四胺-間苯二醛席夫堿(L2)的合成
二乙烯三胺先用鈉絲處理數日,至搖晃時沒有明顯氣泡出現。小心地濾除二乙烯三胺中的鈉絲,加入40 g(每500 mL)無水氫氧化鈉顆粒,攪拌加熱2 h。減壓蒸餾,取沸點為156 ℃(0.05 atm下)的餾分作為備用試劑。重蒸后二乙烯三胺顏色明顯變淡,為透明略帶淡黃色液體。
三乙烯四胺處理方法與二乙烯三胺相似,其沸點略高,0.05 atm下約為165 ℃,重蒸后顏色明顯變淡,為透明澄清淡黃色液體。
取重蒸過的二乙烯三胺0.01 mol(1.031 g)溶于20 mL無水乙醇中,將其緩緩滴入40 mL溶有0.021 mol(2.82 g)間苯二醛的乙醇中,于1 h內滴完。滴加完成后繼續反應5 h,期間可見淡黃色沉淀緩緩生成。反應結束后收集沉淀并用甲醇多次洗滌,于40 ℃真空干燥24 h,所得淡黃色粉末即配體L1,備用。
取重蒸過的三乙烯四胺0.01 mol(1.462 g)同法合成配體L2。
1.3 殼聚糖凝膠的制備[18]
將1.5 g 殼聚糖溶于500 mL 1%(m/V)乙酸溶液中,攪拌至完全溶解后靜置1 h使之穩定。后經蠕動泵(100 mL·min-1)將殼聚糖溶液泵入500 mL 0.5 mg·mL-1TPP溶液中,并劇烈磁力攪拌。泵完后繼續劇烈攪拌1 h,所得象牙白懸濁液靜置24 h后,經高速離心(9 000 r·min-1,15 min)分離,并用超純水洗滌5次,保存于水中備用。
1.4 L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料的合成
取L1 0.0025 mol(0.836 g)于40 mL無水DMF中,加熱攪拌使之溶解,再將20 mL溶有0.0026 mol(0.6372 g)二水合醋酸錳的DMF緩緩滴入其中,滴完后繼續攪拌反應5 h。將約1 g殼聚糖凝膠超聲分散于20 mL DMF中,傾倒入上述溶液中,反應24 h。所得固體離心收集,并用乙醇與水各洗滌5次,每次洗滌時固體至少在乙醇或水中浸泡2 h,最終得到紅棕色凝膠,于 40 ℃真空干燥24 h,所得固體仔細研磨,得L1-Mn(Ⅱ)-殼聚糖復合材料。
取L2 0.0025 mol(0.9425 g)同法合成L2-Mn(Ⅱ)-殼聚糖復合材料。
分別用傅立葉變換紅外光譜(FTIR)、掃描電子顯微鏡(SEM)、X-射線光電能譜(XPS)對復合材料進行表征。
1.5 L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料的SOD活性及重復利用性測試
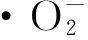
實驗步驟如下:首先稱取12 mg復合材料分散在50 mL PBS溶液中,依照逐級稀釋法配制多種不同濃度的樣品溶液,備用。在測試時,精確量取1 mL樣品溶液以及4.99 mL 0.05 mol·L-1蛋氨酸、1 mL 1.16×10-3mol·L-1NBT、1 mL 8.50×10-5mol·L-1核黃素以及0.01 mL 2.55×10-6mol·L-1EDTA(反應液中添加EDTA是為了掩蔽可能存在的微量金屬離子,避免對測試結果的干擾)。在反應前,先向混合液中鼓入空氣并在黑暗條件下攪拌5 min,之后在光照條件下反應10 min,測定樣品溶液吸光度Asample。用1 mL PBS溶液代替樣品溶液進行空白實驗,測定吸光度Ablank。樣品的抑制率按下式計算:
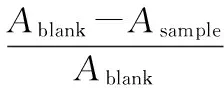
對兩種復合材料進行重復利用性測試。實驗步驟如下:首先進行空白實驗,配制溶液I(總體積為4 mL的PBS溶液中包括0.05 mol·L-1蛋氨酸、1.16×10-3mol·L-1NBT、8.50×10-5mol·L-1核黃素以及2.55×10-6mol·L-1EDTA),向溶液Ⅰ中投入約2 mg樣品,在反應開始前,向混合液中通入空氣在黑暗條件下攪拌5 min,接著在光照條件下反應10 min。測定光照前(Aa)和光照后(Ab)混合液在560 nm處的吸光度,計算抑制率。然后將上述光照后的混合液標記為溶液Ⅱ,向溶液Ⅱ中加入新制得的溶液Ⅰ,重復如上所述的實驗步驟,循環5次。
2 結果與討論
2.1 L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料的表征
2.1.1 紅外光譜分析(圖2)

圖2 L1-Mn(Ⅱ)-殼聚糖(a)/L2-Mn(Ⅱ)-殼聚糖(b)復合材料的紅外光譜Fig.2 FTIR spectra of L1-Mn(Ⅱ)-chitosan(a) and L2-Mn(Ⅱ)-chitosan(b)
由圖2可知,在未與殼聚糖交聯前,配體在1 641 cm-1與1 639 cm-1處可見明顯的吸收峰,為C=N振動吸收峰,該峰的存在表明在合成L1與L2時形成了C=N。同時,在1 692 cm-1與1 693 cm-1處可見清晰吸收峰,該吸收峰為C=O振動吸收峰,說明在合成席夫堿的同時,L1與L2分子中仍存在未反應的醛基,后續反應是可以進行的。在與殼聚糖交聯后,L1的1 692 cm-1處與L2的1 693 cm-1處的吸收峰消失,只剩下1 654 cm-1處的吸收峰,該吸收峰為C=N振動吸收峰,表明L1、L2成功與殼聚糖交聯。
2.1.2 XPS分析(圖3)
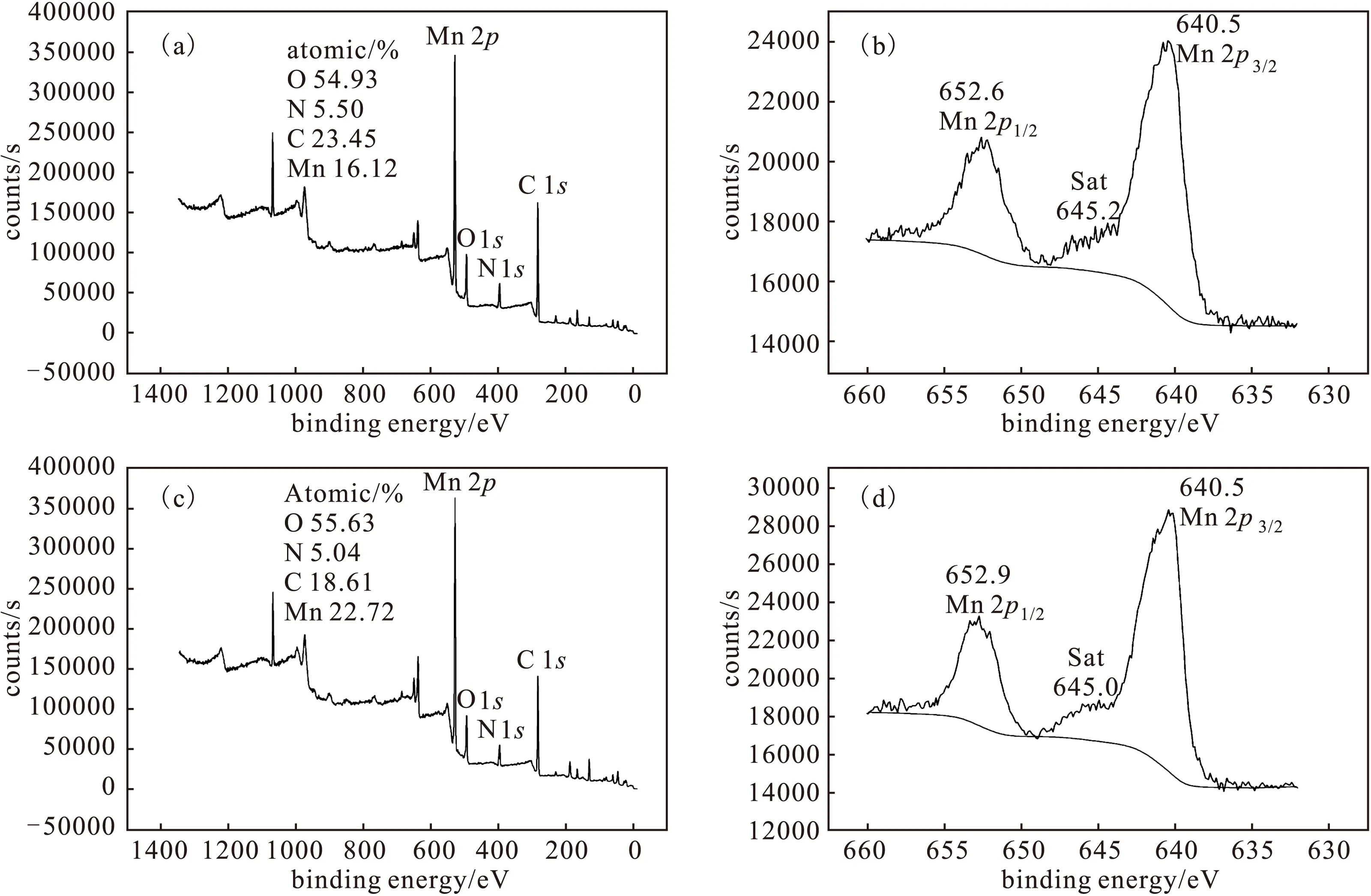
圖3 L1-Mn(Ⅱ)-殼聚糖(a,b)/L2-Mn(Ⅱ)-殼聚糖(c,d)復合材料的XPS全掃描和Mn 2p分峰圖Fig.3 XPS full scan and Mn 2p core-level spectra of L1-Mn(Ⅱ)-chitosan(a,b) and L2-Mn(Ⅱ)-chitosan(c,d)
由圖3a可知,L1-Mn(Ⅱ)-殼聚糖復合材料中含Mn、C、O、N 4種元素,其表層原子含量分別為Mn 16.12%、C 23.45%、N 5.50%、O 54.93%。進一步對Mn元素進行分峰,可見Mn的結合能裂分為2p1/2與2p3/2兩個峰(圖3b),其能量分別為652.6 eV與640.5 eV。
由圖3c可知,L2-Mn(Ⅱ)-殼聚糖復合材料中也含Mn、C、O、N 4種元素,其表層原子含量分別為Mn 22.72%、C 18.61%、N 5.04%、O 55.63%。Mn 2p分峰圖(圖3d)中,Mn的結合能裂分為2p1/2與2p3/2兩個峰,其能量分別為652.9 eV與640.5 eV。
與文獻報道的醋酸錳中Mn元素的結合能2p1/2653.7 eV、2p3/2641.8 eV相比,兩種復合材料中Mn元素的結合能均有明顯的不同。L1的2p1/2與2p3/2的結合能分別減少了1.1 eV和1.3 eV,L2的2p1/2與2p3/2的結合能分別減少了0.8 eV與1.3 eV,這種結合能的減少是由N與Mn的配位引起的。在制備過程中樣品經過多次超聲、離心、洗滌、浸泡,表面不含游離的金屬離子,可以初步判斷Mn與配體發生了配合。
2.1.3 SEM分析(圖4)

a.殼聚糖凝膠 b.干燥并研磨的殼聚糖凝膠 c.未干燥的L1-Mn(Ⅱ)-殼聚糖 d.干燥并研磨的L1-Mn(Ⅱ)-殼聚糖
Fig.4 SEM images of chitosan gel and composites
由圖4可見,干燥前,殼聚糖呈單個顆粒凝膠狀且每個凝膠顆粒由多個更小的顆粒聚合而成(圖4a);干燥并研磨后,殼聚糖表面呈粗糙且富有裂痕的狀態(圖4b)。而未干燥的復合材料呈明顯的交聯狀態,殼聚糖不再是一顆顆單獨的膠粒狀態而是被交聯成一種不規則的凝膠狀(圖4c、e);在干燥后,復合材料的表面均呈光滑且較少龜裂的狀態(圖4d、f)。這種形態上的明顯不同可進一步說明配體對殼聚糖的交聯作用。表明,已成功合成L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料。
2.2 L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料的SOD活性(圖5)
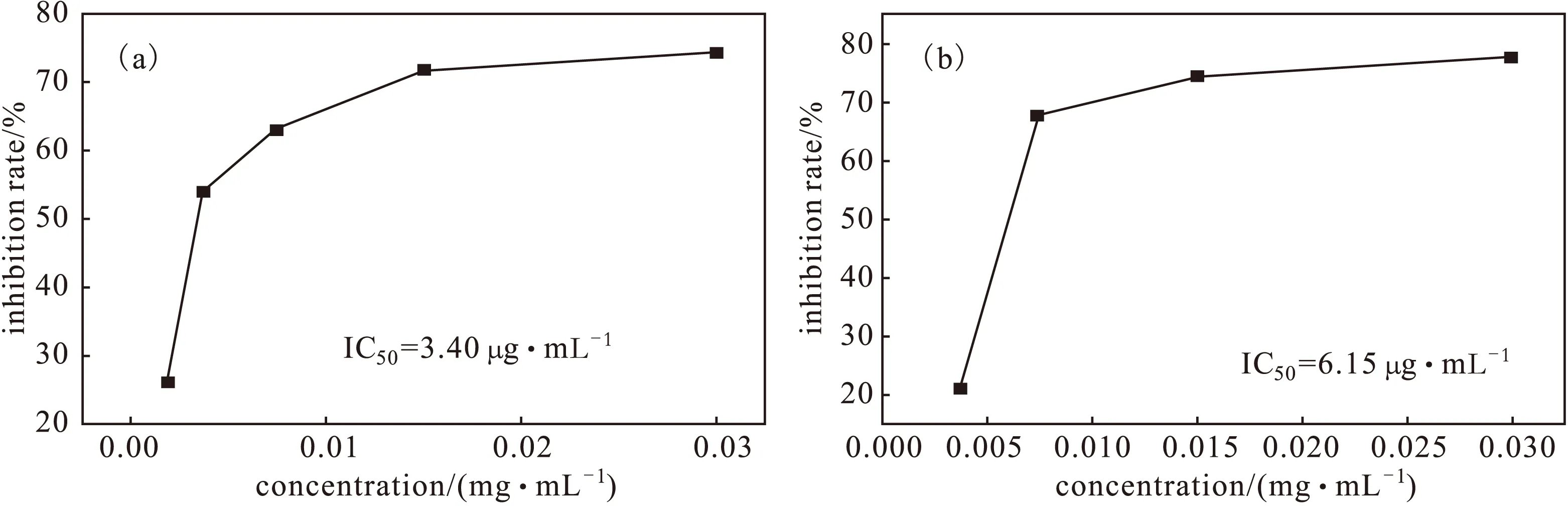
圖5 L1-Mn(Ⅱ)-殼聚糖(a)/L2-Mn(Ⅱ)-殼聚糖(b)復合材料的SOD活性Fig.5 SOD like activities of L1-Mn(Ⅱ)-chitosan(a) and L2-Mn(Ⅱ)-chitosan(b)
由圖5可知,L1-Mn(Ⅱ)-殼聚糖的IC50為3.40 μg·mL-1,而L2-Mn(Ⅱ)-殼聚糖的IC50為6.15 μg·mL-1。
在相同條件下測定了不添加EDTA時天然酶(1 500 U·mg-1)的IC50,為0.7015 μg·mL-1。所合成復合材料的酶活性可達到天然酶的約20%與10%。相比于其它復合材料,如一種席夫堿金屬配合物-白蛋白氨基酸復合材料,其IC50報道為0.1 μmol·L-1,換算結果約為6.643 μg·mL-1。與之相比,所合成的復合材料SOD活性明顯較優。
2.3 重復利用性結果(表1)
表1 L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料的重復利用性結果

Tab.1 Reusability data of L1-Mn(Ⅱ)-chitosan and L2-Mn(Ⅱ)-chitosan
由表1可看出,L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料均有良好的重復利用性,在重復利用5次后仍保持較高的SOD活性。
2.4 殼聚糖與可能存在的游離金屬離子對實驗結果的影響
因殼聚糖本身就具有良好的染料吸附性能,而甲瓚是一種藍色染料。故為排除殼聚糖自身吸附對結果造成的影響,進行如下實驗。取0.2 g新鮮制備的殼聚糖凝膠,超聲分散于10 mL PBS溶液中,取1 mL作為樣品,測定SOD活性。結果表明,濃度為20 μg·mL-1的殼聚糖凝膠因其吸附所產生的SOD 活性(以抑制率表示)為4.25%,而所合成的復合材料在達到50%抑制率時濃度均小于20 μg·mL-1,所以可以排除殼聚糖凝膠吸附甲瓚對實驗結果的影響。
因Mn(Ⅱ)本身就具有很強的SOD活性,為了排除實驗中可能存在的游離Mn(Ⅱ)對結果造成的影響,進行如下實驗。分別取2 mg L1-Mn(Ⅱ)-殼聚糖與L2-Mn(Ⅱ)-殼聚糖,超聲45 s分散于10 mL PBS溶液中,所得懸濁液靜置24 h后于9 000 r·min-1離心15 min,共計3次,所得上清液視為0.2 mg·mL-1溶液。小心取出上清液,將其稀釋至20 μg·mL-1、10 μg·mL-1與1 μg·mL-1,測定SOD活性,結果均未檢出SOD活性。表明復合材料中沒有游離Mn(Ⅱ),復合材料的SOD活性均來源于復合材料本身。
3 結論
以二乙烯三胺、三乙烯四胺分別與間苯二醛反應合成二乙烯三胺-間苯二醛席夫堿(L1)、三乙烯四胺-間苯二醛席夫堿(L2),然后與醋酸錳反應合成了兩種席夫堿-Mn(Ⅱ)配合物,進而與殼聚糖凝膠反應成功合成了L1-Mn(Ⅱ)-殼聚糖/L2-Mn(Ⅱ)-殼聚糖復合材料。XPS結果表明Mn(Ⅱ)與配體生成了配合物,FTIR、 SEM結果表明,配合物與殼聚糖產生了交聯。NBT法測定L1-Mn(Ⅱ)-殼聚糖與L2-Mn(Ⅱ)-殼聚糖的IC50分別為3.40 μg·mL-1與6.15 μg·mL-1,均具有良好的SOD活性和重復利用性。兩種復合材料合成簡單,在醫藥及化妝品領域具有應用潛力。
[1] HE J,JIANG B H.Interplay between reactive oxygen species and microRNAs in cancer[J].Current Pharmacology Reports,2016,2(2):1-9.
[2] ERBAS M,SEKERCI H.Importance of free radicals and occurring during food processing[J].Gida,2011,36(6):349-356.
[3] RAHAL A,KUMAR A,SINGH V,et al.Oxidative stress,prooxidants,and antioxidants:the interplay[J].BioMed Research International,2014,2014:761264.
[4] KANG K A,MEI J P,KIM K C,et al.Fisetin attenuates hydrogen peroxide-induced cell damage by scavenging reactive oxygen species and activating protective functions of cellular glutathione system[J].Vitro Cellular & Developmental Biology Animal,2014,50(1):66-74.
[5] CHATTERJEE S K,MAJI R C,BARMAN S K,et al.Hexacoordinate nickel(Ⅰ)/(Ⅲ) complexes that mimic the catalytic cycle of nickel superoxide dismutase[J].Angewandte Chemie,2014,126(38):10348-10353.
[6] 岳愛國,劉綱勇.SOD在食品和化妝品行業中的應用研究進展[J].廣東化工,2014,41(19):117-118.
[7] ISAACS E J,GREGORY E.Antioxidant for use in cosmetic,medicated and pharmaceutical preparations:US 8221746[P].2012-07-17.
[8] HU X,LIU J,HOU S,et al.Research progress of nanoparticles as enzyme mimetics[J].Science China Physics,Mechanics and Astronomy,2011,54(10):1749-1756.
[9] LU Q,LI X,WANG Y,et al.Catalytic activities of dismution reactions of Cu(bpy)Br2compound and its derivatives as SOD mimics:a theoretical study[J].Journal of Molecular Modeling,2009,15 (11):1397-1405.
[10] PELMENSCHIKOV V,SIEGBAHN P E M.Copper-zinc superoxide dismutase:theoretical insights into the catalytic mechanism[J].Inorganic Chemistry,2005,44:3311-3320.
[11] MILLER A F.Redox tuning over almost 1 V in a structurally conserved active site:lessons from Fe containing superoxide dismutase[J].Accounts of Chemical Research,2008,41:501-510.
[12] PELMENSCHIKOV V,SIEGBAHN P E M.Nickel superoxide dismutase reaction mechanism studied by hybrid density functional methods[J].Journal of the American Chemical Society,2006,128:7446-7475.
[13] BARONDEAU D P,KASSMANN C J,BRUNS C,et al.Nickel superoxide dismutase structure and mechanism[J].Biochemistry,2004,43:8038-8047.
[14] LIN Y,ZHANG L,YAO W,et al.Water-soluble chitosan-quantum dot hybrid nanospheres toward bioimaging and biolabeling[J].ACS Applied Materials & Interfaces,2011,3(4):995-1002.
[15] KIM J Y,JUN J H,KIM S J,et al.Wound healing efficacy of a chitosan-based film-forming gel containing tyrothricin in various rat wound models[J].Archives of Pharmacal Research,2015,38 (2):229-338.
[16] NAGPAL K,SINGH S K,MISHRA D N.Chitosan nanoparticles:a promising system in novel drug delivery[J].Chemical & Pharmaceutical Bulletin,2010,58(11):1423-1430.
[17] YU H,TRAN T T,TEO J,et al.Dry powder aerosols of curcumin-chitosan nanoparticle complex prepared by spray freeze drying and their antimicrobial efficacy against common respiratory bacterial pathogens[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2016,504:34-42.
[18] GAN Q,WANG T,COCHRANE C,et al.Modulation of surface charge,particle size and morphological properties of chitosan-TPP nanoparticles intended for gene delivery[J].Colloids and Surfaces B:Biointerfaces,2005,44(2/3):65-73.
Synthesis,Characterization of Two Novel Schiff Base Manganese(Ⅱ) Complex-Chitosan Composites and Their SOD Like Activity
QU Jun-shen,ZHOU Hong*,PAN Zhi-quan
(SchoolofChemistryandEnvironmentalEngineering,WuhanInstituteofTechnology,Wuhan430073,China)
Using diethylenetriamine,triethylenetetramine,andp-phthalaldehyde as raw materials,we synthesized two novel Schiff base ligands(L1,L2),then synthesized L1/L2-manganese(Ⅱ) complexes with manganese acetate,and further synthesized L1/L2-manganese(Ⅱ)-chitosan composites with chitosan through sol-gel reaction.Moreover,we characterized the structures of the composites by Fourier transform infrared spectroscopy(FTIR),scanning electron microscopy(SEM),and X-ray photoelectron spectroscopy(XPS),and measured their SOD like activities by a nitrobluetetrazolium (NBT) method and reusability.The results showed that the crosslinking of complexes and chitosan were successful,L1/L2-manganese(Ⅱ) complex-chitosan composites had good SOD like activities with IC50of 3.40 μg·mL-1and IC50of 6.15 μg·mL-1,respectively.Two composites were stable,and had good reusability.
Schiff base complex;chotisan;SOD like activity
國家自然科學基金項目(21171135)
2017-03-22
瞿雋申(1989-),男,湖北武漢人,碩士研究生,研究方向:功能配合物合成與性質,E-mail:625797595@qq.com;通訊作者:周紅,教授,E-mail:hzhouh@126.com。
10.3969/j.issn.1672-5425.2017.07.005
O625.632
A
1672-5425(2017)07-0024-07
瞿雋申,周紅,潘志權.兩種新型席夫堿-Mn(Ⅱ)配合物-殼聚糖復合材料的合成表征及其SOD活性[J].化學與生物工程,2017,34(7):24-30.

