載辛伐他汀硫酸鈣對去卵巢大鼠脛骨骨缺損修復的影響
佘遠時 韋敏祥 陳廣祥* 徐又佳
1.南京醫(yī)科大學附屬蘇州醫(yī)院關節(jié)外科,江蘇蘇州215002
2.蘇州大學附屬第二醫(yī)院關節(jié)外科,江蘇蘇州215000)
骨折延遲愈合或骨不連是骨科醫(yī)師臨床上常常遇到的難題,據(jù)統(tǒng)計,大約5% ~10%的骨折會發(fā)生骨折延遲愈合或骨不連接[1],花費巨額的醫(yī)療費用,臨床上對于骨折不連接的治療通常是使用自體髂骨移植,然而,供區(qū)髂骨缺損及供區(qū)的疼痛是我們面臨的問題。
BMP-2(bone morphogenetic protein-2,骨形態(tài)發(fā)生蛋白-2)因其局部成骨活性,而被廣泛應用于臨床骨缺損修復,但是價格非常昂貴[2],同時,BMP-2是異種蛋白,術中大劑量使用,其比較嚴重的并發(fā)癥是導致局部炎癥反應[3],傷口長期滲出,因此,尋找不具有免疫原性同時具有成骨活性的小分子物質(zhì)是我們骨科醫(yī)生長期探索的目標。
辛伐他汀,臨床上常規(guī)使用的降血脂藥物,其作用機制是抑制羥甲基戊二酰輔酶A還原酶(HMGCoA),從而降低肝臟膽固醇的合成[4]。Mundy 等[5]的研究首次表明,他汀類藥物具有激活成骨細胞,同時有學者[6]研究發(fā)現(xiàn)辛伐他汀同時也具有抑制破骨細胞作用,從而促進骨合成代謝作用,促進骨折愈合,而且,已有研究發(fā)現(xiàn),局部應用辛伐他汀同樣具有上述作用,同時,由于口服辛伐他汀肝臟首過效應明顯,生物利用度較低,僅有不到5%的藥物夠能進入血液循環(huán),骨骼中的濃度則更低,同時,在全身使用辛伐他汀,其副作用明顯[7],局部應用辛伐他汀顯得更有前景[8]。
目前使用的骨移植替代物中,硫酸鈣由于具有理想的生物相容性和骨誘導活性而在臨床上大量使用,同時,硫酸鈣作為理想的抗生素或生長因子載體在文獻中也時有報道[9]。
據(jù)此,我們也嘗試將硫酸鈣作為辛伐他汀的載體,隨著硫酸鈣的吸收,辛伐他汀逐漸釋放于靶區(qū),從而持久作用,治療骨質(zhì)疏松骨缺損模型。
1 材料和方法
1.1 材料、試劑與實驗設備
硫酸鈣為Osteoset,(Wright醫(yī)療器械公司,美國),辛伐他汀(海正制藥有限公司),10%水合氯醛,青霉素(華北制藥,中國);Micro-CT機(Siemens公司,美國);生物力學機(MTS公司,美國)。QDR-4 500 W型雙能X線骨密度儀。
1.2 方法
1.2.1 大鼠骨質(zhì)疏松模型的建立及其分組:隨機分組對照動物實驗于2013年6月至2015年6月在蘇州大學骨科研究所完成。健康3月齡雌性SD大鼠48只(體重250~300 g),購自蘇州大學醫(yī)學部實驗動物科學部。質(zhì)量濃度10%的水合氯醛3.3 mL/kg體重腹腔內(nèi)注射麻醉后,仰臥位固定、常規(guī)消毒后經(jīng)腹部正中切口進入腹膜外,切除雙側(cè)卵巢;肌肉注射青霉素4萬U,低鈣飲食,3個月后,隨機選取12只,使用QDR-4 500 W型雙能X線骨密度儀測量骨密度,其余隨機分為3組,分別為骨缺損組,硫酸鈣植骨組,載辛伐他汀硫酸鈣植骨組,每組12只。
1.2.2 辛伐他汀-硫酸鈣混合物的配置:將辛伐他汀溶于75%的酒精中,并制成濃度為200 mg/mL的辛伐他汀酒精溶液,20 mg的硫酸鈣,2.5 μL的辛伐他汀溶液,和5 μL的蒸餾水充分混合,攪拌15 s,然和將混合物轉(zhuǎn)入直徑3 mm,長度3 mm的模具,最后,形成的每粒辛伐他汀-硫酸鈣混合物中含辛伐他汀0.5 mg。單純硫酸鈣顆粒作為對照組。γ射線輻照滅菌備用。
1.2.3 實驗方法:質(zhì)量濃度10%水合氯醛3.3 mL/kg體重腹腔內(nèi)注射麻醉后,置于無菌37℃熱墊上,取右脛骨上段縱行切口,約2 cm,切開脛骨骨膜,并切除3 mm骨膜,用電動擺鋸截斷脛骨,并在骨膜剝離處截除3 mm長脛骨,骨缺損組直接縫合傷口,其余各組分別植入相應的植骨材料,克氏針髓內(nèi)固定脛骨,縫合肌膜(不縫合骨膜),縫合傷口,術后給予患肢克氏針縫線綁扎外固定,肌肉注射4萬U青霉素,自由攝食,自由活動。
1.2.4 主要觀察指標:①大體觀察:定期觀察植入后每組大鼠的切口愈合及活動情況。②Micro-CT檢查:在植入后8周,每組隨機處死4只大鼠,進行Micro-CT掃描,觀察骨痂生長情況,③組織學檢查:于植入后4周、8周,每組隨機處死4只大鼠的標本用10%福爾馬林固定,并用pH7.4,40%的甲酸脫鈣4周,然后石蠟包埋,矢狀位進行標本切片,層厚7 μm,用 HE 染色,然后用光鏡(Olympus,日本東京)進行觀察,參照Lane-Sandhu X射線和組織學評分標準,對各組動物骨愈合程度進行評分。④生物力學分析:將剩余的術后12周的標本剔除軟組織,置于生物力學試驗機,進行三點彎曲試驗,跨徑20 mm,以加壓桿中點在骨折端逐漸施加垂直壓力(2 mm/min)至出現(xiàn)骨折,記錄載荷-變形曲線,得出其最大抗壓載荷及最大彎曲位移。
1.3 統(tǒng)計學處理
測定數(shù)據(jù)采用均數(shù) ±標準差表示,采用SPSS16.0(SPSS公司,美國)進行統(tǒng)計學分析,組間比較采用方差分析和LSD檢驗,P<0.05時差異有統(tǒng)計學意義。
2 結(jié)果
2.1 動物實驗
48只大鼠均進入結(jié)果分析。去勢后,大鼠脛骨骨密度為31.5±5.12 mg/cm2,證實造模成功。術后各組動物進食與活動正常,未發(fā)生切口紅腫、滲液。術后8周,處死動物,骨缺損組及硫酸鈣組,骨折端無骨橋形成,骨折端充滿軟骨細胞及纖維組織,骨折未愈合,而載辛伐他汀硫酸鈣組,骨折遠端與近端部分連接,骨折線消失,骨折端軟骨細胞為骨細胞代替,說明骨折愈合。
2.2 放射學檢查
應用小動物Micro-CT,在相同條件下對小鼠脛骨進行三維CT掃描重建,掃描的各項參數(shù)設置如下:空間分辨率 18 μm,電壓 600 kV,電流 300 μA,掃描時間900 ms。將脛骨骨折端設置為感興趣區(qū)(region of interest,ROI),ROI為圓柱體型,長度為 3 mm,其縱軸與脛骨縱軸平行。掃描結(jié)束后,應用Inveon research workplace分析軟件(Version 3.0,Siemens Medical Solutions,美國),根據(jù)文獻介紹的方法對骨微結(jié)構(gòu)進行分析。測量指標包括骨體積分數(shù)(BV/TV)、組織骨密度(tBMD),骨小梁數(shù)量(Tb.N)①未植骨組:植入后8周,骨折端間隙清楚,未見連續(xù)骨小梁,骨缺損形成。②硫酸鈣組:植入后8周,骨折線模糊,異種骨顯示不清。③載辛伐他汀硫酸鈣組:植入后8周,骨折端骨小梁連續(xù),形成骨性融合。植入后8周,ROI區(qū)內(nèi) BV/TV,tBMD,Tb.N,載辛伐他汀組較硫酸鈣組和未植骨組相比,差異具有統(tǒng)計學意義。載辛伐他汀硫酸鈣組優(yōu)于后兩組。
2.3 組織學檢查
植入后4周(圖1),8周(圖2)①未植骨組:骨折間隙存在,僅見纖維組織。②硫酸鈣組:新生骨逐漸成熟,但中間仍是纖維組織,硫酸鈣人工骨仍可見殘余;可見大量編織骨相互融合成片。③載辛伐他汀硫酸鈣組:硫酸鈣人工骨可見殘余顆粒,可見編織骨,硫酸鈣人工骨內(nèi)部可見纖維組織增生,血管長入;逐漸出現(xiàn)編織骨,軟骨組織增多并開始分化為骨組織,見新生骨逐漸改建,并在8周有大量編織骨相互融合成片。按照Lane-Sandhu組織學標準評分,各時間點3組骨愈合程度組內(nèi)差異均有統(tǒng)計學意義(P<0.05),組間比較載辛伐他汀硫酸鈣組優(yōu)于硫酸鈣組和未植骨組。
2.4 生物力學測試
術后12周,生物力學測試顯示,三組最大載荷分別為:辛伐他汀硫酸鈣組103.96±6.32 N,硫酸鈣組81.16±6.67 N,未植骨組為9.42±5.51 N,辛伐他汀硫酸鈣組較硫酸鈣組和未植骨組相比差異有統(tǒng)計學意義(P<0.05)。
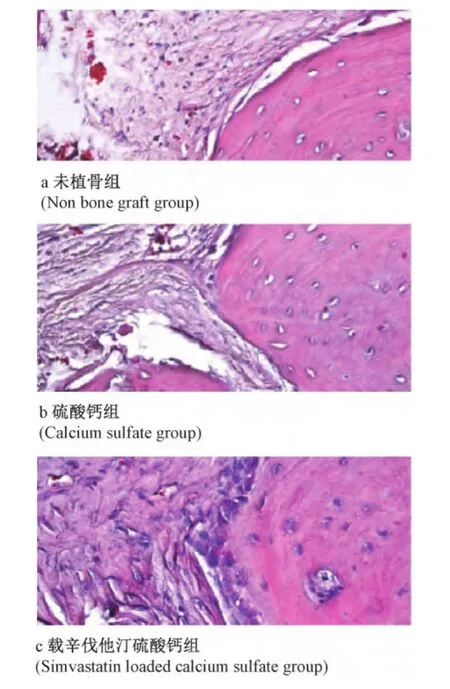
圖1 術后4周骨折端組織學檢查(HE染色)a未植骨組;b硫酸鈣組;c載辛伐他汀硫酸鈣組Fig.1 Histological observation of fracture site in each group at 4 weeks after surgery(H&E staining)(Non bone graft group);(Calcium sulfate group);(Simvastatin loaded calcium sulfate group)
3 討論
隨著人口的老齡化,骨折延遲愈合甚至骨不連給社會造成了嚴重的經(jīng)濟負擔。盡管不少促進骨代謝的藥物得到研究并發(fā)展,但是還沒有被美國FDA允許獲得通過。辛伐他汀,作為臨床常用的降脂藥物,顯示了相當?shù)墓谴x作用[5]。
硫酸鈣人工骨作為臨床上常用的骨移植替代材料,其應用研究已有1個世紀之久,在骨科領域硫酸鈣具有獨特的優(yōu)勢:生物相容性好,其與骨界面間無明顯炎癥、異物反應,未見中性粒細胞、巨噬細胞聚集;可被破骨細胞吸收,體內(nèi)完全降解,其降解的時間為4~8周,與新骨形成的速度基本一致[10]。良好的空間充填作用;有一定支撐強度;有骨傳導作用和潛在的骨誘導活性,這可能與其降解過程中局部的微環(huán)境有關,硫酸鈣在體內(nèi)逐漸降解,局部可以形成高鈣環(huán)境,可為新生的骨組織提供鈣源,從而不同程度地促進成骨細胞增殖、分化。目前主要是作為抗生素載體和成骨因子載體[9]。Turner等[11]把含有10%硫酸妥布霉素的硫酸鈣片植入狗肱骨近端骨缺損內(nèi),發(fā)現(xiàn)植入部位周圍組織硫酸妥布霉素濃度可以持續(xù)增高至14 d,一些動物可以持續(xù)到28 d,4周時缺損區(qū)內(nèi)被新生骨組織填充。Beardmore等[12]成功應用含10%硫酸妥布霉素的硫酸鈣片與脫鈣骨基質(zhì)聯(lián)合治療預防了羊脛骨近端污染骨折感染的發(fā)生,提示硫酸鈣促進成骨但不妨礙抗生素防治感染的作用。本實驗中,術后8周,影像學及組織學結(jié)果均顯示,硫酸鈣組較骨缺損組,骨痂形成量明顯增加。
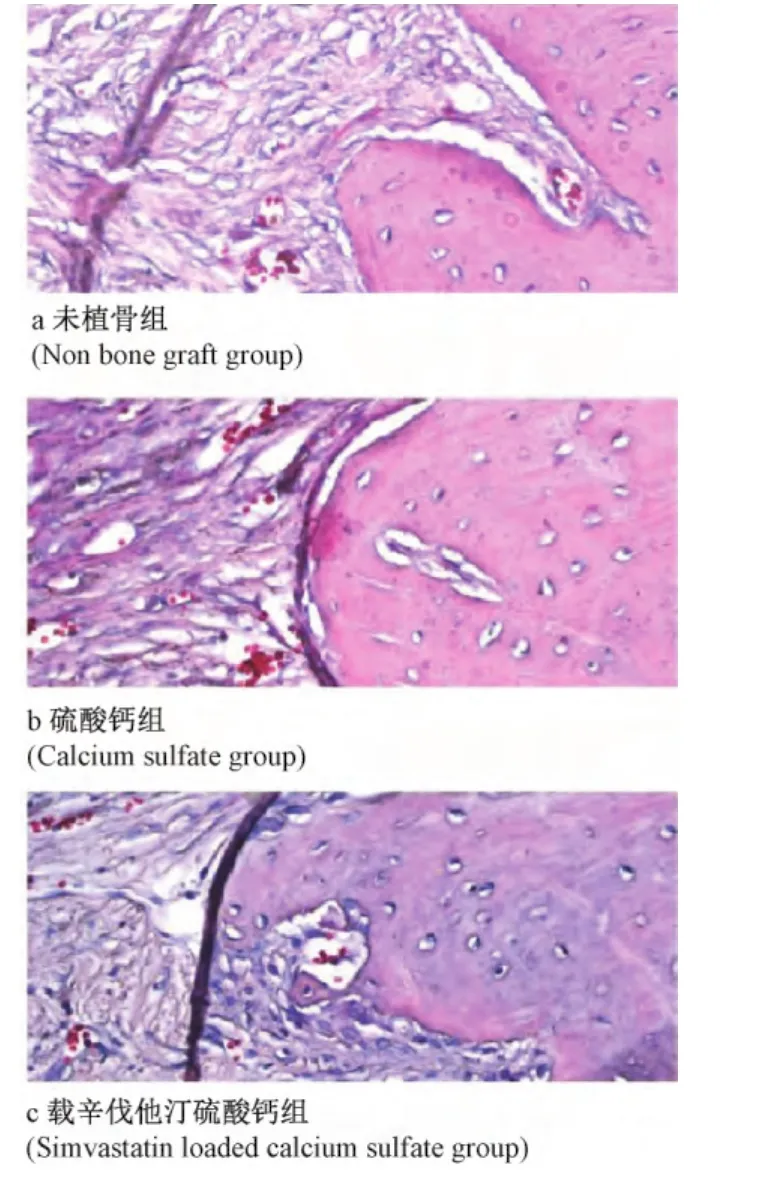
圖2 術后8周骨折端組織學檢查(HE染色)a未植骨組;b硫酸鈣組;c載辛伐他汀硫酸鈣組Fig.2 Histological observation of fracture site in each group at 8 weeks after surgery(H&E staining)(Nonbonegraftgroup);(Calciumsulfategroup);(Simvastatin loaded calcium sulfate group)
既往文獻報道,骨折端局部使用辛伐他汀對骨折愈合有促進作用,目前比較一致的觀點認為,辛伐他汀的促進成骨作用與BMP-2的表達水平增加有關[5]。辛伐他汀是通過增加BMP-2啟動因子的數(shù)量,從而促進成骨細胞合成BMP-2,BMP-2是公認的成骨細胞轉(zhuǎn)化促進因子,Sugiyama等[13]建立含人骨形態(tài)發(fā)生蛋白(BMP-2)啟動因子基因部分,并將其轉(zhuǎn)入人的骨肉瘤細胞,克隆培養(yǎng),并向培養(yǎng)液中加入辛伐他汀,利用蟲熒光素酶作媒介體進行檢測,發(fā)現(xiàn)辛伐他汀可以大大增加BMP-2啟動因子數(shù)量,從而促進成骨細胞合成BMP-2,因此認為辛伐他汀對骨組織的作用是通過BMP-2的介導促進骨生成。BMP-2具有募集間充質(zhì)細胞并誘導其向成軟骨細胞或成骨細胞分化;同時可以協(xié)同其他調(diào)節(jié)因子參與骨組織形成[14]。本研究發(fā)現(xiàn),術后8周,載辛伐他汀硫酸鈣組Micro-CT片顯示骨折端骨折線較模糊,骨痂量增加,骨痂BMD明顯升高,組織學檢查鏡下編織骨已轉(zhuǎn)化為板層骨,骨小梁成熟度高,排列規(guī)整,術后12周時生物力學表現(xiàn),載辛伐他汀硫酸鈣組,其最大載荷103.96±6.32 N,可以看出,辛伐他汀-硫酸鈣不僅可以顯著增加骨折愈合的數(shù)量和質(zhì)量,而且加速骨折愈合的速度,縮短骨折愈合時間,這為尋找用于臨床治療和預防骨質(zhì)疏松性骨折的他汀類藥物或擬似物提供了實驗依據(jù).
由于辛伐他汀具有良好的生物相容性和穩(wěn)定性,加上硫酸鈣良好的藥物載體,局部使用可以減輕全身使用所引起的副作用,避免骨折端的感染發(fā)生,已有文獻報道關于局部使用辛伐他汀的用量問題。Wang等[15]發(fā)現(xiàn)0.5 mg辛伐他汀聯(lián)合膠原基質(zhì)局部應用治療兔顱蓋骨骨缺損,術后14 d,其新骨形成較單獨使用膠原基質(zhì)組增加308%;Stein等[16]發(fā)現(xiàn)0.5 mg辛伐他汀可以產(chǎn)生最佳的骨生長/炎癥比,從而認為該量是理想的單次局部應用劑量。基于這些文獻,本實驗中,骨折端植骨使用的復合物也含0.5 mg辛伐他汀,術后,載辛伐他汀硫酸鈣組局部骨痂量增加,骨形成增加,局部最大載荷增加,說明局部使用辛伐他汀硫酸鈣具有良好的骨形成調(diào)節(jié)作用,此外,本研究未發(fā)現(xiàn)嚴重的副作用。
綜上所述,載辛伐他汀硫酸鈣具有與自體骨移植相似的骨修復能力,可以促進骨缺損的修復,促進骨折愈合,但實驗并沒有進行深入探討辛伐他汀在顆粒中的分布、釋放情況,這也是本次實驗的局限性。

