低溫振蕩法提取甘草酸工藝優(yōu)化研究
豆康寧,王飛
(漯河醫(yī)學(xué)高等專科學(xué)校 食品營養(yǎng)系,河南 漯河 462002)
低溫振蕩法提取甘草酸工藝優(yōu)化研究
豆康寧,王飛
(漯河醫(yī)學(xué)高等專科學(xué)校 食品營養(yǎng)系,河南 漯河 462002)
低溫振蕩法是提取植物生物活性物質(zhì)的一種有效方法,文章研究了低溫振蕩法提取甘草酸的工藝條件。首先用單因素試驗(yàn)研究了提取時(shí)間、料液比、振蕩速度對(duì)甘草酸提取率的影響,然后用正交試驗(yàn)設(shè)計(jì)對(duì)工藝條件進(jìn)行了優(yōu)化。試驗(yàn)結(jié)果表明:甘草酸提取率隨著提取時(shí)間的延長和振蕩速度的增加而增加,隨著料液比的增加而降低。甘草酸提取最佳條件是:提取時(shí)間150 min、料液比0.01 (g/mL)、振蕩速度140 r/min,其中提取時(shí)間因素影響顯著。在該條件下,甘草酸提取率達(dá)到2.51%。低溫振蕩法與蒸煮法和超聲波法相比,提取150 min后,甘草酸提取率相差不大。
甘草酸;低溫振蕩;提取工藝
甘草酸是甘草中生理活性成分之一[1],是甘草甜味的主要成分,由1分子甘草次酸和2分子葡萄醛酸組成,其甜度為蔗糖的150倍,有濃郁的甘草特殊香味,是高血壓、糖尿病、肥胖癥、心臟病患者食用的最理想的甜味劑,具有低熱能、高甜度、安全、無毒和較強(qiáng)的保健功能,有解毒、護(hù)肝、消炎、增香等功效,是非常理想的純天然甜味劑[2]。除此之外,甘草酸能使咸味很重的食品口感變得更柔和,使食品的后味更醇香,常作為醬菜、面醬、醬油中的矯味劑,可抑制鹽味和苦味[3]。在果汁飲料或其他非碳酸飲料的產(chǎn)品中配合使用甘草酸,會(huì)讓口感變得清涼可口。在涼果、蜜餞中使用,能有效突出產(chǎn)品風(fēng)味,使其甘甜味綿長[4]。
目前,對(duì)甘草酸提取方法的研究比較多,如用水蒸煮浸提,用混合溶劑浸提,用銨性醇溶液浸提,采用微波、超聲波輔助浸提等[5]。但是,這些方法普遍采用的提取溫度都比較高,對(duì)甘草酸的生物活性具有一定影響;根據(jù)文獻(xiàn)報(bào)道,對(duì)低溫振蕩提取法研究相對(duì)較少,對(duì)甘草酸提取工藝參數(shù)的優(yōu)化研究相對(duì)較少。因此,本文采用低溫振蕩法提取甘草中的甘草酸,先用單因素試驗(yàn)研究提取時(shí)間、料液比、振蕩速度對(duì)甘草酸提取率的影響,然后用正交試驗(yàn)對(duì)該提取工藝參數(shù)進(jìn)行優(yōu)化[6],最后對(duì)低溫振蕩法、蒸煮法和超聲波法提取甘草酸進(jìn)行比較。甘草酸的測(cè)定方法應(yīng)用液相色譜法(HPLC)測(cè)定,所用溶劑是甲醇、醋酸銨溶液和乙酸復(fù)合物。本研究為低溫振蕩法提取甘草酸工藝及甘草酸的應(yīng)用提供了實(shí)驗(yàn)依據(jù)。
1 實(shí)驗(yàn)材料與設(shè)備
1.1 主要試劑與材料
甘草:品種為烏拉爾甘草,生長方式為種植,產(chǎn)地為寧夏鹽池,生長期為3年,通過市售采購;甘草酸銨標(biāo)準(zhǔn)品:色譜純,西安匯林生物科技有限公司;甲醇:色譜純,天津四友精細(xì)化學(xué)品有限公司;乙酸、醋酸銨:分析純,天津市科密歐化學(xué)試劑有限公司;水:一級(jí)純凈水,實(shí)驗(yàn)室自制。
1.2 主要儀器與設(shè)備
LC1260型高壓液相色譜儀(HPLC),100 Conc型紫外可見分光光度計(jì) Agilent公司;YP3001N型電子天平 上海精密科學(xué)儀器有限公司;DFT-200型萬能粉碎機(jī) 溫嶺市林大機(jī)械有限公司;RYC-111型搖床 上海福瑪實(shí)驗(yàn)設(shè)備有限公司;X-22R型冷凍離心機(jī) Allegra公司;202A型電熱恒溫干燥箱 南京萊步科技實(shí)業(yè)有限公司;VS-100UE 型恒溫超聲波提取機(jī) 無錫沃信儀器有限公司。
2 實(shí)驗(yàn)方法
2.1 流動(dòng)相的制備[7]
流動(dòng)相的制備方法按照GB/T 22248-2008《保健食品中甘草酸的測(cè)定》進(jìn)行制備,具體方法是:先將醋酸銨配制成0.2 mol/mL,然后配制流動(dòng)相,流動(dòng)相的組成比例為:甲醇∶0.2 mol/mL醋酸銨溶液∶乙酸為67∶32∶1。
2.2 甘草酸銨標(biāo)準(zhǔn)曲線的建立
配制不同濃度的甘草酸銨溶液(0~400 μg/mL),采用HPLC測(cè)定不同濃度甘草酸銨溶液的吸收峰面積,建立甘草酸銨濃度和吸收峰面積之間的標(biāo)準(zhǔn)曲線,作為測(cè)定計(jì)算甘草中甘草酸含量的依據(jù)。
2.3 HPLC樣品的制備
將甘草根部用萬能粉碎機(jī)粉碎成20目的粉末,稱量一定量的甘草樣品,放入錐形瓶中,再加入50 mL流動(dòng)相,放入搖床中,設(shè)置好搖床振蕩速度,溫度為30 ℃,然后振蕩提取。提取結(jié)束后,用高速離心機(jī)分離甘草提取液,轉(zhuǎn)速為10000 r/min,時(shí)間為10 min。取離心后的上清液,用0.45 μm微孔濾膜過濾后作為HPLC試樣。
2.4 甘草酸銨吸收波長的確定
配制1%的甘草酸銨溶液,用紫外可見分光光度計(jì)掃描甘草酸銨的吸收峰位置,作為HPLC檢測(cè)器的波長。
2.5 HPLC分析條件
色譜柱:C18柱,尺寸為4.6 mm×20 cm,柱溫35 ℃;流動(dòng)相組成比例:甲醇∶0.2 mol/mL醋酸銨溶液∶乙酸為67∶32∶1;UV檢測(cè)波長:252 nm;進(jìn)樣方式:手動(dòng);進(jìn)樣量10 μL;流量0.8 mL/min。
2.6 甘草中水分含量的測(cè)定[8]
在計(jì)算甘草酸的提取率時(shí),按照甘草的干重計(jì)算,便于分析比較,因此需要測(cè)定計(jì)算2.3中甘草樣品的水分含量。甘草中水分含量的測(cè)定按照GB 5009.3-2010《食品中水分的測(cè)定》方法進(jìn)行測(cè)定。
2.7 甘草酸提取率的計(jì)算
甘草酸提取率(%)=M甘草酸/[M甘草樣品×(1-7.2%)]×100%,其中M表示質(zhì)量(g),7.2%表示甘草中的水分含量。
2.8 甘草酸提取方法對(duì)比
對(duì)低溫振蕩法、蒸煮法、超聲波法提取甘草中甘草酸的提取率進(jìn)行比較,分析提取率的大小與差距。其中,低溫振蕩法提取參數(shù)是:提取時(shí)間150 min、料液比0.01 (g/mL)、振蕩速度140 r/min;蒸煮法提取參數(shù)是: 提取時(shí)間150 min、料液比0.01 (g/mL)、溫度100 ℃;超聲波提取參數(shù)是:提取時(shí)間150 min、料液比0.01 (g/mL)、超聲頻率20 kHz、功率200 W。
3 實(shí)驗(yàn)結(jié)果與分析
3.1 甘草酸銨的吸收峰波長確定
將1%濃度的甘草酸銨溶液用紫外可見分光光度計(jì)進(jìn)行掃描吸收光譜,結(jié)果見圖1。

圖1 甘草酸銨吸收光譜
圖1中最大吸收峰位置為252.0 nm。因此,進(jìn)行測(cè)定甘草樣品中甘草酸含量時(shí),HPLC檢測(cè)器的波長也設(shè)置為252.0 nm。
3.2 甘草酸銨標(biāo)準(zhǔn)曲線建立

圖2 甘草酸銨標(biāo)準(zhǔn)曲線圖
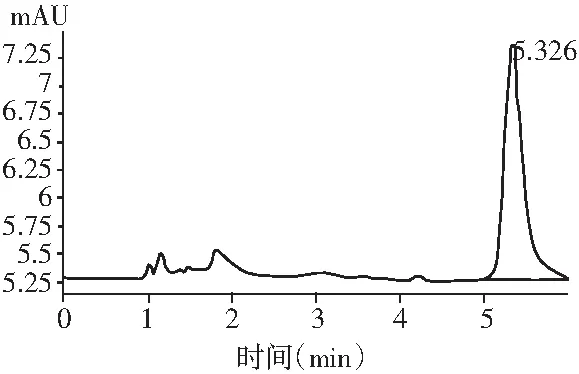
圖3 甘草酸銨HPLC測(cè)定出峰圖
3.3 提取時(shí)間、料液比和振蕩速度對(duì)甘草酸提取率的影響
3.3.1 提取時(shí)間對(duì)甘草酸提取率的影響
在振蕩速度為120 r/min、料液比為0.01 (g/mL)的條件下,分別提取0,30,60,90,120,150 min,甘草酸提取率見圖4。
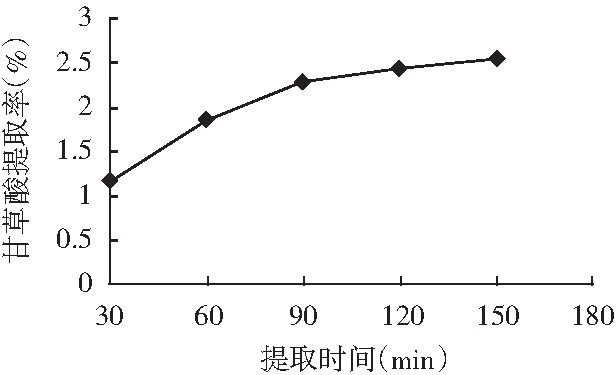
圖4 提取時(shí)間對(duì)甘草酸提取率的影響
由圖4可知,隨著提取時(shí)間的延長,甘草酸提取率開始增加較大,90 min后提取率增加幅度變得緩慢,提取150 min與90 min相比,對(duì)甘草酸提取率增加很小。這說明開始提取時(shí),物料中甘草酸含量高,溶劑中甘草酸濃度低,甘草酸的溶解速度較快,當(dāng)大部分提取后,物料中少部分的甘草素溶解速度大大下降。因此,在正交試驗(yàn)因素水平設(shè)計(jì)中,選擇提取時(shí)間為90,120,150 min進(jìn)行優(yōu)化。綜合考慮提取效率與成本,下面的單因素試驗(yàn)中提取時(shí)間取120 min進(jìn)行。
3.3.2 料液比對(duì)甘草酸提取率的影響
根據(jù)硼鎂改性磷酸二氫鋁的穩(wěn)定性研究,當(dāng)Na2B4O7·10H2O添加量超過3.0g時(shí)粘結(jié)劑穩(wěn)定性變差,在固定MgSO4加入量為4g且不加入H3PO4改性聚乙烯醇的情況下,使用硼鎂改性磷酸鹽混砂制樣,測(cè)試強(qiáng)度圖1。
當(dāng)提取時(shí)間為120 min、振蕩速度為120 r/min時(shí),料液比分別為0.01,0.02,0.03,0.04,0.05 (g/mL)的甘草酸提取率見圖5。
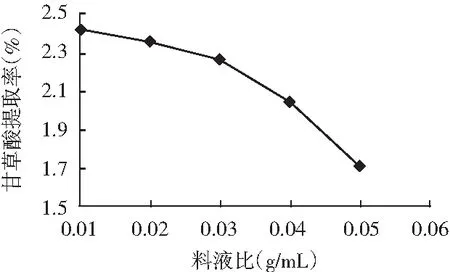
圖5 料液比對(duì)甘草酸提取率的影響
由圖5可知,隨著料液比的增加,甘草酸提取率開始下降幅度較小,料液比超過0.03 (g/mL)之后,提取率下降幅度較大。物料濃度對(duì)甘草酸在溶劑中的浸出具有一定影響,物料濃度越大,甘草酸的浸出速度會(huì)下降,需要多次提取。因此,在正交試驗(yàn)因素水平設(shè)計(jì)中,選擇料液比為0.01,0.02,0.03 (g/mL)進(jìn)行優(yōu)化。
3.3.3 振蕩速度對(duì)甘草酸提取率的影響
當(dāng)提取時(shí)間為120 min、料液比為0.01 (g/mL),振蕩速度為60,80,100,120,140 r/min時(shí),甘草酸的提取率見圖6。
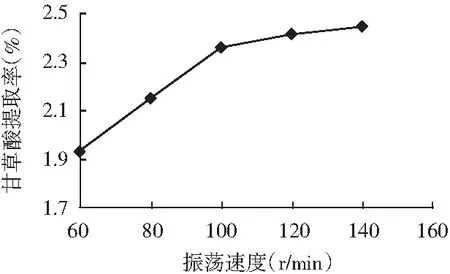
圖6 振蕩速度對(duì)甘草酸提取率的影響
由圖6可知,隨振蕩速度的增加,甘草酸提取率開始增加幅度較大,振蕩速度超過100 r/min之后,提取率增加幅度變小。隨著振蕩速度的增加,物料在溶劑中混合越充分,甘草酸的浸出率增加,但是當(dāng)振蕩速度達(dá)到一定值時(shí),甘草酸提取率受其影響變得較小。因此,在正交試驗(yàn)因素水平設(shè)計(jì)中,選擇振蕩速度為100,120,140 r/min進(jìn)行正交試驗(yàn)優(yōu)化。
3.4 正交優(yōu)化試驗(yàn)結(jié)果與討論
3.4.1 正交試驗(yàn)表頭設(shè)計(jì)
根據(jù)前面的單因素試驗(yàn)所得三因素三水平,制作成正交試驗(yàn)表頭,見表1。
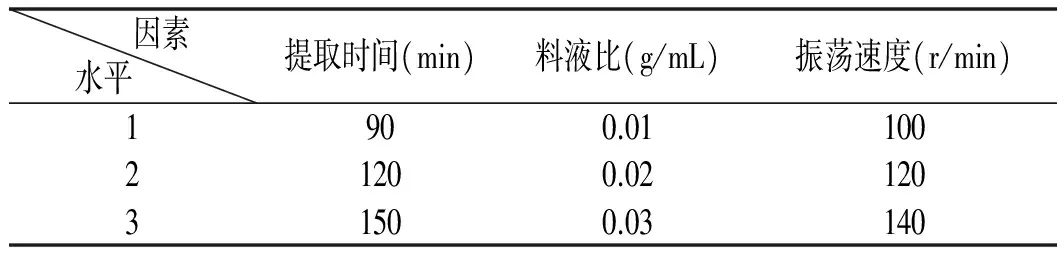
表1 正交試驗(yàn)表頭
3.4.2 正交試驗(yàn)結(jié)果
采用正交設(shè)計(jì)軟件助手,對(duì)表1中的數(shù)據(jù)進(jìn)行三因素三水平試驗(yàn),試驗(yàn)結(jié)果見表2。
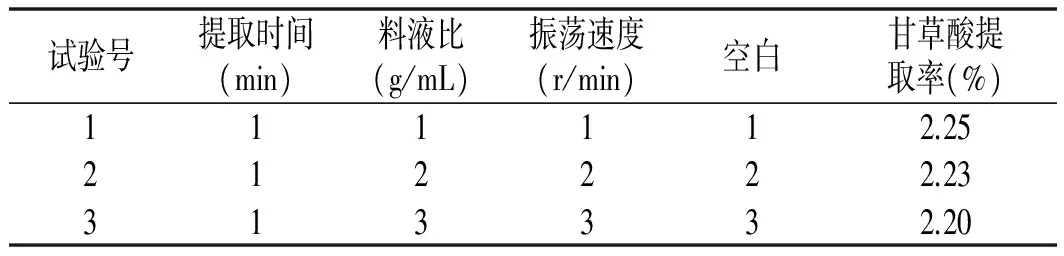
表2 正交試驗(yàn)結(jié)果
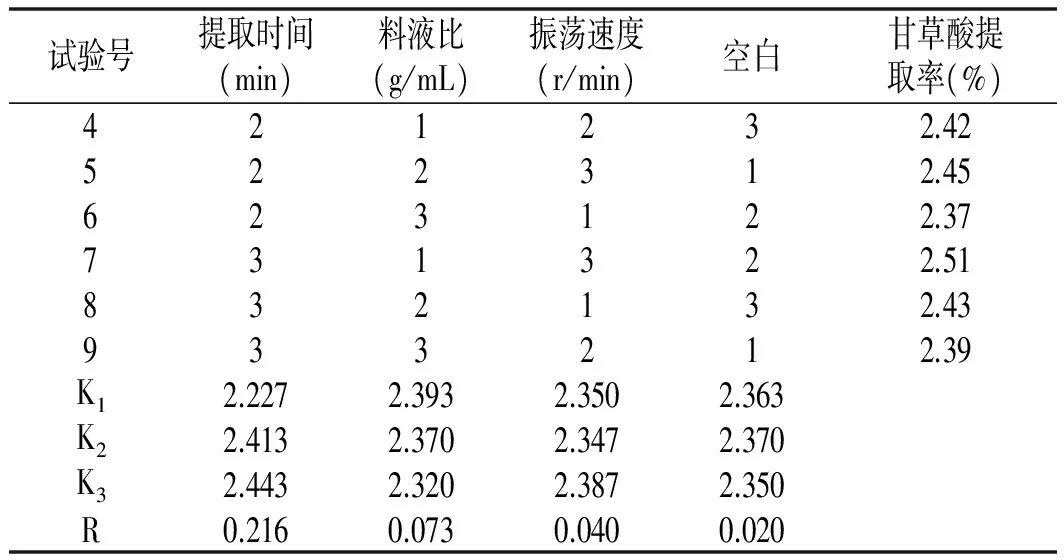
續(xù) 表
3.4.2.1 極差分析結(jié)果
由表2中正交試驗(yàn)統(tǒng)計(jì)分析結(jié)果R值可知,影響甘草酸提取率的因素大小順序依次是提取時(shí)間、料液比、振蕩速度,最佳因素組合是:提取時(shí)間150 min、料液比0.01 (g/mL),振蕩速度140 r/min。經(jīng)試驗(yàn)驗(yàn)證,在該條件下,甘草酸的提取率達(dá)到2.51%,與表2中試驗(yàn)序號(hào)6相同。
3.4.2.2 方差分析
以空白列為誤差,在顯著水平為0.05的基礎(chǔ)上,對(duì)甘草酸低溫振蕩提取正交試驗(yàn)進(jìn)行方差分析,其結(jié)果見表3。
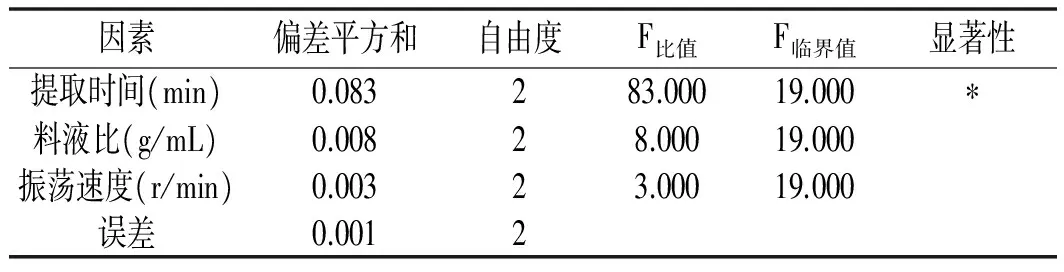
表3 方差分析結(jié)果
由表3方差分析可知,提取時(shí)間對(duì)甘草酸提取率影響顯著,而料液比、振蕩速度對(duì)甘草酸提取率影響不顯著。這說明在正交試驗(yàn)的因素水平范圍內(nèi),影響甘草酸提取率的因素是提取時(shí)間。但是,如果因素的水平不在該正交試驗(yàn)范圍內(nèi),通過單因素試驗(yàn)發(fā)現(xiàn),當(dāng)料液比較大、振蕩速率比較小時(shí),對(duì)提取率的影響也比較大,因此不能忽略。
3.4.3 幾種甘草酸提取方法對(duì)比
通過低溫振蕩法、蒸煮法、超聲波法提取甘草中甘草酸,其甘草酸提取率隨時(shí)間的延長見圖7。

圖7 提取時(shí)間對(duì)甘草酸提取率的影響
由圖7可知,在低溫振蕩法、蒸煮法、超聲波法提取甘草中甘草酸的過程中,隨著提取時(shí)間的延長,甘草酸提取率增加幅度開始較快,提取一段時(shí)間之后,增加幅度變得較小。其中,在前60min內(nèi),超聲波法提取效率最高,其次是蒸煮法和低溫振蕩提取法。但是,提取時(shí)間超過120min后,該3種提取方法的甘草酸提取率越來越接近,提取時(shí)間達(dá)到150min時(shí),超聲波法甘草酸提取率比蒸煮法高1.96%,比低溫振蕩法高3.58%。應(yīng)用蒸煮法提取甘草酸時(shí),提取溫度比較高,在超聲波提取過程中,溶劑因超聲波的作用,溫度也會(huì)逐漸升高[10],這對(duì)甘草酸的生物活性有一定的影響。因此,為了保證甘草酸的生物活性,將原料顆粒度粉碎到很細(xì)之后,采用低溫振蕩提取法,與蒸煮法和超聲波法相比,其甘草酸的提取率相差不大。
4 結(jié)論
采用低溫振蕩法提取甘草酸時(shí),隨著提取時(shí)間的延長,甘草酸提取率先增加較快,之后增加幅度變小;隨著料液比的增大,甘草酸提取率下降速度開始較小,之后下降幅度較大;隨著振蕩速度的增加,甘草酸提取率先增加較快,之后增加幅度變小。低溫振蕩法提取甘草酸的最佳因素水平組合是提取時(shí)間150 min、料液比0.01(g/mL),振蕩速度120 r/min,提取率達(dá)到2.51%。與蒸煮法和超聲波法相比,低溫振蕩法提取甘草酸的速度較慢,但是,當(dāng)提取150 min時(shí),提取率相差不大,而且能夠保護(hù)甘草酸的生物活性。
[1]常雅萍,畢無邪,楊貴貞.甘草多糖抗病毒作用研究[J].中草藥,1989,14(4):44-46.
[2]汲晨鋒,姜薇,王曉晶.甘草多糖的化學(xué)與藥理研究[J].哈爾濱商業(yè)大學(xué)學(xué)報(bào)(自然科學(xué)版),2004,20(5):515-518.
[3]隋敬達(dá).低鹽甘草保健醬油及其制造工藝[P].中國專利:98100015.0,1997.
[4]鄭炯,黃明發(fā),張甫生.甘草甜素的生理功能及其在食品工業(yè)中的應(yīng)用[J].中國食品添加劑, 2007(2):165-168.
[5]程謙偉,孟陸麗,何仁,等.響應(yīng)面優(yōu)化超聲波輔助提取百香果籽油工藝研究[J].糧油加工,2010(8):6-8.
[6]章銀良.食品與生物試驗(yàn)設(shè)計(jì)與數(shù)據(jù)分析[M].北京:中國輕工業(yè)出版社,2010.
[7]GB/T 22248-2008,保健食品中甘草酸的測(cè)定[S].
[8]GB 5009.3-2010,食品中水分的測(cè)定[S].
[9]李炳奇,汪河濱,李學(xué)禹,等.超聲法聯(lián)合提取甘草黃酮和甘草酸的研究[J].山東中醫(yī)雜志,2005,24(1):38-40.
[10]魯守平,孫群,王建華,等.甘草中有效成分甘草酸的提取和測(cè)定方法研究概況[J].中國中藥雜志,2006,31(5):357-360.
Research on Optimization of Glycyrrhizic Acid Extraction byLow-temperature Oscillation
DOU Kang-ning, WANG Fei
(Department of Food Nutrition, Luohe Medical College, Luohe 462002, China)
It is an effective method to extract plant biological active substances by low-temperature oscillation, in this paper, glycyrrhizic acid extracted by low-temperature oscillation is researched. Firstly, the relationship among extraction time, solid-liquid ratio and oscillation speed is researched by single factor experiments, and then the technological conditions are optimized by orthogonal test design. The experimental results show that the extraction yield of glycyrrhizic acid is increased as the extraction time extending and oscillation speed increasing, but the extraction yield of glycyrrhizic acid is decreased as the solid-liquid ratio increasing. The optimum conditions for extracting glycyrrhizic acid are determined as follows: extraction time is 150 min, solid-liquid ratio is 0.01 (g/mL), oscillation speed is 140 r/min, under these experimental conditions, the extraction yield of glycyrrhizic acid reaches 2.51%. Compared with the methods of boiling and ultrasonic wave, the extraction yield of glycyrrhizic acid is low if it is extracted for 150 min by low-temperature oscillation.
glycyrrhizic acid;low-temperature oscillation;extraction process
2017-03-10
河南省漯河市2015年度青年拔尖人才資助項(xiàng)目
豆康寧(1981-),男,甘肅靜寧人,講師,碩士,研究方向:食品加工與檢測(cè)技術(shù)。
TS207.3
A
10.3969/j.issn.1000-9973.2017.08.030
1000-9973(2017)08-0138-04

