工藝流程題解題技巧淺析
林景勝廣東省湛江市徐聞縣實驗中學
工藝流程題解題技巧淺析
林景勝
廣東省湛江市徐聞縣實驗中學
全國Ⅰ卷理綜化學中的工藝流程題得分率不高,是因為該題目考試內(nèi)容變化大,考題模式多,學生難以抓住考試規(guī)律。本文作者從近三年理綜化學工藝流程題常見考試內(nèi)容及考題出題模式進行分析,談?wù)勗擃}如何下手,如何從課本基礎(chǔ)問題進行知識延伸解決部分常見問題。
聯(lián)系課本;金屬;非金屬;流程圖
工藝流程題主要考查無機物性質(zhì),書寫其相關(guān)的化學方程式、離子方程式、電子式、電離方程式和PH值關(guān)系等。只要好好聯(lián)系課本中各種金屬與非金屬性質(zhì)與流程圖中反應(yīng),便有利于推斷出考卷中未涉及物質(zhì)的反應(yīng)。
一、以2016年全國Ⅰ卷理綜化學工藝流程題節(jié)選進行分析,聯(lián)系課本中金屬性質(zhì)進行分析
NaClO2是一種重要的殺菌消毒劑,也常用來漂白織物等,其一種生產(chǎn)工藝如下:
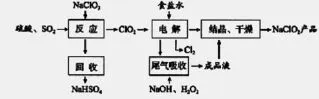
(1)寫出“反應(yīng)”步驟中生成ClO2的化學方程式_____。根據(jù)流程圖可知反應(yīng)物是NaClO3、SO2和H2SO4,生成物是ClO2。非金屬氯元素化合價明顯變化,根據(jù)課本中氧化還原反應(yīng)原理化合價有升必有降,NaClO3反應(yīng)生成ClO2化合價降低,非金屬氧化物SO2具有還原性,此時化合價升高,可得生成Na2SO4。工業(yè)上為使得反應(yīng)更充分,SO2必然過量,產(chǎn)物是NaHSO4。根據(jù)電子得失配平化學方程式得:2NaClO3+SO2+H2SO4==2NaHSO4+2ClO2。
(2)“電解”所用食鹽水由粗鹽水精制而成,精制時,為除去金屬離子Mg2+和Ca2+,要加入的試劑分別為_____、____。除去金屬離子常用沉淀法,Mg(OH)2和CaCO3難溶于水,可推測加入NaOH和Na2CO3可以除去Mg2+和Ca2+。
二、以2015年全國Ⅰ卷理綜化學工藝流程題節(jié)選進行分析,聯(lián)系課本中金屬性質(zhì)進行分析
硼及其化合物在工業(yè)上有許多用途。以鐵硼礦(主要成分為Mg2B2O5·H2O和Fe3O4,還有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)為原料制備硼酸(H3BO3)的工藝流程如圖所示:
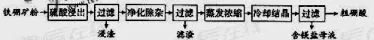
(1)寫出Mg2B2O5·H2O與硫酸反應(yīng)的化學方程式:Mg2B2O5· H2O+2H2SO4===2MgSO4+2H3BO3。
本小題考察化學方程式書寫,化學方程式書寫方面學生最大的問題是產(chǎn)物的確定很困難,工藝流程題中主要考察無機物性質(zhì)。無機物Mg2B2O5可以表示成氧化物的形式MgO和B2O3,以已學知識金屬氧化物與酸反應(yīng),反應(yīng)物MgO可推斷產(chǎn)物MgSO4,B元素反應(yīng)產(chǎn)物由題目可得H3BO3,即使題目沒有給出結(jié)果,B性質(zhì)與Al有相似之處,聯(lián)系課本中元素周期表,同主族性質(zhì)相似進行推斷B反應(yīng)后產(chǎn)物與Al性質(zhì)相似。
(2)“凈化除雜”需先加H2O2溶液,作用____。再調(diào)節(jié)溶液的
(1)H3PO2是一元中強酸,寫出其電離方程式____。一元酸只能電離出分子中的一個H+,按照酸的性質(zhì)H+。
(2)H3PO2及NaH2PO2均可將溶液中的Ag+還原為銀,從而可用于化學鍍銀。
NaH2PO2為____(填“正鹽”或“酸式鹽”),其溶液顯___(填“弱酸性”、“中性”或“弱堿性”)。考察弱酸的共同性質(zhì),H3PO2是一元中強酸,H2PO2-已無法電離出H+,NaH2PO2為正鹽,H3PO2是中強酸,NaOH是強堿,NaH2PO2為弱酸強堿鹽,在課程學習中知道誰強顯誰性得知顯堿性。
(3)H3PO2的工業(yè)制法是:將白磷(P4)與Ba(OH)2溶液反應(yīng)生成PH3氣體和Ba(H2PO2)2,后者再與H2SO4反應(yīng)。寫出白磷與Ba(OH)2溶液反應(yīng)的化學方程式_______。
以單質(zhì)S與NaOH溶液反應(yīng)的化學方程式為雛形,3S+ 6NaOH==2Na2S+Na2SO3+3H2O歧化反應(yīng),推測白磷與溶液反應(yīng)的化學方程式2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑。
雖然理綜化學中的工藝流程題得分率不高,是因為該題目考試內(nèi)容變化大,考題模式多,但是聯(lián)系課本中金屬元素與非金屬元素性質(zhì),利用類比,根據(jù)題干與流程圖的提示進行分析并解體,可以使得部分題目解題思路應(yīng)運而生。在課堂上重點練習,總結(jié)解體經(jīng)驗訣竅,還是可以解決部分題目的。
[1]雷白娟.課堂教學中如何培養(yǎng)學生思維的深刻性[J].中小學教育.教法研究,2015(4) pH約為5,目的是_______。
“凈化除雜”先加H2O2溶液再調(diào)節(jié)溶液的pH約為5,在工藝流程題目中多用于除去亞鐵離子和鐵離子。先加H2O2溶液作用是氧化,應(yīng)從各無機物中具有還原性的金屬離子Fe2+進行思考,此題目中H2O2是為了氧化Fe2+成為Fe3+。金屬離子Fe2+具有還原性是高考考點,在其他題目中依然是重點。氧化之后再調(diào)節(jié)溶液的pH約為5,是使得金屬離子形成沉淀的方法。在酸性條件下形成沉淀的以Fe3+和Al3+為主。按照沉淀順序是PH值接近3時Fe3+完全沉淀形成Fe(OH)3后,PH值接近5時Al3+完全沉淀形成Al(OH)3。利用Fe3+和Al3+酸性條件下沉淀特點與其他離子分離,很好考察了金屬鐵和鋁的性質(zhì)。
(3)非金屬單質(zhì)硼可用于生成具有優(yōu)良抗沖擊性能硼鋼。以硼酸和金屬鎂為原料可制備單質(zhì)硼,用化學方程式表示制備過程_____。
制備單質(zhì)硼應(yīng)當想到如何制備鋁單質(zhì),而且應(yīng)當想到硼酸H3BO3與Al(OH)3相似的特點。如果以Al(OH)3為原料制備鋁單質(zhì),思路無非是Al(OH)3加熱產(chǎn)生Al3O3之后再利用鋁熱反應(yīng)Al3O3產(chǎn)生Al。類比法,利用2H3BO3===B2O3+3H2O B2O3+3Mg=== 3MgO+2B得到B。
三、以2014年全國Ⅰ卷理綜化學工藝流程題節(jié)選進行分析,聯(lián)系課本中非金屬性質(zhì)聯(lián)系進行分析
次磷酸(H3PO2)是一種精細磷化工產(chǎn)品,具有較強還原性。回答下列問題:

