草魚野生與選育群體線粒體DNA控制區D-loop遺傳變異分析
王沈同 張 猛 黨云飛 李立森 黃文吉 方 圓 王 豐 沈玉幫 李家樂
(上海海洋大學省部共建水產種質資源發掘與利用教育部重點實驗室, 上海 201306)
草魚野生與選育群體線粒體DNA控制區D-loop遺傳變異分析
王沈同 張 猛 黨云飛 李立森 黃文吉 方 圓 王 豐 沈玉幫 李家樂
(上海海洋大學省部共建水產種質資源發掘與利用教育部重點實驗室, 上海 201306)
為探究經過2個選育世代后選育群體遺傳多樣性和遺傳結構的變化, 研究對4個野生群體(邗江、九江、石首和吳江)和2個選育世代(F1和F2)進行了線粒體DNA控制區(D-loop)序列的遺傳變異分析。實驗結果表明, 4個野生群體在單倍型數目(H)、單倍型多樣性(Hd)、核苷酸多樣性(π)、平均核苷酸差異數(K)水平上均高于2個選育世代, 在2個選育世代內表現為F1代群體的核苷酸多樣性(π)和平均核苷酸差異數(K)大于F2代群體, 但單倍型多樣性(Hd)小于F2代群體; 單倍型分析結果表明, 6個群體間無共享單倍型, 4個野生群體間共發現2種共享單倍型(Hap1和Hap3), 石首群體和2個選育世代共享1種單倍型(Hap15); 遺傳分化指數(Fst)分析結果表明,邗江、九江、吳江3個野生群體和2個選育世代間存在較大的遺傳分化(Fst范圍為0.41475—0.55128), 石首群體與F1代群體之間存在較小的遺傳分化, 與F2代群體之間存在中等水平的遺傳分化, 同時F1代群體與F2代群體之間存在較小的遺傳分化; 基于6個群體276個個體構建的鄰接(Neighbor-Joining, NJ)進化樹和基于27種單倍型構建的單倍型網絡圖也得到了相似的結論, 即邗江、九江、吳江3個野生群體和2個選育世代間的親緣關系較遠, 石首群體和2個選育世代兩兩之間的親緣關系較近。以上結果表明, 經過2個世代的選擇育種, 選育群體的遺傳結構已發生了變化, 并且隨著選育的進行, 選育世代的遺傳多樣性下降的較為明顯, 這警示著我們在今后的育種工作中應適當改變現有的選育方案, 并實時監測選育群體的遺傳多樣性, 以便為今后進一步的選育工作打下堅實的基礎。
草魚; 選育群體; 野生群體; mt DNA; D-loop; 遺傳變異
草魚(Ctenopharyngodon idella)是我國重要的淡水養殖魚類之一, 主要分布于長江、珠江、黑龍江三大水系, 自1958年草魚人工繁育成功以來, 年產量逐年增長[1], 據FAO統計, 草魚年產量在2012年位于世界水品種產量的第三位[2], 但是近幾年草魚的種質資源日益衰減, 主要表現為性成熟年齡提前,生長速度變慢, 繁殖率低, 疾病發生率變高等, 主要原因歸結為草魚種質資源的退化, 人工繁殖管理的不規范導致草魚的近交系數變高, 群體的遺傳多樣性下降[3]。鑒于上述現象, 開展草魚選擇育種的工作迫在眉睫。
在開展遺傳育種工作過程中群體遺傳多樣性的高低顯得尤為重要, 較高水平的遺傳多樣性能確保每一代在育種過程中可以獲得更可觀的遺傳進展、提高育種的效率, 并能提高群體的適應能力和抗病能力[4,5], 然而在一些物種的育種過程中其后代的遺傳多樣性表現為明顯的下降[6,7], 這將不利于后續育種工作的進行, 因此在開展育種工作過程中, 有必要對選育群體進行遺傳多樣性和遺傳結構評估, 以便為育種工作提供一些指導性的意見、提高育種的效率, 進而加快育種工作的進展。
線粒體DNA具有嚴格的母系遺傳特點, 同時具有拷貝數高、DNA分子量小、缺乏重組、結構和組織簡單而高度保守、DNA突變率高等一系列優點[8]。控制區(D-loop)是線粒體DNA上的一段非編碼區, 受進化壓力小、遺傳變異程度高[9,10], 并且進化速率快, 是其他區段的5倍[10,11], 常被用于群體水平的遺傳變異分析。由于草魚個體大、性成熟周期長、繁殖和測量性狀不易操作等特點, 至今仍沒有選育出新的品種, 而且對于草魚選育過程中選育群體遺傳多樣性評價及比較的工作相對較少。本研究采用PCR擴增和DNA測序技術對草魚4個野生群體和2個選育世代的線粒體D-loop區域部分片段進行了遺傳變異檢測, 初步分析草魚在經過2個世代的選育工作后, 其選育群體遺傳多樣性和遺傳結構的變化, 為今后制定出更加合理有效的選育方案提供參考。
1 材料與方法
1.1 實驗材料與DNA提取
本研究所用的F1代和F2代長江水系選育群體和4個野生群體(邗江、九江、石首和吳江)從蘇州市申航生態科技發展股份有限公司采集(表 1)。2007—2008年收集了4個長江水系野生群體(邗江、九江、石首和吳江), 經過遺傳分析后構建了長江水系基礎群體。2010年從基礎群體中隨機選取88尾親本采用隨機交配和定向交配(個體的遺傳距離設計)結合的方式繁殖產生了F1代[12]。經過5年的培育, 2015年選取來自于不同家系的106尾親本采用隨機交配的方法繁殖產生了F2代。剪取6個群體的草魚胸鰭組織, 保存于無水乙醇中以便于之后的DNA提取, 本實驗中所有樣品采用海洋動物組織基因組DNA提取試劑盒(天根生化科技有限公司)提取基因組DNA, 通過1%的瓊脂糖凝膠電泳檢測其完整性, 經NanoDrop 2000C分光光度計(賽默飛世爾科技有限公司)檢測其純度及濃度, 并將DNA樣品稀釋成20 ng/μL, 于–20℃保存備用。
1.2 PCR擴增及測序
根據草魚現有線粒體D-loop區域區段引物[13]完成PCR擴增, 上游引物和下游引物序列分別為: DLF: 5′-CCTAGCGCCCAGAAAAGGGAGATT-3′; DLR: 5′-GCGGGGGATTGAGGGCATACTC-3′, PCR反應體系總體積為50 μL: Taq PCR Mastermix 13 μL [成分為0.1 U Taq Polymerase/μL、500 μmol/L dNTP each、20 mmol/L Tris-HCl (pH 8.3)、100 mmol/ L KCl、3 mmol/L MgCl2、其他穩定劑和增強劑],上下游引物各1 μL (10 μmol/L), 模板DNA 40 ng, ddH2O 33 μL。該試劑購自天根生化科技(北京)有限公司。PCR擴增程序為: 94℃預變性3min; 94℃變性30s, 50℃復性30s, 72℃延伸2min, 擴增35個循環; 72℃延伸10min。擴增反應在Eppendorf梯度PCR儀上完成, 反應產物經1%瓊脂糖凝膠電泳檢測, 合格的PCR產物由上海生工生物工程股份有限公司進行測序。
1.3 序列整理與數據分析
采用Mega5.1[14]進行序列間的同源對比和序列編輯, 統計各群體的突變位點數、突變類型和核苷酸組成, 并基于Kimura雙參數模型(Kimura 2-Parameter, K2P)構建6個群體276個個體的鄰接(Neighbor-Joining, NJ)進化樹, 系統發育樹中節點的自舉置信水平應用自引導估計, 循環次數為1000次。采用DNASP 5.0軟件[15]統計各單倍型分布情況、單倍型數(H)、單倍型多樣性(Hd)、核苷酸多樣性(π)、平均核苷酸差異數(K)、Tajima’s D值。采用Arlequin3.5軟件進行6個群體的分子方差分析(AMOVA), 并計算6個群體兩兩之間的遺傳分化指數(Fst)。采用Network軟件構建單倍型網絡圖, 用以檢測單倍型之間的進化關系。
2 結果
2.1 線粒體控制區(D-loop)序列分析
對野生群體和選育世代線粒體控制區(D-loop)序列進行同源對比后, 得到894 bp的同源序列。6個群體位點變異情況如表 1所示, 除石首群體存在2個顛換類型, 其他群體堿基突變類型均為轉換類型。堿基組成分析表示各群體堿基組成大致相同, T、C、A、G 4種堿基平均值分別為32.17%、21.03%、34.45%和12.36%, A+T (66.62%)所占比值明顯高于G+C (33.38%), 表現出明顯的AT偏好, 這與其他脊椎動物線粒體控制區(D-loop)核苷酸的組成特點相一致[16]。
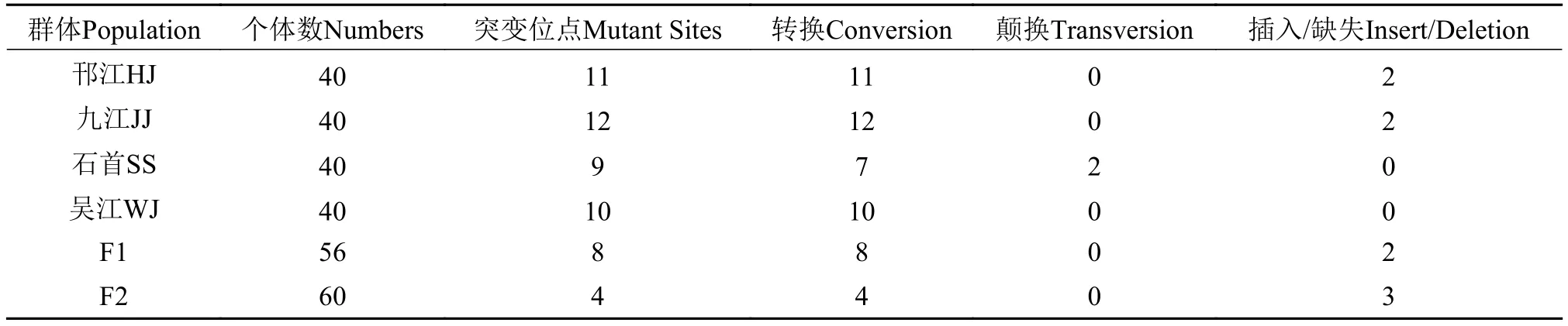
表 1 草魚線粒體DNA控制區(D-loop)序列突變位點數目Tab. 1 The number of mutation sites of mt DNA D-loop region in grass carp
2.2 草魚6個群體的遺傳多樣性及單倍型分析
6個群體線粒體DNA控制區(D-loop)遺傳多樣性參數如表 2所示, 無論是在單倍型數目(H)、單倍型多樣性(Hd)、核苷酸多樣性(π)還是平均核苷酸差異數(K)水平上, 野生群體的遺傳多樣性均比2個選育世代的要高。對4個野生群體而言, 石首群體的單倍型多樣性(Hd)最高(0.637), 吳江群體表現為最低(0.506); 邗江群體的核苷酸多樣性(π)和平均核苷酸差異數(K)最高(π=0.00232, K=2.063), 吳江群體表現為最低(π=0.00142, K=1.271); 2個選育世代相互比較發現, 兩者單倍型數目(H)一致, F1代選育群體的核苷酸多樣性(π)和平均核苷酸差異數(K)均高于F2代選育群體, 但單倍型多樣性(Hd)表現為前者小于后者; 草魚6個群體的Tajima’s D 值為負值,且均未顯著偏離中性(P>0.1)。
其單倍型分布如表 3所示, 6個群體共檢測出27種單倍型, 沒有發現共同享有的單倍型, 其中Hap15、Hap1為優勢單倍型, 分別占6個群體總個體數的39%和32%。4個野生群體間存在2種共享單倍型Hap1和Hap3, 2個選育群體間存在1種共享單倍型Hap15。
2.3 草魚6個群體的遺傳結構
對草魚6個群體兩兩之間遺傳分化情況進行分析, 分析結果如表 4所示, F1代和F2代群體間的遺傳分化指數(Fst)為0.05741(P<0.01), 結果表明2個世代間遺傳分化程度較低, 邗江、九江、吳江3個野生群體與2個選育世代之間的遺傳分化指數(Fst)均大于0.25(P值均小于0.01), 說明這3個野生群體與2個選育世代間存在著較大的遺傳分化, 并發現石首群體與F1代群體的遺傳分化指數Fst值為0.04861,與F2代群體的遺傳分化指數Fst值為0.13205, 結果表明石首群體和F1代群體間幾乎不存在著遺傳分化, 而和F2代群體之間存在著中等水平的分化程度。
以遺傳分化指數(Fst)為依據進一步對草魚6個群體的核苷酸序列變異做分子方差分析, 6個群體分為2組(1組為HJ+JJ+WJ; 2組為SS+F1+F2), 總的方差剖分為組間方差(Va)、組內群體間方差(Vb)和群體內方差(Vc)3個部分, 并進行顯著性檢驗。結果如表 5所示, 組間方差(Va)占總變異的38.11%, 組內群體間的方差組分(Vb)占總變異的2.21%, 群體內的方差組分(Vc)占總變異的59.69%, Fst=0.40312 (P<0.01)。
2.4 草魚6個群體的系統發育樹和單倍型簡約網絡圖
根據草魚4個野生群體和2個選育世代共276個個體構建的NJ系統發育樹發現6個群體在系統發育樹上基本被分成兩大分支, 3個野生群體(邗江、九江、吳江)構成一大分支, 2個選育世代(F1和F2)和石首群體構成另外一個分支, 不同分支內個體間存在相互交叉, 其結果表明F1代、F2代和石首群體三者之間的親緣關系較近, 而這3個群體和另外3個野生群體(邗江、九江、吳江)的親緣關系較遠。基于6個群體27種單倍型的單倍型網絡圖如圖 2所示, F1代、F2代和石首群體3個群體間的親緣關系較近, 而2個選育群體和邗江、九江、吳江3個野生群體的親緣關系較遠, 與NJ系統發育樹的分析的結果基本一致, 并且從圖中可以看出享有Hap15和Hap1單倍型的個體數在種群中所占比例明顯高于其他單倍型所占比例。
3 討論
3.1 草魚野生與選育群體的遺傳多樣性分析
核苷酸多樣性(π)和單倍型多樣性(Hd)是衡量一個群體mt DNA變異程度的重要指標。其中核苷酸多樣性(π)表示各種mt DNA單倍型在群體中所占的比例[17], 是評價群體遺傳多樣性的靈敏指標。本研究中6個群體的核苷酸多樣性(0.00065—0.00232), 平均核苷酸差異數(0.578—2.063)在群體間的變化趨勢一致, 均為野生群體>F1>F2, 以上數據表明野生群體的遺傳多樣性高于2個選育世代,并且隨著選育的進行, F2代選育群體的遺傳多樣性低于F1代選育群體, 2個選育世代的遺傳多樣性較野生群體下降的較為明顯, 這類現象在其他研究中也曾發生過, Eric等[18]發現在大西洋鮭(Salmo salar)選育過程中, 其第一代選育群體的遺傳多樣性下降的較為明顯, 其推測原因可能為參與繁育的親本數目較少所導致的, 頡曉勇等[19]對吉富品系尼羅羅非魚(Oreochromis niloticus)不同世代選育群體D-loop序列進行測定和分析, 發現隨著選育的發展,選育群體遺傳多樣性逐步降低, 基礎群體和選育群體的遺傳距離逐步增大, 趙廣泰等[20]利用微衛星標記對大黃魚(Larimichthys crocea)4個選育群體進行了遺傳變異分析, 結果表明, 連續四代的選育, 選育群體的遺傳基礎逐步純化, 遺傳多樣性逐步下降。本文通過2代選育群體遺傳變異的分析, 發現其遺傳多樣性下降地較為明顯, 推測原因可能有以下幾點:
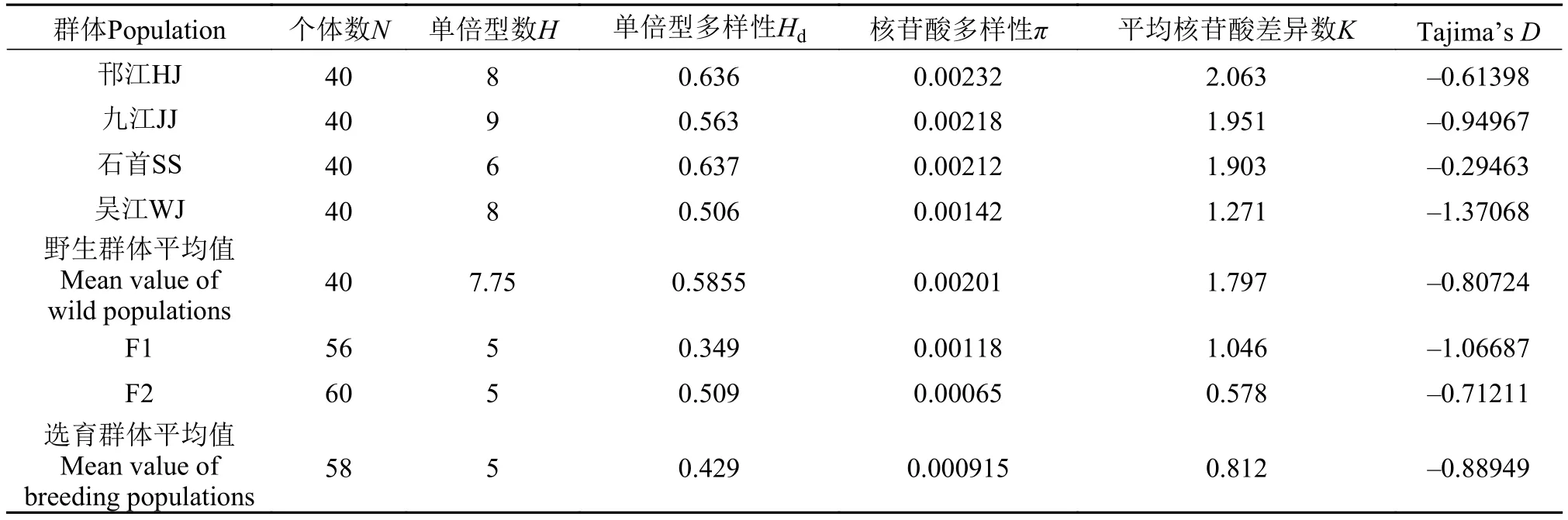
表 2 草魚線粒體DNA控制區(D-loop)遺傳多樣性參數Tab. 2 Genetic diversity parameters of mt DNA D-loop region in grass carp

表 3 草魚6個群體單倍型分布情況Tab. 3 Distribution of the haplotypes among six grass carp populations
首先, 選育方案中各世代參與的親本數較少,有研究表明, 當群體有效親本數量小于100時, 會導致遺傳漂變的加劇, 降低群體的遺傳多樣性[21—23];其二, 有學者指出, 后代群體遺傳多樣性的下降不僅和有限的親本數有關, 親本隨機交配這種交配方案本身會造成后代各家系數目的不均衡[24], Fu等[12]也發現草魚存在后代各家系數目比例失衡的問題,究其原因, Dewoody和Avise[25]認為雄性之間在繁育時具有競爭性會導致個別雄性后代個數的增加, 而且研究表明個頭越大, 體重越重, 肥滿度越高的個體在競爭時更具有優勢, 往往后代越多[26—28], 以上觀點可以從邏輯上解釋在一個密閉環境進行隨機交配會發現后代各家系數目不均衡的現象, 并且隨機交配的交配方案對于后代各家系數目不均衡的這種現象在其他物種中也曾發現過[24,28,29]。在本實驗中, 我們推測在親本繁殖過程中, 由于隨機交配的交配方式, 親本群體的有效群體數目下降得較為明顯, 導致遺傳漂變的發生, 遺傳漂變的發生進而會導致后代群體遺傳多樣性的下降[30], 并且隨著選育的進程這種現象越發明顯; 其三, 有研究發現,較強的人工選擇會導致后代遺傳多樣性的下降[31],本選育方案中只有較理想的個體(體重較高)會被選擇當做候選親本, 其他不理想的個體將會被淘汰掉,而這種較高強度的選擇壓力可能會影響后代群體的遺傳多樣性; 其四, 本實驗繁育的子代是在養殖桶內隨機采集的樣品, 有研究表明不同的飼養環境對于后代群體的遺傳多樣性也具有影響[32], 在養殖桶內開始養殖由于缺乏養殖經驗, 魚苗早期成活率不高, 推測可能由于養殖桶內早期惡劣的生存環境導致群體經歷了瓶頸效應, 只有適應力強的家系和個體保存了下來, 以此降低了后代群體的遺傳多樣性; 其五, 線粒體DNA具有母系無性遺傳特點, 對于遺傳漂變的影響會更為敏感, 因此不排除利用線粒體DNA部分片斷分析群體遺傳漂變現象過分夸大的可能性[33], 其他學者也指出, 當對一個物種運用不同的標記進行遺傳多樣性分析時, 可能會產生不同的結果, 因此我們認為有必要在今后運用不同的分子標記對后代群體的遺傳多樣性進行進一步的分析, 以檢驗當前線粒體DNA部分片斷分析時得出的結果[34]。
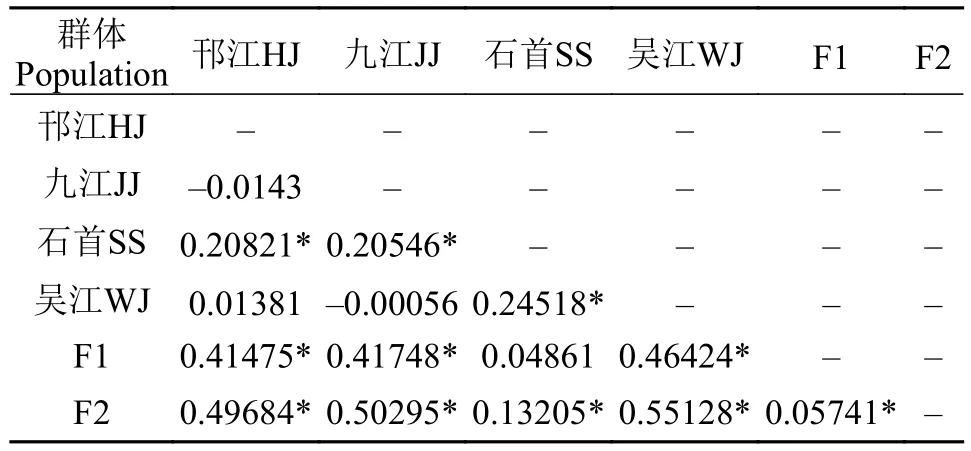
表 4 草魚6個群體間遺傳分化Fst值Tab. 4 Genetic differentiation Fstvalues among six populations of grass carp

表 5 草魚6個群體間遺傳差異的分子方差分析(AMOVA)Tab. 5 Analysis of molecular variance (AMOVA) of six populations of grass carp
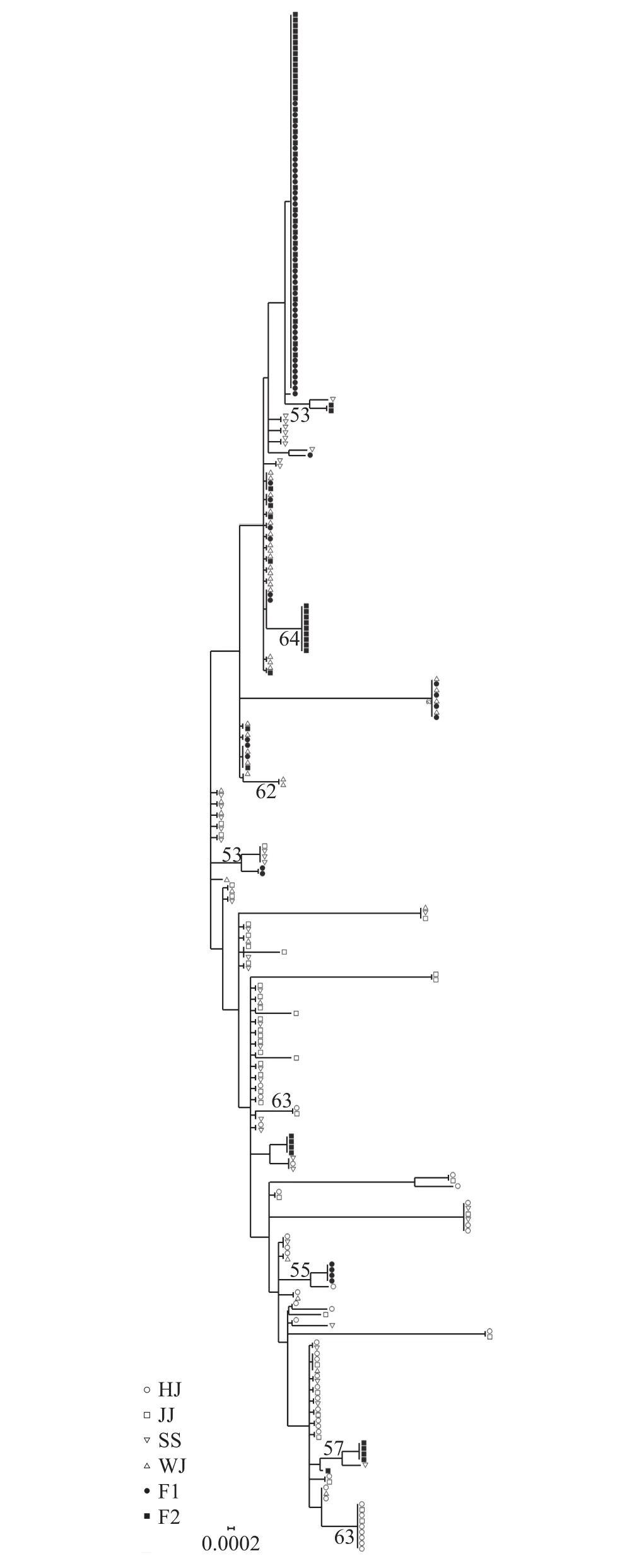
圖 1 基于Kimura 2-Parameter模型構建的線粒體控制區序列的NJ聚類Fig. 1 The NJ clustering diagram of the mitochondrial control region sequences constructed based on Kimura 2-Parameter model
本研究發現單倍型多樣性(Hd)參數在群體間的變化趨勢與上述遺傳多樣性參數變化趨勢有所不同, 表現為野生群體>F2>F1, F2代群體的核苷酸多樣性(π)和平均核苷酸差異數(K)雖小于F1代群體,但單倍型多樣性(Hd)高于F1代群體, 這種現象在其余物種中也曾發現過[35,36]。這可能是因為極少量的堿基突變就會導致單倍型數目的增長, 而核苷酸多樣性的增長是需要時間的積累所影響的[37]。本研究發現F2代選育群體的單倍型多樣性(Hd)大于F1代選育群體, 但由于各個單倍型之間的序列差異不大, 所以其核苷酸多樣性(π)會相對較小, 那么就會導致單倍型多樣性(Hd)和其他遺傳多樣性參數變化趨勢不一致的現象, 但終歸來看, 我們可以認為隨著選育的進程, 選育世代(F1代和F2代)的遺傳多樣性下降的較為明顯, 且F2代群體的遺傳多樣性低于F1代。
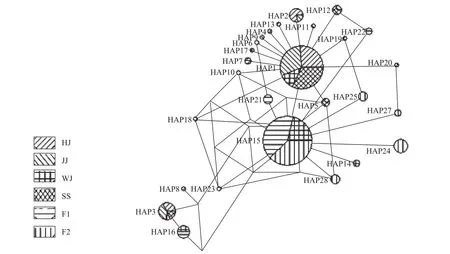
圖 2 基于mt DNA控制區構建的草魚單倍型網絡關系圖Fig. 2 The haploid types network diagram constructed based on mt DNA D-loop of grass carp
3.2 草魚野生與選育群體的遺傳結構分析
根據Wright[38]關于遺傳分化程度的理論認為Fst值在0—0.05表示低度遺傳分化, Fst值在0.05—0.15表示中度遺傳分化, Fst在0.15—0.25表示遺傳分化比較大。遺傳分化分析發現F1代與F2代群體之間Fst值為0.05741, 結果表明選育群體之間存在較小的遺傳分化, 邗江、九江和吳江3個野生群體與2個選育世代間的Fst在0.41475—0.55128, 表明這3個野生群體和2個選育世代間已發生了明顯的遺傳分化, 而石首群體與F1代群體的遺傳分化指數Fst值為0.04861, 與F2代群體的遺傳分化指數Fst值為0.13205, 結果表明石首群體和F1代選育群體間幾乎不存在明顯的遺傳分化, 而和F2代選育群體之間存在著中等水平的分化程度, 進一步對6個群體進行分子方差分析(AMOVA), 其中組間方差組分(Va)占總變異的38.11%, 組內群體間的方差組分(Vb)占總變異的2.21%, 群體內的方差組分(Vc)占總變異的59.69%, 遺傳分化指數(Fst)為0.40312, 且差異極顯著(P<0.01), 結果表明石首群體、F1代、F2代群體和其余3個野生群體已發生了較高程度的遺傳分化, 而石首群體, F1代和F2代之間的遺傳分化不太明顯, 符合分析遺傳分化指數(Fst)得出的結果。
從單倍型分布角度來看, 邗江、九江和吳江3個野生群體與2個選育世代之間不存在共享單倍型, 石首群體與2個選育群體之間共享單倍型為一種(Hap15), 其結果也能從側面說明2個選育世代和邗江、九江、吳江這3個野生群體之間親緣關系較遠, 而和石首群體的親緣關系較近, 符合上述分析得出的結論。
從6個群體276個個體構建的NJ系統發育樹角度來看, 系統發育樹基本被分成2大分支, 2個選育世代(F1代和F2代)與石首群體為一大分支, 邗江、九江、吳江群體為另一分支, 石首群體與2個選育世代(F1代和F2代)在系統發育樹上表現為相互交叉; 27種單倍型的單倍型網絡圖分析結果顯示, 4個野生群體以Hap1單倍型為中心呈發散狀態勢, 2個選育世代及石首群體以Hap15單倍型為中心呈發散狀態勢, 以上數據都能說明邗江、九江、吳江3個野生群體和2個選育世代(F1代和F2代)之間的親緣關系較遠, 而石首群體和2個選育世代之間的親緣關系較近, 符合上述分析得出的結果。
因此從總體來看, 2個選育世代與邗江、九江、吳江3個野生群體之間產生了較明顯的遺傳分化, 而石首群體和2個選育世代(F1代和F2代)兩兩之間存在著較小或中等水平的遺傳分化, 我們推測原因如下: 其一, 在親本交配繁殖過程中由于草魚本身存在后代各家系數目不均等問題[12], 因此可能發生少數親本的子代占據了大部分后代數目的現象, 這種遺傳漂變現象可能會導致2個選育世代與邗江、九江、吳江3個野生群體之間產生較明顯的遺傳分化, 而石首群體可能占據了這少數親本中的大多數, 因此在檢測遺傳結構時, 石首群體和2個選育世代(F1代和F2代)之間并沒有存在較大的遺傳分化; 其二, 在養殖過程中可能由于管理不善, 惡劣的池塘環境導致后代經歷了瓶頸效應, 群體數目的大量減少, 強行的加大了后代群體遺傳結構的分化; 其三, 人工選擇在一定程度上可能改變了選育群體的遺傳結構, 使之往一個方向變化, 并逐步趨向穩定, 而這種現象正是我們選擇育種想要看到的結果; 其四, 有研究發現, mtDNA D-loop序列分析技術在檢測遺傳差異水平上可能具有更高的靈敏性[39], 因此不排除用mtDNA D-loop序列分析技術分析得出的遺傳分化指數(Fst)有過分夸大的可能性。
綜上所述, 經過2個世代的人工選擇, 無論是從遺傳分化指數(Fst), NJ系統發育樹還是單倍型分析的角度來看, 其結果都表明選育群體的遺傳結構已發生了改變, 說明我們的選育方案是有成效的, 但從另一個角度來看, 隨著選育的進行, 其選育群體的遺傳多樣性下降地較為明顯, 因此這警示著我們在今后的育種過程中, 應盡量保持較大的親本繁殖數量, 盡量避免隨機交配這種交配方案, 減少遺傳漂變的發生, 或者增加交配親本的組數, 分配多組親本在不同的孵化環道封閉繁殖, 這樣既能保證讓不同的親本都參與到交配當中去, 又能減少親本定向交配時對于魚體的物理損傷, 同時在幼苗培育時每組取相同的幼體合并培養, 盡可能的使選育群體保持較高的遺傳多樣性[40]。本實驗也反映了在育種過程中實時檢測和監控后代遺傳多樣性的重要性, 啟示著我們在今后的選育過程中應及時運用不同的分子標記檢驗和監控選育群體遺傳多樣性和遺傳結構的變化, 方可有利于今后進一步的育種工作, 為接下來的選育工作打下堅實的基礎。
[1]Shen Y B, Zhang J B, Li J L. Advances in studies on genetic resources of grass carp [J]. Chinese Agricultural Science Bulletin, 2011, 27(7): 369—373 [沈玉幫, 張俊彬,李家樂. 草魚種質資源研究進展. 中國農學通報, 2011, 27(7): 369—373]
[2]FAO. The State of World Fisheries and Aquaculture 2012[M]. Rome, 2012, 209
[3]Liao Y M, Liu J L, Tang X L. The reason of commercial traits degeneration of four major Chinese carps and advice for genetic conservation [J]. Fisheries Science & Technology Information, 1994, 21(2): 62—63 [廖亞明,劉金爐, 湯學林. 淺析“四大家魚”性狀退化的原因及重視種質保護的建議. 水產科技情報, 1994, 21(2): 62—63]
[4]Waples R S. Genetic interactions between hatchery and wild salmonids: lessons from the pacific northwest [J]. Canadian Journal of Fisheries & Aquatic Sciences, 1991, 48(48): 124—133
[5]Ferguson A, Mcginnity P, Stone C, et al. The genetic impact of escaped farm Atlantic salmon on natural populations [J]. Aquaculture, 1995, 137(1): 55—56
[6]Cruz P, Ibarra A M, Mejia-Ruiz H, et al. Genetic variability assessed by microsatellites in a breeding program of Pacific white shrimp (Litopenaeus vannamei) [J]. Marine Biotechnology, 2004, 6(2): 157—164
[7]Wolfus G M, Garcia D K, Alcivar-Warren A. Application of the microsatellite technique for analyzing genetic diversity in shrimp breeding programs [J]. Aquaculture, 1997, 152(1—4): 35—47
[8]Wolstenholme D R. Animal mitochondrial DNA: structure and evolution [J]. International Review of Cytology, 1992, 141(6): 173—216
[9]Rosel P E, Dizon A E, Haygood M G. Variability of the mitochondrial control region in populations of the harbour porpoise, Phocoena, on interoceanic and regional scales [J]. Canadian Journal of Fisheries & Aquatic Sciences, 2011, 52(6): 1210—1219
[10]Rosel P E, Haygood M G, Perrin W F. Phylogenetic relationships among the true porpoises (Cetacea: Phocoenidae) [J]. Molecular Phylogenetics & Evolution, 1995, 4(4): 463—474
[11]Cann R L, Brown W M, Wilson A C. Polymorphic sites and the mechanism of evolution in human mitochondrial DNA [J]. Genetics, 1984, 106(3): 479—499
[12]Fu J J, Shen Y B, Xu X Y, et al. Genetic parameter estimates for growth of grass carp, Ctenopharyngodon idella, at 10 and 18 months of age [J]. Aquaculture, 2016, 450: 342—348
[13]Fu J J, Wang R Q, Shen Y B, et al. Genetic variation analysis based on D-Loop sequences of wild populations of grass carp (Ctenopharyngodon idella) in China [J]. Acta Hydrobiologica Sinica, 2015, 39(2): 349—357 [傅建軍,王榮泉, 沈玉幫, 等. 我國草魚野生群體D-Loop序列遺傳變異分析. 水生生物學報, 2015, 39(2): 349—357]
[14]Tamura K, Peterson D, Peterson N, et al. MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods [J]. Molecular Biology & Evolution, 2011, 28(10): 2731—2739
[15]Rozas J, Sanchez-Delbarrio J C, Messeguer X, et al. DnaSP, DNA polymorphism analyses by coalescent and other methods [J]. Bioinformatics, 2004, 19(18): 2496—2497
[16]Brown G G, Gadaltta G, Pepe G, et al. Structural conservation and variation in the D-loop-containing region of vertebrate mitochondrial DNA [J]. Journal of Molecular Biology, 1986, 192(3): 503—511
[17]Liu Y H, Zhang M H. Population genetic diversity of roe deer (Capreolus pygargus) in mountains of Heilongjiang Province [J]. Zoological Research, 2009, 30(2): 113—120
[18]Verspoor E. Reduced Genetic variability in first-generation hatchery populations of Atlantic salmon (Salmo salar) [J]. Canadian Journal of Fisheries & Aquatic Sciences, 1988, 45: 1686—1690
[19]Jie X Y, Li S F, Cai W Q. Genetic variation analysis of Oreochromis niloticus breeding population based on DLoop sequence [J]. Journal of Shanghai Ocean University, 2011, 20(3): 336—341 [頡曉勇, 李思發, 蔡完其.基于D-Loop序列的羅非魚選育群體遺傳變異分析. 上海海洋大學學報, 2011, 20(3): 336—341]
[20]Zhao G T, Liu X D, Wang Z Y, et al. Genetic structure and genetic diversity analysis of four consecutive breeding generations of large yellow croaker (Pseudosciaena crocea) using microsatellite markers [J]. Journal of Fisheries of China, 2010, 34(4): 500—507 [趙廣泰, 劉賢德,王志勇, 等. 大黃魚連續4代選育群體遺傳多樣性與遺傳結構的微衛星分析. 水產學報, 2010, 34(4): 500—507]
[21]Sekino M, Hara M, Taniguchi N. Loss of microsatellite and mitochondrial DNA variation in hatchery strains of Japanese flounder Paralichthys olivaceus [J]. Aquaculture, 2002, 213(1—4):101—122
[22]WinansG A. Genetic variability in Chinook salmon stocks from the Columbia river basin [J]. North American Journal of Fisheries Management, 1989, 9(9): 47—52
[23]Li Q, Park C, Endo T, et al. Loss of genetic variation at microsatellite loci in hatchery strains of the Pacific abalone (Haliotis discus hannai) [J]. Aquaculture, 2004, 235(1-4): 207—222
[24]Lind C E, Evans B S, Knauer J, et al. Decreased genetic diversity and a reduced effective population size in cultured silver-lipped pearl oysters (Pinctada maxima) [J]. Aquaculture, 2009, 286(1—2): 12—19
[25]Dewoody J A, Avise J C. Genetic perspectives on the natural history of fish mating systems [J]. Journal of Heredity, 2001, 92(2): 167—172
[26]Bekkevold D, Hansen M M, Loeschcke V. Male reproductive competition in spawning aggregations of cod (Gadus morhua, L.) [J]. Molecular Ecology, 2002, 11(1): 91—102
[27]Fessehaye Y, El-Bialy Z, Rezk M A, et al. Mating systems and male reproductive success in Nile tilapia (Oreochromis niloticus) in breeding hapas: A microsatellite analysis [J]. Aquaculture, 2006, 256(1—4): 148—158
[28]Frost L A, Evans B S, Jerry D R. Loss of genetic diversity due to hatchery culture practices in barramundi (Lates calcarifer) [J]. Aquaculture, 2007, 272(2): S272
[29]Sekino M, Saitoh K, Yamada T, et al. Microsatellitebased pedigree tracing in a Japanese flounder Paralichthys olivaceus, hatchery strain: implications for hatchery management related to stock enhancement program [J]. Aquaculture, 2003, 221(1—4): 255—263
[30]Ferguson M. The role of molecular genetic markers in the management of cultured fishes [J]. Reviews in Fish Biology & Fisheries, 1994, 4(3): 351—373
[31]Doebley J F, Gaut B S, Smith B D. The molecular genetics of crop domestication [J]. Cell, 2006, 127(7): 1309—1321
[32]Crossman J A, Scribner K T, Yen D T, et al. Gamete and larval collection methods and hatchery rearing environments affect levels of genetic diversity in early life stages of lake sturgeon (Acipenser fulvescens) [J]. Aquaculture, 2011, 310(3—4): 312—324
[33]Pitcher T J, Cingolani N, Bembo D G, et al. Stock discrimination among European anchovy, Engraulis encrasicolus, by means of PCR-amplified mitochondrial DNA analysis [J]. Oceanographic Literature Review, 1995, 94(1): 31—40
[34]Karl S A, Avise J C. Balancing selection at allozyme loci in oysters: implications from nuclear RFLPs [J]. Science, 1992, 256(5053): 100—102
[35]Peng S M, Shi Z H, Hou J L. Comparative analysis on the genetic diversity of cultured and wild silver pomfret populations based on mt D-loop and COI gene [J]. Journal of Fisheries of China, 2010, 34(1): 19—25 [彭士明, 施兆鴻, 侯俊利. 基于線粒體D-loop區與COI基因序列比較分析養殖與野生銀鯧群體遺傳多樣性. 水產學報, 2010, 34(1): 19—25]
[36]Xiao M S, Cui F, Kang J, et al. Genetic structure and variation of wild Chinese catfish from huaihe river based on cytochrome b gene sequences [J]. Chinese Journal of Zoology, 2013, 48(1): 75—86 [肖明松, 崔峰, 康健,等. 淮河野生鲇魚線粒體Cytb基因的序列變異與遺傳結構分析. 動物學雜志, 2013, 48(1): 75—86]
[37]Arbogast B S. Phylogeography: The History and Formation of Species[J]. Integrative & Comparative Biology, 2000, 41(1):134—135
[38]Wright S. The gentical structure of population [J]. Nature, 1950, 166(4215): 247—249
[39]Xiao W, Wang T, Li D Y, et al. Genetic variation of mitochondrial DNA D-loop region in different generations of Egyptian strain of Oreochromis niloticus [J]. South China Fisheries Science, 2015, (3): 29—34 [肖煒, 王騰,李大宇, 等. 埃及品系尼羅羅非魚不同選育世代 mtDNA D-loop 區遺傳多樣性分析. 南方水產科學, 2015, (3): 29—34]
[40]Domingos J A, Smith-Keune C, Jerry D R. Fate of genetic diversity within and between generations and implications for DNA parentage analysis in selective breeding of mass spawners: A case study of commercially farmed barramundi (Lates calcarifer) [J]. Aquaculture, 2014, 424—425(2): 174—182
GENETIC VARIATION OF MITOCHONDRIAL DNA D-LOOP REGION IN WILD AND BREEDING POPULATIONS OF GRASS CARP
WANG Shen-Tong, ZHANG Meng, DANG Yun-Fei, LI Li-Sen, HUANG Wen-Ji, FANG Yuan, WANG Feng, SHEN Yu-Bang and LI Jia-Le
(Key Laboratory of Exploration and Utilization of Aquatic Genetic Resources, Ministry of Education, Shanghai Ocean University, Shanghai 201306, China)
To evaluate the genetic diversity and genetic structure of grass carp (Ctenopharyngodon idella), we analyzed the genetic variation of mitochondrial DNA D-loop region among four wild populations (Hanjiang, Jiujiang, Shishou, Wujiang) and two domesticated populations after two generations (F1 and F2) of selective breeding. The results showed that the wild populations had higher number of haplotype (H), haplotype diversity (Hd), nucleotide diversity (π) and average number of nucleotide differences (K) compared with the domesticated populations. Between the bred populations, F1 generation was higher than F2 generation in the aspects of nucleotide diversity (π) and average number of nucleotide differences (K), but haplotype diversity (Hd) in F1 generation was lower than F2 generation. Haplotype analysis showed that all six populations did not share a haplotype. By contrast, the four wild populations shared two haplotypes (Hap1 and Hap3). The Shishou population and two domesticated populations shared one haplotype (Hap15). Genetic differentiation index (Fst) analysis showed that there was great genetic differences between wild (Hanjiang, Jiujiang, Wujiang) and domesticated populations (range Fstfrom were 0.41475 to 0.55128). Genetically, Shishou population was closely related with F1 population, but its relationship with F2 was only moderate. Moreover, the genetic differentiation level between two breeding populations was small (Fst=0.05741). The analysis of neighbor-joining phylogenetic trees based on 276 individuals among six populations and haplotype network graph based on 27 haplotypes indicated the wild populations (Hanjiang, Jiujiang, Wujiang) had a distant relationship with those domesticated populations. Although Shishou population and two breeding populations were more closely related. The above results showed that among the two domesticated populations, the genetic structure has already changed after two generations of selective breeding, and the genetic diversity also decreased with the development of the breeding program. The results also urge us that the current breeding strategy should be improved in order to maintain the genetic diversity of the breeding populations and reduce the risk of inbreeding.
Grass carp; Breeding population; Wild population; mt DNA; D-loop; Genetic variation
Q349+.1
A
1000-3207(2017)05-0947-09
10.7541/2017.118
2016-11-07;
2017-04-25
現代農業產業技術體系(CARS-46-04); 上海市工程中心提升項目(16DZ2281200); 通威產學研項目(TW2014F003)資助[Supported by the the China’s Agricultural Research System (CARS-46-04); the Project of Shanghai Engineering and Technology Center for Promoting Ability (16DZ2281200); Tongwei Industry-university-research Project (TW2014F003)]
王沈同(1993—), 男, 山東青島人; 碩士; 研究方向為水產動物種質資源與遺傳育種。E-mail: 2317011197@qq.com
李家樂, 教授, 博士生導師; 研究方向為水產動物種質資源與遺傳育種。E-mail: jlli2009@126.com

