過渡金屬銅修飾的仲鎢酸鹽抑制 人卵巢癌細胞增殖的研究
張 靜,曲小姝,劉樹萍,楊艷艷
(1.海軍92538部隊醫院,大連 遼寧116000; 2.吉林化工學院化學與制藥工程學院,吉林 吉林132022; 3.哈爾濱商業大學旅游與烹飪學院,黑龍江 哈爾濱150076)
過渡金屬銅修飾的仲鎢酸鹽抑制 人卵巢癌細胞增殖的研究
張 靜1,曲小姝2,劉樹萍3,楊艷艷2
(1.海軍92538部隊醫院,大連 遼寧116000; 2.吉林化工學院化學與制藥工程學院,吉林 吉林132022; 3.哈爾濱商業大學旅游與烹飪學院,黑龍江 哈爾濱150076)
研究了過渡金屬銅修飾的仲鎢酸鹽化合物 [Na2(H2O)10][Cu4(H2O)12(H2W12O42)]·15H2O (CuW12)的體外抗腫瘤活性.取人卵巢癌細胞SKOV-3加入不同濃度CuW12處理,應用四甲基偶氮唑鹽(MTT)比色法分析細胞增殖,計算了半數抑制濃度(IC50);采用光學顯微鏡觀察SKOV-3細胞的凋亡形態變化;分析了細胞周期和細胞凋亡,計算了各期細胞比例及細胞凋亡率.結果表明:CuW12對SKOV-3細胞增殖抑制的IC50值為45.2 μmol/L,且呈劑量依賴性;與經典的仲鎢酸鹽Na10(H2W12O42)·26H2O (NaW12)相比,過渡金屬銅修飾的仲鎢酸鹽抗腫瘤活性更強;光學顯微鏡下觀察到CuW12處理組細胞數目明顯減少,出現變圓、縮小、老化等形態變化;不同濃度CuW12處理12 h后早期凋亡細胞所占的百分比顯著增加且呈劑量依賴性.
仲鎢酸鹽;人卵巢癌細胞SKOV-3;抗腫瘤;銅
0 引言
多金屬氧酸鹽 (Polyoxometalates,POMs)又稱多酸,是由d0組態的過渡金屬離子與氧高度聚合形成的具有空間網絡結構的金屬-氧簇合物.[1]1971年M.Raynaud等[2]首次報道了雜多陰離子[SiW12O40]4-的抗病毒活性,開創了多酸的藥物化學.從20世紀80年代中后期開始,多酸藥物研究進入了一個新的發展時期,在抗病毒[3]、抗腫瘤[4]、抗菌[5]等領域都有著重要研究進展.
仲鎢酸鹽-B是一種經典的同多酸,陰離子結構式為[H2W12O42]10-,是由4個共角相連的兩種不同類型的三金屬簇{W3O13}和{W3O14}單元構成的一種中心對稱結構,這一結構有利于構建各種拓展結構,以其為基本建筑單元,利用過渡金屬離子作為連接子,可以構筑各種基于仲鎢酸鹽-B的新型多酸化合物.[6-8]文獻[9]報道仲鎢酸鹽具有優異的抗艾滋病毒活性,但是目前關于其抗腫瘤作用的研究報道還不多.[10-12]仲鎢酸鹽-B型多酸在中性到弱堿性水溶液中是非常穩定的,在生理條件下不分解成小碎片,表面電荷高,具備成為優良抗腫瘤藥物的潛力.因此,研究仲鎢酸鹽化合物的抗腫瘤作用具有重要意義.
另一方面,銅的生物活性近年來一直受到關注.很多本身沒有藥理活性的物質,與銅形成化合物后表現出優異的抗炎活性[13],研究發現癌癥的發生與炎癥反應有關聯,體內外藥理實驗表明很多銅配合物具有抗癌作用[14].用過渡金屬銅修飾仲鎢酸鹽-B以提高其生物活性是一種有意義的嘗試.
本文使用課題組合成的新型銅修飾的仲鎢酸鹽[Na2(H2O)10][Cu4(H2O)12(H2W12O42)]·15H2O (CuW12)[8],選擇人卵巢癌SKOV-3細胞并對其體外抗腫瘤活性進行了研究,與經典的仲鎢酸鈉Na10(H2W12O42)·26H2O(NaW12)的藥理活性進行了對比.
1 實驗部分
1.1 儀器與試劑
儀器:蘇州蘇靜集團FLB-lB型超凈工作室;美國SHELL/JB型CO2恒溫細胞培養箱;日本Olympus倒置相差顯微鏡;日本KA-1000型低速離心機;BIORAD公司680型酶標儀;美國BD公司BD FAC ScantoTM流式細胞儀.
試劑:3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴鹽 (MTT) 及DMSO購自美國Sigma公司;胎牛血清(Fetalbovineserum)、RPMI-1640 (pH7.0-7.2)、胰蛋白酶(tyrsin)購自Gibco公司;雙抗(青霉素鈉、硫酸鏈霉素)購自西安制藥公司;Hoechst33258試劑盒、碘化丙啶(Propidium Iodine,PI)購自南京凱基生物工程研究所; CuW12和NaW12為自制單晶(CuW12和NaW12水溶性較好,經紫外光譜研究發現化合物在pH值2~9范圍內結構保持穩定,且不隨時間變化;兩種化合物均經過X射線單晶衍射、紅外光譜、元素分析進行了表征[10]),分別將其溶于DMSO中,再用含10%滅活新生小牛血清的RPMI-1640培養液稀釋成終濃度為100 mmol/L的母液,4℃保存備用;SKOV-3細胞株,吉林醫藥學院科學實驗室保存.
1.2 MTT法測腫瘤細胞活力
把對數生長期的SKOV-3細胞調成密度為1×105個/mL,在96孔培養板中每孔加入200 μL密度為1×105個/mL的SKOV-3細胞懸液,在37℃、CO2體積分數為5%的條件下培養,24 h后把SKOV-3細胞分為空白對照組和6個實驗組(分別加入濃度為0.1,1,10,20,50,100 μmol/L的藥物溶液200 μL),用DMEM培養基稀釋液分別培養24 h.培養結束每孔加入新鮮配制的MTT溶液20 μL,溫育4 h使MTT還原為甲瓚,當在倒置顯微鏡下看到孔板內的細胞周圍出現絲狀紫色結晶體時倒掉上清液,每孔加入DMSO 150 μL振蕩溶解細胞,用平板搖床搖勻后,使用酶標儀測定光密度值(OD)(檢測波長為570 nm).計算增殖抑制率,增殖抑制率=(1-藥物試驗組吸光度值/對照組吸光度值)×100%.重復實驗 3次,取平均值.
1.3 細胞凋亡的形態學觀察
取對數生長期的SKOV-3細胞,培養24 h后,去上清液,將細胞分成空白對照組及6個實驗組(分別加入濃度為0.1,1,10,20,50,100 μmol/L的藥物溶液200 μL),用DMEM培養基稀釋液培養24 h后,于倒置顯微鏡下觀察不同濃度藥物對腫瘤細胞的影響,從生長抑制、細胞形態進行評估.
1.4 Annex in V-FITC/ PI 雙染法檢測細胞凋亡率
分別取對數生長期SKOV-3細胞5×105個接種于7個25 cm2細胞培養瓶中,待細胞貼壁后,更換培養液,分別加入濃度為0,0.1,1,10,20,50,100 μmol/L的藥物溶液10 mL,其中0為陰性對照,12 h后收集空白對照組和實驗組細胞,PBS洗滌2次,在4℃溫度下用70%乙醇固定30 min,用Annex in V-FITC/PI雙標記染色后上機檢測細胞凋亡率.
2 結果與討論
2.1 MTT比色實驗
由于活細胞的線粒體具有還原MTT形成紫色化合物的能力,該化合物在 570 nm 波長下有強吸收.細胞死亡或增殖功能下降時,還原MTT 的能力下降,570 nm 波長下吸光度值會降低,不同濃度CuW12處理SKOV-3細胞的實驗結果見表1.由表1可知,與空白對照組比較,不同濃度的CuW12處理SKOV-3細胞24 h后,SKOV-3細胞的OD值明顯減小,表明CuW12對SKOV-3細胞具有抑制作用,且隨著濃度的增加細胞的存活率下降,具有藥物劑量依賴性,IC50為45.2 μmol·L-1(見表2).對比經典的仲鎢酸鹽NaW12和CuW12的藥理活性,NaW12體外抑制SKOV-3細胞的IC50為200.6 μmol·L-1[10],經過過渡金屬銅修飾的仲鎢酸鹽對腫瘤細胞的增殖抑制活性顯著增強,這說明Cu2+的引入對仲鎢酸鹽藥理活性的增強發揮了重要作用,但具體作用機制有待進一步研究.
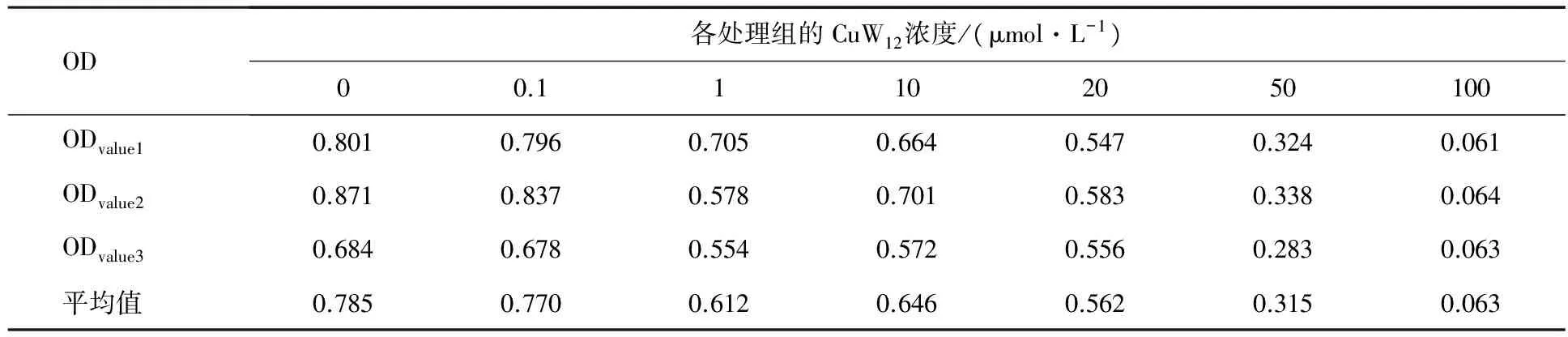
表1 不同濃度CuW12處理SKOV-3細胞24 h后的OD值
注:OD值為光密度值.
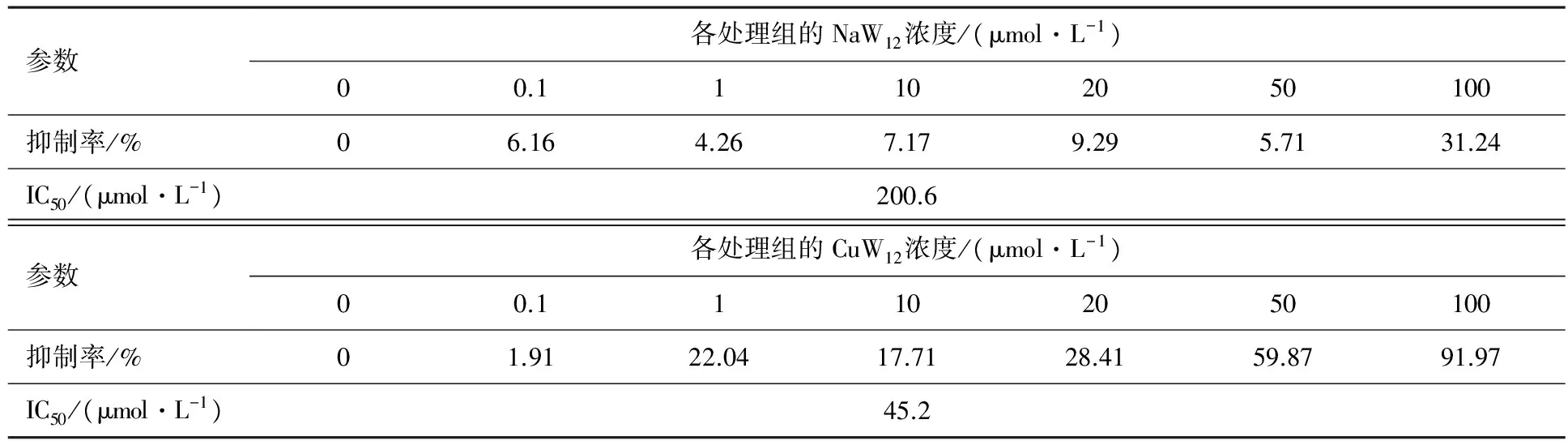
表2 NaW12和 CuW12體外抑制SKOV-3細胞的抑制率和IC50
2.2 不同濃度CuW12對腫瘤細胞形態學的影響
不同濃度CuW12對SKOV-3細胞形態學的影響見圖1,空白對照組卵巢癌細胞SKOV-3緊貼瓶底、細胞密集,細胞間連接緊密,細胞形態飽滿、邊界清晰、圓形細胞少;與空白對照組比較,10 μmol·L-1CuW12組細胞形態變化不明顯;50 μmol/L CuW12組細胞較為稀疏,附壁疏松,脫壁細胞由橢圓形變圓;100 μmol/L CuW12組細胞皺縮變小,細胞邊緣毛糙不規則,胞質致密,細胞核變形,細胞質中顆粒較多.經CuW12處理的細胞呈現凋亡的特征性改變,且隨著藥物濃度的增加,視野內凋亡的細胞也增加,呈現一定的劑量效應關系.

a:對照組;b—d:分別為10,50,100 μmol/L CuW12處理的SKOV-3
2.3 不同濃度的CuW12對腫瘤細胞早期凋亡率的影響
正常生長的SKOV-3細胞早期凋亡率為4.61%.經不同濃度的CuW12處理12 h后,SKOV-3細胞早期凋亡率顯著增加,經0.1,1,10,20,50,100 μmol/L CuW12處理后的凋亡率分別為4%,4.63%,8.1%,20.96%,34.86%和48.4%(見圖2).早期凋亡細胞所占的百分比由4.61%增加到48.4%.表明CuW12誘導SKOV-3細胞的死亡性質為凋亡,且其作用具有明顯劑量依賴性.
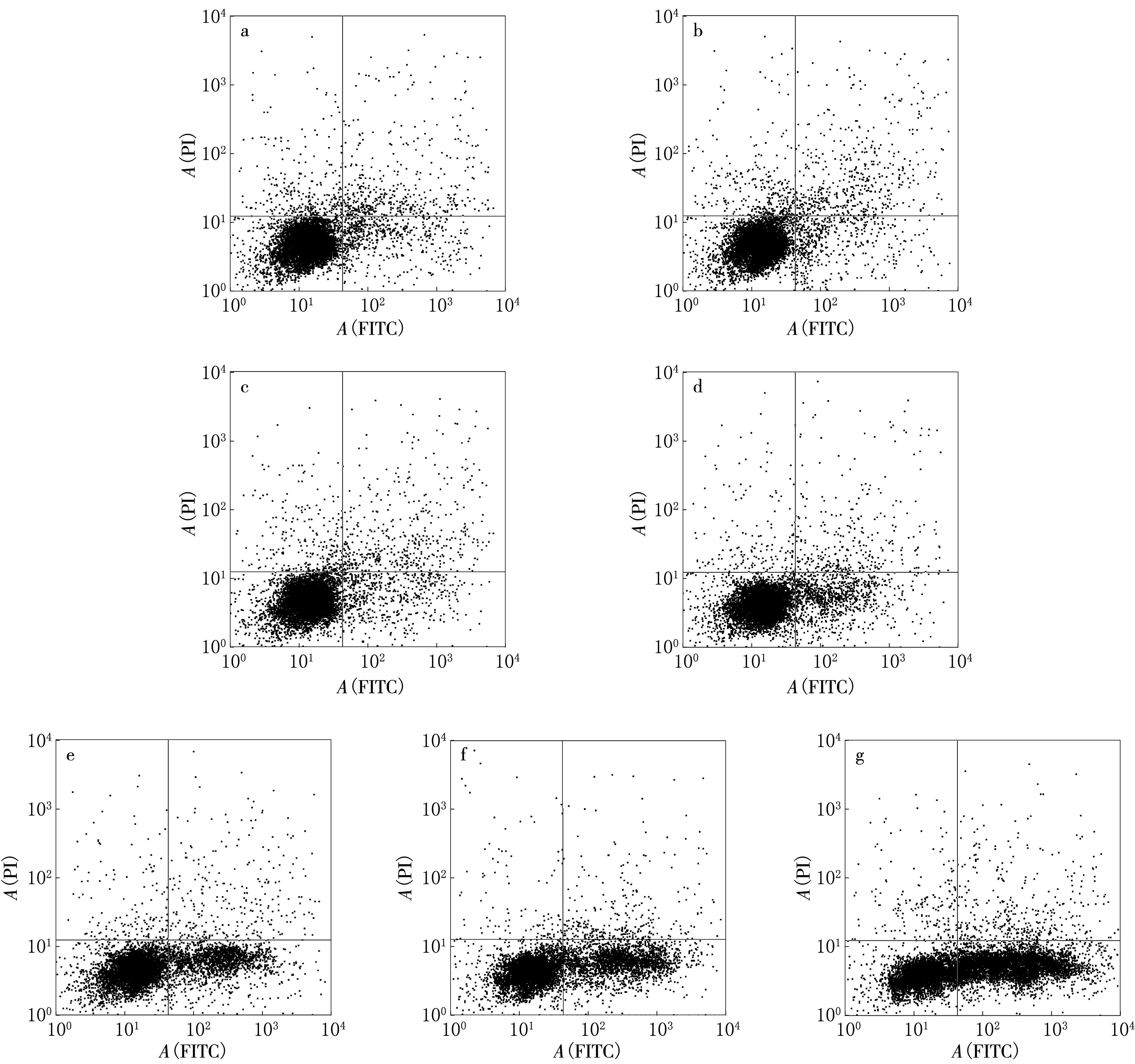
a:正常生長的SKOV-3;b—g分別為0.1,1,10,20,50,100 μmol/L CuW12處理的SKOV-3
3 結論
本文探討了過渡金屬銅修飾的仲鎢酸鹽化合物CuW12對人卵巢癌SKOV-3細胞生長及凋亡的影響.MTT細胞活性檢測表明:CuW12對SKOV-3細胞有較明顯的抑制作用,IC50為45.2 μmol·L-1,與經典的仲鎢酸鹽NaW12相比,Cu2+修飾的仲鎢酸鹽對腫瘤細胞的增殖抑制活性明顯增強,說明過渡金屬銅的引入對改變仲鎢酸鹽的藥理活性有重要作用;光學顯微鏡下CuW12處理組的細胞呈現凋亡的特征性改變,且呈現一定的劑量效應關系;不同濃度CuW12處理12 h后早期凋亡細胞所占的百分比顯著增加且呈劑量依賴性,說明CuW12具有誘導SKOV-3細胞凋亡的作用.凋亡是出現在多細胞生物體內的程序性死亡.近年來,誘導腫瘤細胞凋亡已成為抗腫瘤藥物的主要作用機制,許多化學藥物的治療機制都是通過誘導細胞凋亡發揮作用的.因此,研究仲鎢酸鹽-B型化合物的抗腫瘤作用具有潛在的應用價值,可為發展多酸藥物的臨床應用提供有價值的基礎數據.
[1] 王恩波,胡長文,許林.多酸化學導論[M].北京:化學工業出版社,1998:1-3.
[2] RAYNAUD M,CHERMANN J C,PLATA F,et al.Inhibitors of the murine leukemia sarcoma group viruses silicotungstates[J].C R Acad Sci Hebd Seances Acad Sci D,1971,272 (2):347-348.
[3] HILL C L,JUDD D A,TANG J,et al.Potent inhibition of respiratory syncytial virus by polyoxometalates of several structural classes[J].Antiviral Res,1997,34:27-37.
[4] YU H,LE S L,ZENF X H,et al.Facile synthesis of a novel mono-organoimido functionalized polyoxometalate cluster [(n-C4H9)4N]2[Mo6O18(≡NAr)] (Ar=p-C2H5C6H4) crystal structure,spectral characterization and initial antitumor activity[J].Inorg Chem Comm,2014,39:135-139.
[5] FENG C G,XIONG Y D,LIU X.Synthesis,spectroscopy and antibacterial activity of supermolecular compounds of organotitanium substituted heteropolytungstates containing 8-quinolinol[J].Spectrosc Spect Anal,2011,31:1153-1160.
[6] YUAN L,QIN C,WANG X L,et al.A new series of polyoxometalate compounds built up of paradodecatungstate anions and transitionmetal/alkaline-earth metal cations[J].Solid State Sci,2007,10:967-975.
[7] HE L W,LIN B Z,LIU X Z,et al.A novel layer formed by paradodecatungstate clusters and {Cu(en)2}2+bridging groups:Synthesis and characterization of [{Cu(en)2}4(H2W12O42)]·9H2O[J].Solid State Sci,2008,3:237-243.
[8] QU X S,YANG Y Y,ZHANG F F,et al.Synthesis and characterization of a three-dimentional framework built up of paradodecatungstate-B clusters and transition metals as linkers[J].Struct Chem,2012,23:1867-1872.
[9] RHULE J T,HILL C L,JUDD D A.Polyoxometalates in Medicine[J].Chem Rev,1998,98:327-357.
[10] QU X S,YANG Y Y,YU X Y,et al.A novel paradodecatungstate-B compound decorated by transition metal copper,Na2Cu5(H2O)24(OH)2[H2W12O42]·10H2O synthesis,structure and antitumor activities[J].Inorg Chem Comm,2015,60:126-130.
[11] 曲小姝,劉樹萍,楊艷艷.新型仲鎢酸鹽-B化合物[Na2(H2O)10][Cu4(H2O)12(H2W12O42)]·15H2O體外抗腫瘤活性研究[J].分子科學學報,2016,32(1):28-33.
[12] 曲小姝,劉樹萍,寧波,等.[Na2(H2O)10][Cu4(H2O)12(H2W12O42)]·15H2O抑制人宮頸癌Hela細胞增殖的研究[J].東北師大學報(自然科學版),2016,48(2):103-107.
[13] WEDER J E,DILLON C T,HAMBLEY T V,et al.Copper complexes of non-steroidal anti-inflammatory drugs an opportunity yet to be realized[J].Coord Chem Rev,2002,232:95-126.
(責任編輯:石紹慶)
Inhibitoryeffectofaparadodecatungstate-BcompounddecoratedbytransitionmetalcopperonthegrowthofhumanovariancarcinomaSKOV-3cells
ZHANG jing1,QU Xiao-shu2,LIU Shu-ping3,YANG Yan-yan2
(1.Navy 92538 Force Hospital,Dalian 116000,China; 2.Chemical and Pharmaceutical Engineering Institute,Jilin Institute of Chemical Technology,Jilin 132022,China; 3.College of Tourism and Cusine,Harbin University of Commerce,Harbin 150076,China)
This paper has studied the in vitro anti-tumor activity of a novel paradodecatungstate-B compound decorated by transition metal copper:[Na2(H2O)10][Cu4(H2O)12(H2W12O42)]·15H2O (abbreviated form:CuW12).Human ovarian carcinoma SKOV-3 cell was treated with different concentration of CuW12,then its IC50was measured by MTT assay.The morphological change in SKOV-3 cell was observed by optical microscopes.Flow cytometry was applied to analyze cell cycle and apoptosis by computing the ratio of SKOV-3 cells in different phase and its apoptotic ratio.The results show that CuW12can inhibit SKOV-3 cell proliferation with IC50of 45.2 μmol/L,showing dose-dependent.Compared with CuW12and classic paradodecatungstate compound Na10(H2W12O42)·26H2O (abbreviated form:NaW12),CuW12exhibits higher inhibitory effect owing to the introduction of copper atom.Under the optical microscopes,we observed the number of SKOV-3 cells treated with CuW12decreased significantly,cell rounding,shrinking and aging.Treated with different concentrations of CuW12after 12 h,the proportions of SKOV-3 cells on the early apoptosis increased markedly,showing dose-dependent.
paradodecatungstate-B;human ovarian carcinoma SKOV-3 cells;anti-tumor;copper
1000-1832(2017)03-0092-05
10.16163/j.cnki.22-1123/n.2017.03.020
2016-10-25
國家自然科學基金資助項目(21301041);吉林省教育廳科學技術研究項目(2015431).
張靜(1975—),女,碩士,主治醫師,主要從事臨床醫學研究;通訊作者:曲小姝(1974—),女,博士,教授,主要從事多酸化學研究.
O 611 [學科代碼] 150·15
A

