藥動學(xué)/藥效學(xué)研究在臨床藥敏折點制定中的應(yīng)用
李 鑫, 朱德妹, 張 菁
藥動學(xué)/藥效學(xué)研究在臨床藥敏折點制定中的應(yīng)用
李 鑫, 朱德妹, 張 菁
藥動學(xué)/藥效學(xué)界值;藥敏折點;應(yīng)用
1 概述
抗菌藥物臨床藥敏折點用于判斷病原菌對藥物耐藥或敏感,根據(jù)藥敏試驗方法的不同,折點可以用濃度或抑菌圈直徑表示。藥敏折點作為藥敏試驗結(jié)果的判斷標(biāo)準(zhǔn),為臨床醫(yī)師選擇抗菌藥物治療病原菌感染提供了重要依據(jù)。在不同的文獻中,折點可能被表述為不同的含義,歐洲藥敏試驗委員會 (European Committee on Antimicrobial Susceptibility Testing, EUCAST) 對 折 點 的 不 同表述進行了定義[1]。第1種是指流行病學(xué)界值(epidemiological cutoff,Ecoff),即微生物折點,也稱作野生型界值(wild-type cutoff,COWT),用于將細菌劃分為野生型和突變型。確定Ecoff值需要收集大量臨床野生型菌株,進行藥敏試驗獲得其MIC分布,之后取一個完整MIC分布的MIC90作為Ecoff值,或者根據(jù)野生型菌株MIC呈正態(tài)分布的特性,用非線性最小二乘回歸等統(tǒng)計學(xué)方法得到[2]。第2種即藥動學(xué)/藥效學(xué)(pharmacokinetics/pharmacodynamics, PK/PD)界值,是臨床藥敏折點建立中不可缺少的數(shù)據(jù),EUCAST對PK/PD界值的制定規(guī)定了一系列標(biāo)準(zhǔn)程序[3],包括微生物MIC分布測定,抗菌藥物PK研究,從體外模型、動物模型以及臨床研究中預(yù)測取得目標(biāo)療效的 PD 靶 值(pharmacodynamics target, PDT), 通過Monte Carlo模擬預(yù)測抗菌藥物在目標(biāo)群體中的藥物暴露量以進行達標(biāo)概率(probability of target attainment, PTA)分析等[4-5],最終獲得PK/PD界值。第3種即臨床藥敏折點,是綜合考慮以上2種界值以及臨床治療結(jié)果等數(shù)據(jù)得出,用于微生物實驗室的最終報告,以判斷臨床中抗菌藥物治療病原菌感染成功或失敗的可能性。目前國際公認(rèn)的折點制定機構(gòu),一個為EUCAST,另一個為美國臨床和實驗室標(biāo)準(zhǔn)化協(xié)會(CLSI)。
EUCAST是由歐洲臨床微生物與感染性疾病協(xié)會建立,成立于1997年,其主要職能是為新抗菌藥物制定臨床藥敏折點以及對已有抗菌藥物的藥敏折點進行更新,同時,EUCAST的工作還包括制定Ecoff,在適用地區(qū)范圍內(nèi)統(tǒng)一藥敏試驗方法,發(fā)布抗菌藥物對病原菌的MIC分布數(shù)據(jù)等,本文主要對EUCAST推薦的PK/PD界值制定過程進行介紹(圖1)。
2 EUCAST抗菌藥物PK/PD界值制定過程
EUCAST新版抗菌藥物折點制定標(biāo)準(zhǔn)操作規(guī)程發(fā)布于2016年,規(guī)定了制定折點需要收集的相關(guān)數(shù)據(jù)和制定流程[3],主要包括以下幾部分。
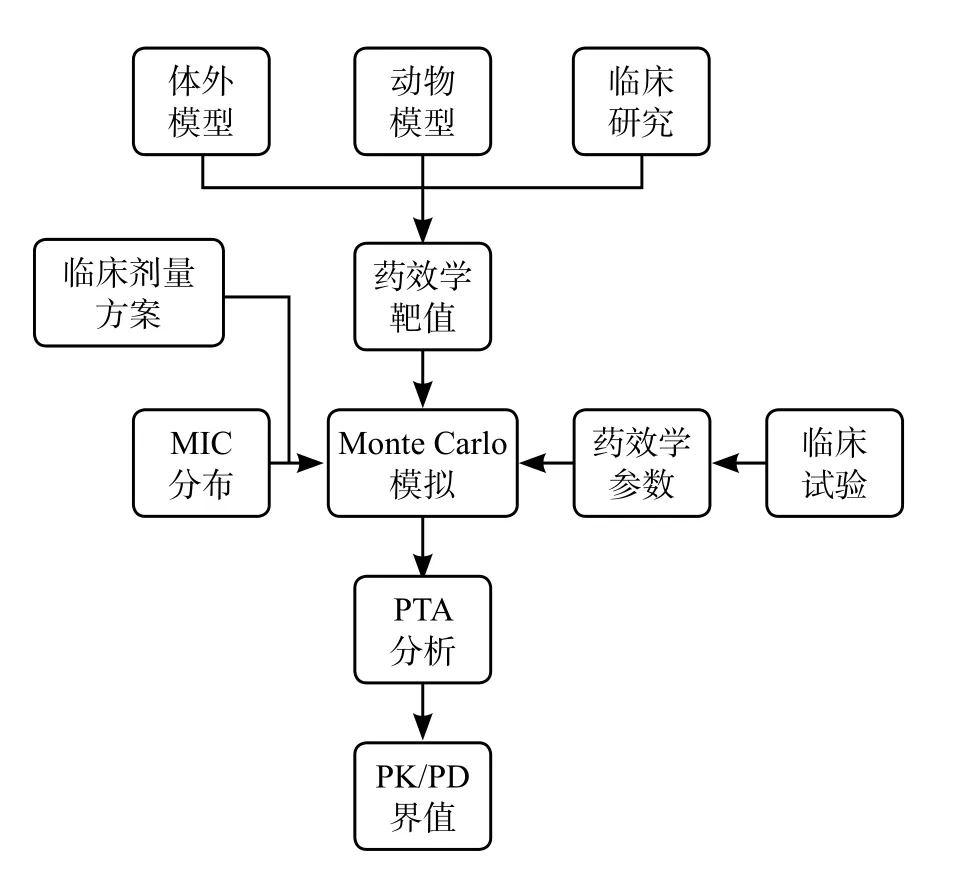
圖1 EUCAST PK/PD界值制定流程
2.1 抗菌藥物基本信息
抗菌藥物基本信息包括其化學(xué)結(jié)構(gòu)分類,抗菌譜及主要適應(yīng)證,常用劑型及給藥方式(口服、靜脈注射、靜脈輸注等),臨床推薦劑量(標(biāo)準(zhǔn)劑量及調(diào)整后劑量)等。對應(yīng)不同的劑型和劑量方案,抗菌藥物藥敏折點可能不同。EUCAST根據(jù)抗菌藥物臨床標(biāo)準(zhǔn)劑量來確定S/I折點,據(jù)其最大劑量確定I/R折點。
2.2 確定抗菌藥物對病原菌的MIC分布
EUCAST的抗菌藥物MIC數(shù)據(jù)來源包括英國、挪威、法國等多個國家的耐藥監(jiān)測系統(tǒng),已發(fā)表論文和會議報告,或由公司自行測定,要求在提交MIC數(shù)據(jù)的同時必須提供其測定方法,由于EUCAST從多種來源收集MIC數(shù)據(jù),其測定方法并不統(tǒng)一,包括了國際標(biāo)準(zhǔn)化組織(ISO)、歐洲EUCAST、美國CLSI、英國抗菌化學(xué)治療學(xué)會(BSAC)等多個組織推薦的標(biāo)準(zhǔn)方法。由不同方法獲得的MIC值可能不同,但其變化較小,通常不超過一個稀釋度,之后進行數(shù)據(jù)匯總繪制MIC分布柱狀圖并獲得MIC50、MIC90和MIC范圍等表征MIC分布特點的參數(shù),對MIC分布進行統(tǒng)計分析后可得到該種細菌的Ecoff[2]。
除MIC值分布外,EUCAST還發(fā)布了抗菌藥物對病原菌的抑菌圈直徑分布,抗菌藥物抑菌圈直徑按照EUCAST規(guī)定的紙片擴散法進行測定[6-7],并根據(jù)抑菌圈直徑與MIC值的相關(guān)性,確定了抗菌藥物紙片擴散法的敏感折點[8]。
2.3 抗菌藥物人體PK研究
藥物療效與感染部位的游離藥物濃度直接相關(guān),而體內(nèi)藥物濃度由給藥劑量、給藥方式以及藥物體內(nèi)PK過程等共同決定。明確抗菌藥物在體內(nèi)的PK過程,能夠保證在感染部位有足夠的藥物濃度發(fā)揮抗菌作用,同時獲得折點制定中所需要的Cmax、AUC、T1/2等PK參數(shù)。該部分?jǐn)?shù)據(jù)來源于制藥公司自己申請進行的臨床試驗或已發(fā)表的相關(guān)文獻及會議報告。
健康人體內(nèi)PK研究在Ⅰ期臨床試驗中完成,通常需進行多種劑量的單劑和多劑給藥。組織部位藥物濃度大多與體循環(huán)中血液藥物濃度呈相關(guān)性,因此在PK研究中通常以血清、血漿或全血為樣本測定體內(nèi)藥物濃度,還要注意考慮蛋白結(jié)合率的影響。但是在某些特殊情況下,則必須測定組織部位的藥物濃度,例如對于腦膜感染患者,由于血腦屏障的存在,藥物在血液和腦內(nèi)感染部位的濃度差異很大,這就需要測定腦脊液中的藥物濃度[9];對于肺炎感染患者,肺泡上皮細胞襯液比血漿更能準(zhǔn)確代表肺組織中的藥物濃度[10-11];還有一些特殊的目標(biāo)適應(yīng)證,可能需要測定中耳液、 前列腺液、白細胞內(nèi)液的濃度。另外,不同目標(biāo)群體的PK特征往往差異較大,例如適應(yīng)證患者群體、肝腎功能有損傷的群體、老年人群體等,進行PK/PD研究時就需要預(yù)測特殊群體的PK參數(shù)。
2.4 抗菌藥物PD研究
根據(jù)PK/PD特點的不同,抗菌藥物可分為濃度依賴性和時間依賴性,濃度依賴性抗菌藥物與療效相關(guān)PK/PD指數(shù)通常為AUC/MIC和Cmax/MIC,時間依賴性抗菌藥物根據(jù)其抗生素后效應(yīng)(postantibiotic effect, PAE)的長短,對應(yīng) PK/PD指數(shù)分別為AUC/MIC和%T>MIC。PK/PD靶值又稱為PDT,是基于對臨床前或臨床研究中藥物暴露量-反應(yīng)關(guān)系的分析,預(yù)測能夠達到目標(biāo)治療效果的PK/PD指數(shù)的最小值。大量研究數(shù)據(jù)表明,臨床前研究尤其是動物模型研究中獲得的PDT與人體具有一致性[12-13],可以用于折點制定或給藥劑量調(diào)整,同時臨床前研究也避免了臨床試驗中的許多限制。
2.4.1動物模型研究 在抗菌藥物的PK/PD研究中,動物感染模型作為重要方法被廣泛采用。動物模型研究不僅可以模擬藥物在人體內(nèi)的吸收、分布、代謝和排泄過程,同時,也模擬了宿主免疫系統(tǒng)發(fā)揮的作用。Ambrose等[13]對各種感染性疾病的動物模型和人體研究獲得的PK/PD指數(shù)進行了總結(jié),發(fā)現(xiàn)在動物和人體內(nèi),能夠達到治療效果的藥物暴露量和PDT是一致的,這并不難理解,因為抗菌藥物作用的對象是病原菌而不是宿主。
Lepak等[14]、Andes等[15-16]最早對嚙齒類動物感染模型的建立和抗菌藥物動物體內(nèi)PK/PD進行了大量研究,在PK/PD研究中常用的動物感染模型有大鼠/小鼠大腿感染模型和肺部感染模型,其建立方法都已經(jīng)比較成熟,例如通過腿部菌液注射建立大腿感染模型[14],利用滴鼻法[17]、氣管穿刺、氣管插管[18]造成動物肺部感染等。隨著動物模型的研究,一些其他模型也逐漸成功建立,包括血流感染模型、腦膜炎模型、皮膚軟組織感染模型、尿路感染模型以及心內(nèi)膜炎感染模型等[19-22]。為避免動物自身免疫系統(tǒng)的干擾作用,準(zhǔn)確評價藥物療效,同時模擬感染患者免疫狀態(tài)不同程度下降的情況,實驗中通常采用腹腔注射環(huán)磷酰胺的方法獲得中性粒細胞減少的免疫缺陷小鼠。
2.4.1.1獲得動物PK參數(shù)[23]計算PK/PD指數(shù)需要獲得藥物在動物體內(nèi)的AUC、Cmax、T1/2等PK參數(shù)。動物體內(nèi)PK研究通常為單劑給藥,設(shè)計3~5個劑量,需覆蓋PD研究的劑量范圍。采樣點根據(jù)藥物半衰期和給藥時間間隔確定。嚙齒類動物的藥物清除率較快,藥物在人體內(nèi)的半衰期是小鼠體內(nèi)的6~9倍[24],可以采用硝酸雙氧鈾造成動物腎小管損傷使藥物在動物體內(nèi)的半衰期與人體內(nèi)接近。
2.4.1.2確定與療效最佳相關(guān)PK/PD指數(shù) 應(yīng)用動物模型確定PK/PD指數(shù)時,只需選用一株代表菌株進行感染。采用劑量分層法給藥,設(shè)計4~5個日給藥劑量,按照不同的時間間隔(例如間隔24、12、8、和6 h)給藥。PD指標(biāo)通常為給藥24 h后動物感染部位每克組織細菌載量對數(shù)變化值(ΔLog10CFU),也可以用5~7 d內(nèi)的生存率作為觀察指標(biāo)。結(jié)合PK研究中獲得的參數(shù)和致病菌MIC值,計算不同給藥方案中PK/PD指數(shù)的大小,用Emax模型對PK/PD指數(shù)和不同給藥方案治療后的PD結(jié)果的關(guān)系進行擬合,相關(guān)系數(shù)最大的指數(shù)即為最佳療效相關(guān)指數(shù)[25](圖2)。

圖2 舒巴坦在小鼠肺炎模型中的PK/PD分析[25]
2.4.1.3確定PDT 確定PDT的研究過程與確定療效相關(guān)PK/PD指數(shù)基本相同,主要在細菌選擇和給藥頻率上有所差別。確定PDT時,要增加感染動物細菌的種類和數(shù)量。對于同一種細菌,通常選用4~5株MIC值不同的菌株,尤其是耐藥菌,用以觀察PD指標(biāo)隨PK/PD指數(shù)的變化,檢驗對于不同菌種,或者同種菌不同敏感性的菌株P(guān)DT是否相同。同時,實驗中可以只采用一種給藥時間間隔,根據(jù)劑量拆分給藥的實驗結(jié)果和藥物自身殺菌特點來確定。最后,分析PD結(jié)果和PK/PD指數(shù)的關(guān)系,在動物PK/PD研究中,通常認(rèn)為Δlog10CFU=0時為取得抑菌效果,Δlog10CFU= -2或-3時為取得良好療效。
2.4.2體外研究 在抗菌藥物PK/PD研究中,體外中空纖維模型也有了越來越多的應(yīng)用。相比動物模型,體外模型可以通過軟件控制更準(zhǔn)確模擬人體血藥濃度變化過程,便于進行多時間點連續(xù)采樣,對于動物體內(nèi)不易生長的細菌尤其重要,同時可用于耐藥性的研究。其缺點是不能模擬體內(nèi)免疫系統(tǒng)的影響。從體外模型中獲得PDT的過程與動物模型基本一致,同樣需要獲得藥物在體外模型中的PK參數(shù),確定PK/PD指數(shù)以及最后確定PK/PD靶值。另外,利用體外模型可以繪制藥物殺菌曲線,對抗菌藥物PK/PD指數(shù)進行初步判斷或者確證。奈諾沙星為新型無氟喹諾酮類抗菌藥物,體外PK/PD模型研究表明,其療效與AUC0-24/MIC、Cmax/MIC相關(guān)性較好,下降3個Log10CFU時的靶值分別為AUC0-24/MIC≈47.05,Cmax/MIC≈5.07[26],該靶值已在人體PK/PD研究中作為藥物劑量調(diào)整的參考數(shù)據(jù)[27]。
2.4.3臨床研究 在臨床試驗中,給藥方案往往比較單一,不能采用劑量分層法來確定最佳療效相關(guān)PK/PD指數(shù),同時,由于臨床試驗的倫理規(guī)范,不能給予患者安慰劑和亞臨床治療劑量,耐藥菌感染患者的入選也有一定困難,可能缺少不敏感細菌感染病例的臨床結(jié)果,在進行統(tǒng)計分析時也缺少臨床和微生物治療失敗的案例 ,因此很少有臨床試驗用于PDT的確定,而是多用于回顧性的研究分析,以對從體外研究和動物模型研究中得到的靶值進行確證[1]。
2.5 進行Monte Crole模擬獲得PK/PD界值
Monte Carlo模擬用于評價抗菌藥物體內(nèi)PK/PD指數(shù)達到PDT的可能性。在進行PK/PD分析時,不論是已有的致病菌MIC分布還是從臨床試驗中獲得的人體PK參數(shù),都只是一個樣本,不能代表整體的MIC分布或者目標(biāo)人群真實的PK參數(shù)。Monte Carlo模擬以現(xiàn)有的MIC分布特點、人體PK參數(shù)及其變異系數(shù)為基礎(chǔ),采用產(chǎn)生“隨機數(shù)”的原理,進行5 000~10 000次模擬,獲得在不同MIC值時的PTA。Drusano等[28-29]最早將Monte Carlo模擬應(yīng)用到了抗菌藥物的PK/PD研究及折點制定中,從2002年起,EUCAST將MCS規(guī)定為藥敏折點制定中的標(biāo)準(zhǔn)方法。Monte Carlo的模擬結(jié)果有兩種表示形式,第1種是用圖表呈現(xiàn)隨著MIC值的變化,達到1個或數(shù)個PDT時的PTA,通常取PTA≥90%時的MIC為PK/PD界值[30]。另1種是直接表示隨著MIC值改變所能達到的PDT的大小,根據(jù)PDT的范圍確定PK/PD界值(圖3)。EUCAST抗菌藥物折點基本文件中多采用第2種表示方法。
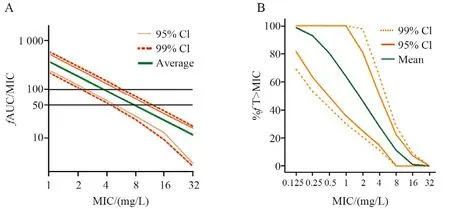
圖3 氟康唑(400 mg/d,靜脈注射,A)和頭孢洛林(600 mg×2,60 min靜脈注射,B)給藥PTA結(jié)果[31-32]
3 EUCAST抗菌藥物PK/PD界值制定實例介紹
氟康唑是唑類抗真菌藥物,對念珠菌屬抗菌活性良好,用于治療念珠菌血癥、侵襲性念珠菌病以及念珠菌引起的尿路感染、下呼吸道感染、骨髓炎、膽囊炎、關(guān)節(jié)炎等。其臨床常用給藥劑量為每天400 mg,最大劑量為每天800 mg,給藥方式為口服或靜脈注射[32]。氟康唑的人體PK參數(shù)如表1所示[33-35]。其療效相關(guān)PK/PD指數(shù)為AUC/MIC, 在播散性念珠菌病小鼠感染模型中,劑量達到ED50所對應(yīng)的PK/PD靶值為25[36],對于侵襲性念珠菌病,臨床推薦靶值為100。圖3為氟康唑Monte Carlo模擬結(jié)果,氟康唑劑量為每天400 mg,取PDT為100時與95%或99%下置信區(qū)間焦點所對應(yīng)MIC值為PK/PD界值,2 mg/ L[32]。
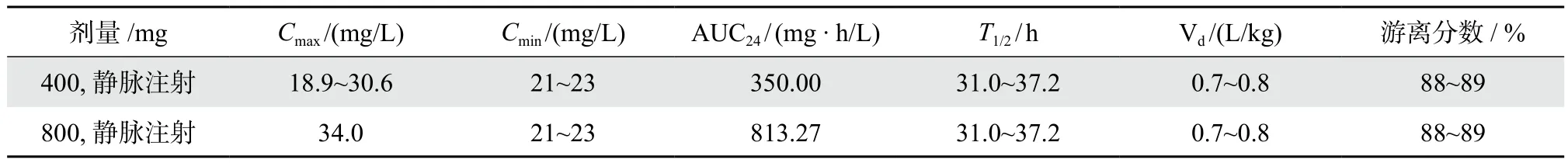
表1 氟康唑健康成年人常用劑量人體PK參數(shù)
頭孢洛林為廣譜頭孢菌素類抗生素,于2010年10月在美國批準(zhǔn)上市,對革蘭陽性菌包括MRSA和耐多藥肺炎鏈球菌以及常見革蘭陰性菌具有殺菌活性,主要用于治療成人社區(qū)獲得性肺炎及復(fù)雜性皮膚軟組織感染。常用給藥方案為600 mg,每12小時1次,靜脈滴注1 h,輕度腎損傷的患者劑量調(diào)整為400 mg。頭孢洛林[31]的人體PK參數(shù)如表2所示。從體外模型、小鼠肺炎模型及小鼠大腿模型均得到頭孢洛林與療效相關(guān)PK/PD指數(shù)為%T>MIC。在體外PK/PD研究中,頭孢洛林對金黃色葡萄球菌殺菌效果達到Δlog10CFU為-2時的靶值為(32.1±8.1)%[37]。在小鼠大腿感染模型中,頭孢洛林對肺炎鏈球菌、金黃色葡萄球菌以及腸桿菌科感染達到Δlog10CFU=-2時的靶值分別為(50±10)%,(45±13)%和(54±3)%[15]。頭孢洛林給藥方案為600 mg,每12小時1次,1 h靜脈滴注給藥,取其PDT為50時獲得的PK/PD界值為0.5 mg/L(置信區(qū)間為95%,圖3)[31]。

表2 頭孢洛林健康成年人臨床常用劑量人體PK參數(shù)
4 結(jié)語
PK/PD界值是制定臨床藥敏折點的重要參考,并不能直接作為臨床折點使用,還需和Ecoff進行平衡比較,從而獲得一個初步的藥敏折點。要求藥敏折點盡量不要落在目標(biāo)病原菌的野生型MIC分布中,即不能小于Ecoff[38],這樣才能保證沒有獲得耐藥機制的野生型菌株均被判斷為“敏感”。初步折點制定后,還需繼續(xù)收集臨床試驗數(shù)據(jù)對其進行確證,同時,如果抗菌藥物有了新的適應(yīng)證、目標(biāo)致病菌和臨床數(shù)據(jù),病原菌敏感性發(fā)生變化,給藥劑量進行了調(diào)整或者獲得了新的PK/PD數(shù)據(jù)時,都應(yīng)該根據(jù)情況對折點進行修訂,EUCAST對已有抗菌藥物折點修訂流程也進行了規(guī)定[39]。
[1] TURNIDGE J, PATERSON DL. Setting and revising antibacterial susceptibility breakpoints[J]. Clin Microbiol Rev,2007,20(3):391-408.
[2] TURNIDGE J, KAHLMETER G, KRONVALL G. Statistical characterisation of bacterial wild-type MIC value distributions and the determination of epidemiological cut-off values[J]. Clin Microbiol Infect, 2006,12(5):418-425.
[3] European Committee on Antimicrobial Susceptibility Testing.Setting breakpoints for new antimicrobial agents, EUCAST SOP 1. 2[EB/OL]. [2016-12-11]. http://www. eucast. org.
[4] MOUTON JW, BROWN DF, APFALTER P, et al. The role of pharmacokinetics/pharmacodynamics in setting clinical MIC breakpoints : the EUCAST approach[J]. Clin Microbiol Infect,2012,18(3):e37-e45.
[5] 李耘, 鄭波, 呂媛, 等. 新抗菌藥物臨床試驗折點制定方案專家共識[J]. 中國臨床藥理學(xué)雜志, 2015,31(11):1069-1076.
[6] EUCAST Disk Diffusion Method for Antimicrobial Susceptibility Testing - Version 6. 0[EB/OL]. [2016-12-11]. http://www.eucast. org.
[7] MATUSCHEK E, BROWN DF, KAHLMETER G, et al.Development of the EUCAST disk diffusion antimicrobial susceptibility testing method and its implementation in routine microbiology laboratories[J]. Clin Microbiol Infect,2014,20(4):O255-O266.
[8] European Committee on Antimicrobial Susceptibility Testing.Procedure for establishing quality control criteria and zone diameter breakpoints for new antimicrobial agents. EUCAST SOP 9. 0[EB/OL]. [2016-12-11]. http://www. eucast. org.
[9] WU Y, KANG J, WANG Q. Drug concentrations in the serum and cerebrospinal fl uid of patients treated with norvancomycin after craniotomy[J]. Eur J Clin Microbiol Infect Dis, 2017, 36(2):305-311.
[10] BERKHOUT J, MELCHERS MJ, VAN MIL AC, et al.Pharmacokinetics and penetration of ceftazidime and avibactam into epithelial lining fluid in thigh- and lung-infected mice[J].Antimicrob Agents Chemother, 2015,59(4):2299-2304.
[11] ZEITLINGER M, SCHWAMEIS R, BURIAN A, et al.Simultaneous assessment of the pharmacokinetics of a pleuromutilin, lefamulin, in plasma, soft tissues and pulmonary epithelial lining fl uid[J]. J Antimicrob Chemother, 2016,71(4):1022-1026.
[12] ABDUL-AZIZ MH, LIPMAN J, MOUTON JW, et al.Applying pharmacokinetic/pharmacodynamic principles in critically ill patients: optimizing ef fi cacy and reducing resistance development[J]. Semin Respir Crit Care Med, 2015,36(1):136-153.
[13] AMBROSE PG, BHAVNANI SM, RUBINO CM, et al.Pharmacokinetics-pharmacodynamics of antimicrobial therapy:it's not just for mice anymore[J]. Clin Infect Dis, 2007,44(1):79-86.
[14] LEPAK AJ, MARCHILLO K, CRAIG WA, et al.In vivopharmacokinetics and pharmacodynamics of the lantibiotic NAI-107 in a neutropenic murine thigh infection model[J]. Antimicrob Agents Chemother, 2015,59(2):1258-1264.
[15] ANDES D, CRAIG WA. Pharmacodynamics of a new cephalosporin, PPI-0903 (TAK-599), active against methicillinresistantStaphylococcus aureusin murine thigh and lung infection models: identi fi cation of anin vivopharmacokineticpharmacodynamic target[J]. Antimicrob Agents Chemother,2006,50(4):1376-1383.
[16] ANDES D, CRAIG WA. Pharmacodynamics of the new fl uoroquinolone gati fl oxacin in murine thigh and lung infection models[J]. Antimicrob Agents Chemother, 2002,46(6):1665-1670.
[17] TAKASHIMA K, TATEDA K, MATSUMOTO T, et al.Establishment of a model of penicillin-resistantStreptococcus pneumoniaepneumonia in healthy CBA/J mice[J]. J Med Microbiol, 1996,45(5):319-322.
[18] 肖舒心, 趙旭, 郭蓓寧. 采用耳窺鏡直視下氣管插管法構(gòu)建小鼠鮑曼不動桿菌肺炎模型[J]. 中國感染與化療雜志, 2015,15(1):51-56.
[19] BRADY RA, BRUNO VM, BURNS DL. RNA-Seq Analysis of the host response toStaphylococcus aureusskin and soft tissue infection in a mouse model[J]. PLoS One, 2015,10(4):e124877.
[20] WANG L, Bi C, WANG T, et al. A coagulase-negative and non-haemolytic strain ofStaphylococcus aureusfor investigating the roles of SrtA in a murine model of bloodstream infection[J].Pathog Dis, 2015,73(6):ftro42.
[21] ROSSI B, SOUBIROU JF, CHAU F, et al. Cefotaxime and amoxicillin-clavulanate synergism against extended-spectrumbeta-lactamase-producingEscherichia coliin a murine model of urinary tract infection[J]. Antimicrob Agents Chemother, 2015,60(1):424-430.
[22] STUCKI A, ACOSTA F, COTTAGNOUD M, et al. Efficacy of ceftaroline fosamil againstEscherichia coliandKlebsiella pneumoniaestrains in a rabbit meningitis model[J]. Antimicrob Agents Chemother, 2013,57(12):5808-5810.
[23] 史軍. 藥物動力學(xué)和藥效動力學(xué)在抗菌藥物新藥開發(fā)和臨床治療上的應(yīng)用[J]. 中國臨床藥理學(xué)與治療學(xué), 2007,12(2):121-133.
[24] ANDES D, CRAIG W A. Animal model pharmacokinetics and pharmacodynamics: a critical review[J]. Int J Antimicrob Agents, 2002,19(4):261-268.
[25] YOKOYAMA Y, MATSUMOTO K, IKAWA K, et al.Pharmacokinetic/pharmacodynamic evaluation of sulbactam againstAcinetobacter baumanniiinin vitroand murine thigh and lung infection models[J]. Int J Antimicrob Agents, 2014,43(6):547-552.
[26] LIANG W, CHEN YC, CAO YR, et al. Pharmacokinetics and pharmacodynamics of nemonoxacin againstStreptococcus pneumoniaein anin vitroinfection model[J]. Antimicrob Agents Chemother, 2013,57(7):2942-2947.
[27] WU XJ, ZHANG J, GUO BN, et al. Pharmacokinetics and pharmacodynamics of multiple-dose intravenous nemonoxacin in healthy Chinese volunteers[J]. Antimicrob Agents Chemother,2015,59(3):1446-1454.
[28] DRUSANO GL, PRESTON SL, HARDALO C, et al. Use of preclinical data for selection of a phase II/III dose for evernimicin and identi fi cation of a preclinical MIC breakpoint[J]. Antimicrob Agents Chemother, 2001,45(1):13-22.
[29] DRUSANO GL, D'ARGENIO DZ, PRESTON SL, et al. Use of drug effect interaction modeling with Monte Carlo simulation to examine the impact of dosing interval on the projected antiviral activity of the combination of abacavir and amprenavir[J].Antimicrob Agents Chemother, 2000,44(6):1655-1659.
[30] FREI CR, WIEDERHOLD NP, BURGESS DS. Antimicrobial breakpoints for Gram-negative aerobic bacteria based on pharmacokinetic-pharmacodynamic models with Monte Carlo simulation[J]. J Antimicrob Chemother, 2008,61(3):621-628.
[31] European Committee on Antimicrobial Susceptibility Testing.Ceftaroline: Rationale for the clinical breakpoints, version 1.0[EB/OL]. [2016-12-15]. http://www. eucast. org.
[32] European Committee on Antimicrobial Susceptibility Testing.Fluconazole : Rationale for the clinical breakpoints, version 2.0[EB/OL]. [2016-12-15]. http://www. eucast. org.
[33] GRANT SM, CLISSOLD SP. Fluconazole,A review of its pharmacodynamic and pharmacokinetic properties, and therapeutic potential in superficial and systemic mycoses[J].Drugs, 1990,39(6):877-916.
[34] BRAMMER KW, FARROW PR, FAULKNER JK.Pharmacokinetics and tissue penetration of fluconazole in humans[J]. Rev Infect Dis, 1990,12 (Suppl 3) :s318-s326.
[35] GOA KL, BARRADELL LB. Fluconazole. An update of its pharmacodynamic and pharmacokinetic properties and therapeutic use in major superficial and systemic mycoses in immunocompromised patients[J]. Drugs, 1995,50(4):658-690.
[36] ANDES D, VAN OGTROP M. Characterization and quantitation of the pharmacodynamics of fl uconazole in a neutropenic murine disseminated candidiasis infection model[J]. Antimicrob Agents Chemother, 1999,43(9):2116-2120.
[37] MACGOWAN AP, NOEL AR, TOMASELLI S, et al.Pharmacodynamics of ceftaroline againstStaphylococcus aureusstudied in anin vitropharmacokinetic model of infection[J].Antimicrob Agents Chemother, 2013,57(6):2451-2456.
[38] ARENDRUP MC, KAHLMETER G, RODRIGUEZ-TUDELA JL, et al. Breakpoints for susceptibility testing should not divide wild-type distributions of important target species[J]. Antimicrob Agents Chemother, 2009,53(4):1628-1629.
[39] European Committee on Antimicrobial Susceptibility Testing.Review and revision of antimicrobial breakpoints, EUCAST SOP 3.1[EB/OL].[2016-12-20].http://www.eucast.org.
Application of PK/PD research in developing clinical susceptibility breakpoints of antimicrobial agents
LI Xin, ZHU Demei, ZHANG Jing. (Institute of Antibiotics, Huashan Hospital, Fudan University, Key Laboratory of Clinical Pharmacology of Antibiotics, Ministry of Health, Shanghai 200040, China)
R969.1
A
1009-7708 ( 2017 ) 05-0602-06
10.16718/j.1009-7708.2017.05.021
2017-02-10
2017-06-08
國家自然科學(xué)基金面上項目(81373494)。
復(fù)旦大學(xué)附屬華山醫(yī)院抗生素研究所,衛(wèi)生部抗生素臨床藥理重點實驗室,上海 200040。
李鑫(1993—),女,碩士研究生,主要從事抗生素動物體內(nèi)藥動學(xué)/藥效學(xué)研究。
張菁,E-mail:zhangj61@fudan.edu.cn。

