醫用透明質酸鈉凝膠中鎢含量的分析研究及其安全性評價*
劉莉莉,駱紅宇,施燕平,潘華先,秦洋
(1. 山東省醫療器械產品質量檢驗中心,濟南 2501012.山東省醫療器械生物學評價重點實驗室,濟南 2501013. 山東恒信檢測技術開發中心,濟南 250101)
1 引 言
醫用透明質酸鈉凝膠為生物可降解高分子聚糖類生物材料,具有良好的生物相容性及生物學活性。所形成的高分子網狀結構具有特有的流變學特性,使其在手術中可作為手術工具和保護工具。醫用透明質酸鈉凝膠小包裝一般采用預灌封包裝設計,再封裝于單包裝容器(袋或塑料泡罩)內。
醫用透明質酸鈉凝膠作為一種可植入體內的特殊醫療產品,其質量優劣直接影響患者身體健康及生命安全。此類產品在生產過程中往往會引入微量金屬元素,如果生產企業和醫療器械監管機構對此風險不加以控制,毒性較大的金屬元素就會隨著產品的植入在體內釋放,對人體各組織器官造成不同程度的損傷。
在對醫用透明質酸鈉凝膠的金屬元素檢測中,發現此類產品中含有不同濃度的鎢元素。追其原因是由于,預灌封注射器玻璃針筒頂部的內部通道成型工藝中會引入金屬鎢,金屬鎢在400℃時會被氧化為氧化鎢,在800℃時,氧化鎢會發生升華,在加工過程中變成蒸汽沉降在玻璃器皿表層[1-2]。
鎢在預灌封注射器包裝組件的加工工藝中引入,隨著樣品可直接進入人體,其安全風險應引起關注。本研究擬采用微波消解和ICP-MS法建立醫用透明質酸鈉凝膠產品中鎢含量的分析方法,并對產品的遷入鎢的安全性進行評價,以對產品標準的完善提供依據。
2 實驗部分
2.1 儀器與材料
美國PE公司電感耦合等離子體質譜儀(NexlON 350D);美國CEM密閉微波消解系統(MARS-OMNI);德國Millipore公司超純水機(Milli-Q?Advantage A10);硝酸(J.T.Baker,A.C.S. Reagent);雙氧水(國藥集團,優級純);鎢W標準溶液(1000 mg/L,國家有色金屬及電子材料分析測試GSB 04-1760-2004);錸Re標準溶液(1000 mg/L,國家有色金屬及電子材料分析測試GSB 04-1745-2004);12家市場可售醫用透明質酸鈉凝膠產品。
2.2 試驗方法
2.2.1樣品前處理 取樣品0.5~1.0 g,加硝酸8 mL,H2O21 mL裝入消解罐內,蓋蓋放置反應2 h,用微波消解儀進行前處理后于120℃趕酸至體積小于1 mL,用1%HNO3定容至50 mL,作為檢驗液,同法制備空白。微波消解具體條件見表1。
2.2.2儀器工作條件 ICP-MS工作條件:載氣流量:0.75 L/min;射頻功率:1600 W;霧化器及霧室:同心霧化器及玻璃旋流霧室;采樣錐截取錐類型:鉑錐;分析模式:標準模式;動態帶寬調節:RPa=0,RPq=0.25。
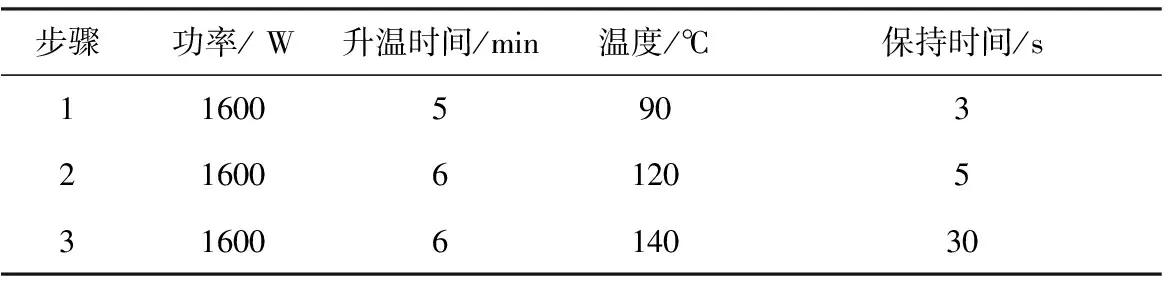
表1 微波消解條件
2.2.3測試方法 以錸187Re作為內標,采用市售標準物質W標準溶液(選用182W和184W),建立標準曲線。空白液和待測樣品采用標準曲線定量。
3 結果
3.1 標準曲線及相關系數
取鎢標準溶液,用1%HNO3稀釋配制濃度為0、0.2、0.5、1、2、5、8、10 ug/L的標準溶液,1%HNO3將內標錸的濃度配制為10 ug/L,進樣檢測。
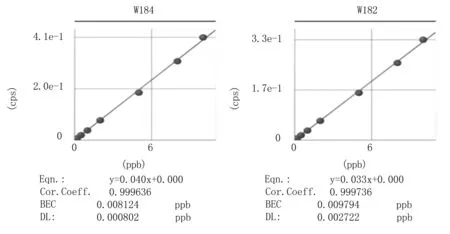
圖1鎢標準曲線圖
Fig.1Tungstenstandardcurve
從圖1可以看出,無論是儀器給出的檢出限(DL)還是等效背景濃度(BEC),均是184W的數值較低,可優先選184W為定量曲線。對于184W的標準曲線,在0~10 ug/L濃度范圍內,線性較好,相關系數R=0.9996。
3.2 檢出限試驗
重復進樣空白溶液11 次,記錄吸光度。以吸光度標準偏差的3 倍與標準曲線的斜率比值,計算得到儀器的檢出限為0.006 ug/L,以吸光度標準偏差的10 倍與標準曲線的斜率比值,計算得到儀器的定量限為: 0.020 ug/L。若按取樣量0.5 g,定容體積50 mL 計算,得方法檢出限為0.0006 mg /kg,方法定量限為0.002 mg /kg。
3.3 精密度試驗
取1份已處理好的供試品溶液,連續進樣11次,測定吸光度,計算11 個結果的RSD 為2.4 %。
3.4 重復性試驗
精密稱取同批次醫用透明質酸鈉凝膠約0.5 g 6 份,按前述方法進行含量測試。結果為0.27、0.25、0.28、0.27、0.26、0.25 mg /kg,RSD為4.60%。
3.5 回收率實驗
精密稱取醫用透明質酸鈉凝膠約0.5 g,準確加入1 ug/mL 的鎢標準儲備液 0.1和0.3 mL,按前述方法進行含量測試,結果見表2。由表2可以看出,待測元素的加標回收率為95.23%和104.54%,表明采用本方法測定醫用透明質酸鈉凝膠中的鎢元素,結果準確可靠。

表2 回收率試驗(n=3)
3.6 樣品分析
用上述方法,對12批市售醫用透明質酸鈉凝膠中的鎢元素進行測定,結果見表3。從表3可以看出,醫用透明質酸鈉凝膠中鎢的含量在0.03~4.56 ug/g之間。
4 討論
因為醫用透明質酸鈉凝膠中鎢的化合物主要來源于預灌封注射器的表層沉積,隨著透明質酸鈉凝膠的灌裝而混入樣品中。因此,鎢的含量與質酸鈉凝膠的體積和濃度無關,只與鎢針在形成內部通道時的升華程度有關。這一點在表3的數據分布上也可以證明。
表3 12批供試樣品鉻含量測定結果
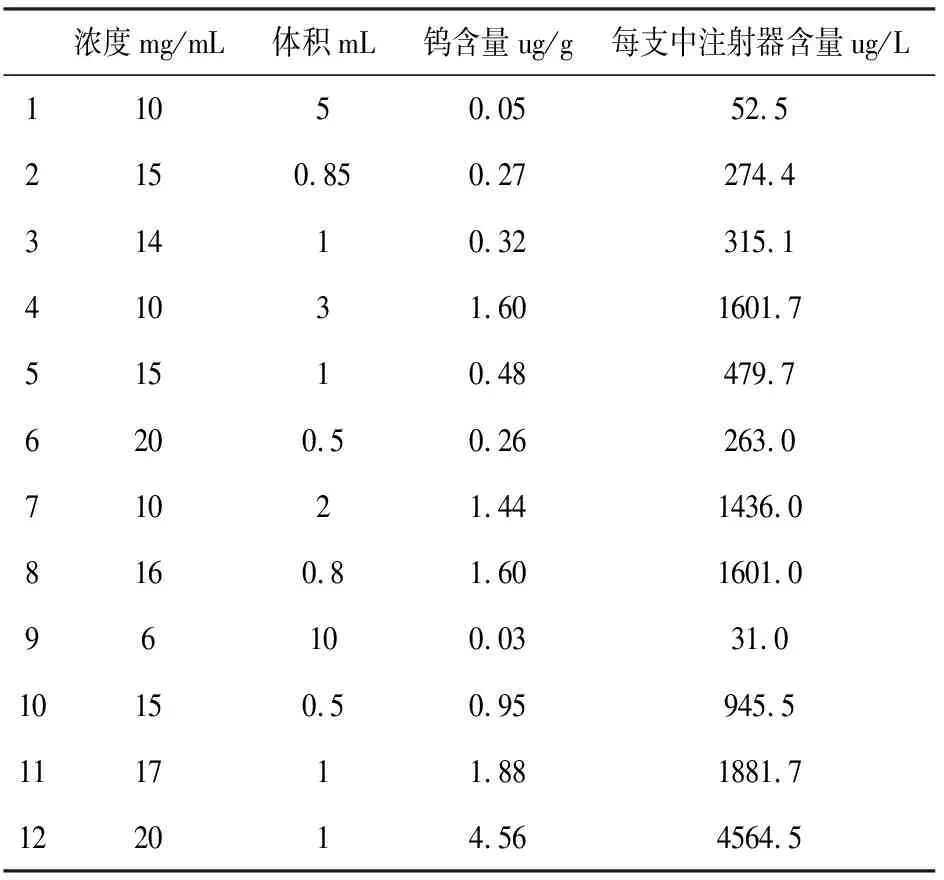
Table 3 Determination result of tungsten in 12 batches of samples
目前國際上關于金屬元素的安全性評價大多參照美國藥典<232藥品元素雜質限度>,人用藥物注冊技術要求國際協調會議< ICH Q3D 元素雜質指導原則>以及EMEA關于金屬催化劑或金屬試劑殘留量限度規定的指導原則。 但在USP 232及EMEA文件中,元素鎢未出現在需要關注的元素列表之中[3-4],在ICH Q3D中也歸類到其他元素雜質中(因其較低的毒性和/或在地方法規中的要求不同,其 PDE 還沒有建立,在指南中并未說明)[5],因此無相關的PDE值可以參考。
金屬元素鎢的毒理機制的研究較少,缺少相關的毒理學數據。目前可查到的一些生態毒性實驗,所有已知的數據集中在單一態鎢酸鹽,鎢酸鈉對小鼠和大鼠的LD50值分別為240 mg/Kg和1190 mg/Kg。但是在最近幾年的研究中,研究人員發現尿液中鎢含量高的人與高中風率之間存在關聯。雖然沒有記載鎢單獨作用并不會造成人體的健康問題,但有通過動物和細胞培養的實驗表明它與癌癥和肺部感染之間存在關聯;另一些研究也顯示了鎢與心臟問題之間存在聯系[6-10]。
國內標準中,查詢器械類、食品類及環境保護類,均未有鎢元素的限量值的相關標準。在國外的標準方面,在美國,除了職業暴露空氣污染指數(難溶鎢類為5 mg/m3,可溶鎢類為1 mg/m3)外,沒有針對鎢的其他規定。鎢污染指標在蘇聯首先建立起來,包括最大允許濃度(環境污染的一個定量指標)。MAC被定義在整個生命周期中某種化學物質影響人類健康的最低濃度。飲用水和漁業水庫中鎢的MAC值分別為0.05和0.0008 mg/L。起初,1966年的飲用水MAC值被定為0.1 mg/L。后來,當有研究發現在更低濃度的鎢和鉬共同作用下會對老鼠產生胚胎毒性時,MAC值被改為如今的0.05 mg/L[6]。
如若按照每個成人日均飲水量設定為1 500至1 700 ml[11],每日攝入的鎢元素的量應控制在75 mg/d。醫用透明質酸鈉凝膠的臨床日使用量假定為5支,則樣品的鎢攝入量見圖2,遠小于飲用水中的控制標準。
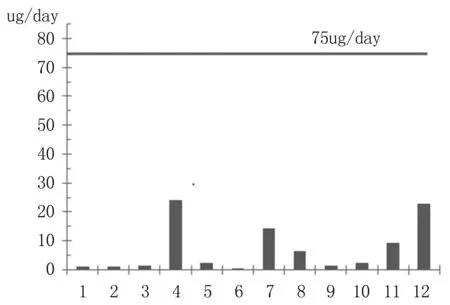
圖2醫用透明質酸鈉凝膠中鎢元素每日最大攝入量示意圖
Fig2ThemaximumdailyintakeofTungsteninmedicalsodiumhyaluronategel
現在,有一種新型成型系統可以降低針頭的處理溫度,并在其表層形成一種保護層,以減少機械接觸。從而可以使鎢的殘留含量大大降低,可浸出的金屬鎢平均殘留量<250 ug/L[2]。按此數據,此次的供試樣品除去5mL和10mL的體積較大的注射器外,其他批次都遠大于此數值。因此,雖然鎢的含量可滿足人體的安全性評價要求,但是預灌封注射器的廠家還是可以通過工藝革新等措施減小人體鎢的攝入量。

