地諾單抗與唑來膦酸治療惡性腫瘤伴骨轉移安全性和有效性的Meta分析
陳皖京 王蓓 高秀飛 徐小宏 張碩 胡袁媛
地諾單抗與唑來膦酸治療惡性腫瘤伴骨轉移安全性和有效性的Meta分析
陳皖京 王蓓 高秀飛 徐小宏 張碩 胡袁媛
目的 系統評價地諾單抗與唑來膦酸治療惡性腫瘤伴骨轉移的有效性和安全性。方法 利用Cochrane library、Pub Med、OVID、Springer Linker、Science Direct、EBSCO等數據庫檢索文獻,按Cochrane風險偏倚評估工具評價納入文獻質量并提取文獻數據,應用Rev Man 5.3軟件進行Meta分析。結果 納入4項臨床隨機對照試驗,共6 029例患者,包含7篇相關文獻。Meta分析結果顯示,與唑來膦酸比較,地諾單抗能明顯延緩骨相關事件(SREs)發生的時間,降低骨轉移標志物Ⅰ型膠原交聯氨基末端肽/肌酐(uNTx/Cr)、骨源性堿性磷酸酶(S-BALP)濃度,預防骨放療,延緩疼痛加劇和干預,同時治療后貧血、急性期反應和腎毒性的發生率更低,差異均有統計學意義(均P<0.01);兩組患者總生存(OS)時間、疾病進展時間、預防病理性骨折、預防骨手術、預防脊髓壓迫、不良事件(AEs,包括惡心、疲勞、背痛、下頜骨壞死等)的發生率等指標比較,差異均無統計學意義(均PP>0.05)。結論 地諾單抗在臨床有效性和安全性方面優于唑來膦酸,為惡性實體瘤伴骨轉移患者的臨床預防與治療提供了新的方案。
地諾單抗 唑來膦酸 骨相關事件 骨轉移 惡性腫瘤
骨是惡性實體腫瘤(尤其是乳腺癌、前列腺癌和肺癌等)常見的轉移部位,惡性實體瘤伴骨轉移常引起嚴重的骨相關事件(SREs),包括病理性骨折、脊髓壓迫綜合征、為緩解骨痛的放療、為預防或治療病理性骨折或脊髓壓迫綜合征的骨手術等[1]。SREs的出現預示著患者住院風險增加,住院時間延長,生存質量下降等[2-6]。目前主要采取全身綜合治療惡性實體瘤伴骨轉移,包括化療、放療、內分泌治療、生物靶向治療、雙磷酸鹽治療、手術和康復等。唑來膦酸是第三代雙磷酸鹽藥物,目前廣泛應用于臨床,可有效預防和延遲SREs的發生[7],但仍有部分患者在用藥后發生SREs[8-9]。此外,唑來膦酸具有腎毒性,臨床上禁用于嚴重腎功能不全(內生肌酐清除率<30ml/min)的患者。地諾單抗是一種靶向人源性RANKL的單克隆抗體。RANKL是破骨細胞的關鍵激活因子,地諾單抗與RANKL特異性結合并阻斷RANKL介導的破骨細胞活化,從而阻斷惡性實體瘤伴骨轉移機制中破骨細胞激活環節。地諾單抗依靠非特異性內皮網狀系統而非腎臟代謝,因此可用于腎功能不全患者或可能造成腎損傷的治療方案。現有多篇文獻表明地諾單抗能有效延遲SREs的發生并提高晚期腫瘤患者的生活質量[1,10-15]。在精準醫學的大背景下,生存質量較生存時間更為重要;因此,有效改善晚期腫瘤患者的生存質量、減輕骨轉移患者疼痛以及對止痛藥物的依賴,是當前醫療研究的熱點。本研究搜索相關文獻,就地諾單抗與唑來膦酸治療惡性實體瘤伴骨轉移的有效性和安全性作一Meta分析。
1 對象和方法
1.1 對象 利用Cochranelibrary、PubMed、OVID、Springer Linker、Science Direct、EBSCO等數據庫檢索文獻。檢索詞:cancers or tumour or tumours or neoplasms or neoplasm、bone metastasis or bone metastases、skeletal-related events、SREs、zoledronic acid、denosumab。納入標準:(1)年齡≥18歲;(2)組織學或細胞學證實為惡性實體瘤或多發性骨髓瘤,X線、CT或MRI等影像學檢查提示存在至少1處骨轉移;(3)美國東部腫瘤協作組(ECOG)體能狀況評分0~2分。排除標準:(1)內生肌酐清除率<30ml/min;(2)既往接受過雙磷酸鹽治療骨轉移;(3)口腔手術后未愈合;(4)3年內罹患過第2種惡性腫瘤;(5)有骨病手術或放療計劃;(6)預計患者生存時間<6個月;(7)惡性腫瘤累及器官的功能良好。按照上述檢索策略,按照納入與排除標準,最終納入4項臨床隨機對照試驗(RCT),共6 029例患者,包含7篇相關文獻[1,10-15](其中3篇文獻[13-15]為相關RCT不同隨訪項目的后續報道)。
1.2 方法
1.2.1 文獻篩選 由2位研究者獨立閱讀文獻題目及摘要,對可能納入的研究閱讀全文,相互核對納入結果,若意見不同則通過討論或由第3人裁定。
1.2.2 文獻質量評價 納入研究的文獻質量評價采用Cochrane風險偏倚評估工具,偏倚風險評估方法的內容包括:(1)隨機分配方案的產生,(2)隱蔽分組,(3)對患者和醫生實施盲法,(4)對結果評價實施盲法,(5)不完整的結果數據,(6)選擇性的結果,(7)其他偏倚。根據低偏倚風險、高偏倚風險和文獻對偏倚評估未提供足夠或不確定的信息等三方面進行評估;同時采用Jadad質量評價標準評價納入研究的文獻質量(包括隨機方法、盲法、退出與失訪等3項內容),Jadad量表滿分為5分,≤2分為低質量研究,>2分為質量較高[16]。
1.3 統計學處理 應用Rev Man 5.3統計軟件進行Meta分析。計算結果用危險比(HR)或OR值及其95%CI表示。異質性檢驗采用χ2檢驗,當PP>0.05且I2<50%時,采用固定效應模型進行分析;當P<0.05且I2>50%時,采用隨機效應模型進行分析。用漏斗圖檢測潛在的表達偏倚。
2 結果
2.1 文獻評估結果及基本特征 Cochrane風險偏倚評估顯示低偏倚風險,見圖1。Jadad量表評分均為5分。7篇文獻的基本特征,見表1。
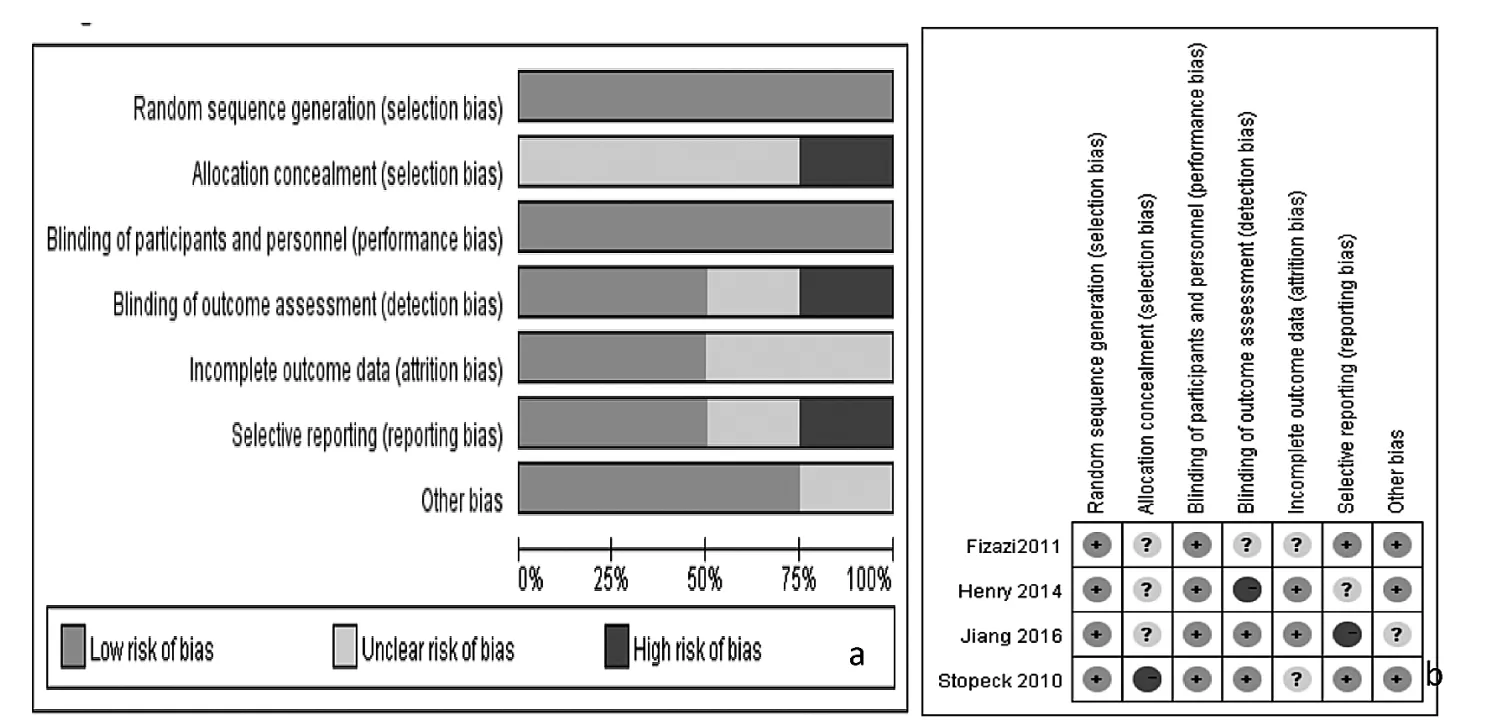
圖1 納入文獻的偏倚風險評估結果(a:偏倚風險百分圖;b:偏倚風險總結圖)
2.2 Meta分析結果 與唑來膦酸比較,地諾單抗能明顯延遲首次SREs發生的時間、首次及隨后SREs發生的時間,降低骨轉移標志物Ⅰ型膠原交聯氨基末端肽/肌酐(uNTx/Cr)、骨源性堿性磷酸酶(S-BALP)的濃度,預防骨放療,延緩疼痛加劇和干預,降低治療后貧血、急性期反應和腎毒性等的發生率,差異均有統計學意義(均P<0.01),見表2和圖2。兩組患者總生存(OS)時間、疾病進展時間、預防病理性骨折、預防骨手術、預防脊髓壓迫、不良事件(AEs,包括惡心、疲勞、背痛、下頜骨壞死等)的發生率等指標比較,差異均無統計學意義(均 P >0.05),見表 2。

表1 納入文獻的基本特征
2.3 發表偏倚分析 使用漏斗圖對納入的主要4篇研究進行測量,發現各指標的樣本相對集中的分布于圖形中部,兩側較對稱,說明發表偏倚存在的可能性較小,見圖3。
3 討論
隨著精準醫學理念的提出以及抗腫瘤藥物、手術技巧的不斷更新,惡性腫瘤患者的生存時間不斷延長,與此同時發生骨轉移的風險也隨之增加。骨轉移誘發的SREs及骨痛嚴重影響著患者的生活質量和生存時間,患者往往需要應用止痛劑甚至阿片類藥物才能緩解疼痛,但這些藥物對消化、神經、呼吸等系統具有不良反應及成癮性[17]。一項回顧性研究結果顯示,骨轉移或SREs的發生與乳腺癌的預后密切相關,無骨轉移、有骨轉移、同時伴有骨轉移和SREs患者的5年OS率分別為76%、8%和3%[18]。因此,關于預防或延緩SREs的治療在惡性實體腫瘤伴骨轉移患者中至關重要。唑來膦酸是
臨床上常用的雙磷酸鹽,廣泛用于惡性實體腫瘤伴骨轉移患者,其作用機制主要包括:(1)抑制破骨細胞的成熟及破骨細胞在骨質吸收部位的聚集;(2)減少腫瘤刺激誘導的生長因子分泌,進而調控骨的微環境[19];(3)抑制血管內皮生長因子誘導的內皮細胞增殖,進而明顯抑制血管生成[20];(4)調節免疫系統而抑制腫瘤增殖[21];(5)經甲羥戊酸途徑抑制腫瘤細胞的生長、黏附、入侵[22]。唑來膦酸主要以原型經腎臟排泄,而惡性腫瘤的多種化療藥物具有腎毒性,長期使用會損害腎功能甚至出現中毒性急性腎小管壞死[23];因此,靜脈注射唑來膦酸所致急性反應發生率較高,從而限制了唑來膦酸的應用。地諾單抗是人源性單克隆抗體(IgG2單抗),可以阻止NF-κB受體活化因子配體RANK-L與其受體結合,抑制破骨細胞活化和發展,減少骨吸收,增加皮質骨和骨小梁的強度和硬度,抑制骨局部侵蝕和骨質溶解,最終發揮預防或治療SREs功能[23]。地諾單抗通過非特異性網狀內皮系統代謝[24],無腎毒性,其皮下注射的給藥方式較唑來膦酸的靜脈注射更為安全、方便,依從性更好,且無需因腎損傷而調節劑量或停藥,可能在療效、依從性方面具有更大的優勢。
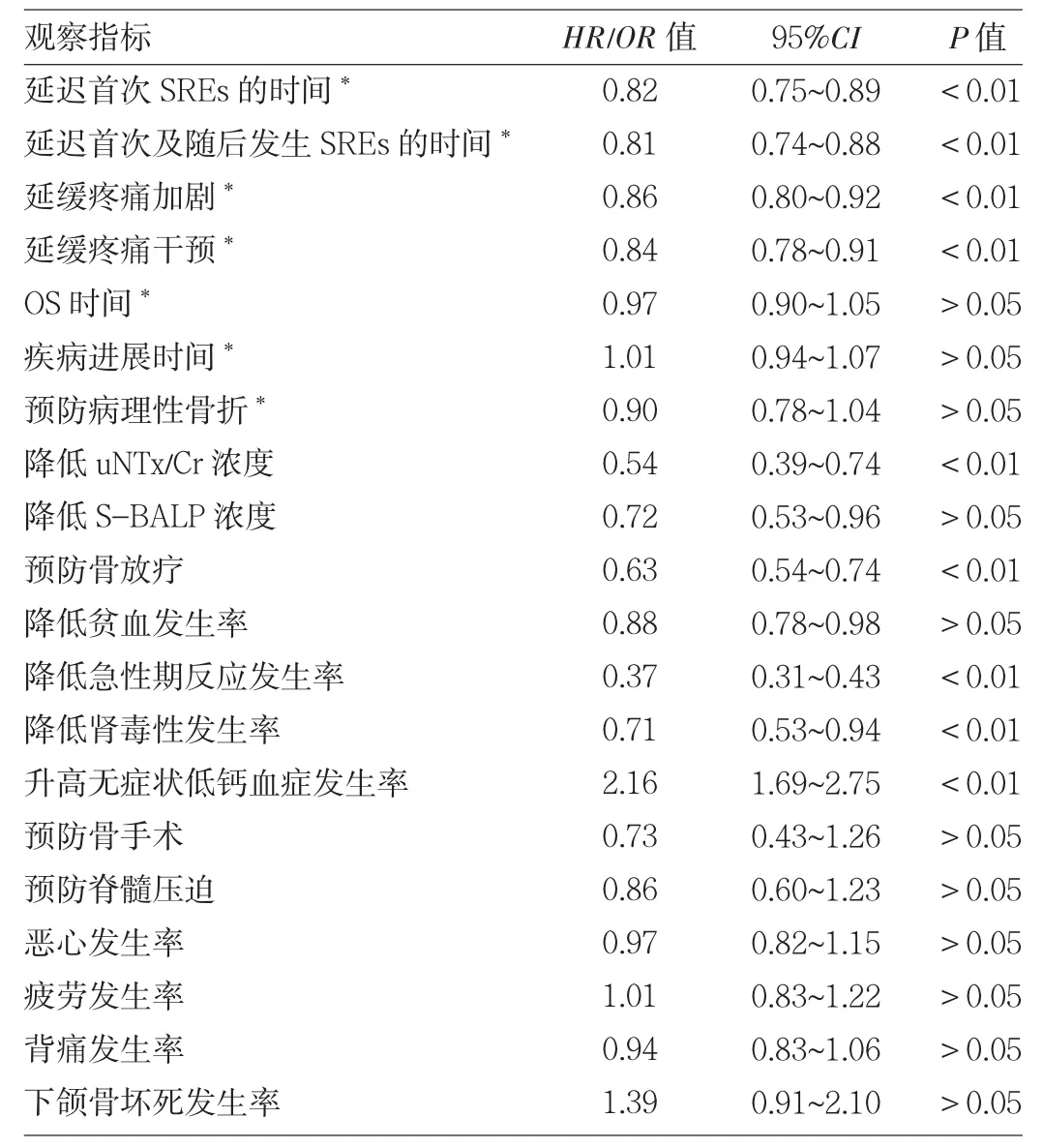
表2 地諾單抗與唑來膦酸有效性和安全性的比較
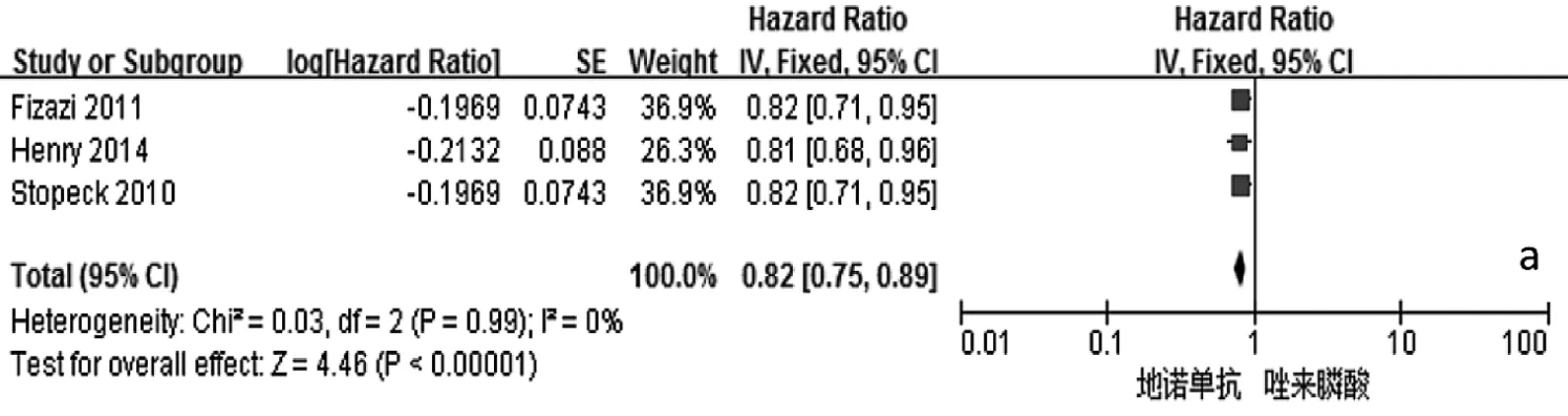
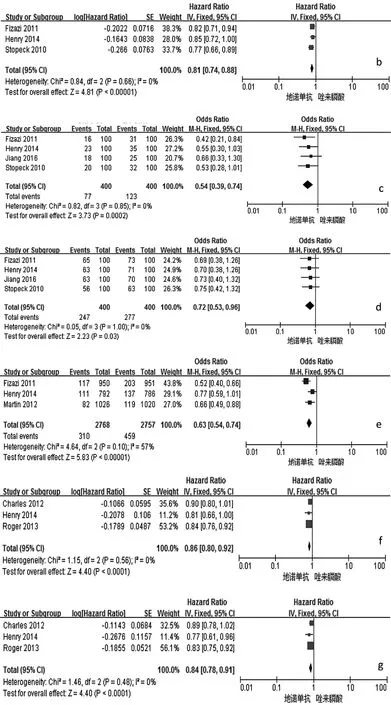
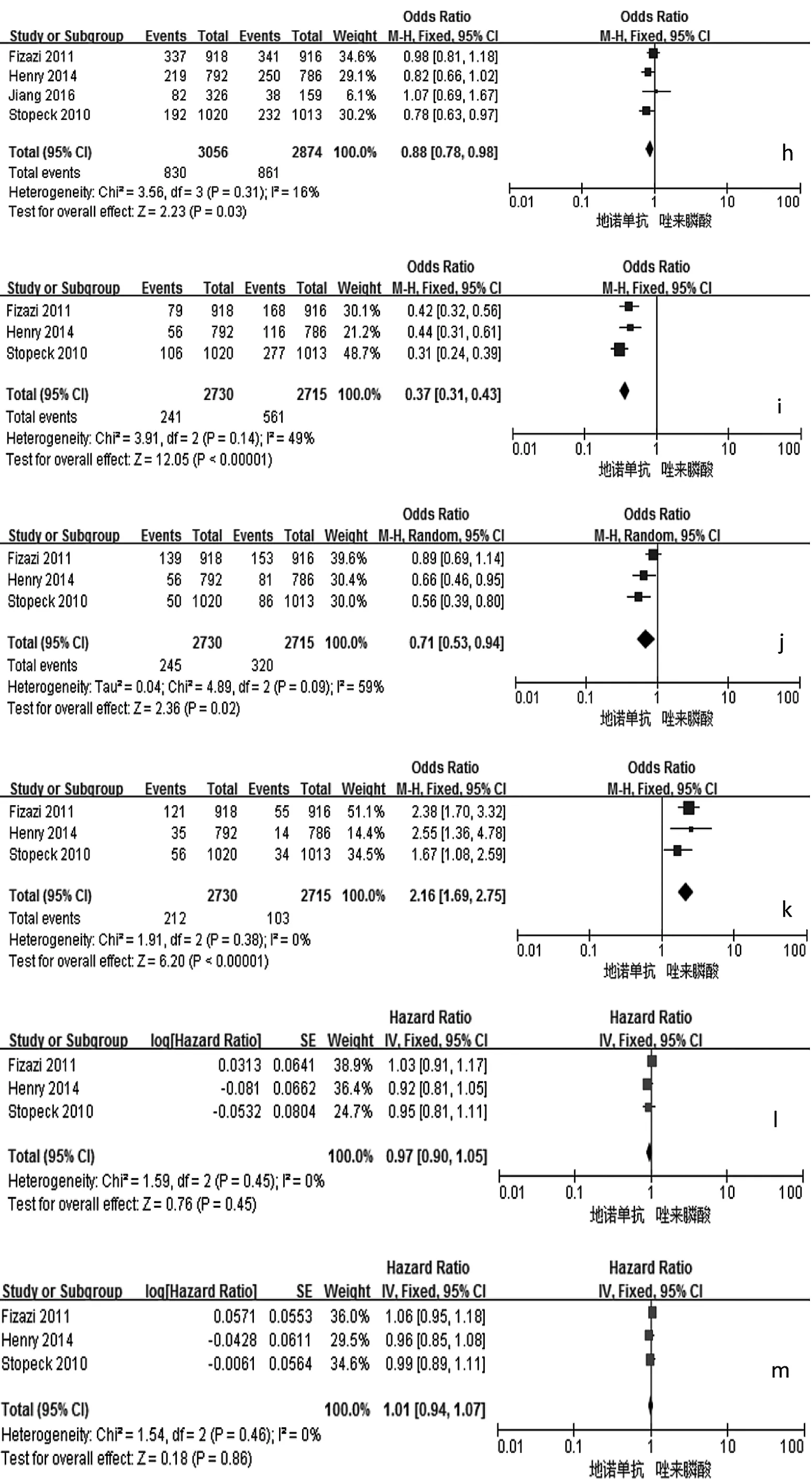
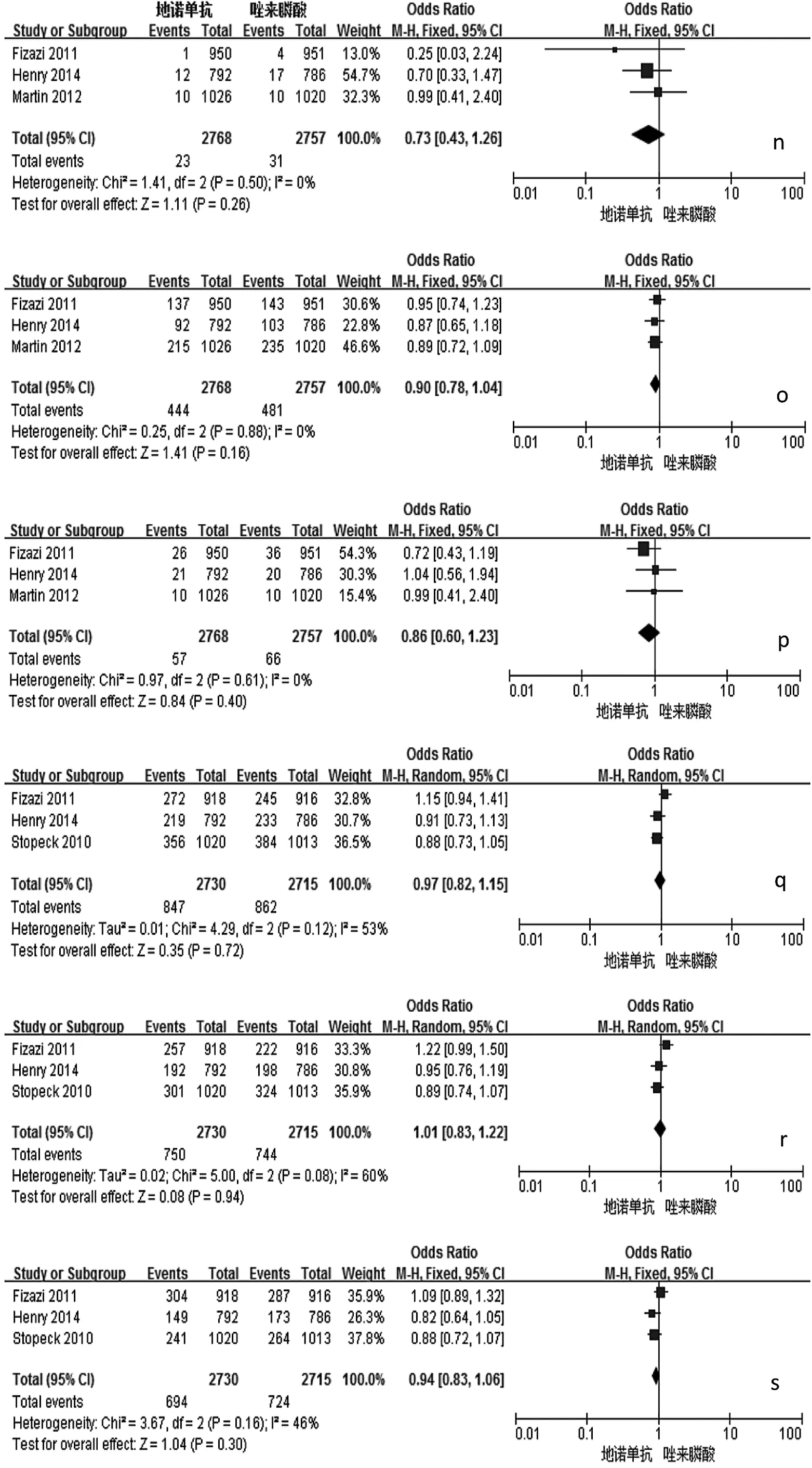
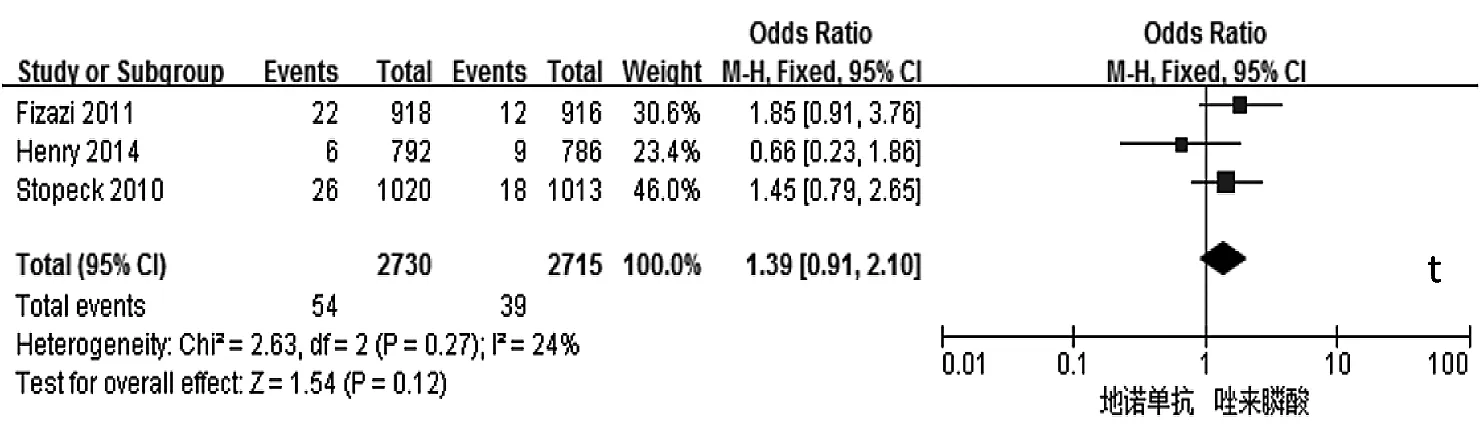
圖2 地諾單抗與唑來膦酸有效性和安全性比較的森林圖(a:首次發生SREs時間;b:首次及隨后發生SREs時間;c:降低uNTx/Cr濃度;d:降低 S-BALP 濃度;e:預防骨放療;f:延緩疼痛加劇;g:延緩疼痛干預;h:貧血發生率;i:急性期反應發生率;j:腎毒性發生率;k:低鈣血癥發生的比較;l:OS 時間;m:疾病進展時間;n:預防病理性骨折;o:預防骨手術;p:預防脊髓壓迫;q:惡心發生率;r:疲勞發生率;s:背痛發生率;t:下頜骨壞死發生率;a-k:P<0.05;l-t:PP>0.05)
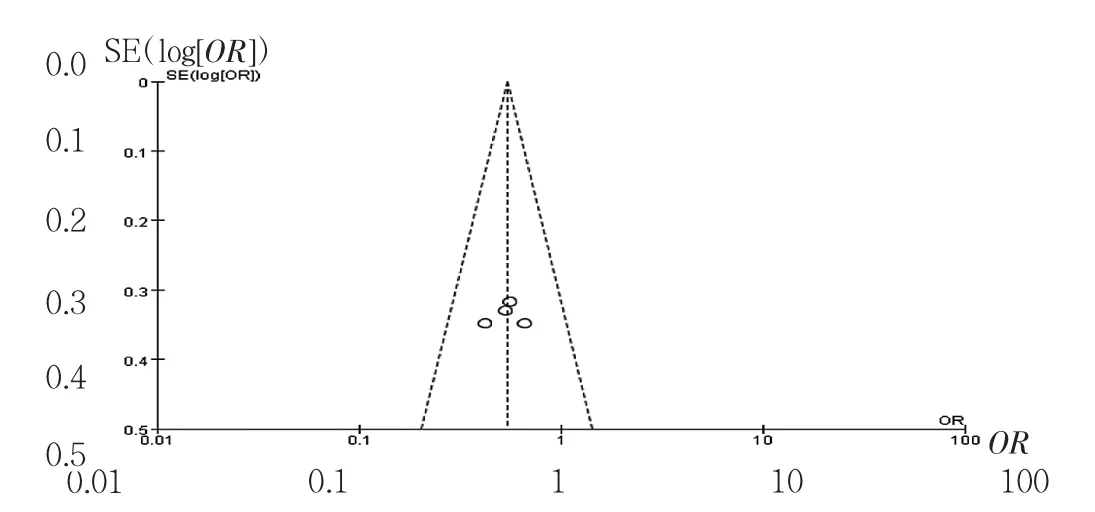
圖3 Meta分析漏斗圖
I型膠原是骨組織中唯一的膠原,其氨基端通過脫氧吡啶啉、吡啶啉與另一膠原分子的930位氨基酸形成NTX[25],NTX在骨吸收時釋放入血,若未降解或代謝則可隨尿液排出。運動與飲食對NTX的影響極小,盡管多處組織中存在NTX,但未經破骨細胞代謝,尿中NTX濃度不受影響。BALP是成骨細胞膜上的一種四聚體蛋白[26],是成骨細胞合成的特異性細胞外酶,主要位于骨化部位,多見于骨基質成熟期。惡性腫瘤發生骨轉移時,因骨內磷酸鈣沉積,成骨細胞代謝旺盛,最終導致BALP濃度升高。多項研究表明uNTx/Cr、S-BALP與惡性腫瘤骨轉移密切相關,可為預測惡性實體瘤骨轉移提供有效參考;因此,本研究納入uNTx/Cr、S-BALP作為評價地諾單抗與唑來膦酸療效的指標[27-28]。本文Meta分析結果顯示,與唑來膦酸比較,地諾單抗可明顯延遲首次發生SREs的時間、首次及隨后發生SREs的時間,明顯降低與骨轉移密切相關的uNTx/Cr、S-BALP濃度,預防骨放療,延緩疼痛加劇和干預;因此,患者生活質量得到明顯改善,且避免了疼痛造成的困擾及經濟負擔。同時,地諾單抗組患者的貧血、急性期反應和腎毒性等發生率均較低,提示更為安全可靠;但低鈣血癥發生率較高,可能與地諾單抗較強的抑制骨吸收作用有關,但在研究中低鈣血癥多無明顯癥狀,易通過口服鈣劑和維生素D糾正,故地諾單抗治療期間強烈建議同時補充維生素D(≥400IU)和鈣劑(≥500mg),以免低鈣癥狀的發生。
綜上所述,與唑來膦酸比較,地諾單抗治療惡性腫瘤伴骨轉移更為安全、有效。本研究納入的7篇文獻偏倚風險較低,納入文獻的質量較高,可信度較強。另外,本研究納入了一篇來自中國Ⅲ期臨床隨機對照雙盲研究,研究對象主要針對中國患者,研究結果為了解地諾單抗治療中國實體惡性腫瘤伴骨轉移是否優于唑來膦酸提供了可靠、實際的依據。Snedecor等[29]報道地諾單抗的治療費用/療效比高于唑來膦酸,這也是患者在選擇藥物時需要考慮的問題。在經濟條件允許的前提下,本研究結果支持優先選用地諾單抗預防與治療惡性腫瘤伴骨轉移,但仍需要更大樣本、多中心的RCT來證實并指導藥物方案的選擇。
[1] Stopeck A T,Lipton A,Body J J,et al.Denosumab compared with zoledronic acid for the treatment of bone metastases in patients with advanced breast cancer:a randomized,double-blind study[J].J Clin Oncol,2010,28(35):5132-5139.
[2] Costa L,Badia X,Chow E,et al.Impact of skeletal complications on patients'quality of life,mobility,and functional independence[J].Support Care Cancer,2008,16(8):879-889.
[3] Weinfurt K P,Castel L D,Li Y,et al.Health-related quality of life among patients with breast cancer receiving zoledronic acid orpamidronate disodium for metastatic bone lesions[J].Med Care,2004,42(2):164-175.
[4] Pockett R D,Castellano D,McEwan P,et al.The hospital burden of disease associated with bone metastases and skeletal-related events in patients with breast cancer,lung cancer or prostate cancer in Spain[J].Eur J Cancer Care(Engl),2010,19(6):755-760.
[5] Wardley A,Davidson N,Barrett-Lee P,et al.Zoledronic acid significantly improves pain scores and quality of life in breast cancer patients with bone metastases:a randomised,crossover study of community vs hospital bisphosphonate administration[J].Br J Cancer,2005,92(10):1869-1876.
[6] Body J J,Diel I J,Bell R,et al.Oral ibandronate improves bone pain and preserves quality of life in patients with skeletal metastases due to breast cancer[J].Pain,2004,111(3):306-312.
[7] Katherine A.Zoledronic acid[J].Drugs,2008,68(18):2661-2682.[8] Rosen L S,Gordon D,Kaminski M,et al.Zoledronic acid versus pamidronate in the treatment of skeletal metastases in patients with breast cancer or osteolytic lesions of multiple myeloma:A phaseⅢ,double-blind,comparative trial[J].Cancer J,2001,7(5):377-387.
[9] Rosen L S,Gordon D,Kaminski M,et al.Long-term efficacy and safety of zoledronic acid compared with pamidronate disodium in the treatment of skeletal complications in patients with advancedmultiple myeloma or breast carcinoma:A randomized,double-blind,multicenter,comparative trial[J].Cancer,2004,100(12):2613-2621.
[10] Fizazi K,Carducci M,Smith M,et al.Denosumab versus zoledronic acid for treatment of bone metastases in men with castrationresistant prostate cancer:a randomised,doubleblind study[J].Lancet,2011,377(9768):813-822.
[11] Henry D,Vadhan-RajS,Hirsh V,et al.Delaying skeletal-related events in a randomized phase 3 study of denosumab versus zoledronic acid in patients with advanced cancer:An analysis of data from patients with solid tumors[J].Supportive Care in Cancer,2014,22(3):679-687.
[12] Jiang Z F,Shao Z M,Zhang Q Y,et al.Efficacy and safety of denosumab from a phaseⅢ,randomized,active-controlled study compared with zoledronic acid in patients of Asian ancestry with bone metastases from solid tumors[J].J Clin Oncol,2016,34(suppl):10116.
[13] Rogervon M,Jean-Jacques B,Blair E,et al.Pain and health-related quality of life in patients with advanced solid tumours and bone metastases:integrated results from three randomized,double-blind studies of denosumab and zoledronic acid[J].Support Care Cancer,2013,21(12):3497-3507.
[14] Charles S C,Jean-Jacques B,Alison S,et al.Pain outcomes in patients with advanced breast cancer and bone metastases results from a randomized,double-blind study of denosumab and zoledronic acid[J].Cancer,2013,119(4):823-828.
[15] Miguel M,Richard B,Hugues B,et al.Bone-related complications and quality of life in advanced denosumab versus zoledronic acid breast cancer:Results from a randomized phaseⅢtrial of denosumab versus zoledronic acid[J].Clin Cancer Res,2012,18(17):4841-4849.
[16]Schulz K F,Ahman D G,Moher D,et al.CONSORT 2010 statement:updated guidelines for reporting parallel group randomized trials[J].Ann Intern Med,2010,152(11):726-732.
[17]Azevedo S,Leao F K,Kimura M,et al.The WHO analgesic ladder for cancer pain control,twenty years of use.How much pain relief does one get from using it?[J].Support Care Cancer,2006,14(11):1086-1093.
[18] Yong M,Jensen A O,Jacobsen J B,et al.Survival in breast cancer patients with bone metastases and skeletal-related events:a population-based cohort study in Denmark(1999-2007)[J].Breast Cancer Res Treat,2011,129(2):495-503.
[19] Coleman R E.Adjuvant bisphosphonates in breast cancer:are we witnessing the emergence of a new therapeutic strategy?[J].Eur J Cancer,2009,45(11):1909-1915.
[20] Fournier P,Boissier S,Filleur S,et al.Bisphosphonates inhibit angiogenesis in vitro and testosterone-stimulated vascular regrowth in the ventral prostate in castrated rats[J].Cancer Res,2002,62(22):6538-6344.
[21] Rogers T L,Holen I.Tumour macrophages as potential targets of bisphosphonates[J].J TranslMed,2011,9:177.
[22] Raikkonen J,Monkkonen H,Auriola S,et al.Mevalonate pathway intermediates downregulate zoledronic aicd-induced isopenteny pyrophosphate and ATP analog formation in human breast cancer cells[J].Biochem Pharmacol,2010,79(5):777-783.
[23] Iranikhah M,Wilborn T W,Wensel T M,et al.Denosumab for the prevention of skeletal-relate eventsin patientswith bone metastasis from solid tumor[J].Pharmaco therapy,2012,32(3):274-284.
[24] Jamal S A,Ljunggren O,Stenham B C,et al.Effects of denosumab on fracture and bone mineral density by level of kidney function[J].J Bone Miner Res,2011,26(8):1829-1835.
[25] Szulc P,Seeman E,Delmas P D.Biochemical measurements of bone turnover in children and adolescents[J].Osteoporosis International,2000,11(4):281-294.
[26] Bayat V,Jaiswal M,Bellen H J.The BMP signaling pathway atthe drosophila neuromuscular junctioin and its links to neurodegenerative disease[J].Current opinion in neurobiology,2011,21(1):182-188.
[27] 王波,楊歡,龐琴霞,等.骨轉移性癌患者血清PINP、BALP檢測的臨床意義[J].中國血液流變學雜志,2010,20(2):256-258.
[28] 佟仲生,王曉蕊,王忱,等.骨膠原代謝指標在乳腺癌骨轉移診斷中的應用[J].中華骨外科雜志,2010,30(5):497-500.
[29] Snedecor S J,Carter J A,Kaura,et al.Costeffectiveness of denosumab versus zoledronic acid in the management of skeletal metastases secondary to breast cancer[J].Clin Ther,2012,34(6):1334-1349.
Efficacy and safety of denosumab versus zoledronic acid in treatment of bone metastasis:a meta-analysis
CHEN Wanjing,WANG
Bei,GAO Xiufei,et al.Department of Mastology,Zhejiang Provincial TCM Hospital,Hangzhou 310006,China
Objective To evaluate the effectiveness and safety of denosumab versus zoledronic acid in treatment of bone metastasis in cancer patients. Methods Clinical studies of denosumab and zoledronic acid in treating bone metastasis were searched from Cochrane Library,PubMed,OVID,Springer Linker,Science Direct,EBSCO and other databases.The quality of literature were evaluated with Cochrane risk of bias assessment tools.The meta-analysis was performed with software Rev Man 5.3. Results Four RCTs reported in 7 papers and involving 6029 patients were included in the meta-analysis.Meta-analysis showed that denosumab was superior to zoledronic acid in delaying the time to skeleton-related events (SREs),decreasing the concentration of bone metastasis markers uNTx/Cr and S-BALP,prolonging the time to radiotherapy,reducing the pain severity and pain interference.The denosumab group had lower incidence rate of anemia,acute phase reactions and renal toxicity.There were no significant differences in overall survival,disease progression,pathologic fractures,surgery to bone,spinal cord compression and incidence rates of nausea,fatigue,back pain,osteonecrosis of the jaw between two groups. Conclusion Denosumab is superior to zoledronic acid in clinical efficacy and safety for treatment of bone metastasis in cancer patients.
Denosumab Zoledronic acid Skeletal-related events Bone metastasis Neoplasms
2017-01-16)
(本文編輯:陳丹)
10.12056/j.issn.1006-2785.2017.39.18.2017-134
310006 杭州,浙江省中醫院乳腺科
王蓓,E-mail:JHWbei@126.com

