鉑類藥物雜質(zhì)及其檢測方法的研究進(jìn)展
還傳靜,李悅,陸靜(中國醫(yī)藥工業(yè)研究總院上海醫(yī)藥工業(yè)研究院/創(chuàng)新藥物與制藥工藝國家重點實驗室,上海200040)
鉑類藥物雜質(zhì)及其檢測方法的研究進(jìn)展
還傳靜*,李悅#,陸靜(中國醫(yī)藥工業(yè)研究總院上海醫(yī)藥工業(yè)研究院/創(chuàng)新藥物與制藥工藝國家重點實驗室,上海200040)
目的:為鉑類藥物的工藝優(yōu)化和質(zhì)量控制提供參考。方法:收集近年國內(nèi)外關(guān)于鉑類藥物雜質(zhì)研究的文獻(xiàn),進(jìn)行歸納、總結(jié)和綜述。結(jié)果與結(jié)論:已經(jīng)上市的鉑類藥物中應(yīng)用最廣泛的是順鉑、卡鉑和奧沙利鉑,《中國藥典》《美國藥典》《歐洲藥典》《日本藥典》中已收載了上述藥物相關(guān)的一些雜質(zhì)檢查項目。鉑類藥物中的雜質(zhì)可分為工藝雜質(zhì)和降解雜質(zhì)兩類,工藝雜質(zhì)可能有其銀鹽、水合物、光學(xué)異構(gòu)體及所對應(yīng)的羧酸等;降解雜質(zhì)是其在光照、酸性條件、氯離子存在時降解或在水溶液中發(fā)生水合反應(yīng)的產(chǎn)物。目前鉑類藥物的雜質(zhì)檢測方法主要有薄層色譜法、高效液相色譜法、電感耦合等離子體發(fā)射光譜法、電感耦合等離子體質(zhì)譜法、流動注射電噴霧質(zhì)譜法等。今后隨著越來越多的全新結(jié)構(gòu)的鉑類藥物問世,采用的雜質(zhì)研究方法可能會有所不同,如何更準(zhǔn)確、快速、高效地檢出鉑類藥物中的雜質(zhì)仍將是該類藥物質(zhì)量控制的一個重要議題。
鉑類藥物;雜質(zhì);檢測;研究
自20世紀(jì)60年代美國科學(xué)家Rosenberg首次觀察到鉑類化合物能抑制腫瘤細(xì)胞生長以來[1],對于該類化合物的研究迅速發(fā)展。鉑類化合物進(jìn)入腫瘤細(xì)胞后可與其DNA結(jié)合,引起DNA復(fù)制障礙,從而起到抗腫瘤的作用。由于鉑類化合物不具有靶向性,在殺傷腫瘤細(xì)胞的同時,正常細(xì)胞也會受到影響,因此該類化合物會產(chǎn)生嚴(yán)重的毒副作用,如神經(jīng)毒性、腎毒性、骨髓抑制、耳毒性等。迄今已有幾十種鉑類化合物被合成[2-7],由于低效、毒性大等原因,大量該類化合物在臨床研究階段被淘汰。已經(jīng)上市的鉑類藥物可分為三代,第一代鉑類藥物為順鉑(Cisplatin),第二代鉑類藥物為卡鉑(Carboplatin)和奈達(dá)鉑(Nedaplatin),第三代鉑類藥物有奧沙利鉑(Oxaliplatin)、洛鉑(Lobaplatin)、米鉑(Miriplatin)和庚鉑(Heptaplatin)等,其中應(yīng)用最廣泛的是順鉑、卡鉑和奧沙利鉑。
近年來,科學(xué)家們正在研究全新結(jié)構(gòu)的鉑類藥物。如英國Novuspharm公司正在進(jìn)行臨床研究的3種多核鉑類配合物順式-雙核鉑配合物(BBR-3610)、反式-雙核鉑配合物(BBR-3611)和反式-三核鉑配合物(BBR-3464)。這種多核鉑類配合物進(jìn)入腫瘤細(xì)胞后,能夠與DNA的多個位點鍵合,從而發(fā)揮更強(qiáng)的抗腫瘤活性,并使腫瘤細(xì)胞難以產(chǎn)生耐藥性。又如德國GPC Biotech AG公司正在研究四價鉑類化合物沙鉑(Satraplatin)。現(xiàn)已上市的鉑類藥物口服給藥均無抗腫瘤作用,而沙鉑被證實口服有效,拓展了新的給藥途徑。
目前已有的鉑類藥物口服生物利用度差,僅有注射劑型,通過注射方式直接進(jìn)入血液循環(huán),無首關(guān)效應(yīng),可提高生物利用度,但與口服給藥相比,藥物中雜質(zhì)引起的安全性問題更為嚴(yán)重。因此,如何快速、準(zhǔn)確、高效檢出鉑類藥物原料藥及注射制劑中的雜質(zhì),對保障該類藥物的用藥安全非常重要。為此,筆者收集近年國內(nèi)外關(guān)于鉑類藥物雜質(zhì)檢測的研究文獻(xiàn),進(jìn)行歸納、總結(jié)和綜述,旨在為鉑類藥物的工藝優(yōu)化和質(zhì)量控制提供參考。
1 鉑類藥物雜質(zhì)檢查的藥典收載情況
目前,《中國藥典》(ChP 2015)、《美國藥典》(USP 39)和《歐洲藥典》(EP 8.0)均收載了順鉑、卡鉑和奧沙利鉑,《日本藥典》(JP 16)收載了順鉑和卡鉑,在我國洛鉑所用標(biāo)準(zhǔn)為國家藥品標(biāo)準(zhǔn)WS-024(X-022)-98。各國藥典對鉑類藥物雜質(zhì)檢查的收載情況如表1所示(各國藥典收載的鉑類藥物原料藥與注射用無菌粉末的雜質(zhì)檢查項相同)。與ChP 2010相比,ChP 2015新增了對奧沙利鉑中奧沙利鉑左旋異構(gòu)體的檢查。另外,各國藥典對相同雜質(zhì)的檢查方法與限量規(guī)定大多相似,有機(jī)雜質(zhì)檢查方法以高效液相色譜法(HPLC)為主,重金屬殘留檢測則采用原子分光光度法和熾灼法。
2 鉑類藥物的雜質(zhì)來源
2.1 工藝雜質(zhì)
工藝雜質(zhì)包括合成過程中引入的起始原料、試劑、中間體、副產(chǎn)物及異構(gòu)體等。第一、第二、第三代鉑類藥物結(jié)構(gòu)類似,合成路徑也相似[8-12],可能的雜質(zhì)來源也類似。除順鉑通過含二氯配體和二鹵素離子配位的鉑類化合物與硝酸鹽反應(yīng)直接制得外,其他鉑類藥物在合成含二氯配體和二鹵素離子配位的鉑類化合物后,通過加入硝酸銀等銀鹽去除鹵素離子獲得鉑配合物中間體,并與相應(yīng)羧酸根反應(yīng)得到最終產(chǎn)物(詳見圖1)。鉑類藥物共有的工藝雜質(zhì)主要有對應(yīng)的銀鹽、水合物以及光學(xué)異構(gòu)體等,且除順鉑外的其他鉑類藥物還可能含有對應(yīng)的羧酸。

表1 各國藥典對鉑類藥物雜質(zhì)檢查的收載情況
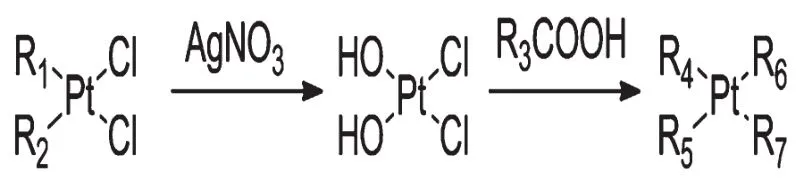
圖1 鉑類藥物的合成路徑
以奧沙利鉑為例,奧沙利鉑的制備主要以反式-(-)-1,2-環(huán)己二胺[trans-(-)-DACH]與四氯鉑酸鉀反應(yīng)生成中間體順式-二氯-(順式-1,2-環(huán)己二胺)合鉑,再與AgNO3反應(yīng),最后加入草酸生成奧沙利鉑。奧沙利鉑工藝雜質(zhì)可能有中間體環(huán)己二胺二水合鉑及其二聚物,副產(chǎn)物雙羥基奧沙利鉑,起始原料草酸也可能殘留在產(chǎn)物中,同時,奧沙利鉑具有手性中心,可能產(chǎn)生光學(xué)異構(gòu)體。
2.2 降解雜質(zhì)
降解產(chǎn)物(降解雜質(zhì))是藥物降解產(chǎn)生的水解、氧化、開環(huán)、聚合等反應(yīng)的產(chǎn)物。USP 39、EP 8.0、JP 16中,對于順鉑的降解產(chǎn)物三氯氨合鉑均規(guī)定了限度,EP 8.0對卡鉑的降解產(chǎn)物順鉑規(guī)定了限度。鉑類藥物除藥典中收載的原料藥和注射用無菌粉末這兩種劑型外,市售劑型還包括加入氯化鈉的注射液,因此在氯離子存在下的降解產(chǎn)物也應(yīng)予以考慮。另外,部分鉑類藥物在水溶液中易發(fā)生水合反應(yīng)[13],光照、酸性條件或氯離子存在時,均可能導(dǎo)致鉑類藥物的降解[14-17]。
3 鉑類藥物的雜質(zhì)檢測方法研究
鉑類藥物中以順鉑、卡鉑、奧沙利鉑臨床上應(yīng)用最為廣泛,故對這3種鉑類藥物的雜質(zhì)研究較為全面深入。
3.1 順鉑
順鉑,又稱順氯氨鉑,是首個被研發(fā)上市的具有抗癌活性的鉑類藥物,抗癌活性強(qiáng),抗瘤譜廣,雖然該藥對神經(jīng)、腎等毒性較嚴(yán)重,目前仍是睪丸癌、卵巢癌的首選用藥。順鉑與培美曲賽、吉西他濱聯(lián)用可治療非小細(xì)胞肺癌[18-21],與紫杉醇聯(lián)用可治療卵巢癌、食道癌、非小細(xì)胞肺癌等[22-24]。
順鉑的雜質(zhì)主要有反式-二氯二氨合鉑(反鉑)、三氯氨合鉑以及順二氨二水合鉑。諶喜珠等[25]以丙酮-水為展開劑,建立了薄層色譜法(TLC)檢測相關(guān)雜質(zhì),水合鉑由于在溶液中轉(zhuǎn)化為順鉑因此無法檢測。Macka M等[26]采用離子交換色譜法分離了不同的鉑類化合物;Ari?z F等[27]改進(jìn)了這一方法,選用4-甲基-2-硫脲嘧啶(MTU)衍生化色譜柱,檢測反鉑與三氯氨合鉑并考察了pH、流動相組成、MTU的濃度與柱溫對分離度的影響,最優(yōu)的條件為:pH 3.7、0.04 mol/L乙酸鈉緩沖液(加入4%甲醇、6 mmol/L硫酸氫四丁銨與4 mmol/L硫氧化鈉)、22倍于鉑濃度的MTU濃度、室溫。Dole?el P等[28]建立了流動注射電噴霧質(zhì)譜法(FI-ESI-MS)檢測順鉑與其異構(gòu)體反鉑,順鉑的特征峰為m/z 304[M-Cl+CH3CN]、602[2M-Cl+CH3CN];由于反鉑的極性更大,并且會異構(gòu)化為順鉑,因此反鉑的特征峰僅有m/z 304[M-Cl+CH3CN]。劉祝東等[29]則采用HPLC法進(jìn)行了順鉑與反鉑、水合鉑、三氯氨合鉑的分離,色譜柱為C18柱(250 mm×4.0 mm,5 μm),流動相為純水,波長為210 nm。Ehrsson HC等[30]在多孔石墨碳(PGC)柱上分離并測定了順鉑及其水合物,流動相為0.001 mol/L氫氧化鈉溶液,并以四級桿質(zhì)量分析器作為檢測器進(jìn)行檢測。順鉑的主要雜質(zhì)信息匯總見表2。

表2 順鉑的主要雜質(zhì)信息匯總
3.2 卡鉑
卡鉑是在順鉑之后上市的第2個鉑類藥物,屬于第二代鉑類藥物,由美國施貴寶公司、英國癌癥研究所及JohnsonMatthey公司合作開發(fā),于1986年首次在英國上市,1988年開始在中國生產(chǎn)。卡鉑的抗癌活性與順鉑類似,但毒副作用明顯低于順鉑,水溶性優(yōu)于順鉑。卡鉑與紫杉醇聯(lián)合用藥可用于非小細(xì)胞肺癌、卵巢癌等的治療[31-33],與多西他賽聯(lián)用可治療非小細(xì)胞肺癌、宮頸癌等[34-36]。
卡鉑已知的雜質(zhì)主要有1,1-環(huán)丁烷二羧酸、順鉑、二水二氨合鉑、二碘二氨合鉑、銀等。諶喜珠等[37]采用TLC法分離卡鉑及其雜質(zhì)二碘二氨合鉑(Ⅱ)與1,1-環(huán)丁烷二羧酸銀,其中二碘二氨合鉑為起始原料,1,1-環(huán)丁烷二羧酸銀為光解產(chǎn)物。試驗采用硅膠G板為吸附劑,苯-丙酮-水(3∶17.5∶4,V/V/V)為展開劑,以碘蒸氣顯色。Vivekanandan K等[38]建立了LC-ESI/MS法檢測卡鉑注射液中的降解產(chǎn)物。色譜柱為YMC-pack ODS-A column(250 mm×4.6 mm,5 μm),流動相為0.02%甲酸水溶液-甲醇(0~10 min:0.02%甲酸水溶液100%;10~11 min:0.02%甲酸水溶液100%→75%),檢測波長為210 nm。除已知降解產(chǎn)物1,1-環(huán)丁烷二羧酸與二水二氨合鉑之外,該試驗檢測出了4個未知雜質(zhì)CP-Ⅰ、CP-Ⅱ、CP-Ⅲ和CP-Ⅳ,并推導(dǎo)出了這4個雜質(zhì)的結(jié)構(gòu)。CP-Ⅲ與CP-Ⅱ的相對分子質(zhì)量相同,可能為CP-Ⅱ螯合環(huán)異構(gòu)化的產(chǎn)物。卡鉑的主要雜質(zhì)信息匯總見表3。

表3 卡鉑的主要雜質(zhì)信息匯總
3.3 奧沙利鉑
奧沙利鉑是第三代鉑類藥物,又被稱為草酸鉑,由法國賽諾菲公司開發(fā),于1996年在法國批準(zhǔn)上市。奧沙利鉑與多種抗腫瘤藥物具有良好的協(xié)同作用,其與5-氟尿嘧啶和亞葉酸的聯(lián)合方案是治療轉(zhuǎn)移性結(jié)直腸癌的一線方案。而臨床研究顯示,雷替曲塞聯(lián)合奧沙利鉑治療轉(zhuǎn)移性結(jié)直腸癌或優(yōu)于奧沙利鉑與5-氟尿嘧啶的聯(lián)合治療方案[39];并且,奧沙利鉑還可與多種抗腫瘤藥物聯(lián)用治療胃癌、肝癌、卵巢癌等[40-42]。
奧沙利鉑已知的雜質(zhì)包括起始原料草酸(雜質(zhì)A)、可能產(chǎn)生的副產(chǎn)物環(huán)己二胺二水合鉑(雜質(zhì)B)及其二聚體(雜質(zhì)E)、雙羥基奧沙利鉑(雜質(zhì)C)以及起始原料環(huán)己二胺中混有的反式-1S,2S-環(huán)己二胺參與反應(yīng)生成的奧沙利鉑左旋異構(gòu)體(雜質(zhì)D)。此外,合成所用硝酸銀溶液可能引入重金屬銀。
李佐鑫等[43]參照EP 6.0,建立HPLC法,對奧沙利鉑的雜質(zhì)A進(jìn)行分離與含量測定。試驗采用CAPCELL PAK C18色譜柱(250 mm×4.6 mm,5 μm),流動相為磷酸緩沖液(40%氫氧化四丁基銨溶液適量,用磷酸調(diào)節(jié)pH至6.00)-乙腈(80∶20,V/V),流速為2 mL/min,柱溫為40℃,檢測波長為205 nm。牛沖等[44]則以HPLC法測定了奧沙利鉑的雜質(zhì)B,色譜柱采用C18柱,流動相為庚烷磺酸鈉溶液-乙腈(83∶17,V/V),流速為1 mL/min,檢測波長為215 nm,柱溫為40℃。由于EP 8.0收載的測定奧沙利鉑中雜質(zhì)D的方法所采用的色譜柱其適宜的溶劑與所用流動相不匹配,對色譜柱損傷較大,且分析速度慢,故劉祝東等[45]采用Chiralcel OD-RH手性色譜柱,流動相改為乙腈-乙醇(60∶40,V/V),提高了色譜柱使用壽命,且分析時間較EP 8.0方法更短;同時,Gallinella B等[46]采用親水作用色譜法對雜質(zhì)D進(jìn)行了分析,色譜柱為Chiralpak IC-3(100 mm×4.6 mm,5 μm),流速為1 mL/min,柱溫為40℃,流動相為乙腈-水(100∶5,V/V),柱效更高的同時也縮短了檢測時間。另外,董微等[47]建立了一種以谷胱甘肽包被的CdTe量子點為探針測定奧沙利鉑中微量的重金屬銀的方法;李光俐等[48]則采用電感耦合等離子體發(fā)射光譜法(ICP-AES)檢測了奧沙利鉑中的銀、鈀、鎘,試驗證明鉑類化合物基體對銀、鈀、鎘的測定無影響。奧沙利鉑的主要雜質(zhì)信息匯總見表4。
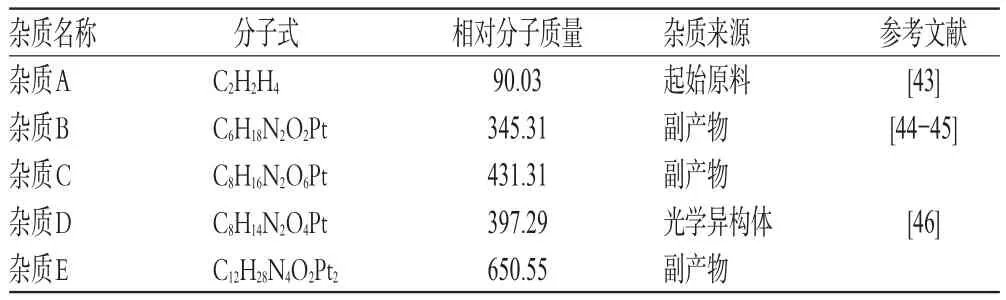
表4 奧沙利鉑的主要雜質(zhì)信息匯總
3.4 其他
除上述3種鉑類藥物外,奈達(dá)鉑、洛鉑、米鉑、庚鉑也被應(yīng)用于腫瘤的治療中,這4種藥物僅在部分地區(qū)上市,對其雜質(zhì)研究的報道相對較少。
奈達(dá)鉑是第二代鉑類藥物,由日本鹽野義制藥公司開發(fā),于1955年在日本批準(zhǔn)上市。奈達(dá)鉑血液學(xué)毒性高于順鉑,而腎毒性和胃腸道副反應(yīng)較順鉑有所降低,可用于治療頭頸部腫瘤、非小細(xì)胞肺癌、食道癌、膀胱癌、睪丸癌、子宮頸癌等[49-50]。奈達(dá)鉑未收錄于各國藥典。畢同香等[51]采用HPLC法初步分離了奈達(dá)鉑原料藥及其有關(guān)物質(zhì),色譜柱為Spherisorb NH2柱,流動相為40 mmol/L磷酸二氫鉀-乙腈(80∶20,V/V),檢測波長為210 nm。賈元超等[52]同樣采用HPLC法測定了注射用奈達(dá)鉑中的有關(guān)物質(zhì),色譜柱為Shimpak CLC-ODS C18柱(150 mm×4.6 mm,5 μm),流動相為甲醇-0.01 mol/L枸櫞酸溶液(三乙胺調(diào)pH至6.0)(30∶70,V/V)。
庚鉑是由韓國SunKyong Industries公司研發(fā)的第三代鉑類藥物,于1999年在韓國上市,可用于治療小細(xì)胞肺癌、胃癌、宮頸癌和結(jié)腸直腸癌。朱思思等[53]采用HPLC法測定了庚鉑中的有關(guān)物質(zhì),色譜柱為ShimPack CLC-ODS柱(150 mm×4.6 mm,5 μm),流動相為甲醇-水(40∶60,V/V),檢測波長為210 nm。楊小明等[54]則采用HPLC法測定了庚鉑中的S-異構(gòu)體,色譜柱為Chirobiotic R手性柱(250 mm×4.6 mm,5 μm),流動相為0.1%三乙胺溶液(乙酸調(diào)pH至6.8)-異丙醇(55∶45,V/V),檢測波長為210 nm,柱溫為30℃。
洛鉑是由德國愛斯達(dá)制藥有限公司開發(fā)的又一個第三代鉑類藥物,海南長安國際制藥有限公司于2002年購買了洛鉑在中國的專利權(quán),國家食品藥品監(jiān)督管理總局于2005年批準(zhǔn)洛鉑作為國家一類新藥上市。洛鉑抗瘤活性強(qiáng),毒副作用較順鉑低,且與順鉑無交叉耐藥性。該藥的質(zhì)量標(biāo)準(zhǔn)WS-024(X-022)-98中采用TLC法檢測洛鉑的兩個雜質(zhì)乳酸和二氨甲基環(huán)丁烷草酸鹽。趙振東等[55]則采用離子色譜法測定了洛鉑中乳酸的含量,色譜柱為Ionpac AS9-HC陰離子分析柱,淋洗液為Na2CO3-NaHCO3,檢測器為抑制性電導(dǎo)檢測器。
米鉑是由日本住友制藥株式會社研發(fā)的另一個第三代鉑類藥物,于2009年在日本上市,用于治療肝癌[56]。王雪微等[57]采用HPLC法測定了米鉑中的2個光學(xué)異構(gòu)體雜質(zhì),采用的色譜柱為Sumichiral OA-2500手性色譜柱(250 mm×4.6 mm,5μm),流動相為正己烷-甲醇(97∶3,V/V),檢測波長為216 nm。
此外,一些研究還對正處于臨床試驗階段的新型鉑類化合物中的雜質(zhì)進(jìn)行了檢測。劉祝東[58]采用HPLC法對沙鉑的原料藥及其雜質(zhì)JM118、JM149進(jìn)行了檢測,色譜柱為ODS柱(150 mm×4.6 mm,5 μm),流動相為乙腈-水(梯度洗脫,20~25∶75~80,V/V),流速為0.8 mL/min,檢測波長為210 nm。Vacchina等[59]則應(yīng)用HPLCICP-MS法檢測了BBR3464中潛在的有關(guān)物質(zhì)BBR3497、BBR3583、BBR3005、IE7-065和IE7-068。
4 結(jié)語
惡性腫瘤作為威脅人類生命的一種主要疾病,是亟待攻克的一大醫(yī)學(xué)難題。鉑類藥物作為一類抗瘤譜廣、作用顯著、臨床應(yīng)用廣泛的抗腫瘤藥物對治療惡性腫瘤非常重要,而其雜質(zhì)研究則直接影響著其使用的安全性。藥典中收錄的鉑類藥物有機(jī)雜質(zhì)檢查方法主要為HPLC法。鉑類藥物的工藝雜質(zhì)和降解雜質(zhì)極性較強(qiáng),因此常采用C18柱與強(qiáng)極性的流動相進(jìn)行洗脫;由于部分雜質(zhì)中含有氨基,也可采用氨基柱進(jìn)行分離;而其光學(xué)異構(gòu)體則多采用手性柱進(jìn)行分離。為了更準(zhǔn)確、快速、有效地檢測鉑類藥物的雜質(zhì),其他的檢測方法如TLC法、離子色譜法、原子吸收分光光度法、ICP-MS法、FI-ESI-MS法等也逐漸得到應(yīng)用。現(xiàn)有研究文獻(xiàn)主要對藥典中已收錄的雜質(zhì)進(jìn)行檢測并優(yōu)化相關(guān)檢測方法。隨著對鉑類藥物研究的深入,越來越多的新的該類藥物正在進(jìn)行臨床試驗或即將上市,而這些藥物部分與已有鉑類藥物結(jié)構(gòu)差異較大,采用的雜質(zhì)研究方法可能會有所不同。如何更準(zhǔn)確、快速、高效地檢出鉑類藥物中的雜質(zhì)今后仍將是該類藥物質(zhì)量控制的一個重要議題。
[1] Rosenberg B,van Camp L,Krigas T.Inhibition of cell division in Escherichia coli by electrolysis products from a platinum electrode[J].Nature,1965,205(4972):698-699.
[2] Cutillas N,Yellol GS,de Haro C,et al.Anticancer cyclometalated complexes of platinum group metals and gold[J].Coordination Chemistry Reviews,2013,257(19):2784-2797.
[3] Xu G,Zhao J,Gou S,et al.Antitumor platinum(Ⅱ)complexes of N-cyclobutyl-1R,2R-diaminocyclohexane with dicarboxylates as leaving groups[J].Bioorganic&Medicinal Chemistry Letters,2015,25(2):221-224.
[4] Quiroga AG.Understanding trans platinum complexes as potential antitumor drugs beyond targeting DNA[J].Journal of Inorganic Biochemistry,2012,114:106-112.
[5] Westendorf AF,Woods JA,Korpis K,et al.Trans,trans,trans-[PtIV(N3)2(OH)2(py)(NH3)]:a light-activated antitumor platinum complex that kills human cancer cells by an apoptosis-independent mechanism[J].Molecular Cancer Therapeutics,2012,11(9):1894-1904.
[6] Wilson JJ,Lippard SJ.Synthetic methods for the preparation of platinum anticancer complexes[J].Chemical Reviews,2013,114(8):4470-4495.
[7] Sharma R,K Rawal R,Malhotra M,et al.Design,synthesis and in-vitro cytotoxicity of novel platinum(Ⅱ)complexes with phthalate as the leaving group[J].Letters in Drug Design&Discovery,2013,10(9):872-878.
[8] 王慶琨,彭娟,普紹平.一種合成抗腫瘤藥物庚鉑的新方法:CN201410389065.X[P].2014-12-17.
[9] 王浦海,高鵬,朱磊,等.一種含銀量極低的奈達(dá)鉑的制備方法:CN201110319271.X[P].2012-04-18.
[10] 李美松.奧沙利鉑的合成研究[J].浙江化工,2011,42(4):4-5.
[11] 王慶琨,普紹平,欒春芳,等.鉑類抗腫瘤藥物米鉑的合成及結(jié)構(gòu)表征[J].中國新藥雜志,2011,20(17):1715-1717.[12]趙小偉,蔡繼蘭,杜有國,等.一種洛鉑的制備方法:CN 201310367025.0[P].2013-12-25.
[13] Daley-Yates PT,McBrien DCH.Cisplatin metabolites in plasma,a study of their pharmacokinetics and importance in the nephrotoxic and antitumour activity of cisplatin[J].Biochemical Pharmacology,1984,33(19):3063-3070.
[14] 劉偉平,闕振寰,楊一昆,等.卡鉑水溶液的光分解產(chǎn)物[J].藥學(xué)學(xué)報,1996,31(1):72-74.
[15] Mukherjee S,Mitra I,Mahata S,et al.Hydrolysis mechanism of anticancer drug lobaplatin in aqueous medium under neutral and acidic conditions:a DFT study[J].Chemical Physics Letters,2016,663:115-122.
[16] Allsopp MA,Sewell GJ,Rowland CG,et al.The degradation of carboplatin in aqueous solutions containing chloride or other selected nucleophiles[J].International Journal of Pharmaceutics,1991,69(3):197-210.
[17] Mehta AM,van den Hoven JM,Rosing H,et al.Stability of oxaliplatin in chloride-containing carrier solutions used in hyperthermic intraperitoneal chemotherapy[J].International Journal of Pharmaceutics,2015,479(1):23-27.
[18] 劉延霞,劉峰.培美曲塞或吉西他濱聯(lián)合順鉑治療晚期NSCLC隨機(jī)對照研究[J].中華腫瘤防治雜志,2013,20(22):1748-1750.
[19] 胡興勝,焦順昌,張樹才,等.培美曲塞及吉西他濱分別聯(lián)合順鉑治療初治晚期非小細(xì)胞肺癌安全性和有效性的隨機(jī)對照研究[J].中國肺癌雜志,2012,15(10):569-575.
[20] 黃文波.培美曲賽聯(lián)合順鉑治療35例老年晚期非小細(xì)胞肺癌的療效觀察[J].中國實用醫(yī)藥,2012,7(2):160-160.[21]曲琳莉,周愛霞,賀文茜.培美曲賽聯(lián)合順鉑一線治療晚期非小細(xì)胞肺癌臨床觀察[J].中國民康醫(yī)學(xué),2011,23(19):2372-2373.
[22] 劉文彬,閆海山,牛紅衛(wèi).紫杉醇聯(lián)合順鉑治療晚期卵巢癌的臨床療效觀察[J].腫瘤藥學(xué),2012,2(3):220-222.
[23] 蘇文智,彭方,陳森福,等.紫杉醇與順鉑聯(lián)合治療晚期食道癌的臨床療效觀察及安全性評估[J].腫瘤藥學(xué),2012,2(2):133-136.
[24] 俞斐,崔冉,朱方,等.白蛋白結(jié)合型紫杉醇聯(lián)合洛鉑與順鉑治療晚期非小細(xì)胞肺癌臨床療效比較[J].藥學(xué)與臨床研究,2014,22(6):536-538.
[25] 諶喜珠,劉偉平,何鍵,等.順鉑注射液有關(guān)物質(zhì)的檢測[J].中國藥事,2003,17(3):173-174.
[26] Macka M,Borak J.Chromatographic behaviour of some platinum(Ⅱ)complexes on octadecylsilica dynamically modified with a mixture of a cationic and an anionic amphiphilic modifier[J].Journal of Chromatography A,1993,641(1):101-113.
[27] Ari?z F,Yalcin G,D?len E.Determination of cisplatin,transplatin and amminetri-chloroplatinate by high performance liquid chromatography in one run using 4-methyl-2-thiouracil as derivatizing agent[J].Chromatographia,1999,49(9/10):562-566.
[28] Dole?el P,Kubáň V.Mass spectrometric study of platinum complexes based on cisplatin[J].Chem Pap,2002,56(4):236-240.
[29] 劉祝東,劉洋,楊一昆,等.順鉑注射液的高效液相色譜分析[J].貴金屬,2001,22(2):32-35.
[30] Ehrsson HC,Wallin IB,Andersson AS,et al.Cisplatin,transplatin,and their hydrated complexes:separation and identification using porous graphitic carbon and electrospray ionization mass spectrometry[J].Analytical Chemistry,1995,67(19):3608-3611.
[31] Sandler A,Gray R,Perry MC,et al.Paclitaxel-carboplatin alone or with bevacizumab for non-small-cell lung cancer[J].New England Journal of Medicine,2006,355(24):2542-2550.
[32] 鄧旭,楊三春.紫杉醇聯(lián)合卡鉑治療晚期非小細(xì)胞肺癌的臨床分析[J].中國腫瘤臨床與康復(fù),2015(3):298-300.
[33] 陳霄紅.紫杉醇聯(lián)合卡鉑治療卵巢癌的臨床研究[J].中國臨床研究,2014,27(3):327-329.
[34] 張雪芳,張純.多西他賽聯(lián)合卡鉑同步放化療治療中晚期宮頸癌的近期療效評估[J].中國醫(yī)療前沿,2013,8(10):61-62.
[35] 檀建平.多西他賽聯(lián)合卡鉑治療老年非小細(xì)胞肺癌的療效與安全性[J].臨床合理用藥雜志,2013,6(14):65-66.
[36] 林深.國產(chǎn)多西他賽聯(lián)合卡鉑治療老年晚期非小細(xì)胞肺癌的療效[J].實用臨床醫(yī)藥雜志,2014,18(16):115-115.
[37] 諶喜珠,楊一昆,熊惠,等.抗癌藥物卡鉑薄層色譜分析方法研究[J].貴金屬,1999,20(2):40-42.
[38] Vivekanandan K,Swamy MG,Prasad S,et al.Identification of degradation products from aqueous carboplatin injection samples by electrospray mass spectrometry[J].International Journal of Pharmaceutics,2006,313(1):214-221.
[39] 王佳蕾,李進(jìn),秦叔逵,等.雷替曲塞或氟尿嘧啶/亞葉酸鈣聯(lián)合奧沙利鉑治療局部晚期或復(fù)發(fā)轉(zhuǎn)移性結(jié)直腸癌的隨機(jī)對照多中心Ⅲ期臨床試驗[J].臨床腫瘤學(xué)雜志,2012,17(1):6-11.
[40] 吳福道,張小靜,蔡輝,等.替吉奧聯(lián)合奧沙利鉑治療晚期胃癌的臨床療效觀察[J].重慶醫(yī)學(xué),2015,44(13):1835-1837.
[41] 陳敬華,申維璽,夏俊賢,等.多西他賽聯(lián)合奧沙利鉑和替吉奧與DCF方案一線治療晚期胃癌的對比研究[J].中華腫瘤防治雜志,2015,22(2):134-137.
[42] 彭小波,顏芳,王斌,等.多西他賽、奧沙利鉑聯(lián)合替吉奧(DOS)與奧沙利鉑聯(lián)合替吉奧(SOX)治療晚期胃癌的臨床觀察[J].現(xiàn)代腫瘤醫(yī)學(xué),2015,23(1):88-91.
[43] 李佐鑫,廖聲華,劉冰潔,等.奧沙利鉑原料藥中雜質(zhì)草酸測定的條件摸索和檢測[J].海峽藥學(xué),2013,25(4):34-36.
[44] 牛沖,李軍,李濤,等.HPLC法測定奧沙利鉑雜質(zhì)B的研究[J].中國藥品標(biāo)準(zhǔn),2012,13(4):255-258.
[45] 劉祝東,欒春芳,普紹平.奧沙利鉑及其手性異構(gòu)體的高效液相色譜分析[J].貴金屬,2007,28(2):49.
[46] Gallinella B,Bucciarelli L,Zanitti L,et al.Direct separation of the enantiomers of oxaliplatin on a cellulose-based chiral stationary phase in hydrophilic interaction liquid chromatography mode[J].Journal of Chromatography A,2014,1339:210-213.
[47] 董薇,徐淑坤,王瑩.CdTe量子點熒光猝滅法測定奧沙利鉑中微量銀[J].分析試驗室,2012,32(9):5-8.
[48] 李光俐,徐光,何姣,等.ICP-AES法測定抗癌藥物奧沙利鉑中微量銀、鈀、鎘[J].貴金屬,2009,30(3):34-35.
[49] 莫娟梅,崔建東,張羽,等.奈達(dá)鉑在惡性腫瘤中的應(yīng)用[J].實用臨床醫(yī)藥雜志,2013,17(9):162-165.
[50] 魯云,張偉京.奈達(dá)鉑治療惡性腫瘤研究進(jìn)展[J].中國醫(yī)院用藥評價與分析,2012,12(1):93-96.
[51] 畢同香,劉明潔,薛克亮,等.奈達(dá)鉑的HPLC測定[J].中國醫(yī)藥工業(yè)雜志,2000,31(10):457-458.
[52] 賈元超,伏世建.注射用奈達(dá)鉑的制備及質(zhì)量研究[J].中國藥事,2014,28(8):875-879.
[53] 朱思思,王長斌.HPLC法測定庚鉑的含量及有關(guān)物質(zhì)[J].西北藥學(xué)雜志,2009,24(6):443-445.
[54] 楊小明,趙冬梅,劉欽偉,等.HPLC法測定庚鉑中S-異構(gòu)體含量[J].藥學(xué)進(jìn)展,2010,34(2):85-88.
[55] 趙振東,吳璐陽,謝艷麗,等.離子色譜用于洛鉑中乳酸定值的方法研究[J].化學(xué)分析計量,2009,18(3):56-58.
[56] Okusaka T,Kasugai H,Ishii H,et al.A randomized phase II trial of intra-arterial chemotherapy using SM-11355(Miriplatin)for hepatocellular carcinoma[J].Investigational New Drugs,2012,30(5):2015-2025.
[57] 王雪微,井麗麗,李泉妙,等.米鉑原料中光學(xué)異構(gòu)體雜質(zhì)研究[J].中國新藥雜志,2015,24(2):231-234.
[58] 劉祝東.新型口服四價鉑族抗癌藥賽特鉑原料藥及其雜質(zhì)的高效液相色譜測定[J].貴金屬,2007,28(S1):62-65.
[59] Vacchina V,Torti L,Allievi C,et al.Sensitive speciesspecific monitoring of a new triplatinum anti-cancer drug and its potential related compounds in spiked human plasma by cation-exchange HPLC-ICP-MS[J].Journal of Analytical Atomic Spectrometry,2003,18(8):884-890.
R917
A
1001-0408(2017)30-4315-06
DOI10.6039/j.issn.1001-0408.2017.30.38
*碩士研究生。研究方向:藥物分析。E-mail:huanchuanjing@gmail.com
#通信作者:研究員。研究方向:藥物分析。E-mail:liy ue13204109@163.com
2016-12-28
2017-09-11)
(編輯:周箐)

