高效液相色譜-原子熒光光譜聯用法測定牛肝菌中無機汞、甲基汞、乙基汞的不確定度評估
毛永楊,楊 桐,蘇 濤,李智高,田金蘭
高效液相色譜-原子熒光光譜聯用法測定牛肝菌中無機汞、甲基汞、乙基汞的不確定度評估
毛永楊1,楊 桐2,蘇 濤1,李智高1,田金蘭1
(1.大理州食品檢驗檢測院,云南 大理 671000;2.大理市洱海保護管理局,云南 大理 671000)
采用高效液相色譜-原子熒光聯用法測定牛肝菌中無機汞、甲基汞、乙基汞,通過建立評估的數學模型,分析不確定度的主要來源,計算出不確定度的各主要分量,得出合成不確定度和擴展不確定度。結果表明:影響結果不確定度的主要因素是濃度因素、儀器、樣品不均勻性及回收率,其中濃度因素主要受標準曲線擬合的影響。該評估系統可為今后采用高效液相色譜-原子熒光聯用法測定食用菌中無機汞、甲基汞、乙基汞的不確定度評估提供參考。
高效液相色譜-原子熒光聯用法;汞形態;不確定度;牛肝菌
汞及其化合物廣泛存在于自然界中,汞的毒性與其存在的形態密切相關,有機汞的毒性大于無機汞,在有機汞中甲基汞的毒性最大。無機汞在生物體烷基化的作用下可生成甲基汞、乙基汞等有害物質,汞及其化合物被動植物吸收后通過食物鏈的富集作用進入人體,其富集倍數可達106~107[1-3]。牛肝菌對土壤及生長環境中的汞具有較強的生物富集作用[4],因此分析牛肝菌中不同形態汞的含量對避免人體因食用含高毒性有機汞造成汞中毒具有重要的意義[5]。目前在新修訂的食品安全國家標準GB 5009.17—2014《食品中總汞及有機汞的測定》[6]中增加了甲基汞的測定方法(高效液相色譜-原子熒光聯用法),但標準中所規定的樣品前處理方法主要是針對有甲基汞限值規定的魚類產品且該方法未涉及乙基汞的測定方法,因此本研究有針對性的建立了適用于食用菌基質,且能同時測定無機汞、甲基汞、乙基汞含量的快速檢測方法。由于該方法為非國家標準檢測方法,為確保檢測結果的準確性、可比性及符合測量結果的表達、質量評定、方法確認、量值溯源[7-8]等方面的要求,對該方法進行不確定度評估具有重要的應用價值。本實驗依據JJF 1059.1—2012《測量不確定度評定與表示》[9]以及CNAS-GL06《化學分析中不確定度的評估指南》[10]規定的程序和方法,對高效液相色譜-原子熒光聯用法測定牛肝菌中的無機汞、甲基汞、乙基汞的實驗方法進行不確定度評估,分析不確定度的主要來源,找出影響檢測結果的主要因素,為評估檢測結果的科學性和檢測結果的質量水平提供可靠的理論依據。
1 材料與方法
1.1 材料與試劑
牛肝菌 市售;乙腈、乙酸銨為色譜純;氯化鉀、硝酸、硼氫化鉀、氫氧化鉀、鹽酸均為優級純;其他試劑均為分析純;無機汞(Hg2+)標準溶液(100 μg/mL±0.8%)、甲基汞(CH3Hg+)標準溶液(76.6 μg/g±2.9 μg/g)、乙基汞(C2H5Hg+)標準溶液(75.3 μg/g±2.8 μg/g) 國家標準物質中心。
1.2 儀器與設備
1260高效液相色譜儀 美國Agilent公司;9780原子熒光光譜 北京海光公司;Milli-Q超純水處理系統(出水電阻率18.2 MΩ·cm) 美國Milli-pore公司;渦旋振蕩器 美國Thermo公司;高速臺式冷凍離心機 德國Eppendorf公司;AB-204s電子天平 瑞士Mettler Toledo公司。
1.3 方法
1.3.1 樣品前處理
準確稱取試樣0.25 g(精確到0.000 1 g)于15 mL離心管中,加入3.0 mL的1.5% KCl-1.0%硫脲與鹽酸的混合提取劑充分混合,置于2 500 r/min的渦旋混合器上振蕩提取10 min,4 ℃、9 000 r/min離心10 min,取出上清液,再向離心管中加入3.0 mL混合提取劑重復提取1 次;合并2 次提取液,加入0.8 mL的氨水,用純水定容至10 mL,用0.22 μm的濾膜過濾后分析測定,同時做空白對照。
1.3.2 標準溶液的配制
1.3.2.1 單標儲備液的配制
分別準確稱取甲基汞標準溶液130.55 mg、乙基汞標準溶液132.80 mg,用純水定容至10 mL配制成質量濃度為1 000 μg/L的標準儲備液;用20~200 μL移液器準確吸取100 μL的無機汞標準溶液,用純水定容至10 mL配制成質量濃度為1 000 μg/L的無機汞標準儲備液,4 ℃避光保存。
1.3.2.2 混合標準液的配制
分別用1 mL的單標線吸量管各吸取1 mL的無機汞、甲基汞、乙基汞的標準儲備液于10 mL容量瓶中,用純水定容至刻度,配制成質量濃度為100 μg/L的混合標準溶液;再分別使用100~1 000 μL移液器吸取混合標準溶液500 μL、1 mL的單標線吸量管吸取混合標準溶液1 mL、2 mL的單標線吸量管吸取混合標準溶液2 mL、500~5 000 μL的移液器吸取混合標準溶液4 000 μL、5 mL的單標線吸量管吸取混合標準溶液5 mL于不同的10 mL容量瓶中,用純水定容至刻度,配制成質量濃度分別為5、10、20、40、50 μg/L的混合標準工作液。
1.3.3 儀器條件
1.3.3.1 高效液相色譜工作條件
色譜柱:C18反相色譜分離柱(250 mm×4.6 mm,5 μm);流動相:5.0%乙腈-0.46%乙酸銨-0.10% L-半胱氨酸;進樣體積:100 μL;流速:1.0 mL/min。
1.3.3.2 原子熒光檢測條件
載流:7% HCl溶液;氧化劑:1.0% K2S2O8+0.5% KOH;還原劑:2.0% KBH4+0.5% KOH;紫外消解儀:開;負高壓:300 V;原子化器高度:10 mm;燈電流:30 mA;載氣流量:400 mL/min;屏蔽氣流量:900 mL/min;泵轉速:80 r/min。
1.3.4 數學模型的確立與不確定度的分析
1.3.4.1 數學模型
根據測量的原理建立測量值的數學模型,進行不確定度來源的分析。本實驗中汞形態分析的數學模型如下:
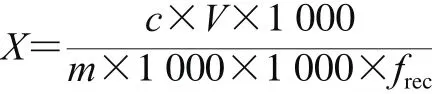
式中:X為試樣中某組分的含量/(mg/kg);c為由標準曲線得到的試樣中某組分的質量濃度/(μg/L);V為試樣溶液的體積/mL;m為試樣質量/g;frec為樣品加標回收率/%。
1.3.4.2 不確定度分量的主要來源[11-17]
根據測量過程,該方法測定牛肝菌中無機汞、甲基汞、乙基汞不確定度的來源主要包括:標準品引入的不確定度、標準溶液的配制過程、標準工作曲線的擬合及樣品前處理引入的不確定度等。
2 結果與分析
2.1 質量濃度引入的不確定度u(C)[18-21]
由質量濃度因素引入的標準不確定度,主要包括標準品濃度引入的不確定度、標準品稱量和移取過程中引入的不確定度、標準溶液稀釋過程中玻璃量器和移液器引入的不確定度、溫度變動引入的不確定度、擬合標準曲線引入的不確定度。
2.1.1 標準品濃度引入的不確定度u1(C)
本實驗所采用的標準品均購自國家標準物質中心,根據其所提供的標準物質證書,無機汞、甲基汞、乙基汞的擴展不確定度分別為:u(Cs(Hg2+))=±0.8%、u(Cs(CH3Hg+))=±2.9 μg/g、u(Cs(C2H5Hg+))=±2.8 μg/g;按B類評定取矩形分布,由標準品引入的相對不確定度分別為:
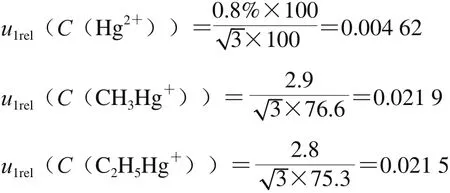
2.1.2 標準品稱量和移取過程中引入的不確定度u2(m)
實驗中分別稱取甲基汞標準溶液130.55 mg、乙基汞標準溶液132.80 mg;用200 μL的移液器準確吸取100 μL的無機汞標準溶液;根據鑒定證書天平的最大允許誤差為±0.05 mg,200 μL移液器的最大誤差為±1.5%,按照矩形分布計算由稱量標準品引入的相對不確定度分別為:
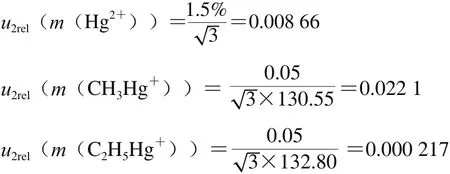
2.1.3 標準溶液稀釋過程中玻璃量器和移液器引入的不確定度u3(V)
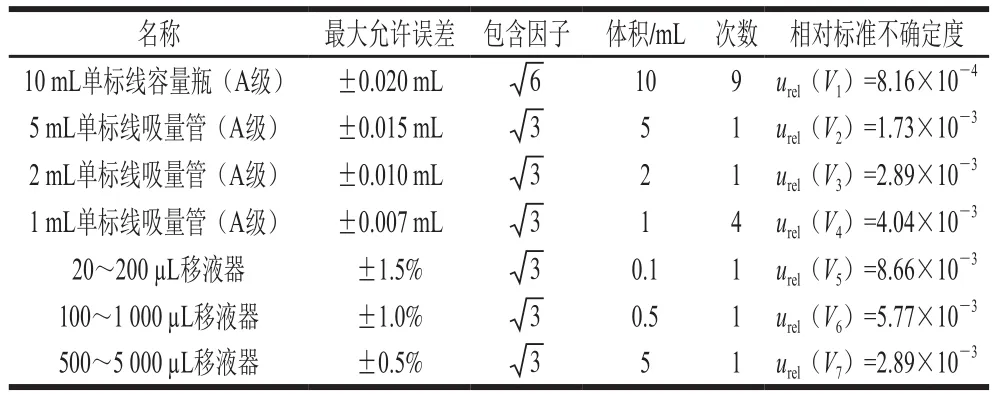
表1 標準溶液配制過程中玻璃量器和移液器引入的不確定度Table 1 Uncertainty resulting from the preparation of standard solution by volumetric flasks and pipettes
標準溶液的配制過程中所用的玻璃量器和移液器的最大允許誤差,按照JJG 196—2006《常用玻璃量器檢定規程》[22]和JJG 646—2006《移液器檢定規程》[23]的要求確定。各玻璃量器和移液器的不確定度按B類不確定度評定,其中吸量管和移液器取矩形分布,容量瓶按三角分布計算[9],結果見表1。根據表1中的數據合成標準溶液稀釋過程中玻璃量器與移液器引入的相對標準不確定度為:
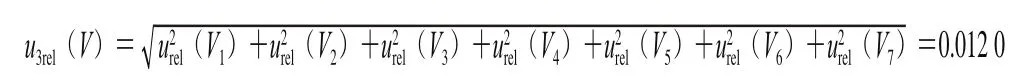
2.1.4 標準溶液稀釋過程中溫度引入的不確定度u4(T)
標準溶液在稀釋過程中的溶劑為純水,各量具均在20 ℃的條件下進行檢定,標準溶液配制室的溫度控制在(20±5) ℃的范圍內;由于玻璃量器的膨脹系數遠小于液體的膨脹系數,可忽略不計,水在20 ℃的膨脹系數為2.1×10-4℃-1,取溫度變化為均勻分布,據此計算的溫度變化引入的不確定度見表2。
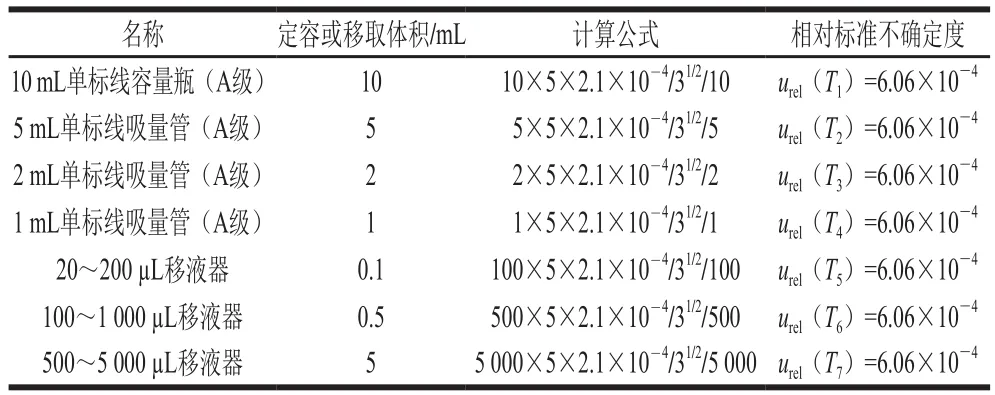
表2 標準溶液配制過程中溫度變化引入的不確定度Table 2 Uncertainty resulting from the preparation of standard solution by temperature variation
根據表2中的數據標準溶液在配制過程中由溫度變化引入的相對標準不確定度為:
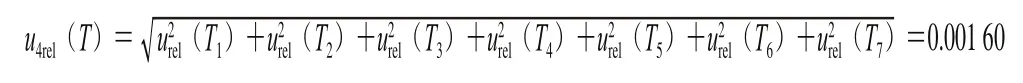
2.1.5 最小二乘法擬合標準曲線的不確定度u5(C?)
通過對質量濃度分別為5、10、20、40、50 μg/L的無機汞、甲基汞、乙基汞的混合標準工作液進行測定,每個校準點測定2 次,采用最小二乘法擬合標準溶液的質量濃度與峰面積曲線,各數據結果詳見表3;同時對一組陽性樣品在擬合標準曲線的狀態下進行兩次重復測定,根據如下公式對標準曲線擬合引入的不確定度進行計算:
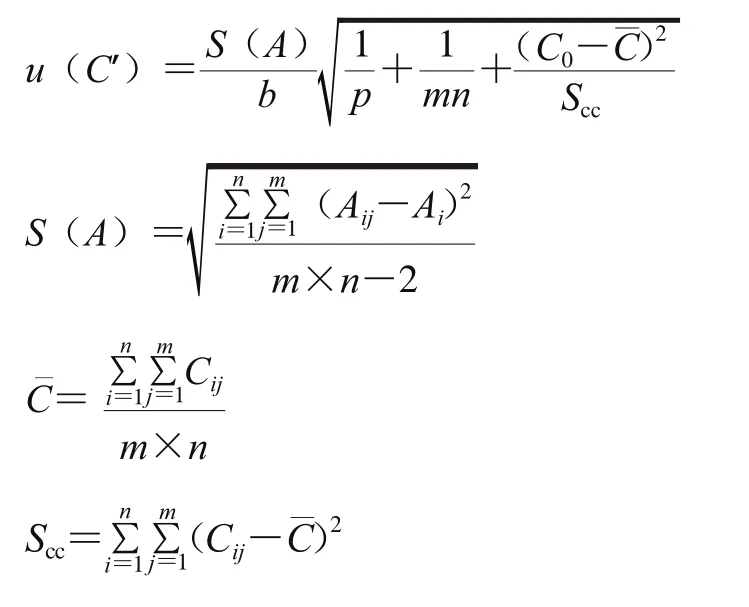
式中:b為校準曲線斜率;C0為陽性樣品測定質量濃度的平均值;p為測試樣品的次數;m為標準工作液的測定次數;n為標準溶液校準點的總數;為標準溶液各校準點Cij的質量濃度平均值;Aij為各質量濃度點測定的峰面積;Ai為由校準方程計算得到的各質量濃度點的峰面積;Cij為標準溶液各校準點的濃度。對陽性樣品進行2次測定,其含量分別為:C0(Hg2+)=21.64 μg/L、C0(CH3Hg+)=10.12 μg/L、C0(C2H5Hg+)=15.17 μg/L。根據表3中的數據計算得到:Scc=3 000;由以上數據計算出標準曲線擬合的相對不確定度分別為:
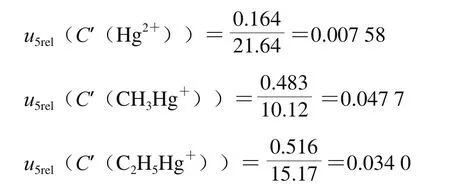
在樣品的測定過程中由濃度引入的相對合成不確定度按如下公式計算:
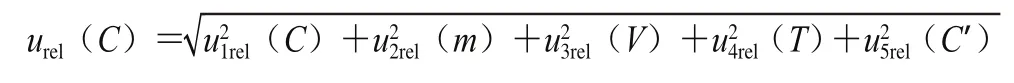
分別計算出urel(C(Hg2+))= 0.017 3;urel(C(CH3Hg+))=0.053 9;urel(C(C2H5Hg+))=0.042 0。

表3 校準曲線擬合數據及不確定度Table 3 Data for fitting calibration curve and uncertainty
2.2 樣品前處理引入的不確定度[24-29]
2.2.1 試樣質量稱量引入的不確定度u(W)
在實驗中稱取0.25 g(精確到0.000 1 g)的試樣,根據鑒定證書天平最大允許誤差為±0.05 mg,按B類評定取矩形分布,由試樣稱量引入的相對不確定度為:
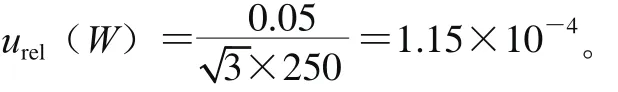
2.2.2 試樣定容引入的不確定度u(V?)
試樣處理完成后采用10 mL的容量瓶進行定容,溫度變化范圍為(20±5)℃,其中10 mL A級單標線容量瓶的最大允許誤差為±0.020 mL,由容量瓶和溫度變化引入的不確定度分別如下:
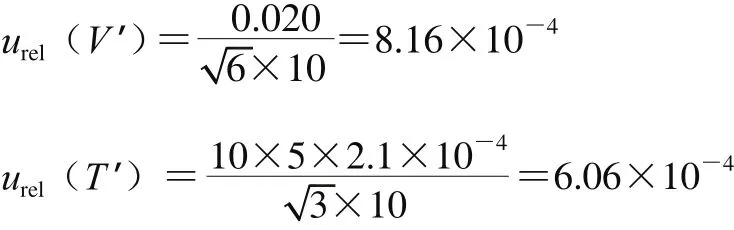
由試樣定容過程引入的相對標準不確定度為:
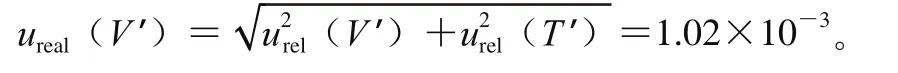
2.2.3 由樣品不均勻性引入的不確定度u(f)
由于處于不同生長時期和處于同一生長時期的牛肝菌中不同組織部位對無機汞、甲基汞和乙基汞的富集作用及烷基化的能力差異較大[5],因此在不確定度評定中應包含由樣品非均勻引入的不確定度分量。在本實驗中通過充分混勻樣品、加大樣品的制樣量,經過科學的取樣和縮分及平行實驗來保障試樣的均勻性和檢測結果的代表性。實驗對同一陽性樣品進行了7 組獨立試樣的平行實驗結果見表4,同時按A類評定對其不確定度進行計算,計算公式如下:

根據此公式分別計算得到由樣品非均勻性引入的相對標準不確定度為:urel(f(Hg2+))=0.016 7;urel(f(CH3Hg+))=0.029 3;urel(f(C2H5Hg+))=0.018 4。
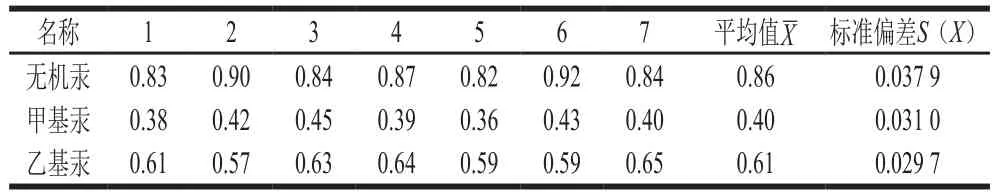
表4 樣品中無機汞、甲基汞、乙基汞的測定結果Table 4 Determination results of inorganic mercury, methyl mercury and ethyl mercury in the samplemg/kg
2.2.4 提取效率引入的不確定度
在空白試樣中添加7 組不同的混合標準溶液,考察回收率對不確定度的影響,按A類進行評定,由回收率引入的相對不確定度根據如下公式計算:;同時對回收率進行顯著性檢驗,計算公式為:,結果見表5;查t檢驗臨界值分布表(f = n-1=6)得雙側臨界值t(0.05,6)為2.447。在本實驗中t值均大于t(0.05,6),故實驗中所得到的回收率與100%具有顯著差異,因此必須在計算結果的公式中采用回收率因子R對結果進行修正。
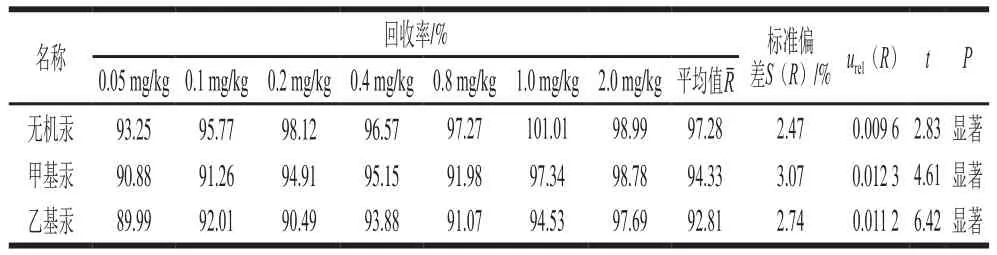
表5 無機汞、甲基汞、乙基汞的回收率和不確定度Table 5 Recoveries and uncertainties of inorganic mercury, methyl mercury and ethyl mercury
在樣品前處理過程中各分量引入的相對標準不確定度按如下公式計算:
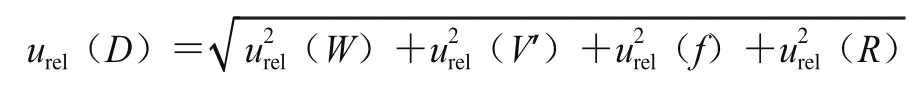
根據此公式分別計算得到由樣品前處理過程中引入的相對標準不確定度為:urel(D(Hg2+))=0.019 3;urel(D(CH3Hg+))=0.031 8;urel(D(C2H5Hg+))=0.021 6。
2.3 高效液相色譜-原子熒光分析系統引入的不確定度u(E)
根據檢定證書高效液相色譜-原子熒光分析系統的擴展不確定度u=5%,k=2,因此由分析儀器引入的不確定度為:
2.4 合成不確定度及擴展不確定度
2.4.1 合成標準不確定度
各不確定分量相互獨立,相對合成標準不確定度計算公式為:
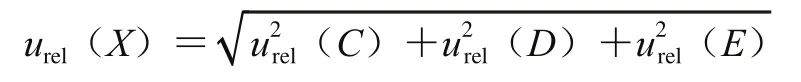
由此公式分別計算得到無機汞、甲基汞、乙基汞的相對合成標準不確定度為:urel((Hg2+))=0.036 0;urel(X(CH3Hg+))=0.067 4;urel(X(C2H5Hg+))=0.053 4;根據合成標準不確定度的計算公式uC(X)=urel(X)×,其中為表4中陽性樣品經測定后按1.3.4.1節中的公式計算結果的平均值,分別計算得到無機汞、甲基汞、乙基汞的合成標準不確定度為:uC((Hg2+))=0.031 8;uC(X(CH3Hg+))=0.028 6;uC(X(C2H5Hg+))=0.035 1。
2.4.2 擴展不確定度
依據JJF 1135—2005《化學分析測量不確定度評定》[30],在95%的置信水平下,取包含因子k=2,擴展不確定度U=k×uC(X),據此得到的高效液相色譜-原子熒光聯用法測定牛肝菌中的無機汞、甲基汞、乙基汞含量的結果見表6。
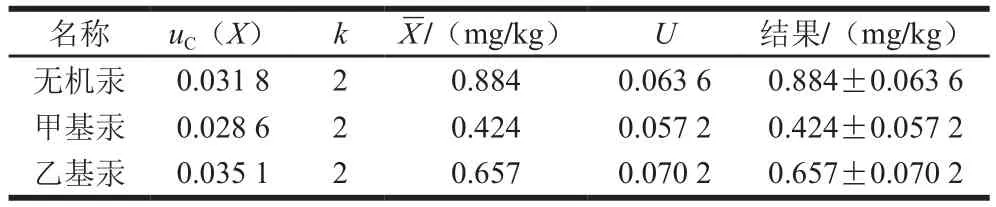
表6 不確定度評定結果Table 6 Uncertainty evaluation for the determination of inorganic mercury, methyl mercury and ethyl mercury
3 結 論
通過對牛肝菌中無機汞、甲基汞、乙基汞的測定過程中各分量因素引入的不確定度進行評定,結果表明:在無機汞的測定過程中對不確定度貢獻最大的因素依次為儀器、濃度因素、樣品不均勻性和樣品提取效率,其中在濃度因素中主要受到標準曲線的擬合及體積因素的影響。在甲基汞和乙基汞的測定過程中不確定度的主要來源為:濃度因素、儀器、樣品不均勻性以及樣品提取效率引入的不確定度;其中在濃度因素中主要受到標準曲線的擬合及標準品純度的影響。因此,在今后的實際檢測過程中,通過保持儀器較高的靈敏度并按時進行檢定、選擇高純度的標準品、科學制樣與縮分、選擇高精密度的量器、提高檢驗人員的熟練水平和操作的規范性等方法減小測量數據的不確定度,保障檢測結果的準確性從而提高檢測質量。
[1] ULLRICH S M, TANTON T W, ABDRASHITOVA S W. Mercury in the aquatic environment∶ a review of factors affecting methylation[J].Critical Reviews in Environmental Science and Technology, 2001,1(3)∶ 241-293. DOI∶10.1080/20016491089226.
[2] 陳邵鵬, 顧海東, 秦宏兵. 高效液相色譜-氫化物發生-原子熒光光譜聯用技術測定水中的烷基汞[J]. 中國環境監測, 2012, 28(5): 79-82.
[3] BENDER M, LYMBERIDI-STTIMO E, RD G. New mercury treaty exposes health risks[J]. Journal of Public Health Policy, 2014, 35(1):1-13. DOI:10.1057/jphp.2013.39.
[4] 楊天偉, 張霽, FALANDYSZ J, 等. 云南常見牛肝菌屬真菌中汞含量及食用安全評價[J]. 生態學雜志, 2015, 34(12): 3518-3525.DOI:10.13292/j.1000-4890.2015.0330.
[5] 毛永楊, 舒平, 趙浩軍, 等. 高效液相色譜-原子熒光聯用測定食用菌中無機汞、甲基汞、乙基汞[J]. 云南大學學報(自然科學版), 2016,38(3): 471-476. DOI:10.7540/j.ynu.20150697.
[6] 國家衛生和計劃生育委員會. 食品中總汞及有機汞的測定: GB 5009.17—2014[S]. 北京: 中國標準出版社, 2014.
[7] 馮歆軼, 蘆智遠, 吳正昌, 等. ICP-AES法測定復合蛋白飲料中鈉含量的不確定度評定[J]. 糧食與食品工業, 2015, 22(1): 93-96.DOI:10.3969/j.issn.1672-5026.2015.01.027.
[8] 霍曉敏. 氣相色譜法對干海參中的六六六滴滴涕測量結果不確定度的評定[J]. 食品科學, 2013, 34(8): 224-248. DOI:10.7506/spkx1002-6630-201308053.
[9] 國家質量監督檢驗檢疫總局. 測量不確定度評定與表示: JJF 1059.1—2012[S]. 北京: 中國計量出版社, 2012.
[10] 中國合格評定國家認可委員會. 化學分析中不確定度的評估指南:CNAS-GL06:2006[S]. 北京: 中國標準出版社, 2006.
[11] 王靜, 顧文龍, 端禮欽. 禽肉中總汞測定的不確定度評定[J].安徽農業科學, 2015, 43(32): 186-187. DOI:10.3969/j.issn.0517-6611.2015.32.063.
[12] 興麗, 王梅, 趙鳳敏, 等. ICP-MS兩種模式下測定亞麻籽中微量元素及其不確定度評定[J]. 光譜學與光譜分析, 2014, 34(1): 226-230.DOI:10.3964/j.issn.1000-0593(2014)01-0226-05.
[13] 張建輝, 張繼紅, 張麗, 等. ICP-MS法和石墨爐原子吸收法測定大米中鎘含量不確定度評估的比較[J]. 食品科學, 2016, 37(18): 185-188.DOI:10.7506/spkx1002-6630-201618030.
[14] 孫玲玲, 宋金明, 于穎, 等. 微波消解-電感耦合等離子體發射光譜法測定牡蠣中鋅的不確定度評定[J]. 食品科學, 2016, 37(16): 187-192.DOI:10.7506/spkx1002-6630-201616030.
[15] BANERJEE K, OULKAR D P, DASGUPTA S, et al. Validation and uncertainty analysis of a multi-residue method for pesticides in grapes using ethyl acetate extraction and liquid chromatography-tandem mass spectrometry[J]. Journal of Chromatography A, 2007, 1173(2): 98-109.DOI:10.1016/j.chroma.2007.10.013.
[16] HASEGAWA H, SHINOHARA Y, HASHIMOTO T, et al. Prediction of measurement uncertainty in isotope dilution gas chromatography/mass spectrometry[J]. Journal of Chromatography A, 2006, 11363(2):226-230. DOI:10.1016/j.chroma.2006.09.073.
[17] 趙一霖, 李姍, 何霜, 等. 電感耦合等離子體質譜法測定水產品中16 種元素的不確定度評定[J]. 食品安全質量檢測學報, 2016, 7(10):4156-4162.
[18] 許光, 楊波, 李愛李, 等. ICP-AES測定大豆中錳、鐵、鋅含量的不確定度評價[J]. 食品研究與開發, 2013, 34(9): 69-72. DOI:10.3969/j.issn.1005-6521.2013.09.019.
[19] 高端峰, 高孟朝, 凌睿, 等. ICP-MS測定淀粉鋁含量的不確定度評定及改進方法[J]. 光譜學與光譜分析, 2016, 36(4): 1211-1216.DOI:10.3964/j.issn.1000-0593(2016)04-1211-06.
[20] 陸美斌, 李為喜, 李靜梅, 等. 電感耦合等離子體質譜法測定谷物中砷和鎘的不確定度評定[J]. 中國食品學報, 2014, 14(5): 180-185.
[21] 徐幸, 張曉鳴, 舒平, 等. 超高效液相色譜-穩定性同位素稀釋質譜法測定米線中烏洛托品的不確定度評估[J]. 食品科學, 2015, 36(16):246-250. DOI:10.7506/spkx1002-6630-201516047.
[22] 國家質量監督檢驗檢疫總局. 常用玻璃量器檢定規程: JJG 196—2006[S]. 北京: 中國計量出版社, 2006.
[23] 國家質量監督檢驗檢疫總局. 移液器檢定規程: JJG 646—2006[S].北京: 中國計量出版社, 2006.
[24] WALORCZYK S. Validation and use of a QuEChRS-based gas chromatography-tandem mass spectrometric method for multiresidue pesticide analysis in blackcurrants including studies of matrix effects and estimation of measurement uncertainty[J]. Talanta, 2014, 120:106-113. DOI:10.1016/j.talanta.2013.11.087.
[25] JIMéNEZ J J. Determination of aminopolycarboxylic acids in river water by solid-phase extraction on activated charcoal cartridges and gas chromatography with mass spectrometric detection. Method performance characteristics and estimation of the uncertainty[J].Analytica Chimica Acta, 2013, 770: 94-102. DOI:10.1016/j.aca.2013.01.060.
[26] 楊波, 段鳳敏, 保志娟, 等. 微波消解-原子熒光光譜法測定煙草中汞的不確定度分析[J]. 計量與測試技術, 2016, 43(3): 90-92.DOI:10.15988/j.cnki.1004-6941.2016.03.042.
[27] 樊繼鵬, 汪洋, 魏曉培, 等. ICP-MS法測定飲用水中鉛砷鎘的不確定度評定的研究[J]. 包裝與食品機械, 2016, 34(3): 70-72.DOI:10.3969/j.issn.1005-1295.2016.03.016.
[28] 杜德賢, 林曉君. ICP-MS法測定白酒中鉛及其不確定度[J]. 食品與發酵科技, 2016, 52(3): 77-80. DOI:10.3969/j.issn.1674-506X.2016.03-018.
[29] 舒平, 楊衛花, 徐幸. 氣相色譜法-三重四級桿質譜聯用法測定核桃油中酚類抗氧化劑的不確定度評估[J]. 食品科學, 2016, 37(6): 194-198. DOI:10.7506/spkx1002-6630-201606035.
[30] 國家質量監督檢驗檢疫總局. 化學分析測量不確定度評定: JJF 1135—2005[S]. 北京: 中國計量出版社, 2005.
Uncertainty Evaluation of for Determining Inorganic Mercury, Methyl Mercury and Ethyl Mercury in Boletus by High Performance Liquid Chromatography Combined with Atomic Fluorescence Spectrometry
MAO Yongyang1, YANG Tong2, SU Tao1, LI Zhigao1, TIAN Jinlan1
(1. Food Inspection and Testing Institute of Dali, Dali 671000, China;2. Erhai Lake Conservation and Management Bureau of Dali, Dali 671000, China)
In this study, we identified the main sources of uncertainty by mathematical modeling and calculated the main uncertainty components and combined and expanded uncertainties for the determination of inorganic mercury, methyl mercury and ethyl mercury in Boletus by high performance liquid chromatography combined with atomic fluorescence spectrometry (HPLC-AFS). The results showed that the major factors of uncertainty were concentration, instrumental measurement, sample heterogeneity, and recovery. Moreover, the curve fitting was the major factor causing the uncertainty for concentration. This study may provide a guideline for uncertainty evaluation for determining inorganic mercury, methyl mercury and ethyl mercury in edible fungus by HPLC-AFS.
high performance liquid chromatography combined with atomic fluorescence spectrometry; mercury specie;uncertainty; Boletus
DOI∶10.7506/spkx1002-6630-201724044
O657.3
A
1002-6630(2017)24-0272-06
毛永楊, 楊桐, 蘇濤, 等. 高效液相色譜-原子熒光光譜聯用法測定牛肝菌中無機汞、甲基汞、乙基汞的不確定度評估[J].食品科學, 2017, 38(24): 272-277.
10.7506/spkx1002-6630-201724044. http://www.spkx.net.cn
MAO Yongyang, YANG Tong, SU Tao, et al. Uncertainty evaluation of for determining inorganic mercury, methyl mercury and ethyl mercury in Boletus by high performance liquid chromatography combined with atomic fluorescence spectrometry[J]. Food Science, 2017, 38(24)∶ 272-277. (in Chinese with English abstract) DOI∶10.7506/spkx1002-6630-201724044. http∶//www.spkx.net.cn
2016-12-08
云南省衛生廳科研項目(云衛[2014]DB005)
毛永楊(1985—),男,助理工程師,碩士,研究方向為食品安全質量檢測。E-mail:maoyongyang@163.com

