個(gè)體化飲食對肥胖孕婦妊娠糖尿病患者外周血單核細(xì)胞亞群的影響
吳鳳會, 錢 雷, 孫海玲, 李 明, 藺 昕
(江蘇省濱海縣人民醫(yī)院, 1. 婦產(chǎn)科; 2. 檢驗(yàn)科, 江蘇 濱海, 224500; 3. 南京醫(yī)科大學(xué)附屬南京醫(yī)院 檢驗(yàn)科, 江蘇 南京, 210029)
個(gè)體化飲食對肥胖孕婦妊娠糖尿病患者外周血單核細(xì)胞亞群的影響
吳鳳會1, 錢 雷2, 孫海玲2, 李 明2, 藺 昕3
(江蘇省濱海縣人民醫(yī)院, 1. 婦產(chǎn)科; 2. 檢驗(yàn)科, 江蘇 濱海, 224500; 3. 南京醫(yī)科大學(xué)附屬南京醫(yī)院 檢驗(yàn)科, 江蘇 南京, 210029)
妊娠糖尿病; 個(gè)性化飲食干預(yù); 肥胖; 單核細(xì)胞亞群
妊娠糖尿病(GDM)是在妊娠前糖代謝正常,但孕期發(fā)現(xiàn)糖代謝異常的高危妊娠,個(gè)體化飲食有利于GDM患者病情的控制[1]。研究[2]表明,單核細(xì)胞根據(jù)其表面CD14和CD16表達(dá)分為3種細(xì)胞亞群: 經(jīng)典型(CD14++CD16-)、中間型(CD14+CD16+)和非經(jīng)典型(CD14dimCD16+)3個(gè)亞群,單核細(xì)胞亞群比例改變,引起機(jī)體慢性低密度炎癥反應(yīng)是肥胖人群2型糖尿病發(fā)病率增加的重要因素。本研究通過檢測肥胖孕婦GDM患者個(gè)體化飲食干預(yù)后外周血單核細(xì)胞亞群的變化,并檢測單核細(xì)胞表面趨化因子受體CCR2和CX3CR1表達(dá),以及單核細(xì)胞在單核細(xì)胞趨化蛋白-1 (MCP-1, CCR2的配體)、RANTES(CCR5的配體)和IP-10(CXCR3的配體)等趨化因子作用下的趨化能力,從而闡明個(gè)體化飲食的作用機(jī)制,現(xiàn)報(bào)告如下。
1 資料與方法
1.1 一般資料
選擇2016年1—11月本院門診產(chǎn)檢、BMI≥30 kg/m2單胎妊娠GDM孕婦50例,隨訪至住院分娩。入選標(biāo)準(zhǔn): 孕8~12周,進(jìn)行葡萄糖耐量試驗(yàn)(OGTT),口服75 g葡萄糖,血糖參考值上限是空腹(FBG)5.1 mmol/L、餐后1 h 10.0 mmol/L和餐后2 h 8.5 mmol/L, 在任何時(shí)間點(diǎn)高于參考值即診斷為GDM。隨機(jī)分為干預(yù)組和對照組各25例。排除標(biāo)準(zhǔn): 糖尿病、自身免疫性疾病、高血壓、腎臟病、甲狀腺功能亢進(jìn)或感染。2組孕婦身體質(zhì)量指數(shù)(BMI)、年齡、OGTT試驗(yàn)等指標(biāo)差異無統(tǒng)計(jì)學(xué)意義(P>0.05), 具有可比性。干預(yù)組年齡(28.2±4.32)歲,孕周(10.5±1.7)周, BMI(30.93±3.81) kg/m2, 75 g OGTT: FBG(5.12±1.43) mmol/L, 1 h(12.5±1.97) mmol/L, 2 h(9.75±1.84) mmol/L。對照組年齡(28.3±4.01)歲,孕周(10.4±1.8)周,BMI(30.16±3.62) kg/m2,75 g OGTT: FBG(5.03±1.27) mmol/L, 1 h(12.9±2.01) mmol/L, 2 h(9.84±1.92) mmol/L。醫(yī)院倫理委員會批準(zhǔn)本次研究(倫研2016-05),參加者均知情同意。
1.2 儀器和試劑
Beckman 7300全自動(dòng)生化分析儀檢測血糖、甘油三酯和總膽固醇濃度等生化指標(biāo),試劑由上海執(zhí)誠公司提供。C反應(yīng)蛋白(CRP)采用韓國艾科美熒光檢測儀及配套試劑。流式抗體FITC-鼠抗人 CD14、PerCP-Cy5.5-鼠抗人CD16、PE-鼠抗人CCR2、APC-鼠抗人CX3CR1、紅細(xì)胞裂解液均購自BD 公司。趨化因子MCP-1、RANTES、IP-10購自德國Pepro公司。
1.3 方法
1.3.1 個(gè)體化飲食指導(dǎo)和干預(yù): 2組孕婦均在本院建立個(gè)人健康檔案,進(jìn)行圍產(chǎn)期檢查。在診斷為GDM入組后,營養(yǎng)師調(diào)查近期飲食結(jié)構(gòu),按奇偶數(shù)隨機(jī)分為2組,對照組孕婦在產(chǎn)科門診接受常規(guī)產(chǎn)檢和營養(yǎng)指導(dǎo),參加孕期健康教育講座。干預(yù)組在此基礎(chǔ)上,營養(yǎng)師分析其飲食結(jié)構(gòu),專科護(hù)士進(jìn)行宣教、監(jiān)測和評估。根據(jù)患者BMI、胎兒體質(zhì)量增長情況、孕周和活動(dòng)量制定每日總熱量,總熱量=理想體質(zhì)量×(25~30) kcal/kg+200 kcal。孕早期、孕中期、孕晚期分別不低于1 500、1 800和2 200 kcal/d。根據(jù)總熱量制訂食譜,飲食中應(yīng)富含纖維素、維生素和礦物質(zhì)。蛋白質(zhì)、碳水化合物和脂肪和分別占總能量的25%~30%、45%~55%和20%~25%。堅(jiān)持低油、少鹽和少糖飲食,每日分為6餐,即早餐/早點(diǎn)、午餐/午點(diǎn)、晚餐/晚點(diǎn),分別占總熱量的20%、5%、35%、5%、30%和5%。責(zé)任護(hù)士應(yīng)用微信登記患者的食物種類和數(shù)量,輸入圍產(chǎn)營養(yǎng)管理系統(tǒng),直至入院分娩。
1.3.2 臨床指標(biāo)檢測: 患者入組時(shí)和分娩入院時(shí)抽取靜脈血4 mL, 用生化分析儀檢測血清中血糖、總膽固醇、高密度脂蛋白膽固醇(HDL-c)、低密度脂蛋白膽固醇(LDL-c)甘油三酯濃度; 免疫熒光儀檢測C反應(yīng)蛋白(CRP)濃度。記錄GDM患者胰島素使用、孕期體質(zhì)量增加、早產(chǎn)和新生兒出生體質(zhì)量。
1.3.3 流式細(xì)胞術(shù)檢測單核細(xì)胞亞群比例及表面趨化因子受體表達(dá): 100 μL靜脈血與10 μL FITC-鼠抗人CD14、10 μL PerCP-Cy5.5-鼠抗人CD16、10 μL PE-鼠抗人CCR2、APC-鼠抗人CX3CR1單克隆抗體或10 μL同型對照共孵育30 min, 紅細(xì)胞裂解液破壞紅細(xì)胞后,流式細(xì)胞儀根據(jù)前向散射光(FSC)和側(cè)向散射光(SSC)區(qū)別單核細(xì)胞,然后檢測單核細(xì)胞亞群比例及細(xì)胞表面趨化因子受體CCR2和CX3CR1平均熒光強(qiáng)度(MFI)。
1.3.4 單核細(xì)胞遷移能力檢測: 取3 mL靜脈血,用淋巴細(xì)胞分離液分離單個(gè)核細(xì)胞(PBMCs), 經(jīng)磷酸鹽緩沖液(PBS)洗滌后,用RPMI-1640細(xì)胞培養(yǎng)液重懸,在細(xì)胞培養(yǎng)瓶內(nèi)培養(yǎng)4 h, 用貼壁法收集單核細(xì)胞,移去非貼壁的淋巴細(xì)胞。經(jīng)流式檢測CD14陽性單核細(xì)胞比例>95 %。RPMI-1640完全培養(yǎng)液重懸單核細(xì)胞,細(xì)胞終濃度為5×105cells/mL, 取100 μL等份細(xì)胞懸液接種在transwell小室上部,小室下部分別是終濃度100 ng/mL MCP-1、100 ng/mL IP-10、1 ng/mL RANTES和空白對照。置于37 ℃的5%CO2孵箱孵育150 min, 檢測小室下部單核細(xì)胞數(shù),與空白對照數(shù)細(xì)胞數(shù)相除得知單核細(xì)胞趨化指數(shù)。
2 結(jié) 果
干預(yù)組入組后至分娩入院時(shí)每日蛋白質(zhì)、碳水化合物、脂肪、攝入總熱量與對照組相比降低,差異均有統(tǒng)計(jì)學(xué)意義(P<0.05), 見表1。
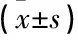
表1 患者干預(yù)后飲食結(jié)構(gòu)比較
與對照組比較, *P<0.05。
2組空腹血糖、LDL-c和CRP降低, HDL-c升高,差異均有統(tǒng)計(jì)學(xué)意義(P<0.05), 總膽固醇和甘油三酯濃度差異無統(tǒng)計(jì)學(xué)意義(P>0.05), 見表2。
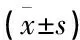
表2 GDM患者干預(yù)后生化指標(biāo)比較
與對照組比較, *P<0.05。
干預(yù)組胰島素使用率、新生兒體質(zhì)量和孕期體質(zhì)量增加均低于對照組(P<0.05), 但2組羊水過多發(fā)生率、早產(chǎn)發(fā)生率差異無統(tǒng)計(jì)學(xué)意義(P>0.05), 見表3。
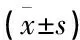
表3 GDM患者干預(yù)后臨床指標(biāo)比較
與對照組比較, *P<0.05。
2.4 飲食干預(yù)對單核細(xì)胞亞群的影響
干預(yù)組與對照組相比,在入院時(shí)中間型單核細(xì)胞和非經(jīng)典型單核細(xì)胞降低,經(jīng)典型單核細(xì)胞升高,差異均有統(tǒng)計(jì)學(xué)意義(P<0.05), 見表4。
2.5 單核細(xì)胞趨化因子表達(dá)和體外遷移能力
與對照組相比,干預(yù)組單核細(xì)胞表面趨化因子受體CCR2和CX3CR1平均熒光強(qiáng)度(MFI)降低(P<0.05)。干預(yù)組單核細(xì)胞在MCP-1和RANTES作用下的趨化指數(shù)降低(P<0.05), 但在IP-10作用下的趨化指數(shù)差異無統(tǒng)計(jì)學(xué)意義(P>0.05), 見表5。

表4 GDM患者外周血單核細(xì)胞亞群比較[M(P25~P75), %]
與對照組比較, *P<0.05。
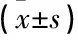
表5 單核細(xì)胞趨化因子受體表達(dá)及遷移指數(shù)比較
與對照組比較, *P<0.05。
3 討 論
個(gè)體化飲食干預(yù)是GDM基本治療方法,本研究發(fā)現(xiàn), GDM患者在個(gè)體化飲食干預(yù)后,做到定時(shí)定量、平衡膳食,并控制個(gè)體化總熱量,生化指標(biāo)、妊娠結(jié)局良好,孕婦體質(zhì)量增加控制在《孕期體質(zhì)量增長指南》推薦的范圍內(nèi)[3]。
單核細(xì)胞3個(gè)亞群具有不同的功能。經(jīng)典型單核細(xì)胞在炎癥的早期階段通過CCR2依賴性機(jī)制轉(zhuǎn)移到炎癥部位,表現(xiàn)為吞噬作用和產(chǎn)生活性氧(ROS), 具有抗病原微生物感染的功能; 中間型單核細(xì)胞可發(fā)揮抗原提呈,產(chǎn)生大量細(xì)胞因子促進(jìn)炎癥反應(yīng); 非經(jīng)典CD14+、CD16++單核細(xì)胞主要巡邏血管壁并分化為巨噬細(xì)胞,在炎癥反應(yīng)的后期階段通過CX3CR1依賴性途徑募集,參與多種慢性炎癥疾病[2]。外周血循環(huán)非經(jīng)典型和中間型單核細(xì)胞的比例在肥胖人群外周血顯著升高,并導(dǎo)致機(jī)體慢性炎癥反應(yīng)。
單核細(xì)胞亞群與2型糖尿病也具有密切的聯(lián)系。2型糖尿病患者外周血中間型和非經(jīng)典型單核細(xì)胞亞群比例升高,且非經(jīng)典型單核細(xì)胞比例和血糖值存在正相關(guān)[4]。本研究也發(fā)現(xiàn),對GDM患者進(jìn)行飲食干預(yù)后,中間型和非經(jīng)典型單核細(xì)胞顯著降低,而經(jīng)典型單核細(xì)胞顯著升高。以上分析表明,個(gè)性化飲食干預(yù)可降低中間型單核細(xì)胞和非經(jīng)典型單核細(xì)胞,從而降低機(jī)體的炎癥反應(yīng)。
單核細(xì)胞參與2型糖尿病的發(fā)生發(fā)展還與其具有更高的趨化活性有關(guān),從而浸潤脂肪組織增加,引起慢性炎癥,導(dǎo)致機(jī)體胰島素抵抗增加[5]。單核細(xì)胞表面趨化因子受體CCR1, CCR2, CCR3和CCR5表達(dá)升高,在趨化性細(xì)胞因子MCP-1、RANTES和IP-10的作用下,單核細(xì)胞可遷移到脂肪組織。研究證實(shí), 2型糖尿病和肥胖人群外周單核細(xì)胞上CCR2、CCR5表達(dá)增加,單核細(xì)胞具有更高的趨化活性,在內(nèi)皮細(xì)胞和脂肪組織分泌的趨化因子作用下,聚集到脂肪組織形成巨噬細(xì)胞,參與炎癥反應(yīng),并與胰島素抵抗相關(guān)[6]。BMI和機(jī)體脂肪量與單核細(xì)胞對MCP-1, RANTES和趨化因子混合物的遷移活性呈正相關(guān)。也有研究者對單核細(xì)胞亞群表面趨化因子受體進(jìn)行研究,經(jīng)典型單核細(xì)胞表達(dá)高水平的CCR2, 低表達(dá)CCR5和CX3CR1; 中間單核細(xì)胞和非典型單核細(xì)胞表達(dá)高水平的CX3CR1和CCR5, 但不表達(dá)CCR2[7]。肥胖人群外周血單核細(xì)胞亞群CX3CR1表達(dá)都增加,經(jīng)典型和中間型CCR2和CCR5表達(dá)增加,且CCR2和CX3CR1表達(dá)和HDL-c濃度負(fù)相關(guān)[8]。本研究也表明,個(gè)性化飲食干預(yù)降低了單核細(xì)胞表面趨化因子受體CCR2 和CX3CR1表達(dá),單核細(xì)胞遷移能力降低。
個(gè)性化飲食干預(yù)影響單核細(xì)胞的功能可能與飲食干預(yù)引起肥胖和2 型糖尿病患者脂質(zhì)代謝的變化有關(guān)。肥胖人群異常脂質(zhì)代謝可影響單核細(xì)胞表型和功能。另外,肥胖人群較高BMI和脂肪量影響機(jī)體內(nèi)環(huán)境,導(dǎo)致單核細(xì)胞活化。2型糖尿病患者中間型單核細(xì)胞比例升高,與血清CRP和IL-6水平呈正相關(guān),且單核細(xì)胞對脂多糖的刺激有異常的反應(yīng)性,產(chǎn)生高濃度的IL-6和MCP-1, 促進(jìn)機(jī)體的炎癥反應(yīng)[9]。
綜上所述,對GDM肥胖孕婦進(jìn)行個(gè)體化飲食干預(yù),改變膳食結(jié)構(gòu),降低攝入總熱量,可顯著改善患者糖代謝,降低胰島素使用率, GDM病情得到滿意控制,其機(jī)制可能是飲食干預(yù)可改變外周血單核細(xì)胞亞群比例和表面趨化因子的表達(dá),降低單核細(xì)胞遷移,從而減輕機(jī)體的炎癥反應(yīng),降低胰島素抵抗,改善糖代謝狀況。但是,由于調(diào)查性研究的局限性,個(gè)體化飲食干預(yù)和單核細(xì)胞之間的內(nèi)在機(jī)制尚不完全清楚。另外,本次研究樣本量偏小,個(gè)體化飲食干預(yù)對單核細(xì)胞產(chǎn)生促炎細(xì)胞因子的作用也有待進(jìn)一步進(jìn)行大樣本、多中心的臨床評估和驗(yàn)證。
[1] Santangelo C, Zicari A, Mandosi E, et al. Could gestational diabetes mellitus be managed through dietary bioactive compounds Current knowledge and future perspectives[J]. Br J Nutr, 2016, 115(7): 1129-1144.
[2] Pushpanathan P, Srikanth P, Seshadri K G, et al. Gut Microbiota in Type 2 Diabetes Individuals and Correlation with Monocyte Chemoattractant Protein1 and Interferon Gamma from Patients Attending a Tertiary Care Centre in Chennai, India[J]. Indian J Endocrinol Metab, 2016, 20(4): 523-530.
[3] Rasmussen K M, Yaktine A L. Weight gain during pregnancy: reexamining the guidelines[M]. Washington (DC): National Academies Press(US), 2009: 254-263.
[4] Wise A F, Williams T M, Rudd S, et al. Human mesenchymal stem cells alter the gene profle of monocytes from patients with Type 2 diabetes and end-stage renal disease[J]. Regen Med, 2016, 11(2): 145-158.
[5] Dai X, Zhan J, Demmy T A, et al. Monocytes play different roles in stimulating T cells in obese diabetic individuals[J]. Int J Immunopathol Pharmacol, 2015, 28(3): 374-383.
[6] Krinninger P, Ensenauer R, Ehlers K, et al. Peripheral monocytes of obese women display increased chemokine receptor expression and migration capacity[J]. J Clin Endocrinol Metab, 2014, 99(7): 2500-2509.
[7] Geissmann F, Manz M G, Jung S, et al. Development of monocytes, macrophages, and dendritic cells[J]. Science, 2010, 327(5966): 656-661.
[8] Devêvre E F, Renovato-Martins M, Clément K, et al. Profiling of the three circulating monocyte subpopulations in human obesity[J]. The Journal of Immunology, 2015, 194(8): 3917-3923.
[9] Yang M, Gan H, Shen Q, et al. Proinflammatory CD14+CD16+monocytes are associated with microinflammation in patients with type 2 diabetes mellitus and diabetic nephropathy uremia[J]. Inflammation, 2012, 35(1): 388-96.
R 473.71
A
1672-2353(2017)22-193-03
10.7619/jcmp.201722083
2017-04-16
江蘇省鹽城市醫(yī)學(xué)科技發(fā)展計(jì)劃項(xiàng)目(YC2015065)

