FOXC2對肺腺癌細胞惡性增殖及侵襲遷移能力的影響
饒習敏 邢時云 歐陽瑤 (遵義醫學院附屬醫院呼吸內科,貴州 遵義 563000)
FOXC2對肺腺癌細胞惡性增殖及侵襲遷移能力的影響
饒習敏 邢時云1歐陽瑤 (遵義醫學院附屬醫院呼吸內科,貴州 遵義 563000)
目的探究叉頭框C2蛋白(FOXC2)對肺腺癌細胞惡性增殖及侵襲遷移能力的影響。方法利用慢病毒轉染的方法在人肺腺癌細胞系A549中構建過表達FOXC2細胞(實驗組)及相應對照細胞系(對照組),Western印跡檢測兩組細胞FOXC2及干性相關分子Oct4、Sox2及Nanog的表達水平,MTT法檢測兩組細胞0、24、48、72、96 h的惡性增殖能力,Transwell侵襲及遷移實驗檢測兩組細胞侵襲遷移能力。結果與對照組細胞比較,實驗組細胞FOXC2、Oct4、Sox2及Nanog表達水平均顯著上調(P<0.05),細胞惡性增殖能力在48、72及96 h出現顯著升高(P<0.05),細胞侵襲及遷移能力均顯著上調(P<0.05),差異均有統計學意義。結論FOXC2可促進肺腺癌細胞惡性增殖及侵襲遷移能力,其機制與介導腫瘤細胞干細胞特性形成有關。
叉頭框C2蛋白;肺腺癌;惡性增殖;侵襲遷移;腫瘤干細胞
肺腺癌發病占全部肺癌的50%以上,是肺癌主要的病理類型〔1〕。肺腺癌多起源于小支氣管,為周圍型肺癌,故早期臨床癥狀較輕,但肺腺癌細胞增殖轉移能力強,部分早期即發生血行轉移,故多數患者就診時已處于中晚期。因此,明確影響肺腺癌細胞增殖轉移能力的關鍵因子對臨床診斷及治療工作具有重要意義。叉頭框C2蛋白(FOXC2)在正常機體內參與棕色脂肪代謝及血管生成等生物學過程〔2〕,在多種惡性腫瘤的發生發展中起促進作用,但對于肺腺癌惡性行為的影響尚不清楚。本研究擬探討FOXC2對人肺腺癌細胞A549增殖轉移能力的影響及機制。
1 材料與方法
1.1材料 儀器:ECO1.8垂直流超凈工作臺及3110生化培養箱(美國Thermo),5417R高速離心機(德國Eppendorf),DM1000光學顯微鏡(德國Leica),TC20細胞計數儀及Tek多孔酶標儀(美國Bio-Rad),電泳槽、電泳儀、轉膜儀及轉印夾等(上海天能),Gel Doc XR凝膠成像儀(美國Bio-Rad)。
細胞:人肺腺癌細胞系A549及人胚胎腎細胞293T(上海細胞生物研究所)。
試劑:DMEM培養基、DMEM/F12培養基、小牛血清及胎牛血清(美國Hyclone),胰蛋白酶(美國Sigma)轉染脂質體Lipofectamine 2000(美國Thermo),慢病毒包裝載體pLP1-gag/pol、REV和VSV-G(美國Addgene),FOXC2全長載體及空白對照載體(上海吉瑪基因),嘌呤霉素(美國Sigma),MTT細胞增殖及毒性檢測試劑盒(美國Promega),Transwell小室及24孔板、Matrigel基質膠(美國BectonDickinson),RIPA蛋白裂解液、蛋白酶抑制劑(cocktail)及考馬斯亮藍BCA蛋白濃度測定試劑盒(上海碧云天生物),甲醇等無機試劑(國藥集團化學試劑),abcam抗體:一抗:β-actin(ab8226)、FOXC2(ab24340)、Oct4(ab18976)、Sox2(ab92494)及Nanog(ab21624);二抗:鼠二抗(ab6728),兔二抗(ab150077)。PierceECL化學發光液(美國Thermo)。
1.2方法
1.2.1細胞的培養及實驗組與對照組的構建 人肺腺癌細胞系A549采用DMEM/F12+10%胎牛血清培養,1∶3傳代;人胚胎腎細胞293T采用DMEM+10%胎牛血清培養,1∶3傳代。培養環境:37℃,5%CO2,100%相對濕度。
慢病毒包裝:培養對數生長期的293T細胞于6孔板中,當細胞密度達到70%以上時,棄去上清并加入1 ml DMEM培養基備用。將pLP1-gag/pol、REV和VSV-G按0.75 μg、0.45 μg及0.30 μg的比例混合于2支含500 μl無血清DMEM的1.5 ml Eppendorf管中,并將1.5 μg FOXC2全長載體及空白對照載體分別加入2支Eppendorf管中,室溫靜置5 min后與10 μl Lipofectamine 2000充分混合,室溫靜置30 min,將上述混合液緩慢均勻滴加入293T細胞中,生化培養箱中培養6 h,更換DMEM+10%胎牛血清培養基繼續培養48 h后,收集病毒懸液并過濾。慢病毒感染:將制備好的病毒懸液與DMEM/F12+10%胎牛血清1∶2混合培養A549細胞3 d,感染攜帶FOXC2全長載體的A549細胞為實驗組,感染攜帶空白對照載體的A549細胞為對照組,1 μg/μl嘌呤霉素篩選細胞至生長狀態良好。
1.2.2Western印跡檢測兩組細胞FOXC2、Oct4、Sox2及Nanog的表達 收集融合度約為80%,培養于10 cm培養皿中的各組細胞:PBS洗細胞2次,600 μl胰蛋白酶消化,1 ml DMEM/F12+10%胎牛血清培養基終止消化加入Eppendorf管,800 r/min室溫離心5 min,去上清后PBS洗細胞2次,加入RIPA蛋白裂解液及蛋白酶抑制劑混合液500 μl,充分混勻后冰上裂解2 h,13 000 r/min,4℃離心細胞懸液15 min,取上清液置于新的Eppendorf管中,作為抽提的蛋白,經BCA試劑盒進行蛋白定量分析,配平體系后,配置10%聚丙烯酰胺凝膠,上樣量50 μg,80 V穩壓電泳至條帶出積層膠,調整電壓至120 V穩壓電泳1 h,260 mA穩流轉聚偏氟乙烯(PVDF)膜2 h,麗春紅染色,根據染色情況剪取β-actin、FOXC2、Oct4、Sox2及Nanog所在目的條帶,相應抗體室溫孵育2 h(工作濃度為1∶1 000),PBS洗膜3次,每次10 min;二抗孵育1 h(工作濃度為1∶2 000),PBS洗膜3次,每次10 min,電化學發光法(ECL)曝光顯影,ImageLab4.2軟件分析各條帶相比內參基因β-actin的相對灰度值。
1.2.3MTT實驗檢測細胞惡性增殖能力 培養對數生長期的各組細胞于10 cm培養皿中,將待檢測細胞消化,重懸并進行細胞計數,以2×103個細胞/孔的濃度接種至96孔板中,設置5個時間點(0、24、48、72、96 h)及5個重復孔,待細胞貼壁后,以此時為0 h時間點,棄去細胞上清液,將MTT試劑與DMEM/F12+10%胎牛血清培養基1∶5混合加入0 h時間點的孔中,設置空白孔,檢測各孔與空白孔490 nm吸光度,以各孔與空白孔OD值的差值作為增殖能力。同樣,在24、48、72、96 h檢測細胞的OD值,以各時間點細胞OD值與0 h細胞OD值的比值表示細胞惡性增殖能力。
1.2.4Transwell侵襲實驗檢測兩組細胞侵襲能力 將50 mg/L基質膠與DMEM/F12培養基1∶8混合均勻,100 μl加至小室中央,置于37℃孵育6 h后取出備用。將各組細胞消化,PBS洗細胞3次后,DMEM/F12+1%小牛血清重懸細胞并進行細胞計數,取5×104個細胞/孔加入鋪好基質膠的上小室中,下小室加入500 μl DMEM/F12+10%胎牛血清,生化培養箱孵育24 h后,棉簽擦去上室面未穿透的細胞,10%甲醇固定細胞15 min,0.1%結晶紫染色30 min,PBS洗細胞3次,200倍光鏡下計數,隨機統計中間和四周5個視野的細胞數,求其均值及標準差。
1.2.5Transwell遷移實驗檢測細胞遷移能力 將Transwell侵襲實驗中DMEM/F12+1%小牛血清重懸后的細胞取5×104個細胞/孔加入未鋪膠的上小室中,下小室同樣加入500 μl DMEM/F12+10%胎牛血清,生化培養箱孵育24 h后,固定、染色及計數方法同Transwell侵襲實驗。
1.3統計學方法 應用SPSS17.0統計學軟件對數據的組間比較行t檢驗。
2 結 果
2.1各組細胞FOXC2、Oct4、Sox2及Nanog的表達比較 實驗組細胞FOXC2相對灰度值顯著高于對照組細胞,且細胞干性相關分子Oct4、Sox2及Nanog相對灰度值均顯著高于對照組(P<0.05),見表1,圖1。
2.2兩組細胞的惡性增殖能力比較 實驗組細胞在48、72、96 h時增殖能力顯著高于對照組(P<0.05),見表2。
2.3實驗組及對照組細胞的侵襲及遷移能力比較 Transwell侵襲實驗結果顯示,實驗組侵襲基底膜的細胞數為(83.7±10.3)個,顯著多于對照組(54.8±9.5)個(P<0.05);Transwell遷移實驗結果顯示,實驗組細胞遷到下室的細胞數為(119.2±13.6)個,顯著多于對照組(66.3±11.2)個(P<0.05),見圖2。

表1 兩組細胞FOXC2、Oct4、Sox2及Nanog的表達比較
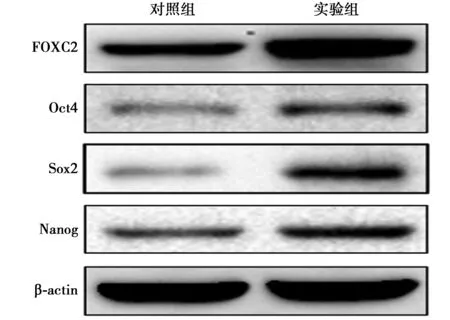
圖1 兩組細胞FOXC2、Oct4、Sox2及Nanog的表達情況比較
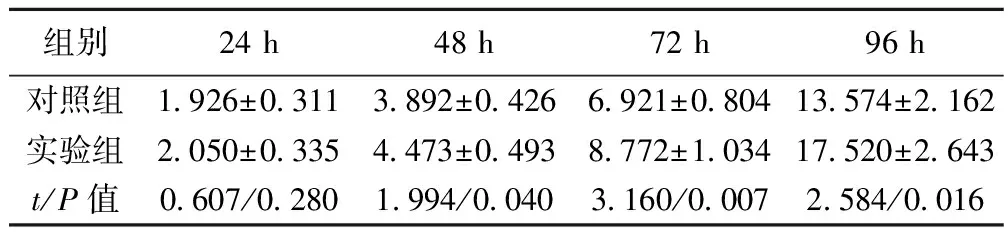
組別24h48h72h96h對照組1926±03113892±04266921±080413574±2162實驗組2050±03354473±04938772±103417520±2643t/P值0607/02801994/00403160/00072584/0016

圖2 兩組細胞的侵襲及遷移能力比較(×200)
3 討 論
FOXC2是人叉頭框蛋白家族轉錄因子之一,在人體生長發育及代謝中發揮重要作用,包括促進胚胎組織的成熟及棕色脂肪組織的代謝,也可增強組織胰島素敏感性及血管的生成〔3~5〕。近年有研究顯示FOXC2參與多種惡性腫瘤的發生發展,包括乳腺癌、結直腸癌、胃癌及前列腺癌等:①FOXC2與乳腺癌:FOXC2被發現在乳腺癌組織中表達上調,且其蛋白表達與腫瘤高組織學分級、TNM分期、早期復發、患者不良預后及原癌基因Twist表達均密切相關〔6〕,提示FOXC2對乳腺癌發生發展的促進作用。另外體外研究顯示,FOXC2可通過激活乳腺癌細胞上皮間充質轉化(EMT)過程促進腫瘤干細胞(CSC)樣特性,進而介導乳腺癌細胞增殖轉移及化療抵抗的形成〔7〕。②FOXC2與結直腸癌:FOXC2在結直腸癌組織中高表達,并與患者淋巴結轉移、高TNM分期及不良預后密切相關〔8,9〕,FOXC2還可在體外促進結直腸癌細胞侵襲轉移能力,其機制與促進原癌基因肝細胞生長因子(HGF)-酪氨酸激酶受體EMT的信號通路表達有關〔10〕。③FOXC2與胃癌:FOXC2在胃癌中同樣高表達,高FOXC2表達與胃癌細胞低分化程度、高TNM分期及不良預后正相關,是影響患者預后的獨立危險因素〔11〕。④FOXC2與前列腺癌:雄激素受體(AR)陰性的前列腺癌中FOXC2表達較高,此類細胞具有干細胞特性,是前列腺癌藥物去勢抵抗形成的關鍵因素,體外敲降FOXC2表達后,前列腺癌細胞EMT進程減弱且藥物去勢敏感性增強,表明FOXC2對前列腺癌發生發展的促進作用〔12〕。⑤FOXC2與卵巢癌:FOXC2在卵巢癌轉移灶中高表達,體外下調FOXC2表達后,細胞EMT進程及侵襲轉移能力均顯著減弱〔13〕。另外,FOXC2可通過促進EMT進程介導卵巢癌細胞體內外順鉑抵抗的發生〔14,15〕。⑥FOXC2與肺癌:FOXC2在非小細胞肺癌組織中高表達,且與患者肺腺癌發生、淋巴結轉移及TNM分期呈正相關,是影響患者預后的獨立危險因素〔16〕。
Oct4基因是POU轉錄因子家族中的一員,主要表達于胚胎干細胞、生殖干細胞以及多種惡性腫瘤細胞中,是腫瘤干細胞樣表型的標志物之一〔17〕;Sox2及Nanog是維持干細胞的多功能性、祖細胞自我更新能力的重要基因,同時也在多種惡性腫瘤細胞中表達上調并促進其發生發展〔18,19〕。本研究結果顯示,FOXC2可顯著上調肺腺癌細胞干性相關分子Oct4、Sox2及Nanog的表達,提示FOXC2可促進肺腺癌細胞干性的維持,進而發揮相應的生物學功能;同時,FOXC2可促進肺腺癌細胞惡性增殖及侵襲遷移能力,在體外揭示了FOXC2的促癌作用。
1楊清海,陳惠玲,鄭智勇.肺腺癌臨床病理研究新進展〔J〕.臨床與實驗病理學雜志,2014;30(1):53-5.
2Xue Y,Cao R,Nilsson D,etal.FOXC2 controls Ang-2 expression and modulates angiogenesis,vascular patterning,remodeling,and functions in adipose tissue〔J〕.Proc Nat Acad Sci U S A,2008;105(29):10167-72.
3Ddin MK,Kimura W,Ishikura T,etal.Foxc2 in pharyngeal arch mesenchyme is important for aortic arch artery remodelling and ventricular septum formation〔J〕.Biomed Res,2015;36(4):235-45.
4Kanady JD,Munger SJ,Witte MH,etal.Combining Foxc2 and connexin37 deletions in mice leads to severe defects in lymphatic vascular growth and remodeling〔J〕.Dev Biol,2015;405(1):33-46.
5Lidell ME,Seifert EL,Westergren R,etal.The adipocyte-expressed forkhead transcription factor foxc2 regulates metabolism through altered mitochondrial function〔J〕.Diabetes,2011;60(2):427-35.
6Lim JCT,Koh VCY,Tan JSY,etal.Prognostic significance of epithelial-mesenchymal transition proteins Twist and Foxc2 in phyllodes tumours of the breast〔J〕.Breast Cancer Res Treat,2015;150(1):19-29.
7Hollier BG,Tinnirello AA,Werden SJ,etal.FOXC2 expression links epithelial-mesenchymal transition and stem cell properties in breast cancer〔J〕.Cancer Res,2013;73(6):1981-92.
8Watanabe T,Kobunai T,Yamamoto Y,etal.Gene expression of mesenchyme forkhead 1 (FOXC2) significantly correlates with the degree of lymph node metastasis in colorectal cancer〔J〕.Int Surg,2011;96(3):207-16.
9Li Q,Wu J,Wei P,etal.Overexpression of forkhead Box C2 promotes tumor metastasis and indicates poor prognosis in colon cancer via regulating epithelial-mesenchymal transition〔J〕.Am J Cancer Res,2015;5(6):2022-34.
10Cui YM,Jiao HL,Ye YP,etal.FOXC2 promotes colorectal cancer metastasis by directly targeting MET〔J〕.Oncogene,2015;34(33):4379-90.
11Zhu JL,Song YX,Wang ZN,etal.The clinical significance of mesenchyme forkhead 1 (FoxC2) in gastric carcinoma〔J〕.Histopathology,2013;62(7):1038-48.
12Paranjape AN,Soundararajan R,Werden SJ,etal.Inhibition of FOXC2 restores epithelial phenotype and drug sensitivity in prostate cancer cells with stem-cell properties〔J〕.Oncogene,2016;35(46):5963-76.
13Liu B,Han SM,Tang XY,etal.Overexpressed FOXC2 in ovarian cancer enhances the epithelial-to-mesenchymal transition and invasion of ovarian cancer cells〔J〕.Oncol Rep,2014;31(6):2545-54.
14Li C,Ding H,Tian J,etal.Forkhead box protein C2 (FOXC2) promotes the resistance of human ovarian cancer cells to cisplatin in vitro and in vivo〔J〕.Cell Phys Biochem,2016;39(1):242-52.
15Li C,Ding H,Tian J,etal.Forkhead box protein C2 promotes epithelial-mesenchymal transition,migration and invasion in cisplatin-resistant human ovarian cancer cell line (SKOV3/CDDP)〔J〕.Cell Phys Pharmacol,2016;39(3):1098-110.
16Wei J,Hong F,Cheng Q,etal.Prognostic value of high FoxC2 expression in resectable non-small cell lung cancer,alone or in combination with E-cadherin expression〔J〕.BMC Cancer,2016;16(1):1-9.
17陳 琛,孟凡榮,萬海粟,等.MicroRNAs與OCT4基因之間的相互作用〔J〕.中國肺癌雜志,2015;26(1):55-8.
18滕 楊,陳公琰.惡性腫瘤中 SOX2基因的研究進展〔J〕.實用腫瘤學雜志,2014;28(2):173-6.
19季 文,姜 政.Nanog基因研究進展〔J〕.醫學綜述,2011;17(5):672-6.
R73
A
1005-9202(2017)24-6033-03;
10.3969/j.issn.1005-9202.2017.24.013
1 遵義醫學院附屬醫院腫瘤科
歐陽瑤(1965-),女,碩士,主任醫師,主要從事慢性阻塞性肺病發病機制研究。
饒習敏(1984-),女,碩士,主治醫師,主要從事慢性阻塞性肺病基礎與臨床研究。
〔2017-02-11修回〕
(編輯 徐 杰)

