巨噬細胞移動抑制因子在腎透明細胞癌組織中的表達與意義
孫連桃 肖偉利 (包頭醫學院醫學技術學院,內蒙古 包頭 04040)
巨噬細胞移動抑制因子在腎透明細胞癌組織中的表達與意義
孫連桃 肖偉利1(包頭醫學院醫學技術學院,內蒙古 包頭 014040)
目的探討巨噬細胞移動抑制因子(MIF)在腎透明細胞癌組織中的表達與意義。方法采用免疫組化法檢測52例腎透明細胞癌組織及相應癌旁正常組織中MIF的表達,并分析其表達與臨床病理特征的關系。結果腎透明細胞癌組織中MIF的陽性率(40/52)顯著高于癌旁正常組織(8/52)(P<0.05)。MIF陽性表達率與分化程度無關(P>0.05)。Ⅲ~Ⅳ期腎透明細胞癌組織中MIF陽性率高于Ⅰ~Ⅱ期。有淋巴結轉移者的MIF陽性率高于無淋巴結轉移者(P<0.05)。MIF表達與腫瘤直徑密切相關(P<0.05),與患者性別及年齡均無關(P>0.5)。結論MIF在腎透明細胞癌組織中高表達,并促進腎透明細胞癌的發生、發展,可成為腎癌診斷的判斷指標。
腎透明細胞癌;巨噬細胞移動抑制因子
腎癌是泌尿系統常見的惡性腫瘤,僅次于膀胱癌。其中腎透明細胞癌約占腎癌的85%,且發病率近年來呈上升趨勢〔1〕。雖然隨著醫學影像技術不斷發展,腎癌的早期診斷率有所提高,但仍有部分患者在診斷初期就發現轉移病灶,使得5年生存率不足10%,而且患者行根除術后仍會復發,成為泌尿外科醫師甚為棘手的問題〔1〕。近年研究發現巨噬細胞移動抑制因子(MIF)在眾多腫瘤組織中高表達,如乳腺癌、膀胱癌、肝癌、胃癌等,而且MIF與上述腫瘤的侵襲轉移密切相關〔2~6〕,但有關其在腎透明細胞癌組織中的表達情況尚未見報道。本文旨在探討MIF在腎透明細胞癌組織中的表達及其與臨床病理特征的關系。
1 材料與方法
1.1標本來源 收集內蒙古自治區人民醫院和包頭市腫瘤醫院泌尿外科2014年3月至2017年3月病理科確診為腎癌的癌組織石蠟標本52例,所有標本均為腎透明細胞癌。其中男34例,女18例,<60歲者24例,≥60歲者28例,年齡42~76歲,中位年齡62歲。腫瘤直徑<3 mm的患者25例,腫瘤直徑≥3 mm的患者27例。根據WHO(2016)推薦WHO/ISUP分級系統分級:Ⅰ~Ⅱ級合并為高分化,26例,Ⅲ級為中分化,15例,Ⅳ級為低分化,11例。根據美國癌癥聯合委員會〔AJCC(2002)〕腎癌臨床分期標準分期:Ⅰ~Ⅱ期29例,Ⅲ+Ⅳ23例。有淋巴結轉移者10例,無淋巴結轉移者42例。另取腎癌旁正常組織52例作為對照。所有患者術前均未接受任何化療、放療、靶向治療及免疫治療。
1.2免疫組化 標本先于二甲苯中脫蠟,再依次于95%、85%、75%無水乙醇中繼續脫蠟。3%過氧化氫消除內源性過氧化物,并于檸檬酸鹽抗原修復盒中修復。10%山羊血清室溫下封閉30 min。一抗溶液,4℃過夜孵育,第2天二抗溶液室溫下孵育,二氨基聯苯胺(DAB)顯色后沖洗。蘇木精復染、1%鹽酸分化,氨水反藍。梯度乙醇中脫水,二甲苯中透明,中性樹脂封片,并于顯微鏡下觀察。以磷酸鹽緩沖液(PBS)液代替一抗作為陰性對照。
1.3結果判斷 MIF蛋白以細胞質內出現棕黃色及棕褐色顆粒為陽性表達,由工作經驗豐富的病理科醫師采用雙盲法閱片。在高倍鏡的條件下隨機的選擇5個視野,觀察細胞的染色情況。按細胞的染色程度評分:未染色為0分,淺黃色為1分,棕黃色為2分,棕褐色為3分。按陽性細胞所占百分率評分:無陽性細胞為0分,陽性細胞數<25%為1分,25%~50%為2分,≥50%為3分。每個視野陽性細胞所占百分率評分乘以染色評分即是該切片的總得分:0~1分表示陰性(-),2~3分表示弱陽性(+),4~6分表示陽性(),6分以上表示()。
1.4統計學方法 應用SPSS17.0統計軟件進行分析,計數資料采用和比率進行統計學描述,并采用卡方檢驗或Fisher確切概率法比較組間MIF陽性表達率的差異,P<0.05為差異有統計學意義。
2 結 果
2.1MIF在腎透明細胞癌組織及癌旁正常組織中的表達MIF定位細胞質中,以棕黃色或棕褐色為陽性表達,腎透明細胞癌組織(40/52)中MIF的陽性率顯著高于癌旁正常組織(8/52)(P<0.05)。見圖1,表1。
2.2MIF與腎透明細胞癌病理分化程度、TNM分期、淋巴結轉移的關系 MIF陽性表達率與分化程度無關(P>0.05)。Ⅲ~Ⅳ期中MIF陽性表達率高于Ⅰ~Ⅱ期(P<0.05)。有淋巴結轉移的MIF陽性表達率高于無淋巴結轉移(P<0.05)。見表2。
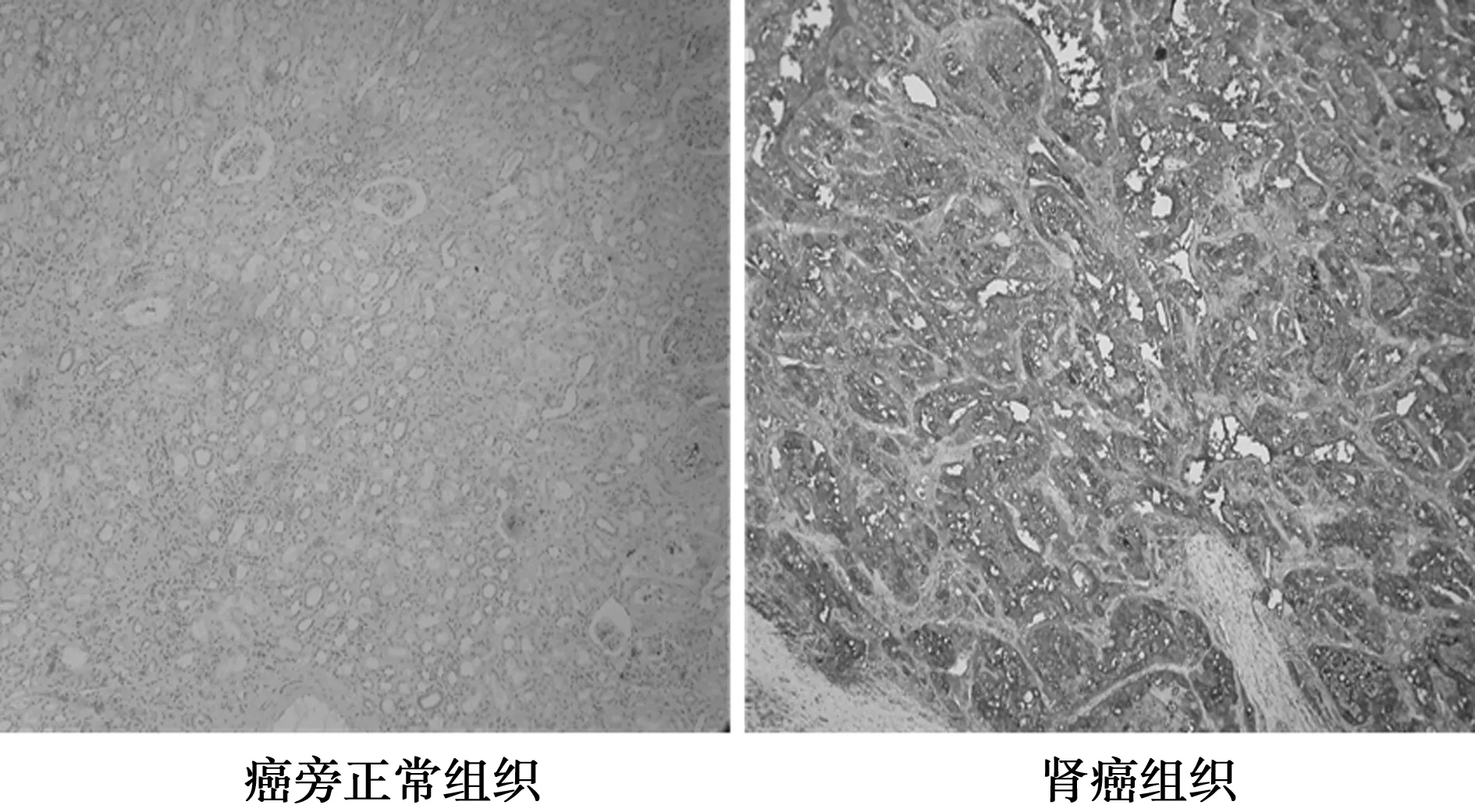
圖1 MIF在腎透明細胞癌組織及癌旁正常組織中的表達(×200)

分組nMIF-+陽性率(%)χ2值P值癌旁正常組織52448153839619<0001癌組織5212407692
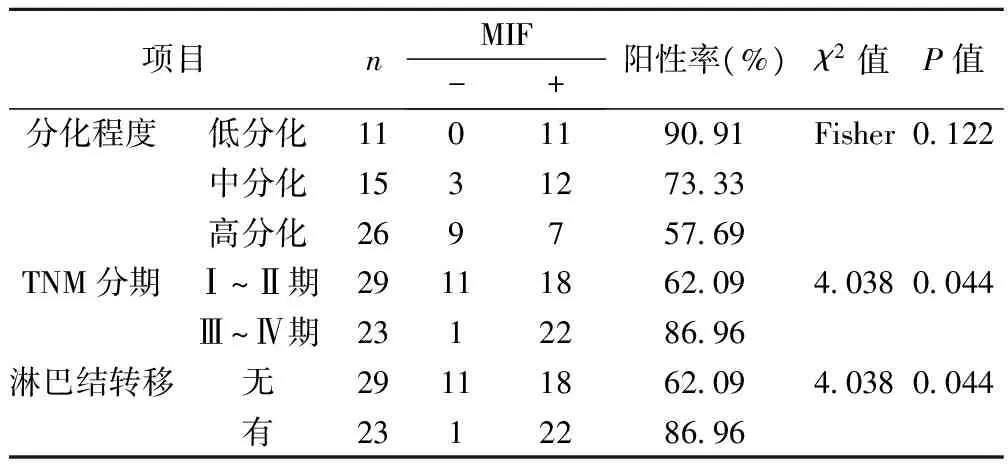
表2 MIF與腎透明細胞癌病理分化程度、TNM分期、淋巴結轉移的關系(n)
2.3MIF與腎透明細胞癌臨床病理特征的關系 MIF的陽性表達率與腫瘤直徑密切相關(P<0.05),MIF的陽性表達率與性別、年齡無關(P>0.05)。見表3。
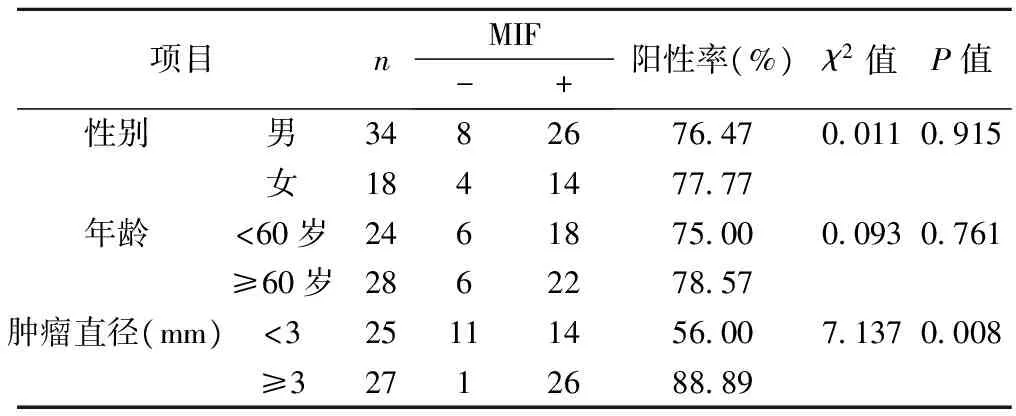
表3 MIF與腎透明細胞癌其他臨床病理特征的關系(n)
3 討 論
MIF是1970年Bloom等在研究遲發型變態反應中發現的一種能夠抑制巨噬細胞移動的多功能因子,MIF基因定位于人第22號染色體上,由于此基因片段中含有內分泌激素調控的序列,所以以往對于MIF的研究主要集中于免疫系統和內分泌系統相關疾病中。MIF主要來源于活化的T細胞,能夠表達于包括腎小管上皮細胞、肝細胞、表皮細胞等,通過內分泌或者旁分泌促進IL-6、IL-8等炎癥因子的分泌,進而引起各種炎癥反應〔7〕。近些年研究還證實MIF與胰腺癌,肝癌,膀胱癌,胃癌等腫瘤的發生、發展密切相關〔2~6〕。而且采用ELISA法證實了腎透明細胞癌患者血清中MIF表達量顯著高于健康對照組,并且發現RNA干擾腎癌細胞中MIF表達,能顯著的降低細胞活力,細胞克隆形成能力及成瘤能力。進一步說明MIF在腎癌的發生、發展中起著重要作用。本研究結果表明腎癌組織(40/52)中MIF的陽性率顯著高于癌旁正常組織(8/52),與MIF在其他腫瘤中的表達趨勢一致〔2-6〕。同時本實驗還分析了MIF與腎癌臨床病理參數的關系,結果發現MIF與腫瘤臨床分期、有無淋巴結轉移及腫瘤大小呈正相關,與患者性別及年齡、組織分化程度無關。另外馬寧等〔3〕研究不僅證實胃癌組織中MIF陽性表達高于瘤旁組織,還證實MIF與TNM分期、浸潤深度、淋巴結轉移呈正相關。陶斌勝等〔5〕研究亦證實肝癌組織中MIF表達顯著高于癌旁正常組織。同時MIF還與腫瘤大小,有無遠處轉移呈正相關。從而說明隨著腎癌增殖程度越強,腫瘤組織塊越大,腫瘤惡性程度越高,MIF陽性率越高,提示高表達的MIF對腎透明細胞癌的增殖、惡性程度及淋巴結轉移起著促進作用,MIF可能能夠成為腎透明細胞癌診斷的有效指標。
另外有研究證實:(1)MIF通過與其受體CD74相互作用,激活細胞外調節蛋白激酶(ERK),蛋白激酶(AKT)及絲裂原活化蛋白激酶(MAPK)信號通路進而促進細胞的增殖〔8〕。將MIF/CD74信號軸抑制劑4-IPP作用于結腸癌細胞,能顯著的抑制AMPK及AKT信號通路活性,并使癌細胞線粒體損傷并誘導細胞凋亡〔9〕。(2)通過提高胃癌細胞(BGC-823)及(MKN-28)中MIF的表達,能顯著的激活MAPK信號通路,并下調CyclinD1及p53表達,上調Mcm2及增殖細胞核抗原(PCNA)表達,進而促使癌細胞細胞周期G1期向S快速轉換〔10〕。siRNA干擾乳腺癌細胞MCF-7中MIF表達,能顯著的降低MAPK,p44/42MAPK磷酸化水平,進而下調血管內皮生長因子(VEGF-C)表達,最終抑制腫瘤細胞的增殖與血管生成〔11〕。(3)RNA干擾口腔鱗狀細胞Tca8113,HN5及SCC25中MIF表達,能顯著的下調MMP9表達,繼而抑制癌細胞侵襲〔12〕。由此推測出MIF可能是通過與其受體CD74相互作用進而激活AKT、ERK及MAPK信號通路繼而促使腎癌細胞的惡性增殖;也可能是MIF直接激活MAPK信號通路繼而調控下游靶基因表達,促使腎癌細胞快速增殖或并發生侵襲轉移;又或者是MIF能直接上調MMPs表達進而促使腎癌細胞發生侵襲轉移。
綜上所述,MIF的表達與腎透明細胞癌組織的TNM分期,淋巴結轉移,腫瘤直徑密切相關,與患者性別、年齡、腎透明細胞癌組織的分化程度無關。因此,MIF在腎透明細胞癌的發生、發展中可能起促進作用,但其具體作用機制仍需深入探討。
1孫飛達,王東文,米振國.腎癌分子靶向治療的現狀及研究進展〔J〕.現代泌尿生殖腫瘤雜志,2012;4(1):1-3.
2Richard V,Kindt N,Saussez S.Macrophage migration inhibitory factor involvement in breast cancer(Review)〔J〕.Int J Oncol,2015;47(5):1627-33.
3馬 寧,周 云.胃癌組織中miR-451與MIF的表達及與臨床病理的關系〔J〕.中國老年學雜志,2015;35(3):655-6.
4張 珺,吳 奎,肖 峻,等.膀胱尿路上皮癌中MIF與VEGF的表達及其臨床意義〔J〕.安徽醫科大學學報,2014;49(3):354-8.
5陶斌勝,熊茂明,曹立宇.肝癌組織中MIF、TNF-α的表達及臨床意義〔J〕.臨床與實驗病理學雜志,2011;27(11):1177-80.
6Tan L,Ye X,Zhou Y,etal.Macrophage migration inhibitory factor is overexpressed in pancreatic cancer tissues and impairs insulin secretion function of beta-cell〔J〕.J Transl Med,2014;12(1):92.
7樊根濤,吳蘇稼.巨噬細胞移動抑制因子在腫瘤發病機制中的研究進展〔J〕.醫學研究生學報,2013;26(1):77-9.
8Ohta S,Misawa A,Fukaya R,etal.Macrophage migration inhibitory factor(MIF)promotes cell survival and proliferation of neural stem/progenitor cells〔J〕.J Cell Sci,2012;125(Pt 13):3210-20.
9Bozzi F,Mogavero A,Varinelli L,etal.MIF/CD74 axis is a target for novel therapies in colon carcinomatosis〔J〕.J Exp Clin Cancer Res,2017;36(1):16.
10Zhang J,Zhang G,Yang S,etal.Macrophage migration inhibitory factor regulating the expression of VEGF-C through MAPK signal pathways in breast cancer MCF-7 cell〔J〕.World J Surg Oncol,2016;14(1):51.
11Li XJ,Luo Y,Yi YF.P115 promotes growth of gastric cancer through interaction with macrophage migration inhibitory factor〔J〕.World J Gastroenterol,2013;19(46):8619-29.
12Zeng J,Quan J,Xia X.Transient transfection of macrophage migration inhibitory factor small interfering RNA disrupts the biological behavior of oral squamous carcinoma cells〔J〕.Mol Med Rep,2016;13(1):174-80.
R737.11
A
1005-9202(2017)24-6113-03;
10.3969/j.issn.1005-9202.2017.24.047
內蒙古自治區自然科學基金(No.2014MS0807)
1 內蒙古自治區人民醫院
孫連桃(1972-),女,碩士,副教授,主要從事醫學檢驗研究。
〔2017-09-03修回〕
(編輯 袁左鳴)

