樹突細胞-細胞因子誘導殺傷細胞聯合術后化療治療非小細胞肺癌的療效
姜海燕 劉達興 徐 剛 宋永祥 (六盤水市人民醫院胸心外科,貴州 六盤水 553000)
樹突細胞-細胞因子誘導殺傷細胞聯合術后化療治療非小細胞肺癌的療效
姜海燕 劉達興1徐 剛1宋永祥1(六盤水市人民醫院胸心外科,貴州 六盤水 553000)
目的評價Ⅱa~Ⅲa期非小細胞肺癌(NSCLC)術后輔助化療聯合樹突細胞(DC)-細胞因子誘導殺傷(CIK)細胞治療的效果。方法NSCLC手術病例79例,隨機分為術后輔助化療組40例(對照組)和術后輔助化療聯合3個療程DC-CIK細胞治療組39例(治療組);兩組完成術后4個療程化療后,對比隨訪1年的復發率和生存率、每次化療前血清癌性標志物癌胚抗原(CEA)、CYFRA21-1含量;密切觀察細胞回輸不良反應,評價患者生活質量評分。結果術后1年,治療組腫瘤復發率明顯低于對照組(P<0.05);死亡率兩組無明顯差異(P>0.05)。治療結束后6個月,兩組功能狀況(KPS)、生活質量(QOL)評分無明顯差異(P>0.05);治療結束后12個月治療組KPS、QOL評分較對照組明顯增高 (P<0.05)。治療結束后6個月、12個月治療組體力狀態(ZPS)評分明顯低于對照組(P<0.05)。兩組患者第2、3、4次化療前比第1次化療前CEA 和CYFRA21-1含量明顯降低(P<0.05)。第4次化療前,治療組CEA水平明顯低于對照組 (P<0.05)。第2、3、4次化療前治療組CYFRA21-1水平均低于對照組(P<0.05)。治療組發生惡心,嘔吐,納差,失眠的人次均明顯低于對照組(P<0.05);而發生乏力人次兩組無明顯差異 (P>0.05)。結論術后化療聯合3個療程DC-CIK細胞治療可降低NSCLC術后1年腫瘤復發率,降低血清癌性標志物CEA和CYFRA21-1的含量,提高患者生活質量。
肺癌;手術;化療;DC-CIK細胞治療
采用手術為主,放、化療為輔的綜合治療是目前中晚期肺癌最有效的治療手段,但肺癌患者總體5年生存率仍不足15%,其治療給患者帶來極大的毒副作用,嚴重影響了肺癌患者的生活質量。相關研究表明樹突細胞(DC)-細胞因子誘導殺傷(CIK)細胞治療晚期肺癌可明顯提高晚期肺癌患者機體免疫功能,減輕放化療引起的不良反應等〔1,2〕。本文觀察DC-CIK聯合術后化療對非小細胞肺癌(NSCLC)的療效。
1 資料與方法
1.1病例納入和剔除標準 (1) 納入標準:①手術病理證實為NSCLC患者;②臨床TNM分期為Ⅱa~Ⅲa期(2011年UICC標準);③均實施根治性手術+規范化系統淋巴結清掃術;④45歲≤年齡≤70歲;⑤術后患者一般情況好,臨床判斷能耐受術后輔助化療≥3 w,體力狀況(ZPS)評分≤ 2分,功能狀況(KPS)評分≥70分;⑥預計生存期≥3個月,心、肝、腎功能、造血系統正常;白細胞數≥3.5×109/L,血小板數≥90×109/L, 血清谷丙轉氨酶≤40 IU/L;血清總膽紅素≤18 μmol/L,肌酐≤130 μmol/L;⑦醫護人員知情告知,患者簽署知情同意書。(2) 剔除標準:①實驗期間病情惡化者;患者出現無法耐受的副作用;要求退出治療者;②器官衰竭者;③患有其他獲得性、先天性自身免疫缺陷疾病,或有器官移植史者;④患有不可控制的嚴重感染性疾病者;⑤對本細胞治療中所有生物試劑過敏者;⑥患有或并發T細胞淋巴瘤者。
1.2臨床資料 收集2012年3月至2013年3月遵義醫學院附屬醫院治療的Ⅱa~Ⅲa期NSCLC手術患者79例,根據住院號末尾數隨機分組,奇數設為治療組,偶數設為對照組。對照組僅予術后輔助化療,共40例,男25例,女15例,腺癌16例,鱗癌24例,年齡45~69〔平均(53.50±8.79)〕歲。治療組予術后輔助化療聯合DC-CIK細胞治療3個療程,共39例,男22例,女17例,腺癌16例,鱗癌23例,年齡45~69〔平均(57.23±9.30)〕歲。對照組與治療組性別、年齡、病理分型、臨床TNM分期比較無明顯差異(P>0.05)。
1.3治療前準備 使用COM.TEC血細胞分離機(Fresenius Kabi)采集患者自體外周血單個核細胞(PBMNCs),立即送細胞制備室。在嚴格無菌條件下,由實驗室技術人員對采集送至臨床級GMP實驗室的患者PBMNCs參照文獻〔3〕及相關標準進行DC-CIK細胞制備,化療前1 d通過細胞分離機與淋巴細胞分離液獲取患者本人PBMNCs。DC培養:經淋巴細胞分離液密度梯度離心獲得PBMNCs,經 RPMI1640培養液洗滌,置于無血清培養基中混懸,在 37℃、5%CO2培養箱中培養 4 h 后加入粒細胞巨噬細胞集落刺激因子(GM-CSF)(1 000 U/ml)和白細胞介素(IL)-4(5 000 U/ml) 繼續培養,每隔2 d換液1次,第5天加入腫瘤壞死因子(TNF)-α(500 U/ml)誘導成熟DC。CIK 細胞培養:分離后淋巴細胞加入重組人干擾素(IFN)-γ(1 000 U/ml)和 10%AB 型人血清RPMI1640培養液,24 h后加入小鼠抗人CD3單抗 (100 ng/ml)、IL-2(1 000 U/ml),以后隔天半量換液維持培養。DC-CIK細胞聯合培養:收獲第7天DC及CIK細胞按1∶5計數混合培養 3 d,隔天補加IL-2(1 000 U/ml) 培養液。
1.4術后治療方案 (1)對照組:遵抗癌協會NSCLC化療指南〔4〕,采用含鉑二聯方案。具體為:長春瑞濱(上海旭東海普藥業有限公司,生產批號11122534)25 mg/m2靜脈注射,第1、8日;順鉑(江蘇恒瑞醫藥股份有限公司,生產批號:12011023)25 mg/m2靜脈注射,第1~3天,4 w為1個周期,共4個周期。(2)治療組:在對照組治療方案的基礎上,聯合DC-CIK細胞治療。在化療周期間隔第 2、4、6、8、10 d,將 DC-CIK細胞用100 ml 0.9%生理鹽水液回輸體內,每次回輸細胞(4~5)×109個,5 次為1個療程,使用3個療程。治療過程中出現胃腸道反應、骨髓抑制、肝腎功損害等對癥處理。
1.5觀察指標 ①治療結束后,評價完成化療6個月和12個月的生存情況并評價其生活質量,主要包括KPS評分、ZPS評分、生活質量(QOL)評分;②每次化療前檢測血清癌性標志物:所有研究對象抽取空腹肘靜脈血3.0 ml,3 000 r/min離心10 min,取上清待測。采用化學發光法測定血清癌胚抗原(CEA)、CYFRA21-1的含量;③記錄并評估兩組治療過程中發生不良反應的人次數。
1.6統計學方法 采用SPSS19.0軟件進行χ2及t檢驗。
2 結 果
2.1兩組腫瘤復發和死亡情況比較 治療后12個月內,治療組腫瘤復發率明顯低于對照組〔2.6%(1/39) vs 17.5%(7/40),χ2=4.840,P=0.028〕;治療組死亡率低于對照組〔7.7%(3/39) vs 15.0%(6/40)〕,但無統計學差異(χ2=1.045,P=0.307)。其中治療組1例死于化療后6個月內,2例死于化療后12個月內;對照組4例死于化療后6個月內,2例死于化療后12個月內。
2.2兩組KPS、ZPS、QOL評分比較 化療后6個月兩組KPS、QOL評分無明顯差異(P>0.05);化療后12個月治療組KPS、QOL評分明顯高于對照組(P<0.05,P<0.01)。化療后6和12個月ZPS評分治療組均明顯低于對照組(P<0.05),見表1。
2.3兩組化療前血清CEA、CYFRA21-1水平比較 兩組第2、3、4次化療前血清CEA 和CYFRA21-1水平均明顯低于第1次化療前(P<0.05)。第4次化療前,治療組血清CEA水平明顯低于對照組(P<0.05);第2、3、4次化療前治療組血清CYFRA21-1水平均明顯低于對照組(P<0.05,P<0.01),見表2。
2.4兩組不良反應比較 治療組發生惡心、嘔吐(34人次)、納差(45人次)、失眠(45人次)人次均明顯低于對照組(67、60、67人次;χ2=7.82,P=0.00;χ2=6.17,P=0.00;χ2=5.03,P=0.02);而乏力人次數治療組與對照組比較無明顯差異 (33人次vs 29人次,χ2=2.11,P=0.19)。
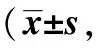
表1 兩組KPS、QOL、ZPS評分比較分)
與對照組比較:1)P<0.05,2)P<0.01
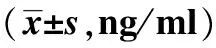
表2 兩組不同時點化療前血清CEA及CYFRA21-1水平比較
與本組第1次化療前比較:1)P<0.05;與對照組同一時點比較:2)P<0.05,3)P<0.01
3 討 論
DC-CIK細胞在臨床應用中特別是對于手術后的癌癥患者,清除殘留極微轉移病灶,防止癌細胞的擴散和復發,提高患者的自身免疫能力等具有重要作用〔5〕,廣泛應用于肝癌、食管癌、直腸癌、乳腺癌、腎癌、宮頸癌、卵巢癌、白血病等惡性腫瘤的術后治療中〔6~9〕。研究表明〔10〕,化療聯合DC-CIK治療NSCLC的有效率高達 41.6%~42.9%。本研究結果顯示,DC-CIK聯合化療治療NSCLC的復發率明顯低于對照組與既往相關研究報道一致〔11〕,其可能的機制是:CIK 細胞是人PBMNCs在體外經多種細胞因子刺激后獲得一群異質性細胞,該細胞表面可以表達 CD3和CD56 這2種膜蛋白分子,兼有T淋巴細胞溶瘤活性和NK細胞非主要組織相溶性復合物限制性殺瘤特點。CIK細胞體外培養細胞表型發生變化,其細胞毒活性與增殖能力大為增強,且對人體骨髓干細胞和造血祖細胞幾乎沒有毒性,因而在腫瘤生物治療上表現出強大優勢。CIK細胞進入體內活化后可以分泌 IL-2、IL-6、TNF-α等多種細胞因子,此類因子可直接發揮細胞毒作用,并可誘導癌細胞表達 Fas 和 FasL 細胞表面分子,加速細胞凋亡。體外實驗表明 CIK 細胞能誘導并加速人肺癌細胞株A549早期凋亡〔12〕。CIK 細胞在體內受到其他因子刺激后,可以將胞質顆粒釋放到胞外,而促進癌細胞裂解。DC是目前功能最強專職抗原提呈細胞,成熟DC可通過Ⅱ型組織相容性抗原等途徑呈遞腫瘤抗原,誘導特異性免疫反應,抵制腫瘤細胞免疫逃逸。它既可有效誘導靜止T細胞增殖,也可促進細胞毒性T淋巴細胞和輔助性T淋巴細胞生成〔13〕。將具有腫瘤抗原提呈能力 DC與細胞毒效應CIK細胞聯合培養,理論上可明顯提高CIK細胞毒活性。肺癌患者外周血清CEA、CYFRA21-1水平的連續動態監測對肺癌的轉移和預后判斷有一定臨床意義,其化療前、后血清中含量變化與治療效果密切相關〔14〕。腫瘤患者生活質量的評價已成為評價腫瘤患者治療療效的重要標準〔15〕。本研究顯示Ⅱa~Ⅲa期NSCLC患者術后化療聯合3個療程DC-CIK細胞治療,可提高肺癌患者綜合治療效果。
1Zhong R,Han B,Zhong H.A prospective study of the efficacy of a combination of autologous dendritic cells,cytokine-induced killer cells,and chemotherapy in advanced non-small cell lung cancer patients〔J〕.Tumour Biol,2014;35(2):987-94.
2Yang L,Ren B,Li H,etal.Enhanced antitumor effects of DC-activated CIKs to chemotherapy treatment in a single cohort of advanced non-small-cell lung cancer patients〔J〕.Cancer Immunol Immunother,2013;62(1):65-73.
3張志偉,宋 鑫.DC-CIK細胞臨床制備規范化研究〔J〕.中國腫瘤,2011;20(2):85-8.
4支修益,吳一龍,馬勝林,等.原發性肺癌診療規范(2011年版)〔J〕.中國肺癌雜志,2012;15(12):677-88.
5Wang QJ,Wang H,Pan K,etal.Comparative study on anti-tumor immune response of autologous cytokine-induced killer (CIK) cells,dendritic cells-CIK (DC-CIK),and semi-allogeneic DC-CIK〔J〕.Chin J Cancer,2010;29(7):641-8.
6Wei XC,Yang DD,Han XR,etal.Bioactivity of umbilical cord blood dendritic cells and anti-leukemia effect〔J〕.Int J Clin Exp Med,2015;8(10):19725-30.
7Gao D,Li C,Xie X,etal.Autologous tumor lysate-pulsed dendritic cell immunotherapy with cytokine-induced killer cells improves survival in gastric and colorectal cancer patients〔J〕.PLoS One,2014;9(4):e93886.
8Zhou P,Liang P,Dong B,etal.Phase Ⅰ clinical study of combination therapy with microwave ablation and cellular immunotherapy in hepatocellular carcinoma〔J〕.Cancer Biol Ther,2011;11(5):450-6.
9Wang ZX,Cao JX,Liu ZP,etal.Combination of chemotherapy and immunotherapy for colon cancer in China:a meta-analysis〔J〕.World J Gastroenterol,2014;20(4):1095-106.
10Yuanying Y,Lizhi N,Feng M,etal.Therapeutic outcomes of combining cryotherapy,chemotherapy and DC-CIK immunotherapy in the treatment of metastatic non-small cell lung cancer〔J〕.Cryobiology,2013;67(2):235-40.
11彭大為,李建旺,元建華,等.自體DC-CIK細胞聯合培美曲塞治療老年非小細胞肺癌的療效與安全性〔J〕.中國免疫學雜志,2012;28(7):648-51,656.
12蔣 濤,付立業,李 妍.CIK細胞對RNAi沉默PD-L1基因的肺腺癌A549細胞的體外抑制作用〔J〕.現代腫瘤醫學,2015;23(12):1641-3.
13Franceschetti M,Pievani A,Borleri G,etal.Cytokine-induced killer cells are terminally differentiated activated CD8 cytotoxic T-EMRA lymphocytes〔J〕.Exp Hematol,2009;37(5):616.
14王群慧,鄭 華,胡范彬,等.伴有EGFR突變的非小細胞肺癌血清CYFRA21-1和CEA水平與EGFR-TKIs的療效關系〔J〕.中國肺癌雜志,2016;19(8):550-8.
15杜軍華,喬洪源,尹宜發.血清CEA、CA125及Cyfra21-1水平對中晚期非小細胞肺癌患者預后的影響〔J〕.腫瘤防治研究,2016;43(2):137-40.
R73
A
1005-9202(2017)24-6118-03;
10.3969/j.issn.1005-9202.2017.24.049
貴州省省長資金臨床應用課題(黔省專合字號2012107號)
1 遵義醫學院附屬醫院胸心血管外科
劉達興(1970-),男,碩士,主要從事心臟血管外科研究。
姜海燕(1986-),女,碩士,主要從事肺癌的診斷與治療研究。
〔2016-07-19修回〕
(編輯 苑云杰/曹夢園)

